La bronquiolitis constrictiva (BC) secundaria al trasplante de progenitores hematopoyéticos (TPH) es una grave complicación que aparece en el contexto de una enfermedad injerto contra huésped (EICH) crónica1. Las pruebas de función pulmonar y, en menor medida (aunque de una manera creciente), la tomografía computarizada (TC), son las pruebas diagnósticas más importantes en la detección de la BC post-TPH2. Los corticoides sistémicos continúan siendo la piedra angular del tratamiento, pero de entre las nuevas terapias destaca el ruxolitinib, un fármaco que ha conseguido resultados esperanzadores en los pacientes con EICH3.
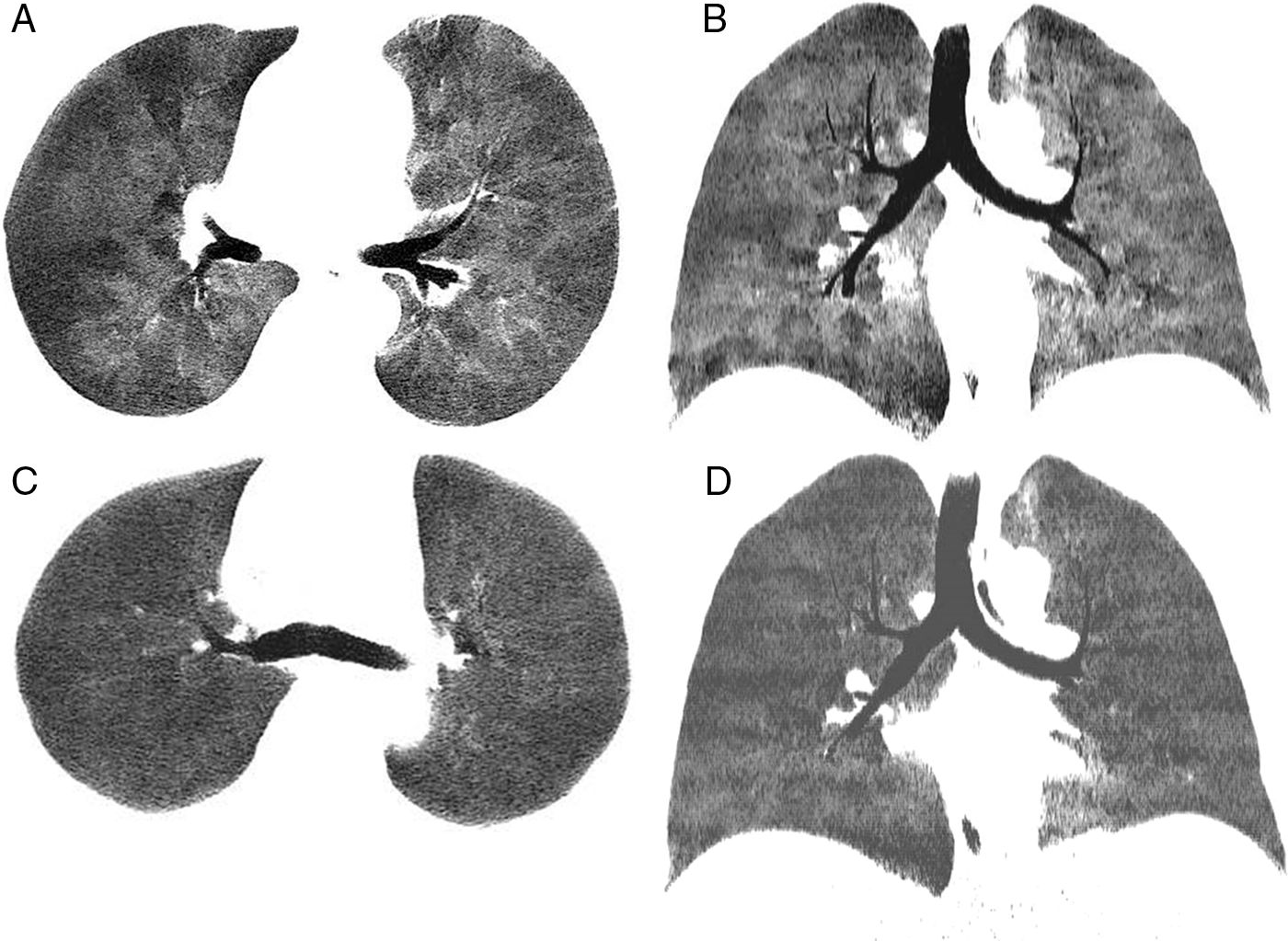
Presentamos el caso de un varón de 39 años con antecedentes de un linfoma B difuso de células grandes estadio iv tratado con varias líneas de quimioterapia y que, una vez alcanzada la remisión completa, se sometió a un TPH de donante emparentado en abril de 2015. Diez meses después del TPH el paciente desarrolló una EICH con manifestaciones cutánea, gastrointestinal y pulmonar, que no respondieron favorablemente al tratamiento con corticoides y fotoféresis extracorpórea. Las pruebas de función pulmonar previas a la EICH eran normales, mientras que tras la EICH mostraron un patrón obstructivo de intensidad moderada, siendo el volumen espiratorio forzado en el primer segundo (FEV1) del 59% sobre su teórico, la capacidad vital forzada (FVC) del 78%, y la relación FEV1/FVC del 68%, asociado a un descenso de la capacidad de difusión de CO del 71% con respecto a los valores pre-TPH. La TC de tórax dinámica (TCd) en inspiración y en espiración demostró la presencia de extensas áreas de atrapamiento aéreo en ambos pulmones (fig. 1A y 1B), al tiempo que descartó complicaciones infecciosas. El lavado broncoalveolar no detectó infecciones oportunistas. Ante estos hallazgos se emitió el diagnóstico de BC refractaria a corticoides y fotoféresis extracorpórea en el contexto de EICH post-TPH. Se decidió administrar ruxolitinib al paciente, lográndose una mejoría progresiva de las manifestaciones de la EICH, incluyendo la BC. Cuatro meses después del inicio del tratamiento con ruxolitinib, las pruebas de función pulmonar mostraron una mejoría significativa, aumentando el FEV1 (72%), la FVC (80%), y la relación FEV1/FVC (71%), si bien persistía un leve atrapamiento aéreo en la pletismografía con un volumen residual del 128% y una relación volumen residual/capacidad pulmonar total del 127. La TCd, realizada 3 meses después del inicio del tratamiento con ruxolitinib, también demostró menos signos de atrapamiento aéreo (fig. 1C y 1D) en la fase espiratoria.
Imagen axial (A) y coronal (B) minIP (proyección de intensidad mínima) de TC de tórax en espiración en la que se observa un llamativo patrón en mosaico del parénquima pulmonar, alternándose áreas geográficas de baja densidad con otras de mayor atenuación. Las áreas de menor densidad corresponden a zonas de atrapamiento aéreo. Imagen axial (C) y coronal (D) minIP de TC de tórax en espiración en la que se aprecia una menor heterogeneidad y mayor uniformidad de la atenuación del parénquima pulmonar con respecto a (A) y (B).
La BC es la complicación pulmonar no infecciosa más frecuente (y una de las más graves) del TPH y uno de los factores de riesgo más importantes de su aparición es la presencia de una EICH crónica. La presentación clínica de la BC suele ser insidiosa y los síntomas son inespecíficos (tos, disnea), aunque un 20% de los pacientes pueden encontrarse asintomáticos4. El Instituto Nacional de la Salud de Estados Unidos indica los siguientes criterios para el diagnóstico de BC post-TPH: 1) demostración de obstrucción al flujo aéreo (FEV1/FVC<0,7 y FEV1<80% del valor predicho); 2) atrapamiento aéreo en TC, volumen residual>120% del valor predicho o confirmación histológica de BC; y 3) ausencia de infección en la vía respiratoria5. Los hallazgos en TC más frecuentes son: atrapamiento aéreo, engrosamiento de las paredes bronquiales, patrón en mosaico y dilatación bronquial6. El pronóstico a largo plazo de la BC es generalmente malo (la supervivencia a los 5 años oscila entre el 13% y el 56%)4, y el objetivo del tratamiento es evitar una progresión de la obstrucción al flujo aéreo. El tratamiento con corticoides sistémicos continúa siendo el pilar terapéutico de la BC, aunque se han utilizado otras opciones terapéuticas combinándolas con fotoféresis extracorpórea, corticoides y/o broncodilatadores inhalados, montelukast, ofatumumab, y bortezomib7. El ruxolitinib es una nueva terapia dirigida que inhibe selectivamente las quinasas asociadas a Janus interfiriendo con la síntesis de varias citocinas y factores de crecimiento importantes para la hematopoyesis y la función inmune; recientemente se ha demostrado su eficacia en el tratamiento de la EICH resistente a corticoides8,9. En nuestro caso el beneficio clínico del ruxolitinib se constató en las primeras semanas tras su administración, demostrándose una correlación clínica, espirométrica y radiológica de dicha mejoría. Apenas existen descripciones en la literatura de casos de respuesta de BC post-TPH al tratamiento con ruxolitinib, y creemos que el caso presentado ilustra el beneficio de este prometedor fármaco en los pacientes con BC post-TPH al tiempo que nos recuerda la importancia de realizar estudios de TCd para correlacionar los hallazgos radiológicos con los espirométricos en estos pacientes10.