La EPOC es una enfermedad de elevada prevalencia pero infradiagnosticada, debido a la escasa implantación de la espirometría forzada (EF) en atención primaria. Los microespirómetros, baratos y de manejo sencillo, que pueden medir FEV6 y FEV1/FEV6, podrían contribuir a reducir el infradiagnóstico. El objetivo del estudio ha sido validar el dispositivo Piko-6 para el cribado de la EPOC, demostrando una buena correlación con la EF convencional.
MétodosSe han realizado una EF y una determinación con Piko-6 a 155 pacientes susceptibles de padecer EPOC. Se han comparado las correlaciones, curvas ROC e índice de Youden con ambos métodos, considerando la EF como patrón de referencia.
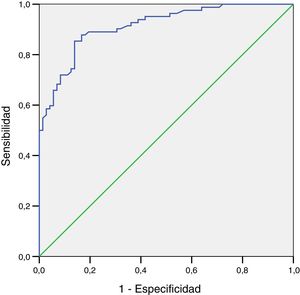
ResultadosLos coeficientes de correlación de FEV1, FVC y FEV6 y los cocientes FEV1/FVC y FEV1/FEV6 fueron de 0,87 (IC 95%: 0,836-0,909), 0,729 (IC 95%: 064-0,795) y 0,947 (IC 95%: 0,928-0,961) respectivamente. La curva ROC para el FEV1 determinado por Piko-6 alcanzó un área bajo la curva de 0,86 (IC 95%: 0,78-0,92). El índice de Youden para el punto de corte de 0,70 del FEV1/FEV6 fue 0,97.
ConclusionesEl Piko-6 puede ser útil para el cribado de la EPOC en atención primaria. Sus determinaciones presentan buena correlación con las obtenidas mediante EF, especialmente el cociente FEV1/FEV6. Esto, junto a su bajo coste y facilidad de uso, puede contribuir a reducir el infradiagnóstico de la EPOC, aunque su rol exacto en el proceso diagnóstico está aún por determinar.
COPD is a highly prevalent but underdiagnosed disease, due to the limited availability of forced spirometry (FS) in primary care (PC). Microspirometers are inexpensive, easy-to-use devices that can measure FEV6 and FEV1/FEV6, and may help reduce underdiagnosis. The aim of this study was to validate the Piko-6 COPD screening device by demonstrating a good correlation with standard FS.
MethodsFS and Piko-6 determinations were made in 155 patients suspected of having COPD. The correlations, ROC curves, and Youden's index of both methods were compared, taking FS as the gold standard.
ResultsFEV1, FVC and FEV6 correlation coefficients and FEV1/FVC and FEV1/FEV6 ratios were 0.87 (CI 0.836-0.909), 0.729 (CI 064-0.795) and 0.947 (95% CI 0.928-0.961), respectively. The ROC curve for FEV1 determined by Piko-6 achieved an area under the curve of 0.86 (95% CI: 0.78-0.92). Youden's index with a cut-off point of 0.70 for FEV1/FEV6 was 0.97.
ConclusionsPiko-6 may be useful for COPD screening in PC. Measurements obtained with this device correlate well with those determined by FS, particularly the FEV1/FEV6 ratio. This, combined with its low cost and ease of use, may contribute to reducing COPD underdiagnosis, although its exact role in the diagnostic process remains to be determined.
La EPOC se diagnostica en estadios avanzados, lo que impide instaurar precozmente un tratamiento eficaz que minimice sus efectos a medio/largo plazo. El estudio EPI-SCAN1 indica una prevalencia del 10% en sujetos de 40 a 80 años. Además, se estima que existe un infradiagnóstico del 73%2. La estrategia EPOC del Sistema Nacional de Salud propone mayor implicación de la atención primaria (AP) y mejorar la coordinación asistencial3.
La espirometría forzada con prueba broncodilatadora (EF) es imprescindible para el diagnóstico2 y tiene valor pronóstico por su relación con la mortalidad4. La generalización de la EF en AP es un desafío para el Sistema Nacional de Salud, pero existen serias dificultades para su implantación debido a factores como la mala técnica de realización y/o interpretación5, lo que contribuye al infradiagnótico6.
En AP el porcentaje de pacientes con sospecha o diagnóstico previo de EPOC que tienen una EF es bajo7. En dicho nivel se deberían realizar espirometrías de calidad por personal adiestrado y acreditado, pero la realidad dista mucho de lo ideal8: la EF se utiliza poco y generalmente la calidad de la prueba no es apropiada, especialmente por la dificultad de obtener una FVC correcta9.
Diferentes sociedades han propuesto recomendaciones, normativas y estándares para homogeneizar y mejorar la calidad de la EF10–12. Sin embargo, los estudios siguen mostrando una accesibilidad a la prueba limitada y un escaso seguimiento de las recomendaciones propuestas13,14.
El cribado de la EPOC en fumadores en AP aún no es una actividad generalizada15,16. La recomendación más extendida es realizar una EF a mayores de 35-40 años con un IPA≥10 paquetes/año y síntomas17; su utilidad en fumadores o exfumadores asintomáticos plantea más dudas. Un estudio realizado en España encontró un 20% de casos en pacientes asintomáticos, pero otros autores han observado cifras inferiores. Por ello, esta técnica debería formar parte del examen rutinario de salud en sujetos en riesgo18.
Las variables necesarias para el diagnóstico de EPOC son la capacidad vital forzada (FVC), el volumen espiratorio forzado en el primer segundo (FEV1) y el cociente FEV1/FVC. Dada la dificultad para obtener la FVC se ha propuesto que el volumen espiratorio forzado en 6segundos (FEV6) podría ser válido: el FEV6 y la relación FEV1/FEV6 pueden ser alternativas cuando se usan equipos portátiles19.
La simplicidad de los microespirómetros podría facilitar su implementación en AP como una alternativa válida que, según la ERS, debe ser investigada20. Existen al menos 2 dispositivos portátiles (COPD-6 y Piko-6) capaces de determinar FEV1 y FEV6. Tienen coste bajo, tamaño pequeño, son de manejo sencillo y no precisan calibración. Estas características podrían hacerlos útiles, al menos, en el cribado de la EPOC en AP21,22, aunque son escasas las publicaciones que evalúan su validez diagnóstica frente a los espirómetros convencionales en España.
El objetivo de este estudio ha sido determinar la utilidad del Piko-6 para el cribado de la EPOC, determinando la concordancia entre FEV1, FEV6 y FEV1/FEV6 realizados con este dispositivo con el FEV1, FVC y FEV1/FVC realizados mediante EF. Así mismo, fueron objetivos de este estudio encontrar el punto de corte del cociente FEV1/FEV6 para el dispositivo Piko-6, que permita descartar la presencia de EPOC en pacientes susceptibles y valorar si el FEV1 obtenido por Piko-6 es útil para clasificar a los pacientes según la clasificación de gravedad funcional.
Material y métodosSe reclutaron en 2 consultas de AP a pacientes que previamente no estaban diagnosticados de EPOC y que cumplían criterios para descartar EPOC: edad ≥40 años, IPA≥10 y síntomas compatibles, tales como tos, expectoración o disnea. Los pacientes que cumplían los criterios citados anteriormente eran invitados a participar en el estudio y, en caso de aceptar, eran derivados al servicio de neumología para realizar una EF y una microespirometría con el dispositivo Piko-6 (siempre en el mismo orden). Se incluyó de forma consecutiva a todos los pacientes que presentaban los criterios previamente descritos para el cribado de EPOC y que aceptaban participar en el estudio, durante el tiempo destinado al reclutamiento hasta alcanzar el n deseado.
Fueron considerados criterios de exclusión la presencia de contraindicaciones para la realización de una espirometría y la incapacidad para realizar correctamente las maniobras con el dispositivo Piko-6 y/o la espirometría. Se utilizaron en el estudio los criterios de aceptabilidad y de repetibilidad según la normativa SEPAR de espirometría de 2013 y se incluyeron en el estudio a los pacientes con grados de calidad de las espirometrías buena y suficiente (A, B y C), según la clasificación de calidad de la espirometría forzada de dicha normativa.
Las variables recogidas fueron: datos demográficos, síntomas, historia de exacerbaciones, determinaciones de FEV1, FVC y FEV1/FVC con EF y de FEV1, FEV6 y FEV1/FEV6 con Piko-6; además se valoró la dificultad subjetiva percibida por los pacientes para la realización de cada una de las pruebas (mediante una escala visual de color graduada de 0 a 10).
Estudio estadísticoEl cálculo del tamaño muestral se realizó a partir de los datos de los primeros 40 pacientes consecutivos registrados, estimando que el Piko-6 podría presentar una sensibilidad (S) del 90% y una especificidad (E) del 80% en la detección de obstrucción, con una prevalencia de la misma del 40% y un error alfa del 5%. Para obtener una precisión del 90% la muestra necesaria resultó ser de 154 pacientes.
Los datos se codificaron en una hoja Excel y se exportaron al programa SPSS 18.0, aplicando los test pertinentes en función de las variables. Para expresar las diferencias se utilizó la media de la diferencia y su intervalo de confianza del 95% (IC 95%). La comparación de variables cuantitativas se realizó por «t» de Student para muestras apareadas. En el análisis bivariante con variables cualitativas se aplicó la Chi cuadrado y el test exacto de Fisher. En todos los contrastes se consideró significativo un valor de p≤0,05.
Se utilizó el índice Kappa para evaluar la concordancia entre ambos dispositivos en la detección de obstrucción. La concordancia y la relación entre los valores se calculó con el coeficiente de correlación intraclase (CCI) y el de Pearson (r) respectivamente, y se representaron con gráficos de correlación.
La validez y seguridad del Piko-6 para detectar la obstrucción se determinó mediante la S, E, valor predictivo positivo, valor predictivo negativo y cocientes de probabilidad positivo y negativo. Así mismo, se calculó el área bajo la curva receiver-operating characteristic (ROC) de la ratio FEV1/FEV6 (con el Piko-6) en la discriminación de la obstrucción, utilizando como patrón oro el cociente FEV1/FVC obtenido mediante EF. Por último, para encontrar el mejor punto de corte del FEV1/FEV6 se utilizó el índice de Youden, estadístico que permite valorar el mejor compromiso entre la S y E de una prueba.
ResultadosSe incluyeron 155 pacientes, 111 varones y 44 mujeres, con edad media de 63±14 años (rango 25-89). Los valores porcentuales de los parámetros medidos con EF y Piko-6 (media y desviación estándar) se muestran en la tabla 1. Los valores de FEV1 y FVC determinados por EF fueron superiores al FEV1 y FEV6 medidos por Piko-6, pero sin diferencias significativas entre FEV1/FVC y FEV1/FEV6 determinados por ambos dispositivos. Se elaboró una tabla de contingencia de los pacientes diagnosticados de obstrucción por EF y Piko-6, considerando en ambos casos un cociente <0,7. La tabla 2 refleja los valores asociados a la prueba.
Valores medios y diferencias de los parámetros determinados por espirometría y Piko-6
| Espirómetro (media; sd) | Piko-6 (media; sd) | Valor de p | Diferencias espirómetro-Piko-6 | |
|---|---|---|---|---|
| FEV1 | 77,5 (28,8) | 73,8 (29,1) | 0,000 | –3,7 (–5,4; –2) |
| FVC | 93,1 (21,3) | 87,7 (23,7) | 0,000 | –5,3 (–7,8; –2,8) |
| FEV1/FVC | 65,7 (17,2) | 64,9 (16,1) | 0,092 | –0,7 (–1,6; 0,1) |
Tabla de contingencia del número de sujetos diagnosticados de obstrucción por espirometría y Piko-6
| Prueba de referencia espirometría forzada | |||
|---|---|---|---|
| Prueba diagnóstica Piko-6 | Enfermos | Sanos | Total |
| Positivo | 82 | 2 | 84 |
| Negativo | 0 | 71 | 71 |
| Total | 82 | 73 | 155 |
| Valor | IC (95%) | ||
|---|---|---|---|
| Sensibilidad (%) | 100 | 99,4 | 100 |
| Especificidad (%) | 97,2 | 92,8 | 100 |
| Índice de validez (%) | 98,7 | 96,6 | 100 |
| Valor predictivo+(%) | 97,62 | 93,7 | 100 |
| Valor predictivo(–)(%) | 100 | 99,3 | 100 |
| Prevalencia (%) | 52,9 | 44,7 | 61,1 |
| Índice de Youden | 0,9 | 0,9 | 1 |
|---|---|---|---|
| Razón de verosimilitud+ | 36,5 | 9,3 | 143,1 |
| Razón de verosimilitud– | - | - | - |
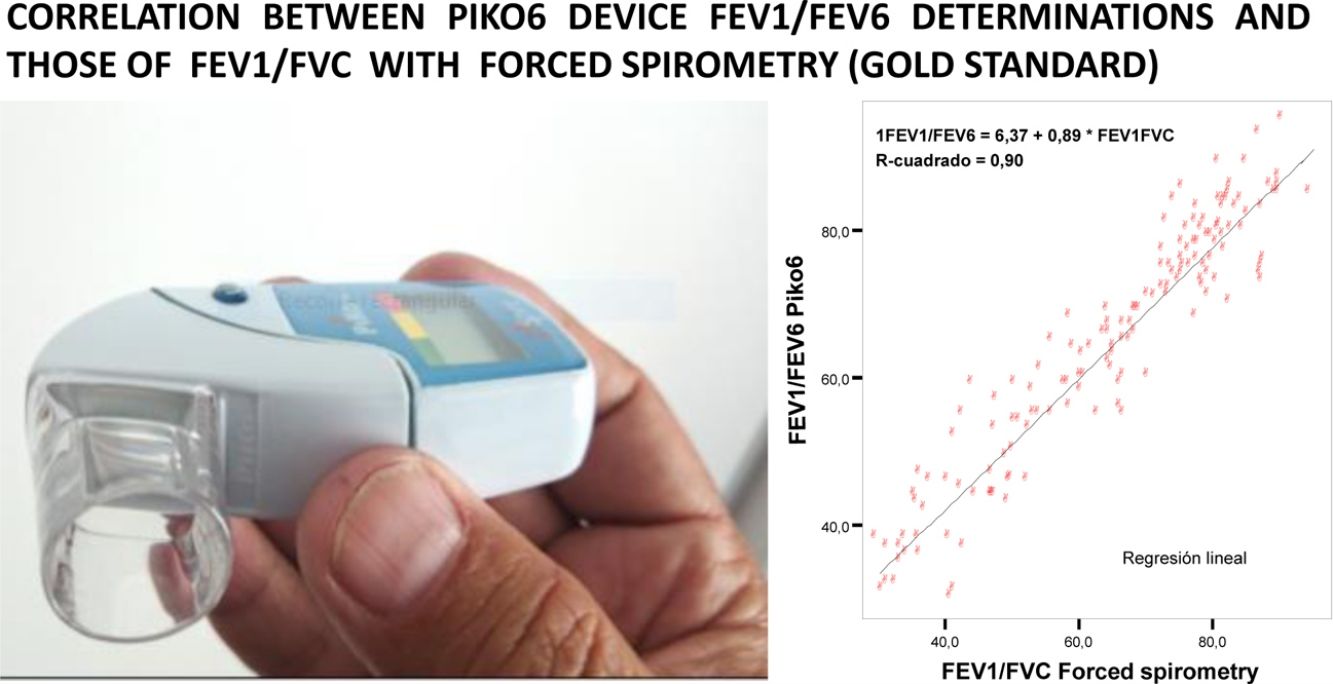
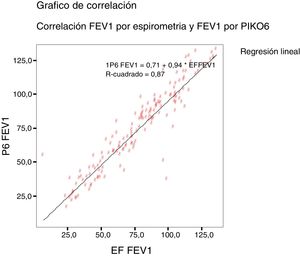
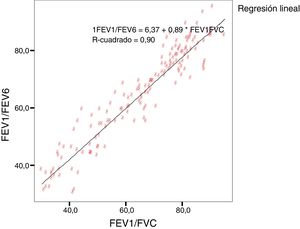
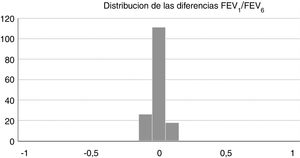
La concordancia y los coeficientes de correlación entre los parámetros fueron: FEV1 (EF) vs FEV1 (Piko-6): CCI 0,87 (IC 95%; 0,83-0,90); FVC vs FEV6: CCI 0,72 (IC 95%; 0,74-0,79); FEV1/FVC vs. FEV1/FEV6: 0,94 (IC 95%: 0,92-0,96). Los gráficos de correlación se muestran en las figuras 1 y 2: se observa que el grado de correlación entre el Piko-6 y la EF es excelente para todos los parámetros estudiados, siempre con significación estadística (p<0,0001). Para representar la dispersión de los valores del Piko-6, respecto a los de EF, se realizó el test de asimetría/curtosis. La variable FEV1 presentó valores de curtosis y asimetría de 6,19 y 2,65 respectivamente; el FEV6 5,65 y 2,52; el FEV1/FEV6 17,5 y 4,09. En los 3 parámetros la dispersión fue pequeña y claramente menor en la variable FEV1/FEV6 (fig. 3).
La curva ROC para el FEV1 (por Piko-6) para la detección de obstrucción mostro un área bajo la curva de 0,86 (IC 95%: 0,78-0,92) que, aun siendo un buen valor, no alcanzó el grado de excelencia obtenido por el cociente FEV1/FEV6 (fig. 4).
La tabla 3 refleja los valores de S, E, valor predictivo positivo, valor predictivo negativo, cocientes de probabilidad positivo y negativo e índice de Youden para determinar obstrucción por Piko-6, utilizando como gold estándar el FEV1/FVC<0,7 obtenido por EF. El mejor compromiso S/E se obtuvo con el punto de corte de 0,7 (utilizado también para descartar obstrucción con EF). Como se refleja en la tabla 3, el valor de 0,70 es el que proporciona mejores indicadores de validez de la prueba, entre el 96,6% y 100%. En cuanto a la concordancia entre ambos dispositivos para determinar obstrucción por el índice de Kappa el resultado fue de 0,97 (error estándar 0,018).
Valores de sensibilidad, especificidad, valores predictivos, coeficientes de probabilidad positivos y negativos para la detección de obstrucción (FEV1/FVC<0,7 por espirometría) para distintos puntos de corte de la razón FEV1/FEV6 medida por Piko-6 e índice de Youden
| FEV1/FEV6 (PIKO-6) | S (%) | E (%) | (%) VPP+ | (%) VPN– | CP+ | CP– | Índice de Youden |
|---|---|---|---|---|---|---|---|
| <0,68 | 87,8 | 83,5 | 85,7 | 85,9 | 13,4 | 0,02 | 0,92 |
| <0,69 | 91,4 | 95,8 | 96,1 | 90,9 | 21,7 | 0,04 | 0,94 |
| <0,70 | 100 | 97,2 | 97,6 | 100 | 35,7 | 0,00 | 0,97 |
| <0,71 | 100 | 91,8 | 93,1 | 100 | 12,2 | 0,00 | 0,93 |
| <0,72 | 100 | 89,0 | 91,1 | 100 | 9,0 | 0,00 | 0,93 |
| <0,73 | 100 | 84,9 | 88,0 | 100 | 6,6 | 0,00 | 0,9 |
| <0,74 | 100 | 80,8 | 85,4 | 100 | 5,2 | 0,00 | 0,83 |
Un objetivo secundario fue valorar si, en caso de existir obstrucción, la determinación del FEV1 por el Piko-6 permite clasificar su gravedad. En la tabla 4 se expone la clasificación de los pacientes según el FEV1 por Piko-6 y EF, y en la tabla 5 las frecuencias de los pacientes en los que hubo concordancia entre ambos procedimientos respecto al diagnóstico de EPOC y la gravedad de la obstrucción. En el 87% hubo concordancia en la categorización según la clasificación GOLD, en el 12,3% hubo concordancia solo en el diagnóstico (los pacientes fueron clasificados correctamente como enfermos o EPOC-FEV1/FEV6<07, pero no en el mismo nivel de gravedad según el FEV1 por el que los clasifica la EF), y en un solo caso (0,6%) no hubo ninguna concordancia entre ambas (el paciente fue clasificado como enfermo sin serlo, considerando siempre la EF como patrón de referencia).
Clasificación de los pacientes según GOLD, en función de los resultados de FEV1 y FVC obtenidos mediante EF y con el dispositivo portátil Piko-6
| GOLD por espirometría | GOLD por Piko-6 | |||
|---|---|---|---|---|
| Frecuencia | % | Frecuencia | % | |
| Grado 0 | 73 | 47,1 | 73 | 47,1 |
| Grado I | 14 | 9 | 12 | 7,7 |
| Grado II | 37 | 23,9 | 34 | 21,9 |
| Grado III | 8 | 14,4 | 25 | 16,1 |
| Grado IV | 1 | 5,2 | 11 | 7,1 |
| Total | 155 | 100% | 155 | 100% |
Concordancia tras el diagnóstico según la clasificación GOLD entre las determinaciones obtenidas por EF y las obtenidas mediante determinación por el dispositivo Piko-6
| Frecuencia | Porcentaje | Porcentaje acumulado | |
|---|---|---|---|
| Concordancia diagnóstica | 19 | 12,3 | 12,3 |
| Concordancia diagnóstica y del grado de severidad | 135 | 87,1 | 99,4 |
| No concordancia | 1 | 0,6 | 100 |
| Total | 155 | 100 |
Se valoró la dificultad subjetiva de ambas pruebas en una escala de 0-10. La dificultad media para la EF fue de 5,68 (DE 2,17), y para el Piko-6 de 3,30 (DE 1,83; p<0,0001). El 73,9% de los pacientes tenía dificultad≤5 con el Piko-6, frente al 45,8% con EF.
DiscusiónEn España el número de personas con EPOC sin diagnosticar es aproximadamente de un millón y medio23. Además, muchos pacientes en cuya historia clínica figura el diagnóstico de EPOC nunca han realizado una EF. Únicamente el 36% de los médicos de AP realiza espirometrías a pacientes con asma y EPOC24, lo que puede provocar errores diagnósticos, incrementar el riesgo de los pacientes y elevar el gasto asistencial25.
El infradiagnóstico se debe al desconocimiento por parte de la población26 y al escaso uso de la espirometría en AP. Diferentes sociedades científicas han editado recomendaciones con estándares mínimos de calidad27. La conferencia de consenso sobre EPOC, que promovió SEPAR, recomendó realizar una EF en AP a fumadores>40 años con síntomas respiratorios. Sin embargo, la EF sigue infrautilizada y, en muchos casos, es de baja calidad28. Solo el 59,2% de los centros de salud realizan EF, el 31% no ha recibido formación y el 63,1% no conoce la frecuencia de calibración de los espirómetros10, a pesar del consenso que es en AP, donde es más rentable implementar el diagnóstico y tratamiento precoz de la EPOC captando población de riesgo29.
Las microespirometrías con capacidad para medir el cociente FEV1/FEV6 (asumiendo que el FEV6 puede sustituir frecuentemente la FVC) pueden ser una alternativa, dado que es más fácil obtener el FEV6 que la FVC, y por ello reducir la variabilidad de la técnica, dado que la variabilidad en las EF viene determinada fundamentalmente por la FVC, por la distinta duración del tiempo de espiración. En la técnica de determinación del FEV6 esta variabilidad se reduce, por cuanto la duración del esfuerzo es siempre la misma (6seg)19,20.
En nuestro estudio se han incluido 155 pacientes. Los valores absolutos y relativos del FEV1 y la FVC determinados con EF fueron significativamente superiores al FEV1 y FEV6 determinados con Piko-6 pero, en cambio, no se observaron diferencias significativas entre los cocientes FEV1/FVC y FEV1/FEV6 determinados por ambos dispositivos (p=0,092), que es lo relevante, dado que es el parámetro que determina la existencia de obstrucción y, por tanto, el que resulta útil en el cribado de la EPOC.
Existe poca bibliografía respecto del uso clínico de estos dispositivos. Rodríguez et al.30 y Dal Negro et al.31 utilizaron el Piko-1 (que no permite la determinación del FEV6). Kauffman et al.22 emplearon el Piko-6, pero con un diseño no enfocado a la validación del dispositivo para diagnosticar EPOC. En el estudio de Frith et al.32, diseñado para valorar la utilidad del Piko-6 para el diagnóstico precoz de EPOC, no realizan test broncodilatador. El trabajo de Represas et al.33, con el COPD-6, presenta más similitudes con nuestra investigación, puesto que la metodología y el diseño son similares. Se han publicado otros estudios con resultados contradictorios: algunos encuentran que, aunque con limitaciones y bajo ciertas premisas, los microespirómetros son útiles para el diagnóstico de la EPOC34–36, y otros concluyen que no existe buena correlación con las determinaciones de la EF37.
Represas observó que los valores absolutos de FEV1 y FVC determinados por EF son significativamente superiores a los obtenidos con el COPD-633. Sin embargo, el valor de FEV1/FVC fue significativamente inferior al del FEV1/FEV6, aunque los valores de referencia utilizados con cada dispositivo fueron diferentes (SEPAR y ECCS respectivamente)3 por lo que, en su análisis de las diferencias porcentuales en función de su valor de referencia, no se objetivaron diferencias significativas, encontrando diferencias medias menores, incluso, de la unidad33.
Obviamente el FEV6 es inferior a la FVC, puesto que esta explica la totalidad del volumen espiratorio. Esto hace que el cociente FEV1/FEV6 medio sea superior al FEV1/FVC, por lo que el punto de corte que determina la obstrucción en algunos estudios no puede ser el de 0,7, tal y como señala el fabricante del COPD-6. Por ello, la concordancia utilizando un mismo punto para los 2 dispositivos fue únicamente moderada. Si se aplican las recomendaciones del fabricante más del 40% de los pacientes con una obstrucción en la EF no se hubieran detectado con el COPD-633, a diferencia de lo que sucede con el Piko-6 en nuestro estudio, que diagnosticó correctamente a la mayoría de los 155 pacientes. El estudio de Fritz32, que compara el Piko-6 con la EF, utiliza un punto de corte del cociente FEV1/FEV6<0,75 y obtiene, a pesar de ello, unos valores de S y E de 81% (68-90) y 71% (63-79), peores que los de nuestro estudio, que son los más comparables con los obtenidos por espirometría.
Ello se ha observado en otros estudios que validaron el FEV6 como sustituto de la FVC, de forma que en varios de ellos el punto de corte del cociente FEV1/FEV6 para la definición de obstrucción fue sensiblemente superior a 0,7. Con el COPD-6, si se sitúa en 0,75-0,76, se obtiene la mejor relación S/E, lo que lo haría útil en la detección de obstrucción. En cambio, en nuestro estudio el Piko-6 ofrece una alta sensibilidad y especificidad con el punto de corte de 0,7, el mismo que se recomienda con la espirometría.
La tabla de contingencia con ambas técnicas no muestra diferencias importantes: el Piko-6 diagnosticaba correctamente a los sujetos con un cociente FEV1/FVC<0,7 con la espirometría. La sensibilidad fue del 99% y la especificidad mayor del 90%, por lo que la microespirometría con el Piko-6 parece ser útil para el diagnóstico de EPOC. Estos valores son superiores a los descritos por Represas33 con el COPD-6, por Rodríguez30 y Dal Negro31 con el Piko-1 y por Kaufman22 y Frith32 con el mismo Piko-6.
Con los test de curtosis se observa la escasa diferencia de los valores respecto a los obtenidos por EF y la acentuada curtosis de las distribuciones, por lo que las determinaciones del Piko-6 guardan buena correlación respecto a la EF. También nuestros resultados son mejores que los obtenidos por los autores que han utilizado otros microespirómetros.
En nuestro estudio todas las correlaciones entre las variables FEV1, FEV6 y FEV1/FEV6 medidas por Piko-6 y FEV1, FVC y FEV1/FVC medidas por espirometría tuvieron buenas rectas de regresión lineal, pero el mejor resultado se obtuvo al comparar FEV1/FEV6 con FEV1/FVC (r=0,947), resultado congruente con los expuestos anteriormente y que confirma la comparabilidad de ambos dispositivos.
Otros autores han encontrado también buenas correlaciones entre las variables medidas por microespirómetros y por EF. Represas et al.33 observaron una excelente correlación entre las determinaciones realizadas con el COPD-6 y el espirómetro para la variable FEV1/FEV6 (r de 0,94, CCI: 0,93; p<0,001), ligeramente inferior al valor obtenido en nuestro estudio. Dal Negro31 encontró una correlación excelente entre las determinaciones del FEV1 con Piko-1 y EF (r=0,98; IC=0,979-0,986).
Establecido que el Piko-6 es útil para detectar obstrucción, buscamos el punto de corte del cociente FEV1/FEV6 que presente mejores valores de S y E para el diagnóstico de obstrucción (cociente FEV1/FVC <0,7). El punto de corte con mejor compromiso S/E ha sido 0,7, con un índice de Youden de 0,97. Ello es relevante, pues es el mismo punto de corte de la EF utilizado para establecer el diagnóstico de EPOC y, por tanto, no requiere adaptaciones ni factores de corrección.
Represas33, al igual que Fritz32 con el Piko-6, concluye que con el COPD-6 para el diagnóstico de EPOC era preciso situar el punto de corte entre 0,75-0,80. Con ello, si bien un resultado superior a estas cifras descartaría obstrucción con aceptable seguridad, un resultado inferior obligaría a realizar una espirometría, porque la especificidad era baja20. En conclusión, nuestro estudio es el único que ha encontrado que el mejor punto de corte del FEV1/FEV6 para el diagnóstico de EPOC con el Piko-6 es 0,7, sin precisarse correcciones o ajustes. Ello puede deberse a que en nuestro estudio todas las pruebas las realizó personal entrenado, y a que la determinación con el Piko6 se realizó tras la espirometría, es decir, bajo efectos del broncodilatador.
Se confeccionó una curva ROC para la variable FEV1/FEV6 con el Piko-6 usando el punto de corte de 0,7. La curva arrojó un resultado de 0,99 que indica una excelente reproductibilidad de las determinaciones con respecto a la espirometría para detectar obstrucción. Así mismo, la concordancia medida por el índice Kappa entre las determinaciones obtenidas por ambos procedimientos fue de 0,97 para la comparación de los cocientes FEV1/FEV6 y FEV1/FVC, y la OR tiende a infinito, lo que indica la validez de la prueba diagnóstica.
Una vez demostrada su utilidad para diagnosticar obstrucción se comprobó si también era de utilidad para valorar la gravedad de la obstrucción y permitía clasificar a los pacientes con el FEV1, según la clasificación de gravedad funcional de GOLD38. La mayoría de los pacientes (135; 87%) fueron clasificados correctamente, un 12,3% lo fueron de forma incorrecta y en un caso se consideró a un paciente como enfermo en ausencia de EPOC. Los pacientes sin alteraciones funcionales fueron clasificados correctamente y, por ello, este dispositivo parece útil para descartar EPOC, pero el Piko-6 sobrevalora la afectación funcional, dado que los valores del FEV1 con el Piko-6 son menores que con EF. Las mayores diferencias entre Piko-6 y EF se dan con los valores más bajos del FEV1 y FEV6, por lo que es posible que pueda encontrarse un punto de corte del FEV1 por encima del cual no fuera preciso realizar una EF en pacientes no exacerbadores poco sintomáticos, que son los que GesEPOC y otros consensos recomiendan que sean diagnosticados y controlados en AP39, pero son necesarios estudios más amplios para poder sostener esta posibilidad. Nuestro grupo ha puesto en marcha un estudio multicéntrico, financiado con una beca SEPAR, con este objetivo.
Finalmente, hemos valorado la dificultad subjetiva de los pacientes para la realización de ambas maniobras (microespirometría con el Piko-6 y EF) y los pacientes encuentran más fácil realizar una microespirometría que una EF, hecho que puede deberse a que se requieren menos maniobras, al menor diámetro de la boquilla o a la menor duración de la espiración. Sin embargo, esta mayor facilidad es muy importante, pues puede facilitar una mejor implementación y uso del Piko-6 en AP que el que ha tenido hasta ahora la espirometría.
Una posible limitación del estudio es el hecho de que tanto la EF como las determinaciones con el Piko-6 se realizaron en el ámbito de la neumología para evitar el sesgo del broncodilatador (las determinaciones con Piko-6 se realizaron siempre tras la EF con prueba broncodilatadora). Actualmente nuestro grupo de trabajo está vehiculando un estudio en el que se compara la calidad de las determinaciones con los microespirómetros y la espirometría entre los niveles asistenciales de AP y neumología, y sus resultados serán publicados próximamente.
En conclusión, el dispositivo Piko-6 puede ser de utilidad para el cribado de la EPOC en AP, pues muestra una buena correlación con la EF, especialmente el cociente FEV1/FEV6, tal y como señalan también Jing et al. en su metaanálisis publicado en Chest19. Esto, junto a su bajo coste, facilidad de manejo, escaso tiempo de realización y buena aceptación por los pacientes, puede contribuir a reducir el infradiagnóstico de la EPOC y a reducir las derivaciones al segundo nivel para la realización de una EF. Aunque el rol exacto de los microespirómetros en el proceso diagnóstico de la EPOC está aún por determinar, podrían resultar útiles en pacientes con obstrucción moderada/severa que son, como ya hemos señalado, los que deberían ser diagnosticados en AP40.
AutoríaHidalgo Sierra V: diseño del estudio, reclutamiento y redacción del manuscrito.
Hernández Mezquita MA: diseño, coordinación, supervisión de resultados y redacción del manuscrito.
Palomo Cobos L: revisión metodológica y estudio estadístico.
García Sánchez M: reclutamiento de pacientes.
Diego Castellanos R: reclutamiento de pacientes y realización de espirometrías.
Jodra Sánchez S: realización de espirometrías y revisión del manuscrito.
Cordovilla Pérez R: búsqueda bibliográfica y revisión del manuscrito.
Barrueco Ferrero M: diseño del estudio, coordinación del equipo, supervisión de resultados y redacción del manuscrito.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.