Los donantes de pulmón que han presentado un traumatismo importante corren el riesgo de desarrollar un síndrome de embolia grasa (SEG). El SEG adquirido a través del donante se manifiesta en el receptor después del trasplante de órgano y es una posible causa de insuficiencia aguda del injerto1. La embolia pulmonar tras un trasplante que se diagnostica por biopsia de pulmón se ha descrito en 3 publicaciones2–4. A continuación informamos de un caso de SEG mortal, adquirido a través del donante, que causó insuficiencia orgánica primaria tras un trasplante unilateral de pulmón.
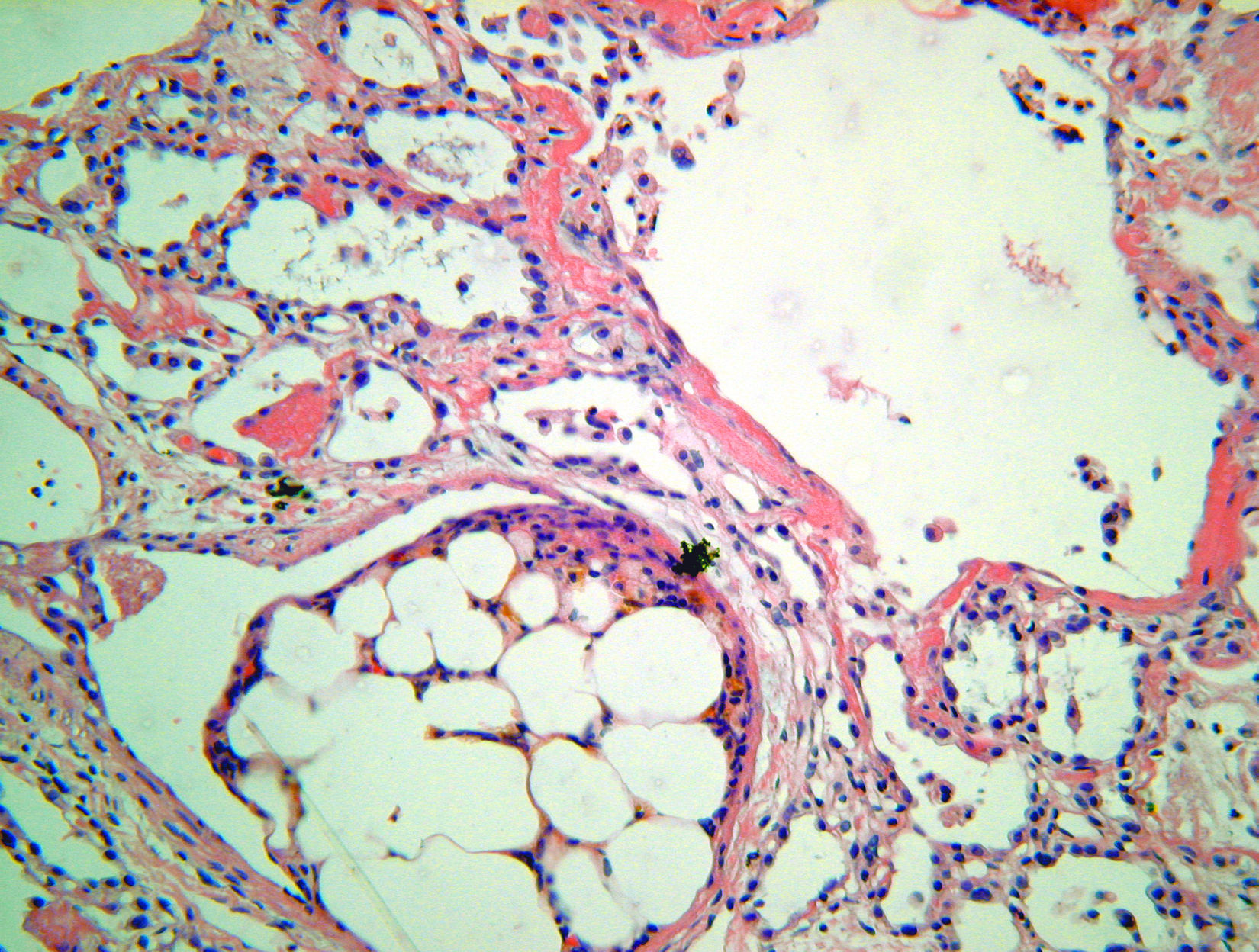
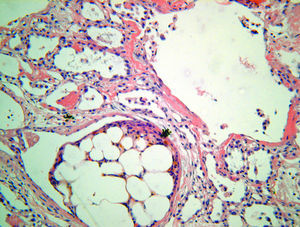
Se realizó un trasplante pulmonar unilateral a un varón de 41 años de edad, con antecedentes de silicosis y tratado con metilprednisolona oral y oxigenoterapia domiciliaria. El donante era un varón de 17 años, fumador, que sufrió muerte cerebral tras traumatismo craneoencefálico en un accidente de tráfico; también presentaba fractura del fémur derecho. Tras el trasplante la radiografía de tórax mostraba marcas alveolares confluentes generalizadas, debidas a edema por reperfusión (razón entre la presión arterial de oxígeno y la fracción inspiratoria de oxígeno: 165). Se extubó al paciente el cuarto día del postoperatorio, pero 12h más tarde su estado se deterioró, pues presentó inestabilidad hemodinámica progresiva, insuficiencia respiratoria que requirió ventilación mecánica, descenso del hematócrito e insuficiencia renal que se trató con dopamina y hemodiafiltración venovenosa continua. En la radiografía se observó un empeoramiento del injerto (patrón alveolar confluente). Se practicó una biopsia pulmonar transbronquial. La microscopia reveló émbolos de médula ósea, trombosis extensa en capilares y vasos de mayor calibre, junto con daño alveolar difuso en las fases exudativa y de organización. El paciente desarrolló un síndrome agudo de dificultad respiratoria e insuficiencia multiorgánica que condujo a la muerte a los 15 días del trasplante pulmonar. La autopsia mostró que las suturas vasculares y bronquiales no habían fallado Se observó daño alveolar difuso grave en las fases exudativa y de organización, así como indicios de embolia grasa en los capilares pulmonares y glomerulares (fig. 1).
El SEG generalmente ocurre como complicación de un traumatismo grave. La presencia de émbolos grasos en el parénquima pulmonar y en la circulación periférica no implica la aparición del SEG agudo. Este síndrome se manifiesta como insuficiencia respiratoria progresiva, trombocitopenia, erupción petequial y deterioro del grado de conciencia5. Los émbolos grasos pueden detectarse en más del 90% de los pacientes con fracturas de hueso largo; sin embargo, el SEG es menos común, con una incidencia del 0,5 al 2,2% en los pacientes con fracturas aisladas de hueso largo y entre el 5% y el 10% en los pacientes con fracturas múltiples de hueso largo y fractura pélvica concomitante6. Recientemente Oto et al1 han observado que la embolia pulmonar insospechada era relativamente común, con una incidencia del 38% en una serie de 74 donantes de pulmón. También informaron de que estaba relacionada de forma significativa con la insuficiencia primaria del injerto pulmonar y la supervivencia al año. Sin embargo, la embolia grasa estaba presente en sólo el 9% de los 74 donantes del pulmón. En su estudio, la muerte debida a un traumatismo craneoencefálico asociado con fractura de hueso largo y ser fumador de más de 20 paquetes/año eran factores relacionados con el donante que suponían un riesgo significativo de embolia pulmonar.
En nuestro caso, tanto la fractura de hueso largo como los antecedentes de tabaquismo estaban presentes en el donante. La hipoxia, que ocurre hasta en el 96% de los pacientes con SEG6, no se presenta en donantes del pulmón, dado que una razón presión arterial de oxígeno/fracción inspiratoria de oxígeno inferior a 300 es una contraindicación para el trasplante pulmonar. Durante la recuperación inicial de un trasplante pulmonar, la hipoxia en el receptor puede estar relacionada con isquemia de reperfusión, infección, rechazo celular agudo o disfunción miocárdica. Todas estas alteraciones, así como la trombosis en la vena pulmonar o la rotura de suturas, se descartaron en nuestro paciente mediante ecocardiografía transesofágica, biopsia y microbiología. La lesión por reperfusión isquémica, que se manifiesta como daño alveolar difuso en las fases de organización y exudativa, estuvo presente desde los primeros días del postoperatorio y persistió hasta la tercera semana; sin embargo, en la necropsia no se consideró que esto fuera la causa de la disfunción del injerto. La sedación y la analgesia, necesarias para la adaptación a la ventilación mecánica, impidieron la adecuada evaluación neurológica del paciente. EL SEG agudo no existía antes del trasplante, dado que no se evidenció embolia grasa en la histopatología del pulmón rechazado del donante ni en el pulmón explantado del receptor.
El tratamiento del SEG incluyó soporte hemodinámico y respiratorio. Los corticoides, que el receptor recibió desde el primer día del postoperatorio como parte del régimen de inmunodepresión, se utilizan en el tratamiento del SEG, pero no han demostrado ejercer un claro efecto beneficioso5. De hecho, parecen tener un efecto paradójico, ya que se considera que desempeñan un papel en la génesis del SEG en pacientes en tratamiento crónico con corticoides5.
Agradecemos a Marta Pulido la revisión del manuscrito y su asistencia editorial.