El asma bronquial es una enfermedad compleja en la que los factores genéticos, los factores ambientales y la lesión oxidativa son responsables del inicio y la modulación de su progresión. Si fracasan los mecanismos antioxidantes, las especies reactivas del oxígeno afectan a las biomoléculas, lo que se sigue de la progresión de la enfermedad. La catalasa es uno de los antioxidantes enzimáticos endógenos más importantes. En el presente estudio examinamos la hipótesis de que un aumento de la lesión oxidativa y el polimorfismo en el gen CAT (región promotora -262C/T) se asocian a asma bronquial infantil.
Pacientes y métodosEn niños sanos (249) y niños asmáticos (248) se efectuó una genotipificación de los polimorfismos en el gen CAT usando la reacción en cadena de la polimerasa-polimorfismo de longitud de fragmentos de restricción. Mediante espectrofotometría, en los niños se analizaron los marcadores de lesión oxidativa: el contenido de grupos sulfhidrilo y de sustancias reactivas al ácido tiobarbitúrico.
ResultadosEl genotipo TT de la catalasa fue más frecuente entre pacientes asmáticos (22,6%) que en niños sanos (4,8%) (odds ratio=5,63; intervalo de confianza del 95%=2,93–10,81; p<0,001). El contenido de grupos sulfhidrilo disminuyó significativamente y, al contrario, el contenido de sustancias reactivas a ácido tiobarbitúrico aumentó significativamente en el asma bronquial y el genotipo TT de catalasa comparado con los otros genotipos catalasa de este gen.
ConclusionesLos resultados del presente estudio sugieren que el polimorfismo del gen de la catalasa podría participar en la aparición de asma bronquial y en el aumento de la lesión oxidativa en niños asmáticos. La variación genética de los antioxidantes enzimáticos podría modular el riesgo de la enfermedad.
Bronchial asthma is a complex disease in which genetic factors, environmental factors and oxidative damage are responsible for the initiation and modulation of disease progression. If antioxidant mechanisms fail, reactive oxygen species damage the biomolecules followed by progression of the disease. Catalase is one of the most important endogenous enzymatic antioxidants. In the present study, we examined the hypothesis that increased oxidative damage and polymorphism in the CAT gene (-262 promoter region, C/T) are associated with childhood bronchial asthma.
Patients and methodsGenotyping of the polymorphisms in the CAT gene in healthy (249) and asthmatic children (248) was performed using polymerase chain reaction–restriction fragment length polymorphism. Markers of oxidative damage: content of sulfhydryl groups and thiobarbituric acid-reactive substances were determined by spectrophotometry in children.
ResultsThe TT genotype of catalase was more frequent among the asthmatic patients (22.6%) than in healthy children (4.8%) (odds ratio=5.63; 95% confidence interval=2.93–10.81, P<.001). The amount of sulfhydryl groups decreased significantly and conversely, the content of thiobarbituric acid-reactive substances increased significantly in bronchial asthma and in catalase TT genotype compared to other catalase genotypes of this gene.
ConclusionsThese results suggest that catalase polymorphism might participate in development of bronchial asthma and in enhanced oxidative damage in asthmatic children. Genetic variation of enzymatic antioxidants may modulate disease risk.
El asma bronquial es una enfermedad inflamatoria crónica, compleja y heterogénea de las vías respiratorias, que incluye la activación de muchas poblaciones de células inflamatorias y estructurales, lo que libera numerosos mediadores inflamatorios, que dan lugar a los cambios fisiopatológicos característicos de la enfermedad1. Los factores ambientales y genéticos desempeñan un papel en su aparición; no obstante, no se han determinado por completo los mecanismos exactos de sus acciones. Los pulmones están expuestos continuamente a los oxidantes generados de forma endógena a partir de las mitocondrias, fagocitos y otras células, o de forma exógena a partir de los contaminantes atmosféricos y del humo de los cigarrillos. Contienen la mayor área de superficie endotelial de todos los órganos, lo que hace que el tejido pulmonar sea la principal diana de los oxidantes y xenobióticos circulantes. Los pacientes asmáticos producen una diversidad de mediadores, incluidas las especies reactivas del oxígeno2. El aumento de la lesión oxidativa puede contribuir tanto al origen como al desarrollo de las enfermedades respiratorias, incluida el asma bronquial. La lesión pulmonar debida a las especies reactivas del oxígeno se relaciona con la oxidación del ácido desoxirribonucleico (ADN), proteínas y lípidos. Estas biomoléculas oxidadas pueden inducir diversas respuestas y una cascada de acontecimientos, tales como hiperreactividad de las vías respiratorias, aumento de la generación de quimioatrayentes, liberación de taquicininas y neurocininas, y aumento de la liberación de mediadores, que, en último término, hacen más profunda la lesión oxidativa1. Los pulmones pueden usar antioxidantes no enzimáticos, como las vitaminas, ácido úrico, glutatión, grupos sulfhidrilo (proteínas, péptidos y aminoácidos) y diversos antioxidantes enzimáticos, como la superoxido dismutasa, catalasa (CAT) y glutatión peroxidada como defensa frente a la lesión oxidativa y las especies reactivas del oxígeno.
La CAT (EC 1.11.1.6) es una enzima antioxidante común responsable del control de las concentraciones de peróxido de hidrógeno en las células. Es ubicua en la mayoría de las células aerobias también detectadas en los pulmones (macrófagos, fibroblastos y neumocitos)3. La CAT como enzima antioxidante intracelular cataliza la descomposición de 2 moléculas de peróxido de hidrógeno en una molécula de oxígeno y 2 de agua y su actividad está determinada genéticamente. El gen de la CAT se localiza en el cromosoma 11p13, tiene una longitud de 34kb, contiene 13 exones y 12 intrones y codifica una proteína de 526 aminoácidos4,5. Se han descrito y caracterizado diferentes polimorfismos de esta enzima tanto en la región codificadora6,7 como en la no codificadora7–11. Un polimorfismo habitual en la región promotora del gen de la CAT consiste en la sustitución de T por C en posición T -262 en la región 5’9, que se considera que da lugar a una disminución de la actividad enzimática. El genotipo CAT TT podría ser responsable de una disminución de la defensa antioxidante y de un aumento posterior de la lesión oxidativa.
Puesto que la lesión oxidativa desempeña un papel en la patogenia del asma, y la CAT es decisiva para proteger las células frente a las especies reactivas del oxígeno, formulamos la hipótesis de que los polimorfismos en el gen de la CAT que influyen en su actividad enzimática contribuyen sustancialmente a la aparición de la enfermedad. En el presente estudio tratamos de evaluar el polimorfismo -262C/T de la CAT en niños asmáticos. Tratamos de determinar los marcadores de lesión oxidativa y analizar una posible asociación entre el genotipo de la CAT y la lesión oxidativa de las proteínas y lípidos en niños asmáticos y sanos.
Pacientes y métodosIndividuos del estudioLa población del estudio consistió en 457 niños participantes. Utilizando las categorías de cuestionarios de referencia se registraron los antecedentes de asma de los niños: edad, sexo, exposición al humo de los cigarrillos y antecedentes familiares de asma, sibilancias y alergia. Los niños o sus padres completaron el Asthma control test®. Acto seguido, se excluyó del estudio a los fumadores activos y a los niños expuestos a tabaquismo pasivo. Los 248 pacientes asmáticos (un 58% niños y un 42% niñas) se reclutaron en el Servicio de Pediatría del Hospital Universitario de Martin (República Eslovaca). Durante las revisiones de salud sistemáticas, los médicos generales reclutaron a otros 249 niños sanos, de sexo y edad comparables (un 54% niños y un 46% niñas). Los niños no experimentaban síntomas clínicos de enfermedades alérgicas y carecían de antecedentes de una enfermedad grave. Los niños asmáticos que participaron en el estudio se caracterizaron por obstrucción recurrente de las vías respiratorias, manifestada por sibilancias y disnea, con su alivio espontáneo mediante tratamiento broncodilatador (según lo definido en la Iniciativa Global para el Asma).
Todos los niños se sometieron al análisis de óxido nítrico espirado fraccional (FENO) y monóxido de carbono espirado (eCO). El FENO se determinó en línea de acuerdo con las recomendaciones de los estándares de la American Thoracic Society/European Respiratory Society (ATS/ERS)12 con un analizador portátil de óxido nítrico (NIOX-MINO®, Aerocrine, Suecia). El eCO se analizó con un Micro 4 Smokerlyzer® (Bedfont, Inglaterra). También llevamos a cabo una espirometría básica (KoKo DigiDoser-Spirometer, nSpire Health, Louisville, Estados Unidos), de acuerdo con las recomendaciones de la ATS/ERS13. Los valores de FENO y eCO se estimaron antes del examen espirométrico.
Aprobó el estudio el Comité de Investigación de la Facultad Jessenius de Medicina de Martin y se obtuvo el consentimiento informado firmado por los padres de todos los niños examinados.
Aislamiento del ácido desoxirribonucleicoSe obtuvieron muestras de sangre venosa en tubos revestidos de ácido etilendiaminotetraacético. Para la preparación del ADN genómico se utilizó sangre de acuerdo con el procedimiento comercial (equipo de purificación Wizard Genomic DNA, Promega, Madison, EE. UU.).
Determinación de los genotipos de catalasaTodas las muestras de ADN de los pacientes asmáticos y niños sanos se genotipificaron mediante reacción en cadena de la polimerasa, seguido de análisis del polimorfismo de longitud de fragmentos de restricción (restriction fragment length polymorphism [RFLP]). El polimorfismo -262C/T de CAT (rs 1001179) se determinó utilizando el cebador directo 5′-AGAGCCTCGCCCCGCCGGACCG-3′, y el cebador inverso de CAT 5′-TAAGAGCAGAGAAAGCATAGCT-3′. Los productos de reacción en cadena de la polimerasa de 185bp se digirieron usando la enzima restrictiva SmaI. Los productos se visualizaron mediante electroforesis en gel de agarosa al 2%. El tipo salvaje del genotipo CC se presentó como fragmentos de 155 y 30bp y el genotipo CT se presentó como fragmentos de 185, 155 y 30bp. Los genotipos TT no fueron digeridos por SmaI (185bp).
Grupos sulfhidrilo de las proteínas plasmáticasEl plasma para la determinación de los marcadores proteicos y lipídicos de lesión oxidativa se obtuvo a partir de sangre preparada mediante centrifugación durante 20min, a 2.000×g a 4°C.
La concentración total de grupos sulfhidrilo reducidos (-SH, proteínas, oligopéptidos, glutatión y aminoácidos) se determinó mediante espectrofotometría14. Se añadieron 2ml de reactivo de Ellman (0,250mol/l de TRIS-HCl; pH 8,2, 10mmol/l de 5,5′-ditiobis-2-ácido nitrobenzoico) a 100μl de la muestra y se incubó durante 15min a temperatura ambiente. La absorbancia se leyó a 412nm y el contenido de grupos-SH se calculó usando el coeficiente de absorción molar de 13.600M−1cm−1 tras sustracción de la absorbancia del blanco de la absorbancia de la muestra. Para determinar el valor normal, se usó una población de 249 individuos sanos.
Análisis de los peróxidos de lípidosLas modificaciones de la estructura de los lípidos plasmáticos se analizaron mediante determinación del nivel de sustancias reactivas a ácido tiobarbitúrico (thiobarbituric acid-reactive substances [TBARS])15. Se incubó una muestra con etanol, un 14% de ácido tricloroacético y un 0,6% de ácido tiobarbitúrico a 80°C durante 30min. Acto seguido, la muestra se incubó durante 5min a 0°C y se centrifugó durante 10min, a 2.000×g a 25°C. La concentración de TBARS se determinó a partir de la absorbancia a 532nm. La población de 249 individuos sanos se utilizó para determinar el valor normal.
Análisis estadísticoLos resultados de ambos grupos de individuos se compararon con un análisis ANOVA, la prueba de la t de Student y la prueba de chi cuadrado (χ2). La asociación del polimorfismo del gen CAT -262C/T con el asma bronquial se determinó mediante la prueba de χ2 de Pearson o la prueba exacta de Fisher. La distribución de los genotipos se examinó para la desviación del equilibrio de Hardy-Weinberg. Para analizar las frecuencias de los genotipos CAT en pacientes con asma bronquial, comparado con niños sanos, se usaron las odds ratios (OR) e intervalos de confianza (IC del 95%). Para calcular la relación entre los marcadores de estrés oxidativo y los marcadores inflamométricos en el aire espirado se usó una correlación de Pearson (con una correlación de Spearman cuando estuvo indicado). Todos los valores se presentan como medias±EEM. Se consideró estadísticamente significativo un valor de p<0,05.
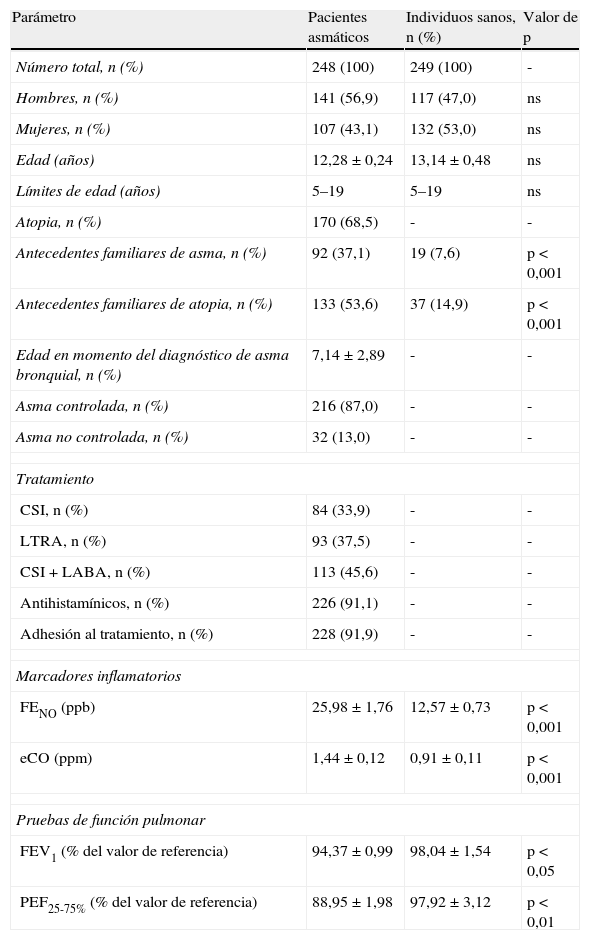
ResultadosPolimorfismo de la catalasa en niños con asma bronquial e individuos sanosEn la tabla 1 se proporcionan la demografía y otras características de la población del estudio. En 92 niños asmáticos (37,1%) y en 19 niños sanos (7,6%) se detectaron antecedentes familiares positivos de asma. De acuerdo con la positividad de la prueba de punción cutánea con un panel estándar de alérgenos inhalados, 170 (68,5%) pacientes eran atópicos y 78 (31,5%) presentaban una variante no atópica de asma.
Características generales de la población de estudio
| Parámetro | Pacientes asmáticos | Individuos sanos, n (%) | Valor de p |
| Número total, n (%) | 248 (100) | 249 (100) | - |
| Hombres, n (%) | 141 (56,9) | 117 (47,0) | ns |
| Mujeres, n (%) | 107 (43,1) | 132 (53,0) | ns |
| Edad (años) | 12,28±0,24 | 13,14±0,48 | ns |
| Límites de edad (años) | 5–19 | 5–19 | ns |
| Atopia, n (%) | 170 (68,5) | - | - |
| Antecedentes familiares de asma, n (%) | 92 (37,1) | 19 (7,6) | p<0,001 |
| Antecedentes familiares de atopia, n (%) | 133 (53,6) | 37 (14,9) | p<0,001 |
| Edad en momento del diagnóstico de asma bronquial, n (%) | 7,14±2,89 | - | - |
| Asma controlada, n (%) | 216 (87,0) | - | - |
| Asma no controlada, n (%) | 32 (13,0) | - | - |
| Tratamiento | |||
| CSI, n (%) | 84 (33,9) | - | - |
| LTRA, n (%) | 93 (37,5) | - | - |
| CSI+LABA, n (%) | 113 (45,6) | - | - |
| Antihistamínicos, n (%) | 226 (91,1) | - | - |
| Adhesión al tratamiento, n (%) | 228 (91,9) | - | - |
| Marcadores inflamatorios | |||
| FENO (ppb) | 25,98±1,76 | 12,57±0,73 | p<0,001 |
| eCO (ppm) | 1,44±0,12 | 0,91±0,11 | p<0,001 |
| Pruebas de función pulmonar | |||
| FEV1 (% del valor de referencia) | 94,37±0,99 | 98,04±1,54 | p<0,05 |
| PEF25-75% (% del valor de referencia) | 88,95±1,98 | 97,92±3,12 | p<0,01 |
CSI: corticoesteroides inhalados; eCO: monóxido de carbono espirado; FENO: óxido nítrico espirado fraccional; FEV1: volumen espiratorio forzado en el primer segundo; LABA: agonistas beta2 de acción prolongada; LTRA: antagonista del receptor de los leucotrienos; n, número de individuos; ns: no significativo; PEF: flujo espiratorio máximo; ppb: partes por billón; ppm: partes por millón.
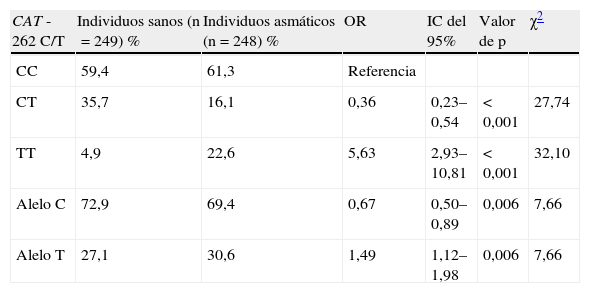
La distribución del genotipo y las frecuencias de alelos en asmáticos y niños sanos se muestran en la tabla 2. Se identificó una diferencia estadísticamente significativa en la distribución de los polimorfismos del genotipo del gen CAT entre niños asmáticos y niños sanos. En pacientes con asma bronquial hubo una mayor prevalencia del genotipo CAT TT (22,6%) que en individuos de control (4,8%) (tabla 2). Hubo un aumento del riesgo de 5,63 veces de asma en el genotipo CAT TT (OR=5,63; IC del 95%=2,93-10,81; p<0,001). El coeficiente de endogamia (consanguinidad) en los individuos de control es -0,019 y de 0,610 en los casos. El alelo C fue el más habitual en asmáticos (72,9%) y en individuos sanos (69,4%). El alelo T representó un factor de riesgo potencial (OR=1,49; IC del 95%=1,12-1,19; p<0,01). La combinación de los genotipos CC+CT demostró ser un factor positivo (OR=0,178; IC del 95%=0,65-1,33, p<0,001, χ2=32,10). La combinación de la variante heterocigota con la variante homocigota no mostró ninguna asociación significativa.
Distribución de genotipos y alelos del gen de la catalasa (CAT) y riesgo de aparición de asma bronquial
| CAT -262C/T | Individuos sanos (n=249) % | Individuos asmáticos (n=248) % | OR | IC del 95% | Valor de p | χ2 |
| CC | 59,4 | 61,3 | Referencia | |||
| CT | 35,7 | 16,1 | 0,36 | 0,23–0,54 | <0,001 | 27,74 |
| TT | 4,9 | 22,6 | 5,63 | 2,93–10,81 | <0,001 | 32,10 |
| Alelo C | 72,9 | 69,4 | 0,67 | 0,50–0,89 | 0,006 | 7,66 |
| Alelo T | 27,1 | 30,6 | 1,49 | 1,12–1,98 | 0,006 | 7,66 |
IC: intervalo de confianza; n: número de individuos; OR: odds ratio.
Los resultados de ambos grupos de individuos se compararon con un análisis ANOVA, la prueba de la t de Student y la prueba chi cuadrado (χ2). La asociación del polimorfismo del gen CAT -262C/T con asma bronquial se determinó mediante la prueba de la χ2 de Pearson o la prueba exacta de Fisher.
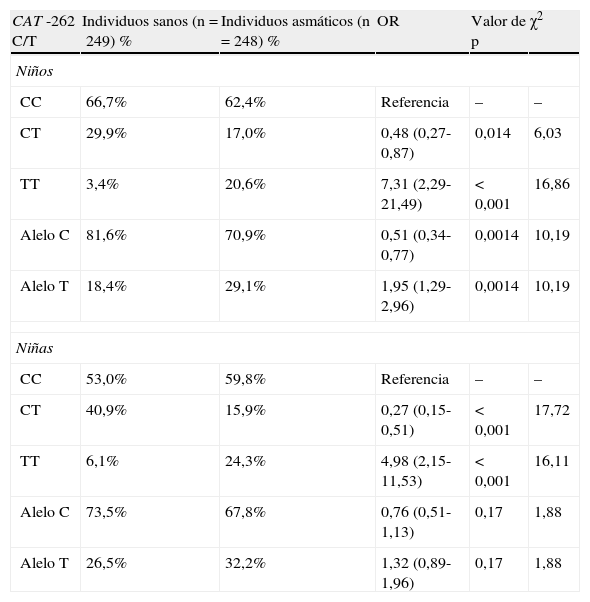
Separamos a la población de nuestro estudio de acuerdo con el sexo (tabla 3). No se encontró una diferencia significativa en la distribución de los genotipos y alelos de CAT entre niños y niñas asmáticos. Se halló una diferencia estadísticamente significativa de la distribución de genotipos y alelos de CAT cuando comparamos a niños o niñas asmáticos con niños o niñas sanos. La variante homocigota se asoció a asma bronquial en ambos sexos (OR=7,31; IC del 95%=2,29-21,49; respectivamente, OR=4,98; IC del 95%=2,15-11,53; p<0,001).
Distribución de genotipos y alelos del gen de la catalasa (CAT) y riesgo de aparición de asma bronquial en niños y niñas
| CAT -262C/T | Individuos sanos (n=249) % | Individuos asmáticos (n=248) % | OR | Valor de p | χ2 |
| Niños | |||||
| CC | 66,7% | 62,4% | Referencia | – | – |
| CT | 29,9% | 17,0% | 0,48 (0,27-0,87) | 0,014 | 6,03 |
| TT | 3,4% | 20,6% | 7,31 (2,29-21,49) | <0,001 | 16,86 |
| Alelo C | 81,6% | 70,9% | 0,51 (0,34-0,77) | 0,0014 | 10,19 |
| Alelo T | 18,4% | 29,1% | 1,95 (1,29-2,96) | 0,0014 | 10,19 |
| Niñas | |||||
| CC | 53,0% | 59,8% | Referencia | – | – |
| CT | 40,9% | 15,9% | 0,27 (0,15-0,51) | <0,001 | 17,72 |
| TT | 6,1% | 24,3% | 4,98 (2,15-11,53) | <0,001 | 16,11 |
| Alelo C | 73,5% | 67,8% | 0,76 (0,51-1,13) | 0,17 | 1,88 |
| Alelo T | 26,5% | 32,2% | 1,32 (0,89-1,96) | 0,17 | 1,88 |
IC, intervalo de confianza; n: número de individuos; OR: odds ratio.
Los resultados de ambos grupos de individuos se compararon con un análisis ANOVA, la prueba de la t de Student y la prueba chi cuadrado (χ2). La asociación del polimorfismo del gen CAT -262C/T con asma bronquial se determinó mediante la prueba de χ2 de Pearson o la prueba exacta de Fisher.
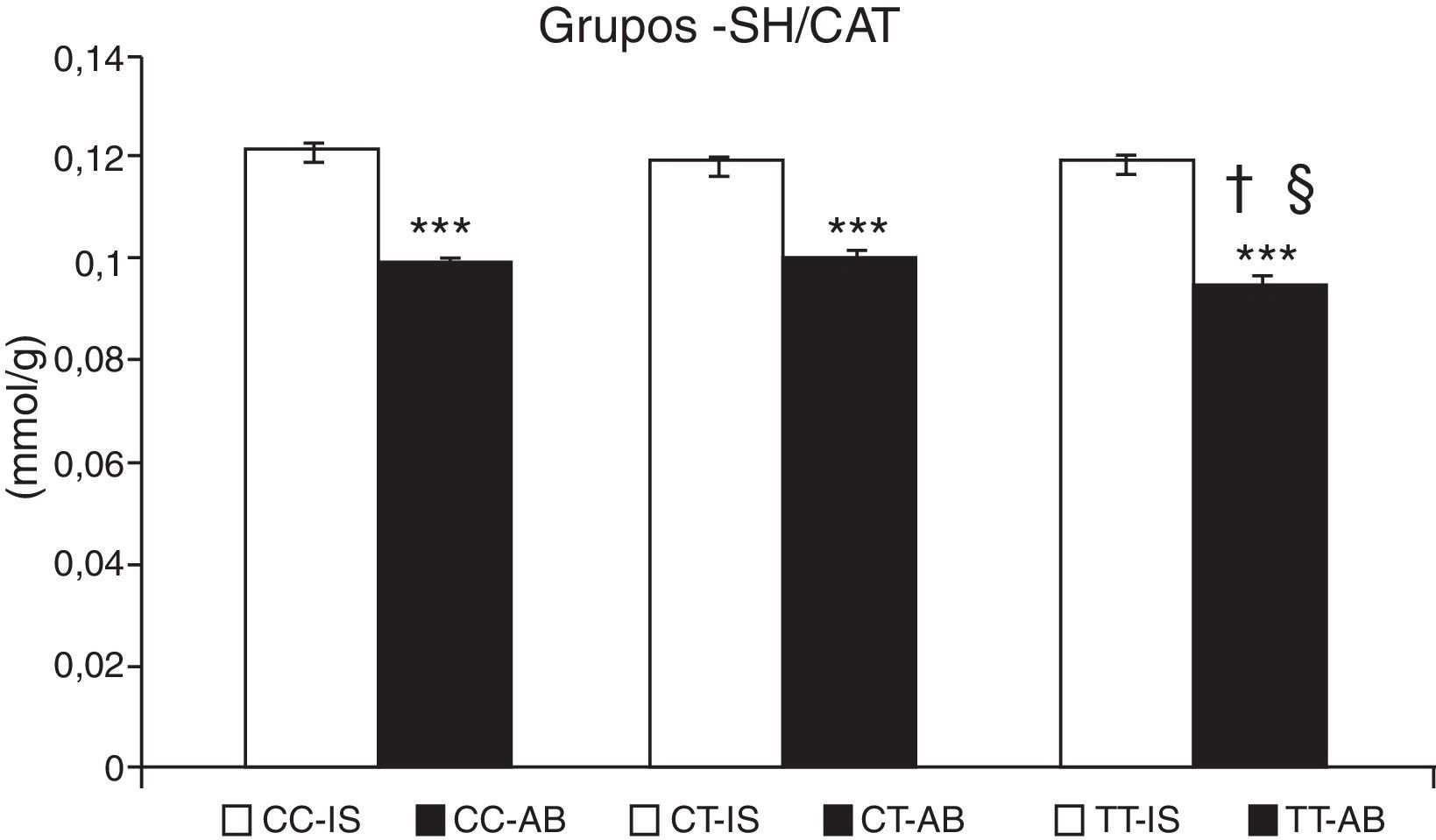
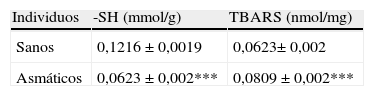
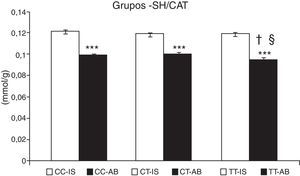
En niños con asma bronquial se detectó una mayor lesión oxidativa de proteínas y lípidos en comparación con niños sanos (tabla 4). La concentración de grupos-SH disminuyó del orden de 18,8±0,7% (p<0,001) en niños asmáticos, comparado con individuos de control. No hubo una diferencia significativa del contenido de grupos SH entre niños con exacerbaciones del asma y con asma controlada. En individuos de control no se observaron diferencias en la concentración de grupos-SH de acuerdo con el genotipo de CAT (fig. 1). En los pacientes con el genotipo TT de CAT fue evidente una menor concentración de grupos-SH (p<0,05), comparado con aquellos con el genotipo CC y CT (p<0,05) (fig. 1).
Marcadores de la lesión oxidativa de las proteínas y lípidos
| Individuos | -SH (mmol/g) | TBARS (nmol/mg) |
| Sanos | 0,1216±0,0019 | 0,0623± 0,002 |
| Asmáticos | 0,0623±0,002*** | 0,0809±0,002*** |
-SH: grupo sulfhidrilo; TBARS: sustancias reactivas a ácido tiobarbitúrico.
Los resultados de ambos grupos de individuos se compararon con un análisis ANOVA, y prueba de la t de Student. Los resultados se expresan como medias± error estándar de la media.
***p<0,001 comparado con individuos sanos.
Concentración de grupos sulfhidrilo (-SH). Comparación de la concentración de -SH en individuos sanos (IS) y en niños con asma bronquial (AB) de acuerdo con el genotipo de catalasa. ***p<0,001, comparación de los genotipos de catalasa, †p<0,05, comparación del genotipo TT frente al genotipo CC de catalasa en pacientes, §p<0,05, comparación del genotipo TT frente al genotipo CT de catalasa en pacientes.
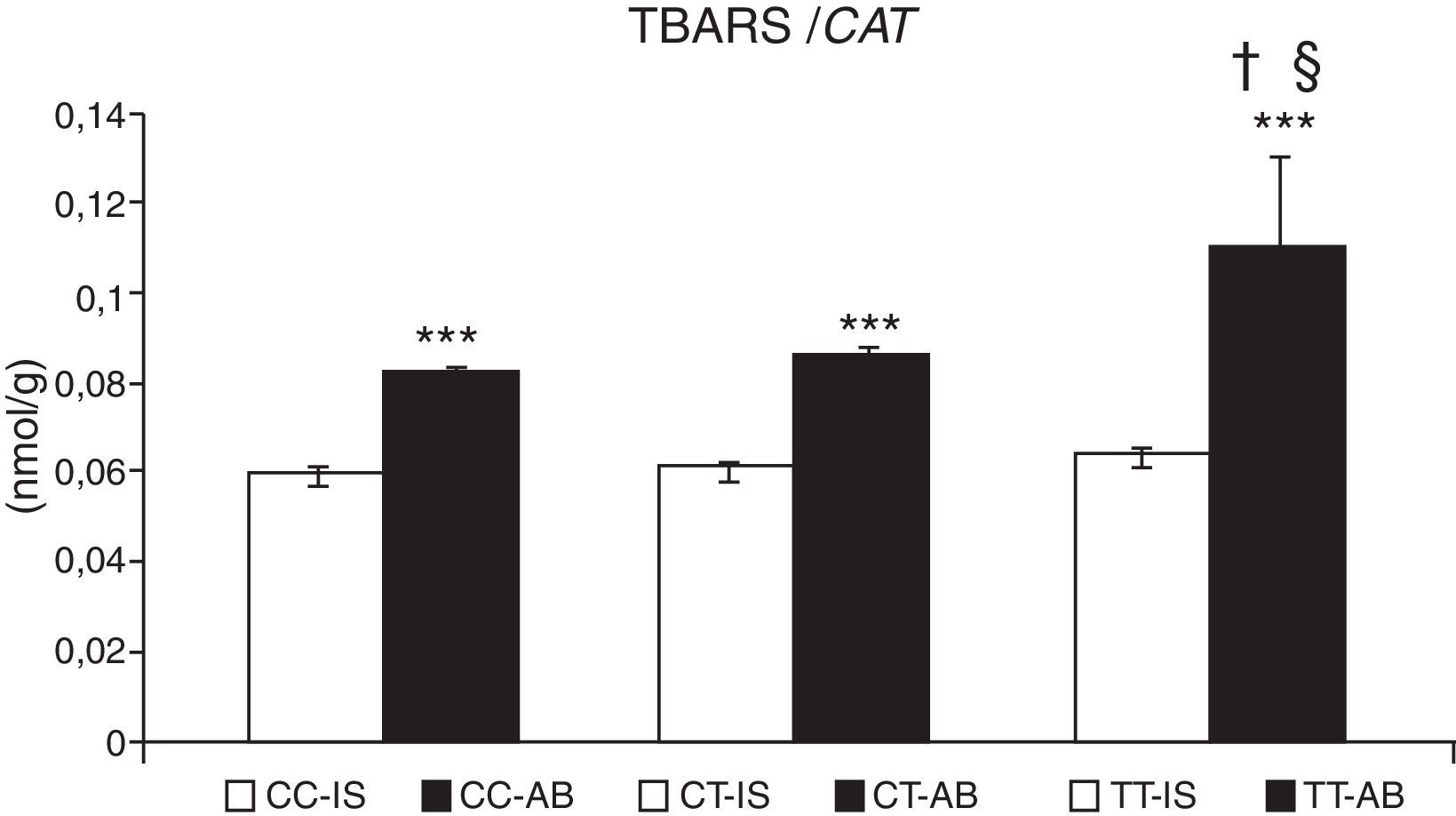
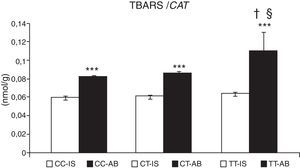
El estrés oxidativo causó la acumulación de TBARS en niños con asma bronquial. En pacientes la concentración de estas sustancias aumentó en un 29,9±3,2% (p<0,001). En pacientes con exacerbación del asma, los marcadores de peroxidación de lípidos aumentaron significativamente en 33,0±3,0%, comparado con pacientes cuya asma era estable (p<0,05). Los valores de TBARS no se modificaron según el genotipo de CAT en individuos sanos (fig. 2). En asmáticos con el genotipo TT de CAT se identificó una mayor concentración de TBARS (p<0,05), comparado con el genotipo CC y también con el genotipo CT (p<0,05) (fig. 2).
Concentración de sustancias reactivas a ácido tiobarbitúrico (TBARS). Comparación de la concentración de TBARS en individuos sanos (IS) y en niños con asma bronquial (AB) de acuerdo con el genotipo de catalasa. ***p<0,001, comparación de los genotipos de catalasa, †p<0,05, comparación del genotipo TT frente al genotipo CC de catalasa en pacientes, §p<0,05, comparación del genotipo TT frente al genotipo CT de catalasa en pacientes.
Encontramos una correlación significativa entre los marcadores de lesión oxidativa y los parámetros inflamométricos en el aire espirado de pacientes asmáticos. Fue evidente una ligera una correlación significativamente positiva entre la concentración de TBARS y los valores de los marcadores en aire espirado (FENO frente a TBARS: r=0,232 [p=0,002]; eCO frente a TBARS: r=0,147 [p=0,044]). Entre la concentración de grupos-SH y los marcadores inflamométricos, se observó una correlación negativa ligera o moderadamente significativa (FENO frente a -SH: r=−0,343 [p<0,001]; eCO frente a -SH: r=−0,232 [p=0,001]). En el grupo de control no se observaron estas correlaciones.
DiscusiónEl asma bronquial es una enfermedad inmunológica compleja, afectada por factores ambientales y genéticos y sus interacciones, y estas probablemente desempeñan un papel clave en su patogenia y pronóstico. El asma pertenece a un grupo de enfermedades en las que desempeñan un importante papel la lesión oxidativa y un desequilibrio entre las sustancias prooxidantes y los antioxidantes. En la población del presente estudio observamos una mayor prevalencia del genotipo TT de la enzima antioxidante CAT y un aumento de la lesión oxidativa de proteínas y lípidos asociado a asma bronquial. También encontramos que en los niños asmáticos con el genotipo TT de CAT estaba presente una mayor lesión oxidativa comparado con otra variación genética de -262C/T de la CAT. Hasta lo que conocen los autores, este es el primer estudio sobre la asociación del polimorfismo genético y la lesión oxidativa en niños o adultos eslovacos con asma.
El polimorfismo de los genes implicados en la vía de la lesión oxidativa NAD(P)H:quinona oxidorreductasa16, glutatión transferasas M1 y P117,18 se ha asociado con asma bronquial16,17. La CAT es una de las enzimas antioxidantes fundamentales y, por consiguiente, el gen de la CAT es un gen candidato de muchas enfermedades que potencialmente se relacionan con una lesión oxidativa y el estrés oxidativo exógeno/endógeno. En el presente estudio, la frecuencia del genotipo TT de la CAT fue de 0,226 en niños asmáticos y de 0,048 en niños sanos (p<0,001). La frecuencia del genotipo CAT -262C/T fue comparable a la descrita en otros estudios europeos (inglés, alemán, polaco y turco)18–21. El análisis de acuerdo con los sexos demostró resultados similares al análisis de toda la población y la variante homocigota se asoció a asma bronquial. Hemos demostrado que el polimorfismo en el gen CAT puede asociarse con una predisposición a asma bronquial. La variante homocigota CAT -262C/T se asoció a asma en niños blancos de origen hispánico pero no en niños de otro origen22. Polonikov et al. (2009) no observaron diferencias en las frecuencias de alelo o de genotipo del polimorfismo -262C/T del gen CAT entre adultos asmáticos e individuos de control23. Sin embargo, observaron una asociación entre el polimorfismo -21A/T del gen CAT y el asma bronquial y encontraron que el riesgo de asma en portadores del genotipo -21AA depende de la exposición tanto a oxidantes como a antioxidantes. Los resultados contradictorios referentes a la relación entre el polimorfismo del gen CAT y el asma bronquial pueden explicarse por la influencia de la etnicidad. En nuestra población seleccionada de niños eslovacos, el genotipo TT se asoció con asma bronquial y esta variación genética del gen de la CAT podría ser responsable de la lesión oxidativa, ya que observamos un aumento de la lesión oxidativa, en particular en niños asmáticos portadores del genotipo TT. En diferentes estudios se ha observado una disminución de la actividad de la CAT en el genotipo TT11,24–26. No obstante, Forsberg et al.9 revelaron un mayor nivel de CAT en el genotipo TT del gen CAT. EL mayor riesgo de asma podría ser consecuencia de la disminución de la actividad de la CAT en el genotipo TT y el aumento posterior de la lesión oxidativa de las biomoléculas. Observamos un aumento de la lesión oxidativa de proteínas y lípidos en niños con asma bronquial. La inflamación crónica se asocia a una mayor producción de especies reactivas del oxígeno y un aumento del estrés oxidativo en el pulmón. Se han demostrado mayores niveles de peróxido de hidrógeno, radical superóxido27 y peroxidación lipídica27,28 en niños con asma bronquial. En la población asmática del presente estudio observamos un aumento del óxido nítrico29 y de eCO. Estos marcadores se caracterizan por una mayor concentración en el genotipo TT de niños asmáticos comparado con el genotipo CC y CT (resultados no publicados). Se ha demostrado que la combinación de la variante heterocigota con la variante homocigota es positiva. Es posible que un alelo C sea suficiente para la función de la CAT, pero se requieren otros estudios genéticos para determinar la actividad y función de la CAT en diferentes genotipos y no solo para este polimorfismo. En niños sanos con una variante del genotipo de CAT se detectan otros antioxidantes enzimáticos (como la hemooxigenasa, superóxido dismutasa, glutatión peroxidasa y glutatión transferasa) en la forma homocigota normal que los protege frente a la lesión oxidativa, y, por otra parte, los niños sanos no presentan el aumento de los valores de las especies reactivas de oxígeno detectado en niños asmáticos. Es probable que la relación entre la lesión oxidativa y la inflamación crónica en asmáticos sea bidireccional. El estrés oxidativo puede exacerbar la inflamación existente y puede contribuir al remodelado de las vías respiratorias y, por otra parte, una inflamación crónica continuada puede traducirse en una mayor producción de especies reactivas del oxígeno y una mayor lesión oxidativa. En el grupo de control, la comparación de la concentración de marcadores de lesión oxidativa de acuerdo con el genotipo de CAT no reveló diferencias significativas. En el presente estudio la mayor peroxidación de lípidos y modificación de proteínas detectada podría ser consecuencia de la producción excesiva de especies reactivas del oxígeno o de la disminución de la capacidad de defensa del sistema antioxidante en asmáticos. Los antioxidantes de la alimentación ayudan a los antioxidantes endógenos a prevenir una lesión oxidativa y representan una posible opción terapéutica. El tratamiento con antioxidantes podría favorecer el tratamiento asmático de referencia y ser un adyuvante, en especial en pacientes asmáticos con genotipos de riesgo de las enzimas antioxidantes. Los factores y las interacciones ambientales entre genes y factores ambientales pueden influir en la actividad de la CAT en los diferentes genotipos. No analizamos estos efectos pero se ha demostrado que la exposición al humo y el consumo de fruta y verduras afectan a la actividad de la CAT en los genotipos CC, CT y TT del gen CAT24–26,28.
El asma bronquial es una enfermedad multifactorial compleja en la que los factores genéticos, factores ambientales y lesión oxidativa son responsables de su inicio, modulación y progresión. Los resultados del presente estudio demuestran que los polimorfismos del gen de la CAT pueden asociarse a asma bronquial en niños y pueden participar en una mayor lesión oxidativa. La variación genética de la CAT, que protege a las células frente a las especies reactivas del oxígeno, puede afectar al proceso asmático. En resumen, el asma no es una enfermedad individual sino un grupo de enfermedades asociadas a un aumento del estrés oxidativo, seguido de la acumulación de una lesión oxidativa. Esta puede representar un importante factor que contribuya al desarrollo y persistencia de la inflamación de las vías respiratorias en niños asmáticos. La mayor lesión oxidativa puede ser consecuencia de reacciones cruzadas entre el polimorfismo del gen de la CAT y factores ambientales, además del polimorfismo del gen de la CAT y otros factores genéticos, que pueden modular el riesgo de la enfermedad. Sin embargo, son necesarios más estudios sobre las interacciones entre el polimorfismo del gen de la CAT y polimorfismos adicionales en genes relacionados con el asma porque pueden contribuir a mejorar nuestra comprensión de una enfermedad compleja como el asma bronquial.
FinanciaciónEl presente estudio estuvo financiado con una beca del Ministerio de Salud 2007/47-UK-12, y por el Ministerio de Educación, Ciencia, Investigación y Deporte de la República Eslovaca, VEGA 1/0071/11.
Conflicto de interesesNinguno de los autores ha declarado conflicto de intereses.
Deseamos dar las gracias a J. Bencatova, Z. Cetlova, y A. Kempna por su ayuda de laboratorio.