Determinar la utilidad de la adenosina desaminasa (ADA) pleural para diagnosticar derrame pleural tuberculoso en población española, según la técnica de medición y punto de corte utilizados, y compararla con la descrita para otras poblaciones.
MétodosMetaanálisis de estudios diagnósticos sobre ADA pleural en población española, extraídos de PubMed y Embase desde sus comienzos hasta julio de 2017, sin restricciones de lenguaje. Se analizó la eficacia diagnóstica global de la ADA, según sus técnicas de medición (Giusti, métodos cinéticos manuales y métodos cinéticos automatizados) y el punto de corte seleccionado. La herramienta QUADAS-2 evaluó la calidad de los estudios. Se utilizó un método bivariante de efectos aleatorios. Se compararon los resultados con los descritos en metaanálisis previos sobre población no española.
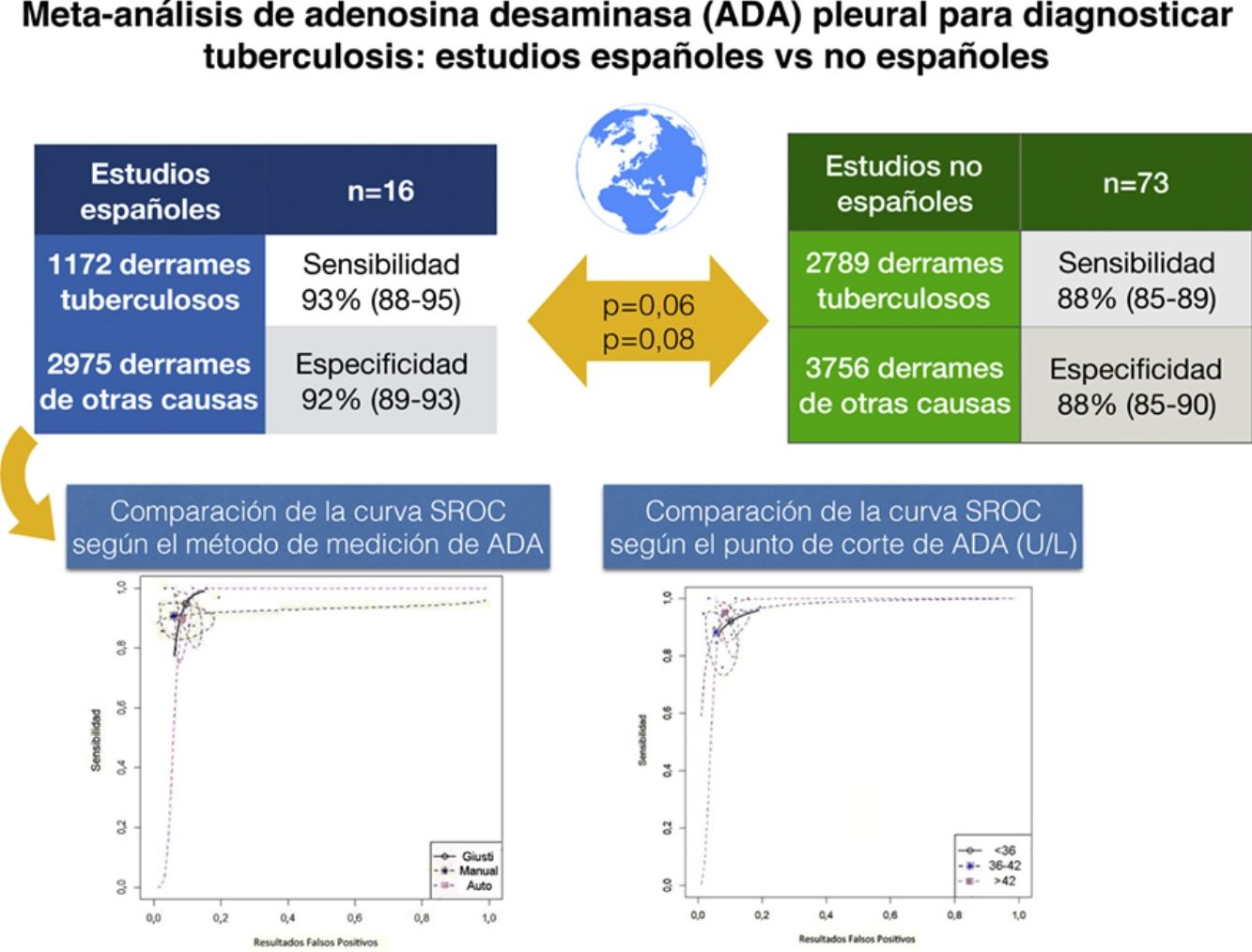
ResultadosSe incluyeron 16 estudios, con 4.147 pacientes, de los que 1.172 tenían derrame pleural tuberculoso. La ADA tuvo una sensibilidad del 93%, especificidad del 92%, likelihood ratio positiva de 12, likelihood ratio negativa de 0,08, y área bajo la curva de 0,968 para identificar tuberculosis. No hubo diferencias de eficacia diagnóstica entre las técnicas de medición de ADA o el punto de corte escogido. En 73 estudios de población no española se observó una tendencia hacia una menor sensibilidad (88%, IC95%: 86-90%) y especificidad (88%, IC95% 86-90%) de la ADA, pero las diferencias no alcanzaron significación estadística.
ConclusionesLa ADA pleural en población española tiene una buena precisión diagnóstica (independientemente de la técnica de medición o punto de corte empleados), similar a la reportada en población no española.
To evaluate the usefulness of pleural fluid adenosine deaminase (ADA) for diagnosing tuberculous pleural effusions in the Spanish population, according to laboratory technique and cut-off point, and to compare the results with other populations.
MethodsMeta-analysis of diagnostic studies on pleural fluid ADA in the Spanish population, extracted from the PubMed and Embase databases from inception until July 2017, with no language restrictions. The overall diagnostic accuracy of ADA and that of each of the measurement techniques (Giusti, manual and automated kinetic methods) and selected cut-offs were analyzed. The QUADAS-2 tool was used to evaluate the quality of studies. A bivariate random effects model was used. Results were compared with those obtained from previous meta-analyses in non-Spanish populations.
ResultsSixteen studies in a total of 4,147 patients, 1,172 of whom had tuberculous pleural effusions, were included. ADA had 93% sensitivity, 92% specificity, positive likelihood ratio of 12, negative likelihood ratio of 0.08, and an area-under-the-curve of 0.968 for identifying tuberculosis. There were no differences in diagnostic accuracy between the techniques used for ADA measurement or the selected cut-offs. In 73 studies from non-Spanish populations a trend toward lower ADA sensitivity (88%, 95% CI:86%-90%) and specificity (88%, 95% CI: 86%-90%) was noted, but differences did not reach statistical significance.
ConclusionsPleural fluid ADA in the Spanish population shows good diagnostic accuracy (regardless of the measurement technique or cut-off), similar to that reported in non-Spanish populations.
Durante el año 2016 se produjeron 10,4 millones de nuevos casos de tuberculosis (TB) en el mundo1. En ese año, la incidencia de TB en España fue de 12 casos por 100.000 habitantes1. En el año 2014, el derrame pleural tuberculoso (DPT) fue la segunda forma más común de TB extrapulmonar (18,4%) en España, después de la afectación ganglionar (23,6%)2. En una serie española, la TB representó la cuarta causa (9%) de 3.077 derrames pleurales sometidos a toracocentesis, después del cáncer (27%), la insuficiencia cardiaca (21%) y la neumonía (19%)3.
El diagnóstico de certeza de un DPT requiere la demostración de bacilos tuberculosos en especímenes de esputo, líquido pleural (LP) o biopsia pleural. Sin embargo, la rentabilidad de los estudios microbiológicos es baja, particularmente cuando se utilizan solo medios de cultivo sólidos. Además, la obtención de los resultados precisa de varias semanas4. La biopsia pleural, que demuestra granulomas en 3 cuartas partes de los casos, permite un diagnóstico más precoz, pero es una técnica invasiva, no exenta de riesgos5.
La adenosina desaminasa (ADA) constituye el biomarcador más utilizado para el diagnóstico de DPT. Su medición en LP ha substituido en muchos centros a la realización de una biopsia pleural con finalidad diagnostica4. De este modo, se suele aceptar el diagnóstico de TB pleural y, consecuentemente, iniciar un tratamiento antituberculoso empírico, en el paciente con un cuadro clínico subagudo de fiebre, síntomas respiratorios y derrame pleural unilateral que corresponda a un exudado linfocitario con estudios citológicos negativos para malignidad y concentraciones de ADA≥35-40U/L (un punto de corte diagnóstico que podría ser inferior en pacientes de mayor edad)4. Hasta la actualidad, se han publicado 6 metaanálisis sobre la utilidad de esta enzima para diagnosticar DPT; ninguno en población exclusivamente española6–11. No obstante, estos estudios presentan algunas limitaciones. Por un lado, ninguno de ellos evaluó la influencia que sobre la eficacia diagnóstica de la ADA pleural pueden tener las distintas técnicas de medición de la misma o los puntos de corte dicotómicos seleccionados. Por otro lado, la mayoría de ellos combinaron poblaciones pertenecientes a áreas geográficas con diferente prevalencia de TB6,7,9,10. Es conocido que el valor predictivo positivo de la ADA pleural disminuye proporcionalmente a la prevalencia de TB; de modo que en un área con baja prevalencia de la enfermedad, una ADA pleural elevada tiene más posibilidades de corresponder a un falso positivo4.
Los objetivos diferenciales de este estudio con respecto a los reportados previamente fueron: 1) evaluar la utilidad de la ADA pleural para el diagnóstico de DPT en población española, 2) valorar si la técnica de medición de ADA o el punto de corte seleccionado influye en su eficacia diagnóstica, y 3) comparar estos resultados con los descritos para población no española en los metaanálisis ya publicados.
Material y métodosEstrategia de búsqueda y selección de estudiosLa revisión sistemática se realizó de acuerdo con las guías Preferred Reporting Items for Systematic Reviews and Meta-analysis (PRISMA)12. Se utilizaron las bases de datos electrónicas PubMed/MEDLINE y Embase, desde sus inicios hasta julio de 2017. La estrategia de búsqueda empleó los términos: («pleural tuberculosis» OR «tuberculous pleuritis» OR «tuberculous pleurisy» OR «pleural») AND («adenosine deaminase» OR «ADA»). También se revisaron todas las referencias de los artículos seleccionados. Dos investigadores (R.M.P. y S.B.) evaluaron los estudios de forma independiente y las discrepancias se resolvieron por acuerdo.
Criterios de inclusión y exclusiónSe incluyeron los estudios realizados sobre población española, sin restricción de lenguaje, que cumplían 2 requisitos: 1) el diagnóstico de DPT se confirmó mediante biopsia pleural o aislamiento microbiológico de Mycobacterium tuberculosis en esputo, LP o biopsia pleural; y 2) se proporcionaban suficientes datos para construir una tabla de contingencia 2×2 que permitiera calcular la eficacia diagnóstica. Se excluyeron los estudios con duplicación o solapamiento de casos; situación en la que se seleccionó el artículo con mayor tamaño muestral.
Extracción de datosSe recogieron las siguientes características de los artículos seleccionados: autores, fecha de publicación, lugar de realización del estudio, diseño, número de pacientes y sus características demográficas, métodos diagnósticos del DPT, etiología de los derrames no tuberculosos, técnica utilizada para la detección de ADA en LP (Giusti, métodos cinéticos manuales o métodos cinéticos automatizados), y los datos necesarios para construir una tabla 2×2.
Evaluación de la calidad de los estudiosDos investigadores (R.M.P. y S.B.) evaluaron de forma independiente la calidad de los estudios mediante el uso de la herramienta Quality Assessment of Diagnostic Accuracy Studies (QUADAS-2)13. Esta se compone de 4 dominios: 1) selección de pacientes, 2) prueba índice, 3) prueba de referencia y 4) flujo de pacientes y tiempo. Cada dominio se evalúa en función de su riesgo de sesgo (bajo, alto o incierto), y los 3 primeros dominios también por su aplicabilidad.
Comparación con estudios internacionalesSe identificaron todos los metaanálisis publicados sobre la precisión diagnóstica de la ADA pleural en la TB6–11, de los que se seleccionaron los estudios realizados sobre población no española. Se revisó el texto completo de dichos estudios y finalmente se consideraron solo aquellos en los que el diagnóstico de DPT se había confirmado mediante biopsia pleural o aislamiento microbiológico en algún espécimen biológico. De cada uno de los artículos seleccionados se extrajeron los mismos datos que los referidos previamente para la población española.
Análisis estadísticoLas variables continuas se expresaron como medias o medianas, y las categóricas como frecuencias y porcentajes. El acuerdo entre observadores para la herramienta QUADAS-2 se determinó usando el estadístico Kappa de Cohen no ponderado; el resultado se consideró bueno si fue>0,6 y excelente cuando superaba 0,8. La sensibilidad, especificidad, likelihood ratio (LR) positiva y negativa, y odds ratio diagnóstica (DOR) de la ADA pleural, con sus correspondientes intervalos de confianza del 95% (IC95%), se calcularon a partir de una tabla 2×2, usando modelos bivariantes de efectos aleatorios. Para el cálculo de las LR se aplicó una corrección de 0,5 a todas las celdas en el caso de que estas contuvieran algún 0. Debido a la correlación negativa entre sensibilidad y especificidad, estos parámetros se analizaron simultáneamente mediante una metarregresión de efectos aleatorios, según los datos de sensibilidad y tasa de falsos positivos obtenidos de los estudios incluidos14. A partir de dicha metarregresión se estimó la curva ROC resumen. La metarregresión se ajustó por la técnica diagnóstica de ADA en LP (Giusti, método cinético manual o método cinético automatizado) y, en caso de diferencias significativas, el análisis se estratificó para cada una de las técnicas por separado. Se siguió el mismo proceso analítico ajustando por el punto de corte de ADA utilizado para el diagnóstico de TB. El sesgo de publicación se estimó mediante un gráfico de embudo (funnel plot) para las medidas de LR positiva y negativa. La heterogeneidad entre estudios se cuantificó mediante el estadístico I2 de Higgins, estimado a partir del metaanálisis univariante basado en el método de DerSimonian y Laird15 para las 3 medidas del efecto (LR positiva, LR negativa y DOR). El análisis estadístico se realizó fijando un nivel de significación estadística de 0,05. Los cálculos se realizaron con el programa «R» (R-project; http://cran.r-project.org/web/packages/mada/index.html).
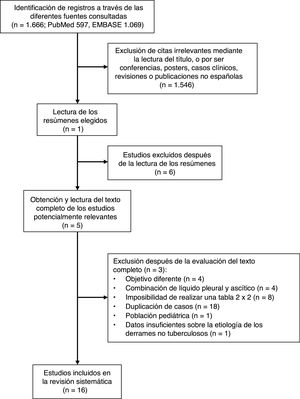
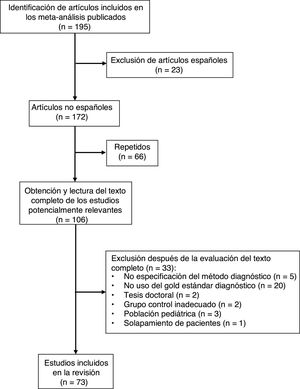
ResultadosMetaanálisis en población españolaSe identificaron 1.666 artículos, de los que se leyó el texto completo de 52 potencialmente relevantes. Solo 16 de ellos cumplieron los criterios de inclusión5,16–30 (fig. 1 y apéndice, tabla A.1). Los estudios seleccionados comprendieron un total de 1.172 pacientes con DPT y 2.975 con derrames de otras causas, entre las que destacaban derrames malignos (1.248, 42%; de los que 78 eran linfomas) y paraneumónicos (539, 18%; de los que 74 eran empiemas). Las características de estos estudios se resumen en la tabla 1. Las técnicas utilizadas para cuantificar la ADA fueron heterogéneas: 6 estudios utilizaron el método Giusti5,17–21, 5 técnicas cinéticas manuales22–24,26,27 y 4 técnicas cinéticas automatizadas25,28–30. El punto de corte de la ADA para el diagnóstico de DPT varió entre 2323 y 45U/L5,16,24, aunque el más utilizado fue 40U/L20,26,27,29,30. No se especificó la edad y el sexo de los pacientes en 817,18,21–23,25–27 y 9 estudios17,21–28, respectivamente; ni la raza en ninguno de ellos5,16–30. No se detectó alta probabilidad de sesgo en ningún dominio del QUADAS-2, aunque el dominio de selección de pacientes fue considerado «incierto» en 8 estudios16,18–24. La concordancia interobservador para la evaluación de los dominios del QUADAS-2 fue de 0,9 (IC95%: 0,78-1).
Características de los estudios españoles que evalúan el rendimiento diagnóstico de la adenosina desaminasa en el líquido pleural
| Autor | Ciudad | Diseño | N.o de pacientes con DPT/otras causas | Derrames no tuberculososa | Técnica de medición de ADA | Punto de corte de ADA (U/L) | VP | FP | VN | FN |
|---|---|---|---|---|---|---|---|---|---|---|
Cardona-Iguacén et al.16 | Barcelona | NE | 30/75 | 35 malignos (2 linfomas y 33 tumores sólidos), 30 paraneumónicos, 10 miscelánea | NE | 45 | 30 | 3 | 72 | 0 |
Ocaña et al.17 | Barcelona | Prospectivo | 170/416 | 126 malignos, 76 paraneumónicos, 100 trasudados, 69 miscelánea, 45 pleuritis inespecíficas | Giusti | 43 | 170 | 23 | 393 | 0 |
Blanco-Vaca et al.18 | Barcelona | NE | 7/64 | 24 malignos (24 tumores sólidos, 0 linfomas), 9 paraneumónicos, 12 trasudados, 5 miscelánea, 14 idiopáticos | Giusti | 43 | 7 | 10 | 54 | 0 |
Fontan-Bueso et al.19 | La Coruña | NE | 61/77 | 42 malignos (4 linfomas, 38 tumores sólidos), 11 paraneumónicos, 14 trasudados, 10 miscelánea | Giusti | 33 | 61 | 9 | 68 | 0 |
Pérez de Oteyza et al.20 | Madrid | NE | 13/53 | 22 malignos (3 linfomas, 19 tumores sólidos), 11 paraneumónicos, 10 trasudados, 10 miscelánea | Giusti | 40 | 11 | 3 | 50 | 2 |
Serra et al.21 | Barcelona | NE | 8/59 | 11 malignos (8 tumores sólidos, 3 linfomas), 17 paraneumónicos, 22 trasudados, 4 miscelánea, 5 idiopáticos | Giusti | 43 | 7 | 7 | 52 | 1 |
López-Jiménez et al.22 | Madrid | NE | 32/106 | 27 malignos, 35 paraneumónicos, 32 trasudados, 12 miscelánea | Cinético manual | 32 | 28 | 11 | 95 | 4 |
Bandrés-Gimeno et al.23 | Vigo | Retrospectivo | 33/31 | 16 malignos (16 tumores sólidos, 0 linfomas), 9 paraneumónicos, 6 trasudados | Cinético manual | 23 | 32 | 6 | 25 | 1 |
Querol et al.24 | Xátiva | NE | 21/83 | 34 malignos (32 tumores sólidos, 2 linfomas), 22 paraneumónicos, 16 trasudados, 9 miscelánea | Cinético manual | 45 | 18 | 2 | 81 | 3 |
Villena et al.25 | Madrid | Prospectivo | 49/179 | 95 malignos (87 tumores sólidos, 8 hematológicos), 32 paraneumónicos, 28 trasudados, 19 miscelánea, 5 idiopáticos | Cinético automatizado | 33 | 44 | 9 | 170 | 5 |
Avilés-Inglés et al.26 | Murcia | Prospectivo | 10/30 | 10 malignos (10 tumores sólidos, 0 linfomas), 10 paraneumónicos, 10 trasudados | Cinético manual | 40 | 10 | 1 | 29 | 0 |
Jiménez-Castro et al.27 | Madrid | Prospectivo | 76/410 | 221 malignos (214 tumores sólidos, 7 linfomas), 35 paraneumónicos, 51 trasudados, 27 miscelánea, 76 idiopáticos | Cinético manual | 40 | 72 | 7 | 403 | 4 |
Porcel et al.28 | Lleida | Retrospectivo | 59/496 | 262 malignos (236 tumores sólidos, 26 linfomas), 62 paraneumónicos, 125 miscelánea, 7 Idiopáticos | Cinético automatizado | 35 | 55 | 47 | 449 | 4 |
García-Zamalloa et al.29 | Gipuzkoa | Retrospectivo | 25/365 | 105 malignos, 121 paraneumónicos, 61 trasudados, 78 miscelánea | Cinético automatizado | 40 | 19 | 28 | 337 | 6 |
Sahn et al.5 | Santiago de Compostela | Retrospectivo | 548/423 | 158 malignos (137 tumores sólidos, 21 linfomas), 113 paraneumónicos, 115 trasudados, 37 miscelánea | Giusti | 45 | 535 | 29 | 394 | 13 |
Sánchez-Otero et al.30 | Vigo | Retrospectivo | 30/108 | 60 malignos (58 tumores sólidos, 2 linfomas), 21 paraneumónicos, 12 miscelánea, 15 idiopáticos | Cinético automatizado | 40 | 29 | 11 | 97 | 1 |
ADA: adenosina desaminasa; DPT: derrame pleural tuberculoso; FN: falsos negativos; FP: falsos positivos; NE: no especificado; VN: verdaderos negativos; VP: verdaderos positivos.
Tumores sólidos hace referencia a neoplasias de pulmón, mama, ovario, gastrointestinal, tracto urinario, genital, origen desconocido y mesotelioma. Miscelánea hace referencia a derrames pleurales secundarios a tromboembolia pulmonar, síndrome de Dressler, postintervención quirúrgica, virus, enfermedades del pericardio, quiste hidatídico, traumatismos, pancreatitis, quilotórax, artritis reumatoide, sarcoidosis, porfiria, vasculitis y trasplante.
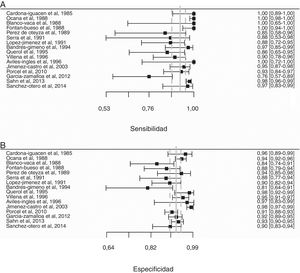
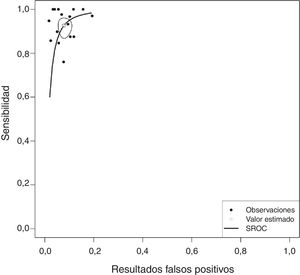
Globalmente, la ADA pleural tuvo una sensibilidad del 93% (IC95% 88-96%), especificidad del 92% (IC95% 90-94%) (fig. 2), LR positiva de 12 (IC95%: 9-16), LR negativa de 0,08 (IC95%: 0,05-0,13), DOR de 156 (IC95%: 80-275) y área bajo la curva ROC resumen de 0,968 (fig. 3) para identificar DPT. No hubo diferencias significativas de sensibilidad o especificidad entre las diferentes técnicas de medición de la ADA. De este modo, la sensibilidad para los métodos Giusti, cinéticos manuales y cinéticos automatizados fue del 95, 91 y 90% (p=0,25); y la especificidad del 91, 94 y 92%, respectivamente (p=0,31) (tabla 2). Tampoco existieron diferencias de sensibilidad o especificidad entre los diferentes puntos de corte de ADA cuando estos se agruparon en 3 rangos de valores: 1) ADA de 23 a 35U/L19,22,23,25,28 (sensibilidad 92%, especificidad 90%); 2) ADA de 36 a 42U/L 20,26,27,29,30 (sensibilidad 88%, especificidad 94%); y 3) ADA de 43 a 45U/L5,16–18,21,24 (sensibilidad 95%, especificidad 92%; p=0,54 para las sensibilidades y p=0,1 para las especificidades).
Forest plot de sensibilidad (A) y especificidad (B) de la adenosina desaminasa para el diagnóstico de derrame pleural tuberculoso. El punto estimado de sensibilidad y especificidad de cada estudio se muestra con un cuadrado sólido sobre una línea que representa el intervalo de confianza. La línea vertical continua representa las sensibilidades (A) y especificidades (B) medias ponderadas y las líneas verticales discontinuas el intervalo de confianza.
Medidas de precisión diagnóstica de la adenosina desaminasa en el derrame pleural tuberculoso, según la técnica de medición utilizada
| Estudios españoles | Estudios no españoles | |||||||
|---|---|---|---|---|---|---|---|---|
| Giusti | Cinético manual | Cinético automatizado | Suma de estudios | Giusti | Cinético manual | Cinético automatizado | Suma de estudios | |
Número de estudios | 6 | 5 | 4 | 16 | 49 | 5 | 14 | 73 |
Sensibilidad, % (IC95%) | 94,7 (84,5-98,4) | 90,6 (84,7-94,4) | 89,8 (78,9-95,4) | 92,6 (88,2-95,5) | 88,8 (85,8-91,2) | 87,8 (80,4-92,7) | 85,1 (79,1-89,5) | 87,9 (85,6-89,9) |
Especificidad, % (IC95%) | 90,6 (86,9-93,3) | 94 (85,4-97,7) | 91,6 (89,5-93,3) | 92,2 (89,7-94,1) | 88,9 (84,9-90,6) | 92,8 (85,1-96,7) | 86,4 (82,6-89,6) | 87,9 (85,6-89,9) |
LR positiva (IC95%) | 10,2 (6,64-14,6) | 16,9 (6,1-38,9) | 10,6 (8,58-13,1) | 12 (8,91-15,8) | 7,5 (5,81-9,58) | 13,3 (5,67-27,2) | 6,32 (4,7-8,34) | 7,32 (6,05-8,79) |
LR negativa (IC95%) | 0,068 (0,02-0,18) | 0,1 (0,06-0,17) | 0,119 (0,05-0,23) | 0,08 (0,05-0,13) | 0,13 (0,09-0,16) | 0,14 (0,07-0,22) | 0,18 (0,12-0,24) | 0,14 (0,11-0,16) |
DOR (IC 95%) | 230 (39,5-657,03) | 183 (44,7-507) | 104 (43,2-211) | 156 (80,3-275) | 59,8 (37,7-90,3) | 112 (28,7-304) | 37,7 (20,5-63,9) | 53,7 (38,3-73,3) |
SROC | 0,951 | 0,921 | 0,939 | 0,968 | 0,941 | 0,941 | 0,92 | 0,937 |
DOR: odds ratio diagnóstica; IC: intervalo de confianza; LR: likelihood ratio; SROC: área bajo la curva resumen.
Se identificaron 6 metaanálisis6–11 que comprendían un total de 195 estudios, de los que se excluyeron 122 por los siguientes motivos: 23 por tratarse de población española (en nuestro metaanálisis, 5 de ellos los excluimos por duplicación de pacientes y 2 por combinar resultados de LP y ascítico); 66 por solapamiento entre los diferentes metaanálisis; 20 por falta de confirmación histológica o microbiológica del DPT; 5 por no especificarse el método diagnóstico del DPT; 3 por realizarse sobre población pediátrica; 2 por tratarse de tesis doctorales sin posibilidad de acceso a los datos; 2 por incluir un grupo comparador inadecuado (TB probables); y uno por duplicación o solapamiento de pacientes (fig. 4 y apéndice, tabla A.2.). Se seleccionaron, por tanto, 73 artículos (apéndice, tabla A.3) que incluyeron un total de 2.789 pacientes con DPT y 3.756 con derrames pleurales de otras causas. Entre estos últimos existían 63 (1,6%) linfomas y 614 (16%) derrames paraneumónicos, de los que 206 eran empiemas. En 49 estudios se utilizó el método Giusti para cuantificar la ADA, en 5 técnicas cinéticas manuales, en 14 métodos cinéticos automatizados y en otros 5 no se especificó la técnica utilizada.
Globalmente, en los estudios no españoles, la ADA pleural mostró una sensibilidad del 88% (IC95%: 86-90%), especificidad del 88% (IC95%: 86-90%), LR positiva de 7 (IC95%: 6-9), LR negativa de 0,14 (IC95%: 0,11-0,16), DOR de 54 (IC95%: 38-73) y área bajo la curva ROC resumen de 0,937 para diagnosticar TB pleural.
Comparación entre estudios españoles y no españolesExistió una tendencia no significativa hacia una mayor sensibilidad (93 vs. 88%, p=0,06) y especificidad (92 vs. 88%, p=0,08) de la ADA pleural en los estudios españoles respecto a los no españoles. También en los primeros la sensibilidad del método Giusti (95% vs. 89%, p=0,05) y la especificidad de las técnicas cinéticas automatizadas (92 vs. 86%, p<0,01) resultaron superiores que en los segundos. Para el resto de las técnicas no hubo diferencias significativas.
En lo referente a los rangos de puntos de corte de ADA antes referidos, el único aspecto diferencial entre estudios españoles y no españoles fue la mayor sensibilidad de los primeros para valores de ADA de 43 a 45U/L (95 vs. 87%, p=0,04) y la mayor especificidad para valores de ADA≥36U/L (ADA 36 a 42U/L, 95 vs. 86%, p=0,04; ADA 43 a 45U/L, 92 vs. 87%, p=0,03, respectivamente) (tabla 3).
Medidas de precisión diagnóstica de la adenosina desaminasa en el derrame pleural tuberculoso, según el punto de corte utilizado
| Estudios españoles | Estudios no españoles | |||||||
|---|---|---|---|---|---|---|---|---|
| ADA 23-35U/L | ADA 36-42U/L | ADA>43 U/L | Suma de estudios | ADA 23-35U/L | ADA 36-42U/L | ADA>43 U/L | Suma de estudios | |
Número de estudios | 5 | 5 | 6 | 16 | 23 | 23 | 27 | 73 |
Sensibilidad, % (IC95%) | 92 (84,4-95,8) | 88,3 (77-94,4) | 95 (84,3-98,5) | 92,6 (88,2-95,5) | 87 (82-90,8) | 88,8 (84,8-91,9) | 88,6 (85,1-91,4) | 87,9 (85,6-89,9) |
Especificidad, % (IC95%) | 89,8 (85,4-92,9) | 94,5 (89,5-97,2) | 91,7 (88,3-94,2) | 92,2 (89,7-94,1) | 90,4 (86,9-93,1) | 86,1 (79,9-90,6) | 86,9 (84,3-89,2) | 87,9 (85,6-89,9) |
LR positiva (IC95%) | 9,12 (6,38-12,8) | 16,9 (7,83-32,1) | 11,6 (7,46-16,7) | 12 (8,91-15,8) | 9,23 (6,53-12,7) | 6,51 (4,34-9,51) | 6,8 (5,51-8,32) | 7,32 (6,05-8,79) |
LR negativa (IC 95%) | 0,092 (0,05-0,15) | 0,13 (0,06-0,25) | 0,065 (0,02-0,18) | 0,08 (0,05-0,13) | 0,15 (0,1-0,2) | 0,13 (0,09-0,18) | 0,13 (0,09-0,18) | 0,14 (0,11-0,16) |
DOR (IC95%) | 106 (57-179) | 158 (35,7-459) | 288 (44,6-993) | 156 (80,3 – 275) | 66,4 (35,6-113) | 51,8 (25,7-93,3) | 52,9 (32,6-81,4) | 53,7 (38,3-73,3) |
SROC | 0,96 | 0,964 | 0,956 | 0,968 | 0,947 | 0,929 | 0,933 | 0,937 |
ADA: adenosina desaminasa; DOR: odds ratio diagnóstica; IC: intervalo de confianza; LR: likelihood ratio; SROC: área bajo la curva resumen.
Respecto a la etiología de los derrames no tuberculosos, los linfomas fueron más numerosos en los estudios españoles (78/2.975, 2,7% vs. 63/3.756, 1,7%; p=0,01) y los empiemas en los estudios no españoles (206/3.756, 5,5% vs. 75/2.975, 2,5%; p<0,01). El porcentaje de linfomas y empiemas considerados conjuntamente fue superior en los estudios no españoles (7,2 vs. 5,2%; p<0,01).
Riesgo de sesgo y heterogeneidadEl gráfico de embudo asimétrico (asymmetric funnel test) para LR no mostró sesgo de publicación significativo en los estudios españoles (p=0,46 para la LR positiva; p=0,62 para la LR negativa). Tampoco lo hubo cuando se consideraron individualmente las técnicas de medición de ADA o sus diferentes puntos de corte (todas las p>0,1). No existió heterogeneidad significativa en el conjunto de estudios españoles (I2=20% para la LR positiva; I2<13% para LR negativa y DOR) ni para los realizados con el método Giusti (I2=0%), cinético manual (I2=0%) o cinético automatizado (I2=0,2%), ni tampoco cuando se utilizó un punto de corte de ADA<36U/L (I2<17,1%), entre 36 y 42U/L (I2=0%) o>42U/L (I2<17,3%).
DiscusiónEste metaanálisis demuestra la alta rentabilidad de la ADA pleural para el diagnóstico de TB en población española. Unas concentraciones elevadas (generalmente≥35-40U/L) incrementan significativamente la probabilidad de DPT (LR positiva=12), mientras que unos valores bajos la reducen (LR negativa=0,08). Ni las diversas técnicas de medición de la ADA (Giusti, cinéticos manuales o cinéticos automatizados) ni los distintos puntos de corte diagnósticos de TB descritos en la literatura influyeron en la eficacia diagnóstica de esta enzima. En los estudios sobre población no española la ADA pleural mostró una sensibilidad (88 vs. 93%) y especificidad (88 vs. 92%) inferiores a la hallada en los estudios españoles, aunque las diferencias no alcanzaron significación estadística.
Existen otras entidades diferentes a la TB que pueden acompañarse de una elevación de ADA pleural. Una serie de 2.100 pacientes con derrame pleural reportó que hasta el 70% de los empiemas y alrededor de la mitad de los linfomas presentaban concentraciones de ADA en LP≥35U/L28. En el presente metaanálisis se observó que el porcentaje de empiemas y linfomas juntos fue superior en los estudios no españoles (7,2 vs. 5,2%). Este hallazgo podría justificar la tendencia hacia una menor especificidad de la ADA en población no española.
Las cifras de sensibilidad y especificidad de la ADA pleural en los estudios españoles fueron comparables a las reportadas en otros metaanálisis (tabla 4). Sin embargo, algunos de estos muestran deficiencias que se han intentado solventar en el presente trabajo. Por ejemplo, 3 de ellos no evaluaron las LR positiva, LR negativa ni la DOR6–8. De 172 estudios no españoles extraídos de los 6 metaanálisis publicados, solo cumplieron nuestros criterios de inclusión 73 (42%) (tabla 4 y apéndice, tabla A.2). Algunos de las motivos de exclusión (p. ej. gold estándar diagnóstico de DPT inadecuado en 20 estudios) podrían cuestionar la fortaleza de los resultados obtenidos en dichos metaanálisis.
Medidas de precisión diagnóstica de la adenosina desaminasa pleural en el derrame pleural tuberculoso, según los diferentes metaanálisis publicados
| Estudio | N.o de estudios españoles/no españoles | Sensibilidad | Especificidad | LR positiva | LR negativa |
|---|---|---|---|---|---|
Greco et al., 20036 | 5/26 | 93% | 90% | 9,3 | 0,07 |
Goto et al., 20037 | 8/32 | 92% | 90% | 9,03 | 0,1 |
Morisson et al., 20088 | 0/9 | 92% | 89% | 8,36 | 0,09 |
Liang et al., 20089 | 9/54 | 92% | 90% | 9,03 | 0,1 |
Gui et al., 201410 | 1/11 | 86% | 88% | 6,32 | 0,15 |
Aggarwal et al., 201611 | 0/40 | 94% | 89% | 8,57 | 0,07 |
Estudio actual | 16/0 | 93% | 92% | 12 | 0,08 |
LR: likelihood ratio.
Este metaanálisis es el primero que valora si las diferentes técnicas de medición de la ADA tienen una eficacia diagnóstica similar. En población española no se observaron diferencias entre ellas. Sin embargo, en la comparación de población española vs. no española, la ADA tuvo una sensibilidad superior en la primera cuando se analizaba mediante el método Giusti (95 vs. 89%; p=0,05) y una mayor especificidad cuando se utilizaban técnicas cinéticas automatizadas (92 vs. 86%; p<0,01).
El presente estudio no está exento de limitaciones. Aunque se ha centrado en población española para disminuir el efecto que, sobre la eficacia diagnóstica de la ADA, puede tener la prevalencia de TB en distintas poblaciones, también esta varía entre las diversas regiones de España. De hecho, la mayoría de los estudios incluidos en este metaanálisis proceden de las comunidades autónomas de Cataluña16–18,21,28, Galicia5,19,23,30 o Madrid20,22,25,27. Además, los estudios comprendieron un periodo de tiempo prolongado, durante el cual también ha variado la prevalencia de TB31. Específicamente, en las 3 comunidades españolas antes mencionadas, la prevalencia de TB se redujo desde 41, 71 y 30 por 100.000 habitantes en 199732,33 hasta 15, 20 y 10 por 100.000 habitantes en 2014, respectivamente2. Existieron, además, otras fuentes de heterogeneidad como la inclusión, entre las causas de derrames no tuberculosos, de etiologías poco definidas o idiopáticas. No obstante, factores como las diferentes técnicas de medición de la ADA o la elección de distintos puntos de corte de ADA descritos en la bibliografía médica se controlaron en el análisis de metarregresión. Finalmente, al no ser este un metaanálisis de datos individuales no se ha podido evaluar la influencia de factores como la edad en el punto de corte idóneo de la ADA pleural para diagnosticar DPT. De este modo, diversos estudios retrospectivos sugieren que se deben adoptar puntos de corte dicotómicos más bajos en pacientes de mayor edad (>45-55 años)34–36.
En conclusión, este estudio solventa algunas deficiencias metodológicas de metaanálisis previos y demuestra que la ADA pleural tiene una buena precisión para diagnosticar DPT en población española, independientemente de la técnica de medición empleada para su análisis.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.