PLATINO es un estudio de base poblacional para medir la prevalencia de la enfermedad pulmonar obstructiva crónica (EPOC) en São Paulo (Brasil), Ciudad de México (México), Montevideo (Uruguay), Santiago de Chile (Chile) y Caracas (Venezuela). El objetivo ha sido describir el tratamiento preventivo y farmacológico en individuos con EPOC y los factores asociados al mismo.
Pacientes y métodosLos sujetos elegibles completaron un cuestionario y realizaron una espirometría posbroncodilatador.
ResultadosDe un total de 5.529 individuos con datos autorreferidos sobre tratamiento, se identificó como afectados de EPOC (relación volumen espiratorio forzado en el primer segundo/capacidad vital forzada<0,7 posbroncodilatador) a 758, de los que 86 tenían diagnóstico médico previo. Considerando la totalidad de los pacientes con EPOC, sólo la mitad de los fumadores o exfumadores había recibido consejo antitabáquico y el 24,7% recibió algún tipo de medicación respiratoria. El uso de esteroides inhalados alcanzó un 13,5% de los individuos más graves. En el grupo de EPOC con diagnóstico médico previo, el 69% de los fumadores o exfumadores había recibido consejo médico para dejar de fumar y el 75,6% medicación respiratoria en el último año, un 43% de ellos por vía inhalada y un 36% broncodilatadores. La cobertura de vacunación antigripal y el uso de mucolíticos e inhaladores fueron variables en los distintos centros. Todas las prescripciones terapéuticas se asociaron a espirometría previa.
ConclusionesLa espirometría surge no sólo como una herramienta diagnóstica, sino como factor asociado al tratamiento, en un contexto dispar de utilización de los recursos disponibles en estas 5 ciudades de Latinoamérica.
PLATINO project is a population-based study designed to determine the prevalence of chronic obstructive pulmonary disease (COPD) in São Paulo, Brazil; Mexico City, Mexico; Montevideo, Uruguay; Santiago de Chile, Chile; and Caracas, Venezuela. The objective of this portion of PLATINO was to describe preventive and pharmacological treatment of COPD patients and factors associated with such treatment.
Patients and methodsEligible subjects completed a questionnaire and underwent postbronchodilator spirometry.
ResultsOf the total of 5529 individuals who answered items referring to treatment, 758 had COPD (ratio of postbronchodilator forced expiratory volume in 1 second to forced vital capacity of <0.7), and 86 of them had been previously diagnosed by a physician. Among all COPD patients, only half of smokers or former smokers had been advised to quit and 24.7% had received some type of respiratory medication. Only 13.5% had used inhaled corticosteroids, and those were the patients with the most severe disease. In the group of patients who had a previous medical diagnosis of COPD, 69% of the smokers or former smokers had been advised to quit by a physician and 75.6% had received respiratory medication in the preceding year: 43% reported having used inhaled medication and 36% had used bronchodilators. Rates of vaccination against influenza and the use of mucolytic drugs and inhalers varied from one health care facility to another. All drug prescriptions were based on previous spirometry.
ConclusionsSpirometry emerged not only as a diagnostic tool, but also as a factor associated with treatment, against a background of uneven use of available health care resources in these 5 Latin American cities.
La enfermedad pulmonar obstructiva crónica (EPOC) es una enfermedad prevenible y tratable, de evolución progresiva y elevada prevalencia tanto en EE.UU. como en Europa1,2, que se prevé será la tercera causa de muerte en los países desarrollados para el año 20203.
El estudio PLATINO (Proyecto Latinoamericano de Investigación en Obstrucción Pulmonar), realizado en 5 ciudades de América Latina, muestra cifras de limitación al flujo aéreo, medida por espirometría posbroncodilatación, que van del 7,8 al 19,7% en la población de 40 años o mayor, de acuerdo con el criterio de la Global Initiative for Chronic Obstructive Lung Disease (GOLD) de relación volumen espiratorio forzado en el primer segundo (FEV1)/capacidad vital forzada (FVC) inferior a 0,704. Por lo tanto, la situación de los países en desarrollo también es inquietante y genera un nuevo desafío para los programas de salud pública.
El importante impacto sanitario, social y económico de la EPOC ha llevado a las sociedades científicas a reunir a expertos en el tema con el fin de publicar y difundir guías para el manejo de pacientes con la enfermedad, para optimizar los recursos de diagnóstico, seguimiento y tratamiento5,6. Sin embargo, la adhesión a las pautas se mantiene baja, con grandes variaciones entre los países2,7,8.
Todas las pautas destacan la importancia de un diagnóstico correcto, guiado por síntomas y confirmado por espirometría. Recomiendan, entre otras estrategias de tratamiento, medidas preventivas como el cese del tabaquismo y la vacunación anual contra la gripe9,10, así como el tratamiento farmacológico broncodilatador, escalonado según los síntomas y la gravedad de la enfermedad, de preferencia por vía inhalada5,6.
El objetivo de este estudio es conocer el tratamiento de los pacientes con EPOC con diferente gravedad, en particular, el uso de medidas preventivas y medicación respiratoria, en 5 ciudades de América Latina y evaluar los posibles factores asociados al mismo.
Pacientes y métodosPLATINO es un estudio multicéntrico, de base poblacional y diseño transversal, para medir la prevalencia de EPOC en 5 ciudades de América Latina: Sao Paulo (Brasil), Ciudad de México (México), Montevideo (Uruguay), Santiago de Chile (Chile) y Caracas (Venezuela)4.
Se seleccionó por conglomerados, en múltiples etapas, una muestra representativa de personas de 40 años o más del área metropolitana de cada ciudad. Los detalles del método de selección y tamaño de la muestra poblacional se han publicado con anterioridad11. El protocolo de trabajo fue aprobado por el comité de ética de cada centro –Universidad Federal de Pelotas y Universidad Federal de Sao Paulo (Brasil), Universidad Pontificia Católica de Chile, Instituto Nacional de Enfermedades Respiratorias de México; Hospital Maciel Universidad de la República (Uruguay) y Universidad Central de Venezuela–y los participantes firmaron el consentimiento informado.
Los sujetos entrevistados completaron un cuestionario sobre síntomas y exposición a factores de riesgo, con especial interés en la historia de tabaquismo, y realizaron una espirometría pre y posbroncodilatador. El cuestionario, validado y estandarizado, se tradujo al español y al portugués.
Se realizó al 10% de los participantes de cada centro un cuestionario mínimo, en un plazo no mayor de 2 semanas, como control de calidad, y se observó una muy buena concordancia en todos los centros. Los cuestionarios están disponibles en internet (http://www.platino-alat.org).
Se obtuvieron retrospectivamente datos referidos a los últimos 12 meses sobre: consejo médico para dejar de fumar, vacunación antigripal, uso de cualquier medicación para "ayudar a la respiración", tipo de medicamento y frecuencia de uso. Se consignó el nombre comercial del fármaco, que posteriormente se codificó como: "cualquier broncodilatador", "esteroide" y/o "jarabes mucolíticos".
Las espirometrías, una basal y la segunda 15min después de la administración de 200μg de salbutamol, se realizaron de acuerdo con los criterios de aceptabilidad y reproducibilidad (entre 150 y 200ml) aceptados por diversos autores12,13. Los criterios de exclusión para la espirometría se describen en detalle en otra publicación14. Los espirómetros de tecnología ultrasónica (Easy One NDD, Medical Technologies, Zurich, Suiza) se revisaron diariamente, verificando la calibración con una jeringa de 3l (Hans Rudolf Inc., EE.UU.). Se siguieron estrictos controles de calidad en todos los centros y participaron técnicos capacitados y entrenados por el mismo equipo siguiendo las normativas del National Institute for Occupational Safety and Health (NIOSH).
El diagnóstico de EPOC se realizó siguiendo las normativas de la GOLD (FEV1/FVC < 0,7 posbroncodilatador). El diagnóstico médico previo se obtuvo de la información aportada por el propio paciente, según si algún médico le había dicho que tenía enfisema, bronquitis crónica o EPOC. De acuerdo con estos criterios diagnósticos se subdividió a los afectados de EPOC en 2 grupos para el análisis (con y sin diagnóstico médico previo de EPOC).
Análisis estadísticoLos datos cuantitativos se expresaron como la media de la variable ± desviación estándar, y los cualitativos como porcentaje. Se utilizó el test de la t de Student para analizar diferencia de medias y la prueba de la χ2 de Pearson para analizar la relación entre los datos cualitativos. Se aplicó un modelo de regresión logística para identificar las variables asociadas con el tratamiento según el diagnóstico y la gravedad de la enfermedad por espirometría. Se consideraron estadísticamente significativos los valores de p < 0,05.
Todos los análisis se realizaron con el paquete estadístico Stata versión 9.0 (Stata Corporation, College Station, TX, EE.UU., 2005).
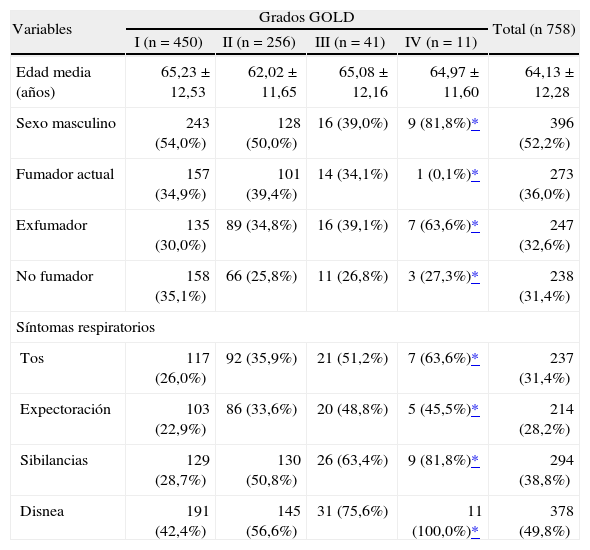
ResultadosDe un total de 6.711 sujetos elegibles en todos los centros, se completaron 5.571 cuestionarios y 5.315 espirometrías. Se dispuso de resultados válidos de espirometría posbroncodilatador e información sobre tratamiento en 5.229 participantes. En esta población se identificó a 758 pacientes con FEV1/FVC inferior a 0,7 posbroncodilatador, de los cuales el 59,4, el 33,8, el 5,4 y el 1,5% se hallaban en grados I, II, III y IV de la GOLD, respectivamente. Como se muestra en la tabla I, hubo diferencias estadísticamente significativas en relación con el sexo, la historia de tabaquismo y los síntomas respiratorios en los diferentes grupos de gravedad de la EPOC, mientras que la media de edad fue similar entre ellos.
Descripción de la población con EPOC, según gravedad (grados GOLD [Global Initiative for Chronic Obstructive Lung Disease])
| Variables | Grados GOLD | Total (n 758) | |||
| I (n = 450) | II (n = 256) | III (n = 41) | IV (n = 11) | ||
| Edad media (años) | 65,23 ± 12,53 | 62,02 ±11,65 | 65,08 ±12,16 | 64,97 ±11,60 | 64,13 ± 12,28 |
| Sexo masculino | 243 (54,0%) | 128 (50,0%) | 16 (39,0%) | 9 (81,8%)* | 396 (52,2%) |
| Fumador actual | 157 (34,9%) | 101 (39,4%) | 14 (34,1%) | 1 (0,1%)* | 273 (36,0%) |
| Exfumador | 135 (30,0%) | 89 (34,8%) | 16 (39,1%) | 7 (63,6%)* | 247 (32,6%) |
| No fumador | 158 (35,1%) | 66 (25,8%) | 11 (26,8%) | 3 (27,3%)* | 238 (31,4%) |
| Síntomas respiratorios | |||||
| Tos | 117 (26,0%) | 92 (35,9%) | 21 (51,2%) | 7 (63,6%)* | 237 (31,4%) |
| Expectoración | 103 (22,9%) | 86 (33,6%) | 20 (48,8%) | 5 (45,5%)* | 214 (28,2%) |
| Sibilancias | 129 (28,7%) | 130 (50,8%) | 26 (63,4%) | 9 (81,8%)* | 294 (38,8%) |
| Disnea | 191 (42,4%) | 145 (56,6%) | 31 (75,6%) | 11 (100,0%)* | 378 (49,8%) |
EPOC: enfermedad pulmonar obstructiva crónica.
Los datos se presentan como número de casos (porcentaje) o media ± desviación estándar.
Los sujetos previamente diagnosticados por un médico –86 de 758 (11,3%)– tenían significativamente más síntomas respiratorios, se habían realizado más espirometrías y presentaban mayor limitación al flujo aéreo. Estos datos han sido previamente publicados15.
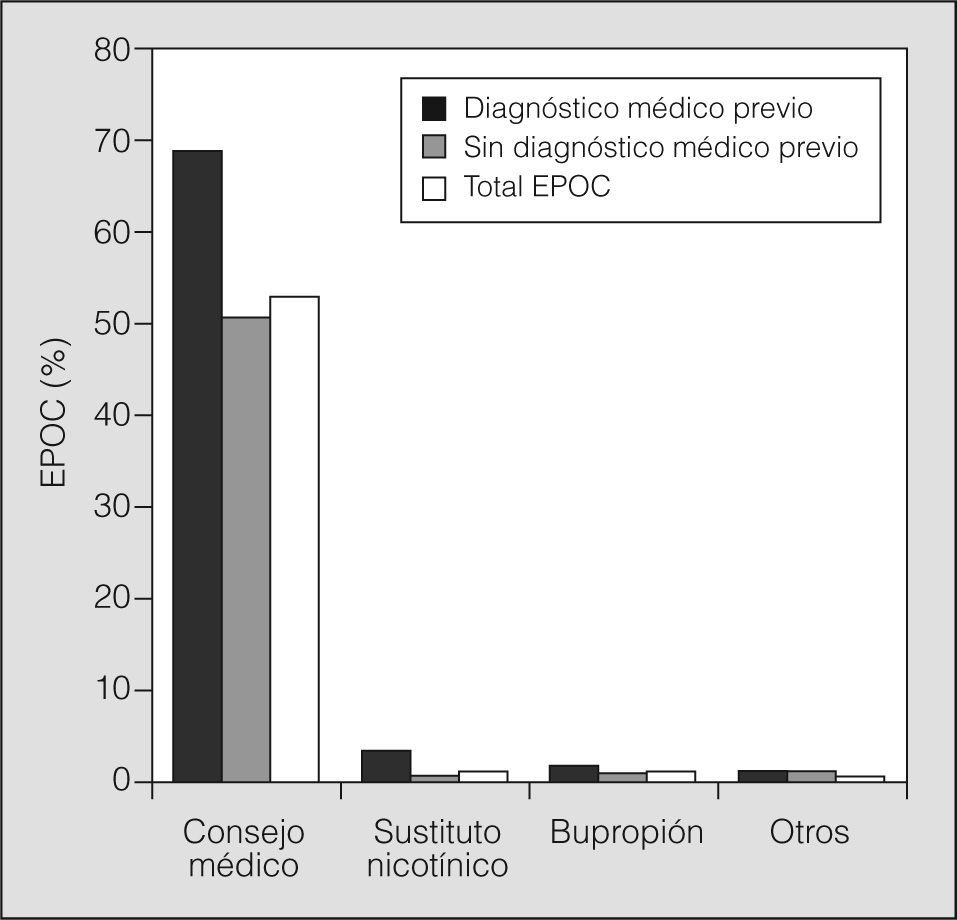
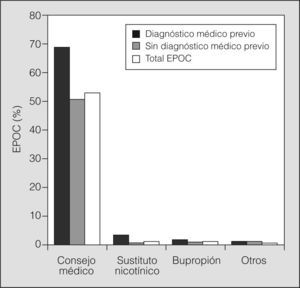
De todos los individuos diagnosticados de EPOC por espirometría, 519 (68,5%) tenían antecedentes tabáquicos (fumadores o exfumadores). En la figura 1 se muestran las intervenciones de abandono del tabaco en el total de pacientes con EPOC y de acuerdo con el diagnóstico médico previo. En la población total con EPOC, sólo la mitad había recibido consejo médico para dejar de fumar alguna vez en la vida, en tanto que el 69% de los pacientes con diagnóstico previo recibieron este consejo. La indicación de tratamiento farmacológico y no farmacológico para el cese del tabaquismo fue escasa en todos los grupos. Los datos fueron similares considerando los grados GOLD de la EPOC en los 5 centros participantes.
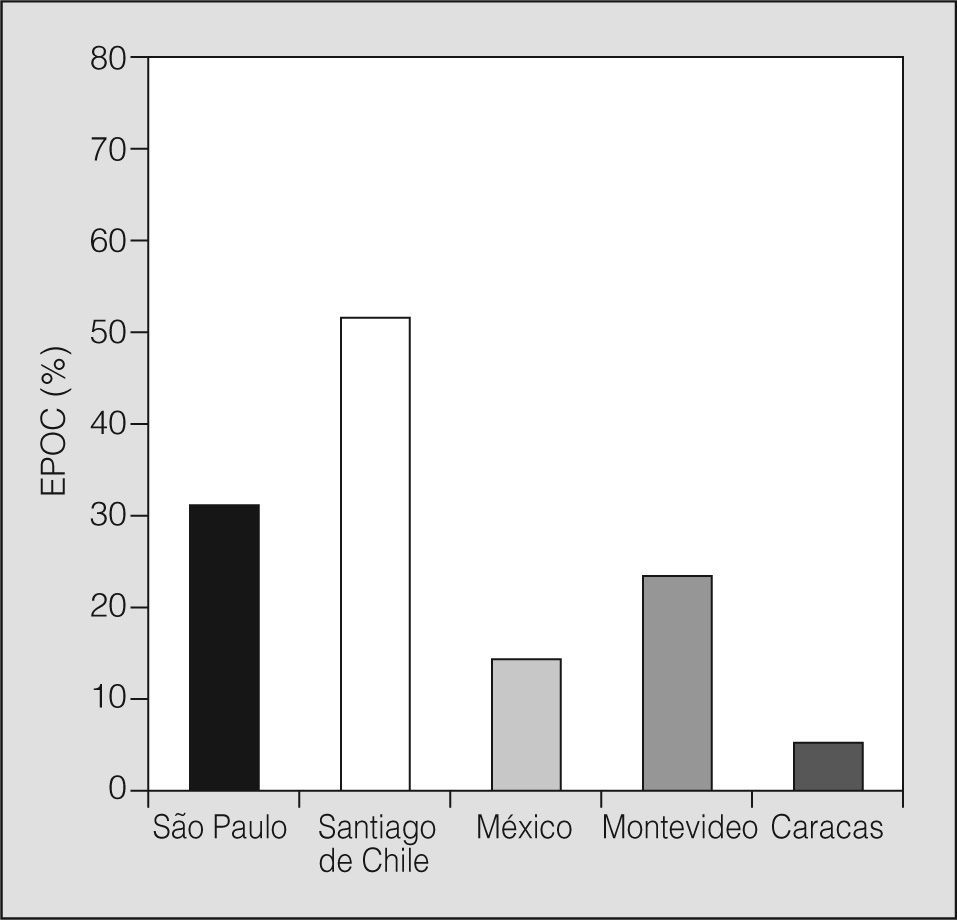
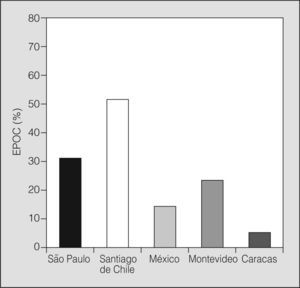
La prescripción de vacuna antigripal fue muy diferente en los distintos centros: desde un 5,1% en Caracas hasta un 52% en Santiago de Chile (fig. 2).
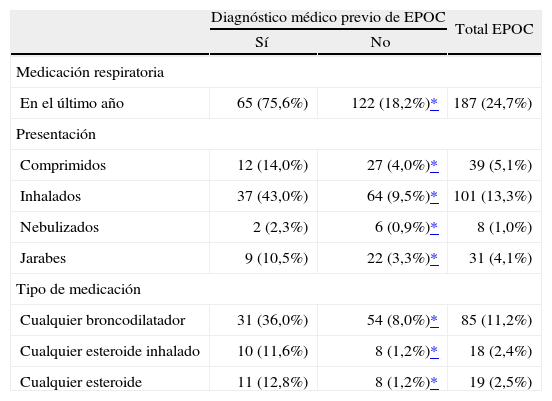
En la tabla II se muestra el uso de medicación respiratoria en la población total de EPOC y de acuerdo con el diagnóstico médico previo. Del total de 758 afectados de EPOC, sólo 187 (24,7%) habían recibido algún tipo de medicación respiratoria en el último año, mientras que las tres cuartas partes (75,6%) de los sujetos con diagnóstico médico previo la recibían. Los pacientes sin diagnóstico médico previo tenían un menor uso de cualquier tipo de medicación respiratoria comparados con los previamente diagnosticados.
Tratamiento farmacológico de los pacientes con EPOC de acuerdo con el diagnóstico médico previo
| Diagnóstico médico previo de EPOC | Total EPOC | ||
| Sí | No | ||
| Medicación respiratoria | |||
| En el último año | 65 (75,6%) | 122 (18,2%)* | 187 (24,7%) |
| Presentación | |||
| Comprimidos | 12 (14,0%) | 27 (4,0%)* | 39 (5,1%) |
| Inhalados | 37 (43,0%) | 64 (9,5%)* | 101 (13,3%) |
| Nebulizados | 2 (2,3%) | 6 (0,9%)* | 8 (1,0%) |
| Jarabes | 9 (10,5%) | 22 (3,3%)* | 31 (4,1%) |
| Tipo de medicación | |||
| Cualquier broncodilatador | 31 (36,0%) | 54 (8,0%)* | 85 (11,2%) |
| Cualquier esteroide inhalado | 10 (11,6%) | 8 (1,2%)* | 18 (2,4%) |
| Cualquier esteroide | 11 (12,8%) | 8 (1,2%)* | 19 (2,5%) |
EPOC: enfermedad pulmonar obstructiva crónica.
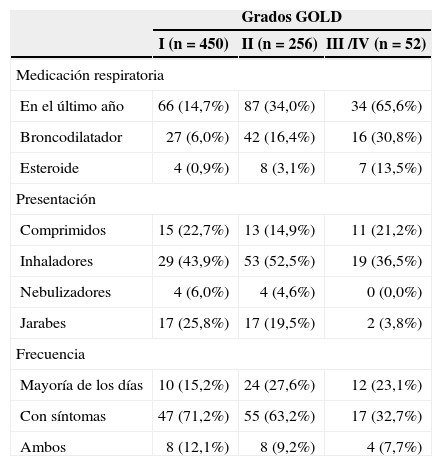
El uso de medicación respiratoria durante el último año en los pacientes con EPOC de acuerdo con los grados GOLD se muestra la tabla III. Estos resultados indican un aumento del tratamiento farmacológico a medida que progresa la gravedad de la enfermedad. El 65,4% de los pacientes más graves (grados III y IV) estaban en tratamiento farmacológico.
Medicación respiratoria en el último año, forma de presentación y frecuencia de uso por grados GOLD (Global Initiative for Chronic Obstructive Lung Disease)
| Grados GOLD | |||
| I (n = 450) | II (n = 256) | III /IV (n = 52) | |
| Medicación respiratoria | |||
| En el último año | 66 (14,7%) | 87 (34,0%) | 34 (65,6%) |
| Broncodilatador | 27 (6,0%) | 42 (16,4%) | 16 (30,8%) |
| Esteroide | 4 (0,9%) | 8 (3,1%) | 7 (13,5%) |
| Presentación | |||
| Comprimidos | 15 (22,7%) | 13 (14,9%) | 11 (21,2%) |
| Inhaladores | 29 (43,9%) | 53 (52,5%) | 19 (36,5%) |
| Nebulizadores | 4 (6,0%) | 4 (4,6%) | 0 (0,0%) |
| Jarabes | 17 (25,8%) | 17 (19,5%) | 2 (3,8%) |
| Frecuencia | |||
| Mayoría de los días | 10 (15,2%) | 24 (27,6%) | 12 (23,1%) |
| Con síntomas | 47 (71,2%) | 55 (63,2%) | 17 (32,7%) |
| Ambos | 8 (12,1%) | 8 (9,2%) | 4 (7,7%) |
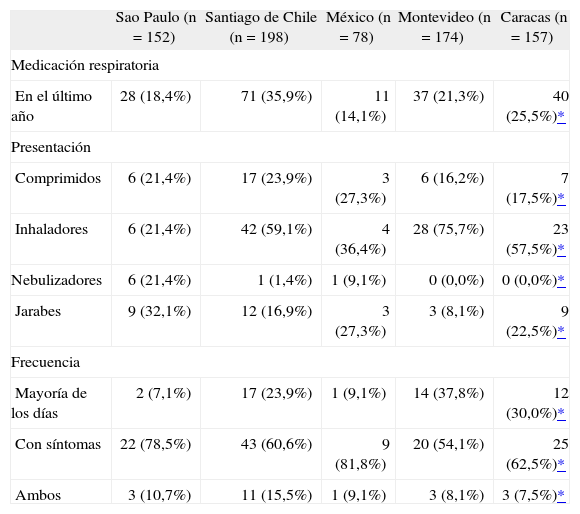
Los resultados sobre la medicación respiratoria en los pacientes con EPOC en los diferentes centros se muestran en la tabla IV. Sólo un 14,1% recibía medicación respiratoria en Ciudad de México, mientras que el 35,9% la recibía en Santiago de Chile. En Sao Paulo la utilización de tratamiento inhalado fue inferior a la de jarabes mucolíticos, mientras que en Santiago de Chile, Montevideo y Caracas el uso de inhaladores fue superior al 50%.
Uso de medicación respiratoria en el último año, forma de presentación y frecuencia de uso en pacientes con EPOC, por centros participantes
| Sao Paulo (n = 152) | Santiago de Chile (n =198) | México (n = 78) | Montevideo (n =174) | Caracas (n =157) | |
| Medicación respiratoria | |||||
| En el último año | 28 (18,4%) | 71 (35,9%) | 11 (14,1%) | 37 (21,3%) | 40 (25,5%)* |
| Presentación | |||||
| Comprimidos | 6 (21,4%) | 17 (23,9%) | 3 (27,3%) | 6 (16,2%) | 7 (17,5%)* |
| Inhaladores | 6 (21,4%) | 42 (59,1%) | 4 (36,4%) | 28 (75,7%) | 23 (57,5%)* |
| Nebulizadores | 6 (21,4%) | 1 (1,4%) | 1 (9,1%) | 0 (0,0%) | 0 (0,0%)* |
| Jarabes | 9 (32,1%) | 12 (16,9%) | 3 (27,3%) | 3 (8,1%) | 9 (22,5%)* |
| Frecuencia | |||||
| Mayoría de los días | 2 (7,1%) | 17 (23,9%) | 1 (9,1%) | 14 (37,8%) | 12 (30,0%)* |
| Con síntomas | 22 (78,5%) | 43 (60,6%) | 9 (81,8%) | 20 (54,1%) | 25 (62,5%)* |
| Ambos | 3 (10,7%) | 11 (15,5%) | 1 (9,1%) | 3 (8,1%) | 3 (7,5%)* |
EPOC: enfermedad pulmonar obstructiva crónica.
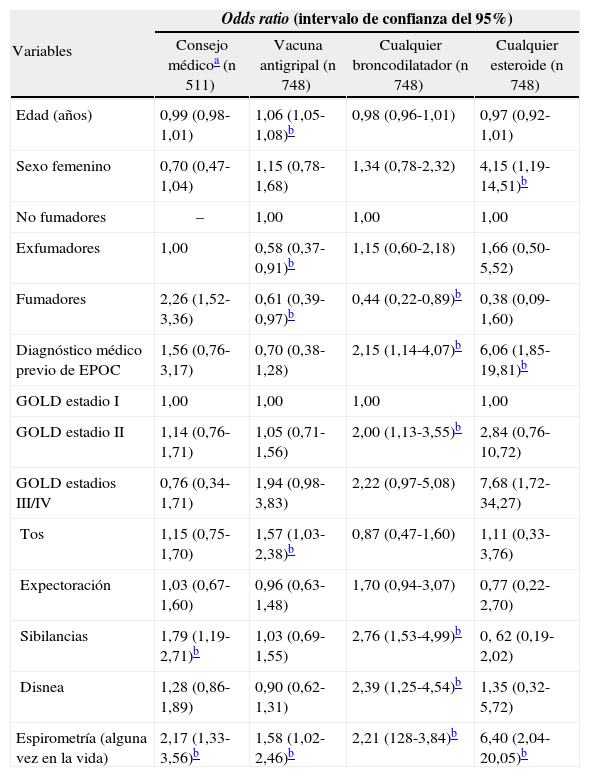
En la tabla V se exponen los factores asociados con algunos aspectos del tratamiento de la EPOC. Por lo que se refiere a la aplicación de medidas preventivas, el consejo médico para el abandono del tabaco se asoció a la presencia de síntomas respiratorios (sibilancias), independientemente del grado de obstrucción bronquial, y la vacunación antigripal, a mayor edad y presencia de tos. El uso de medicación respiratoria broncodilatadora estuvo asociado al diagnóstico médico previo y a la presencia de síntomas respiratorios tales como sibilancias y disnea, mientras que la probabilidad de recibir esteroides fue mayor en mujeres, con diagnóstico médico previo y mayor gravedad de la enfermedad, independientemente de los síntomas respiratorios.
Análisis de regresión logística de los factores asociados a las medidas preventivas y tratamiento farmacológico de los pacientes con EPOC
| Variables | Odds ratio (intervalo de confianza del 95%) | |||
| Consejo médicoa (n 511) | Vacuna antigripal (n 748) | Cualquier broncodilatador (n 748) | Cualquier esteroide (n 748) | |
| Edad (años) | 0,99 (0,98-1,01) | 1,06 (1,05-1,08)b | 0,98 (0,96-1,01) | 0,97 (0,92-1,01) |
| Sexo femenino | 0,70 (0,47-1,04) | 1,15 (0,78-1,68) | 1,34 (0,78-2,32) | 4,15 (1,19-14,51)b |
| No fumadores | – | 1,00 | 1,00 | 1,00 |
| Exfumadores | 1,00 | 0,58 (0,37-0,91)b | 1,15 (0,60-2,18) | 1,66 (0,50-5,52) |
| Fumadores | 2,26 (1,52-3,36) | 0,61 (0,39-0,97)b | 0,44 (0,22-0,89)b | 0,38 (0,09-1,60) |
| Diagnóstico médico previo de EPOC | 1,56 (0,76-3,17) | 0,70 (0,38-1,28) | 2,15 (1,14-4,07)b | 6,06 (1,85-19,81)b |
| GOLD estadio I | 1,00 | 1,00 | 1,00 | 1,00 |
| GOLD estadio II | 1,14 (0,76-1,71) | 1,05 (0,71-1,56) | 2,00 (1,13-3,55)b | 2,84 (0,76-10,72) |
| GOLD estadios III/IV | 0,76 (0,34-1,71) | 1,94 (0,98-3,83) | 2,22 (0,97-5,08) | 7,68 (1,72-34,27) |
| Tos | 1,15 (0,75-1,70) | 1,57 (1,03-2,38)b | 0,87 (0,47-1,60) | 1,11 (0,33-3,76) |
| Expectoración | 1,03 (0,67-1,60) | 0,96 (0,63-1,48) | 1,70 (0,94-3,07) | 0,77 (0,22-2,70) |
| Sibilancias | 1,79 (1,19-2,71)b | 1,03 (0,69-1,55) | 2,76 (1,53-4,99)b | 0, 62 (0,19-2,02) |
| Disnea | 1,28 (0,86-1,89) | 0,90 (0,62-1,31) | 2,39 (1,25-4,54)b | 1,35 (0,32-5,72) |
| Espirometría (alguna vez en la vida) | 2,17 (1,33-3,56)b | 1,58 (1,02-2,46)b | 2,21 (128-3,84)b | 6,40 (2,04-20,05)b |
EPOC: enfermedad pulmonar obstructiva crónica. GOLD: Global Initiative for Chronic Obstructive Lung Disease.
La condición de fumador se asoció tanto a las medidas preventivas como a la indicación de broncodilatadores.
Todas las medidas terapéuticas analizadas se asociaron con el hecho de haber realizado una espirometría alguna vez en la vida.
DiscusiónPLATINO es el primer estudio de base poblacional sobre la prevalencia de EPOC en Latinoamérica en que el diagnóstico se establece por espirometría tras broncodilatación y que utiliza protocolos estandarizados y reproducibles en todos los centros. En tal sentido, ofrece una excelente oportunidad para conocer las pautas de tratamiento en las 5 ciudades participantes y comparar estos resultados con la situación en otros países. Además, son escasos los estudios de base poblacional publicados que valoran el tratamiento general de los pacientes con EPOC2,16. De esta forma, PLATINO contribuye con una importante aportación de datos epidemiológicos sobre la EPOC, a la que Chapman et al17 han caracterizado como una enfermedad pobremente reconocida, infradiagnosticada y, en consecuencia, infratratada.
Los resultados más relevantes se refieren al insuficiente consejo médico y la escasa utilización de los tratamientos farmacológicos para el cese del tabaquismo, así como a las diferencias en la aplicación de la vacuna antigripal y del uso de medicación respiratoria que se observan entre los centros participantes. El empleo de medicación respiratoria se asoció al diagnóstico médico previo, al hecho de haberse realizado una espirometría alguna vez en la vida y a la gravedad de la enfermedad.
En la EPOC interviene una serie de procesos patológicos que interactúan entre sí generando lo que se ha denominado "círculo vicioso" de la enfermedad18. Promover el abandono del tabaco, como se reconoce desde hace más de una década, es el único recurso terapéutico, hasta el momento, de probada eficacia para modificar el deterioro acelerado de la función pulmonar9. De acuerdo con Fiore19, el simple consejo médico para el cese del tabaquismo aumenta el número de fumadores que dejan de fumar hasta en un 4%. Por su parte, Anthonisen et al20 mostraron en el Lung Health Study III, con datos de seguimiento a 11 años, una tasa de abstinencia del 22% en el grupo de fumadores en que se realizó intervención médica intensiva, y el 93% de estos individuos se mantuvo sin fumar durante ese período. Los datos aportados por PLATINO muestran que sólo la mitad de la población con historia previa de tabaquismo había recibido consejo médico para el cese. Los tratamientos farmacológicos que se han mostrado efectivos para mejorar el éxito de los programas de cese de tabaquismo, como los antidepresivos y sustitutos nicotínicos, apenas se utilizaron5.
Por otro lado, todas las guías de tratamiento de la EPOC5,6,21,22 recomiendan la vacunación anual antigripal para evitar complicaciones e incluso reducir la mortalidad, sobre todo en la población de mayor edad10. Los datos de PLATINO muestran importantes diferencias en la aplicación de esta vacuna entre los centros. La mayor cobertura se registró en Santiago de Chile, donde alcanzó alrededor de la mitad de los sujetos, mientras que la mínima aplicación se observó en Caracas (5,1%), hallazgo que podría estar vinculado con el clima tropical, sin variaciones de estación definidas y, por tanto, sin períodos epidémicos del virus de la gripe. La indicación de esta medida preventiva estuvo asociada a mayor edad, independientemente de la gravedad de la enfermedad. Estos resultados son coincidentes con los datos de consenso de infecciones respiratorias publicados recientemente23.
En España el estudio IBERPOC2 mostró que sólo un 19,3% de todos los pacientes con EPOC estaban tratados con medicación respiratoria, más comúnmente en el grupo de mayor gravedad (49,3%). Recientemente un estudio realizado en Corea encontró que un 49% de los afectados de EPOC mayores de 45 años recibía medicación respiratoria, cuyo uso aumentaba con la gravedad de la obstrucción bronquial (un 11,8% entre aquéllos en grados I y II, frente al 36,4% de los pacientes con EPOC en grados III y IV)16. Los resultados del estudio PLATINO coinciden con los anteriores e indican que sólo la cuarta parte de la totalidad de los individuos diagnosticados estaban en tratamiento, aumentando el uso de medicación con la gravedad de la enfermedad (grados III y IV). Analizando a los 86 individuos con diagnóstico médico previo y confirmado como EPOC por PLATINO, un 75,6% recibía medicación respiratoria, cifra algo menor que la encontrada en el estudio IBERPOC (88%)2.
Si bien los broncodilatadores son el tratamiento central de la EPOC, los datos de PLATINO muestran el bajo uso de los broncodilatadores inhalados y la variabilidad entre los centros. Esto podría estar vinculado con la falta de disponibilidad de estos fármacos por razones económicas, pero no puede descartarse el desconocimiento entre los médicos de las ventajas de esta vía sobre la oral. La falta de datos provenientes de estudios de base poblacional sobre el uso del tratamiento broncodilatador impide establecer comparaciones con los presentes resultados.
Además, el uso de broncodilatadores en sujetos con EPOC depende del nivel de atención y muestra una amplia variabilidad en diversos países (un 19% en Italia y un 54% en el Reino Unido)24. Miravitlles25 señala que esta situación se produce fundamentalmente por diferencias entre el manejo clínico diario y el uso de pautas normativizadas. En el mismo sentido, el estudio IDENTEPOC26, que investigó los factores determinantes del tratamiento farmacológico en estos pacientes, destaca que las diferencias en la forma de medicación reflejan que los médicos toman sus propias decisiones y que no necesariamente siguen las guías terapéuticas. Por otra parte, datos provenientes de grupos seleccionados, como la población participante del estudio ISOLDE27 en el momento del ingreso, muestran que los pacientes con EPOC grave (FEV1 del 44%) recibían broncodilatadores inhalados en más del 90% de los casos.
Los esteroides inhalados están fundamentalmente indicados en los pacientes con EPOC de grados más avanzados, con exacerbaciones frecuentes. No se recomienda su uso por vía oral, excepto durante las exacerbaciones5. Apenas un 5% de los casos de EPOC diagnosticados por PLATINO recibía fármacos antiinflamatorios, ya fuera por vía inhalada (2,4%) o por vía oral (2,5%). Si bien su uso estuvo asociado a la gravedad de la enfermedad, sólo alcanzó a un 13,5% de los afectados de EPOC con FEV1 inferior al 50%. En Europa la prescripción de esteroides varía entre países: un 9% en Alemania y un 22% en Reino Unido, en tanto que en Francia se ha publicado una proporción de pacientes tratados con esteroides inhalados mayor que la esperada para la gravedad de la enfermedad8. Esta variabilidad también se observa a lo largo del tiempo, de modo que las cifras más recientes van de un 26 a un 76%25,26.
Es poca la evidencia científica que respalda el tratamiento mucolítico o los jarabes para la EPOC, por lo que no se ha recomendado su uso amplio28. Los resultados de PLATINO indican que hasta una quinta parte de los sujetos (19,8%) recibía este tipo de medicación, que en el caso de Sao Paulo superaba a la utilización del tratamiento inhalado. Los datos publicados en Francia y Alemania muestran que un tercio de los pacientes con EPOC recibe jarabes mucolíticos24.
La espirometría es un indicador de mejor información por parte de los médicos o servicios clínicos en relación con el diagnóstico y tratamiento de la EPOC. PLATINO mostró que su realización previa estuvo asociada tanto al uso de medidas preventivas como a la prescripción de broncodilatadores y esteroides, lo que apoya la evidencia existente de que la disponibilidad de esta técnica optimiza el tratamiento de la enfermedad.
Una de las limitaciones del presente estudio es que los datos sobre el uso de medicación respiratoria se referían al último año, por lo que puede que se infravalorase su empleo (sesgo de memoria); sin embargo, este tiempo de recuerdo es considerado aceptable por otros autores29. Otro aspecto que debe tenerse en cuenta es que la mayoría de los individuos identificados por PLATINO se encontraban en el grado I de la enfermedad; por tanto, los datos globalmente analizados pueden disminuir los resultados.
Las grandes variaciones en cuanto al tratamiento entre los 5 grandes centros urbanos estudiados permiten esperar cuando menos una mayor variabilidad en el tratamiento que se ofrece en las amplias regiones de América Latina, sobre todo si tenemos en cuenta las zonas rurales. Esto genera la imperiosa necesidad de impulsar la formación continuada tanto de los médicos como del personal de salud involucrados en la atención de los pacientes con EPOC, y de promover la implementación de programas nacionales de diagnóstico y tratamiento para esta importante enfermedad, que va en aumento.
En conclusión, PLATINO aporta datos sobre las medidas preventivas y el tratamiento farmacológico de la EPOC estable en 5 ciudades de Latinoamérica, mostrando una desigual utilización de los recursos disponibles de probada eficacia, en particular la aplicación del consejo médico para el cese del tabaquismo. La espirometría fue el principal factor asociado con la indicación de todas las medidas terapéuticas. Surge así como una herramienta fundamental no sólo para el diagnóstico temprano de la enfermedad, sino también a la hora de la toma de decisiones terapéuticas, por lo que deben realizarse todos los esfuerzos para promover su uso extensivo.
AgradecimientosEl estudio PLATINO fue un proyecto original de la Asociación Latinoamericana del Tórax (ALAT) a través de su Comité Ejecutivo (Dres. Juan Manuel Luna, Carmen Lisboa, Carlos Torres y Carlos Luna). También queremos dar las gracias al Comité Asesor de PLATINO (Dres. Bartolomé Celli y Roberto Rodríguez Roisin) por sus permanentes aportaciones, junto al grupo de investigadores de Burden of Obstructive Lung Disesase (BOLD), la Dra. Sonia Buist y el Dr. William Vollmer.
Boehringer-Ingelheim ha financiado el estudio, pero no ha contribuido a la redacción del protocolo, a la conducción del estudio ni a la escritura del presente trabajo.
María Márquez, Pedro Hallal, Dolores Moreno, Fernanda Rosa y Aquiles Camelier.