Las causas más frecuentes de patología obstructiva no maligna de la vía aérea central son las estenosis postintubación y postraqueotomía, seguidas por los cuerpos extraños y la traqueobroncomalacia. Otras causas, como las secundarias a procesos infecciosos y enfermedades sistémicas, son menos frecuentes. A pesar de la existencia de numerosas clasificaciones, todavía no se ha alcanzado consenso sobre la utilización de alguna de ellas en concreto. Un mejor conocimiento de su fisiopatología nos ha permitido aumentar el diagnóstico y mejorar su tratamiento; su presentación clínica inespecífica exige la realización de diversos estudios funcionales, radiológicos y fundamentalmente endoscópicos para su correcto diagnóstico. El tratamiento debe ser multidiciplinario e individualizado, requiriendo tratamiento quirúrgico o endoscópico mediante diferentes técnicas termoablativas y mecánicas.
The most common causes of non-malignant central airway obstruction are post-intubation and post-tracheostomytracheal stenosis, followed by the presence of foreign bodies, benign endobronchial tumours and tracheobronchomalacia. Other causes, such as infectious processes or systemic diseases, are less frequent. Despite the existence of numerous classification systems, a consensus has not been reached on the use of any one of them in particular. A better understanding of the pathophysiology of this entity has allowed us to improve diagnosis and treatment. For the correct diagnosis of nonspecific clinical symptoms, pulmonary function tests, radiological studies and, more importantly, bronchoscopy must be performed. Treatment must be multidisciplinary and tailored to each patient, and will require surgery or endoscopic intervention using thermoablative and mechanical techniques.
La patología obstructiva de la vía aérea central, tráquea y bronquios principales, representa un problema común entre especialidades médicas y quirúrgicas. La incidencia de esta patología parece estar aumentando a causa del cáncer de pulmón; no obstante, también lo está haciendo como consecuencia del creciente diagnóstico de patologías obstructivas no malignas, fundamentalmente debido al uso de vías aéreas artificiales1. El manejo multidisciplinario y el progreso en la utilización de diferentes herramientas radiológicas y endoscópicas han permitido mejorar el diagnóstico y el tratamiento de estas patologías.
Se propone en esta revisión el desarrollo de las causas de obstrucción no maligna de la vía aérea central que a nuestro entender son más relevantes. Las secundarias a intubación y traqueotomía, las relacionadas con traqueobroncomalacia (TBM), procesos infecciosos (tuberculosis) y enfermedades sistémicas (sarcoidosis, amiloidosis, enfermedad de Wegener, policondritis recidivante y traqueobroncopatía osteocondroplástica). Por último, la estenosis traqueal idiopática y la estenosis bronquial postrasplante pulmonar.
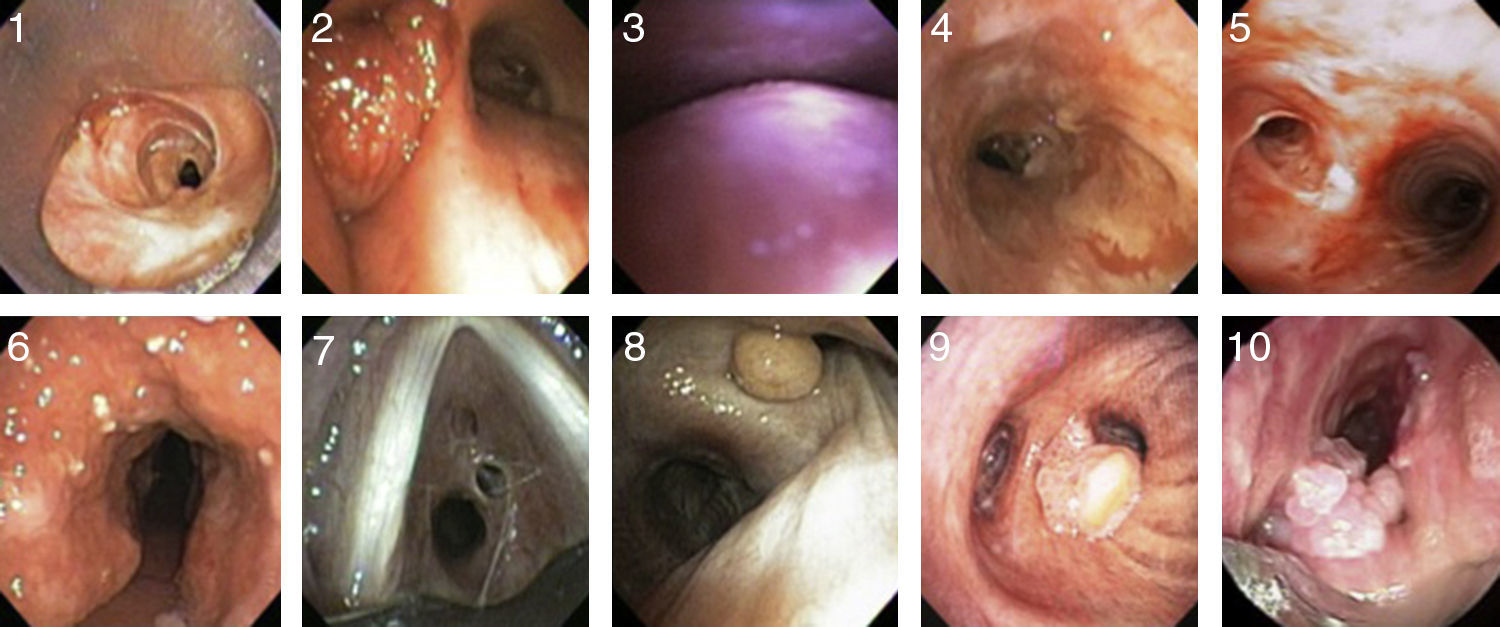
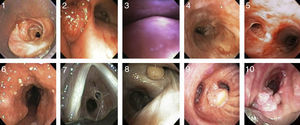
Etiología y clasificaciónLas causas que pueden conducir a la obstrucción de la vía aérea central son muy diversas (tabla 1), siendo las más frecuentes las relacionadas con la intubación orotraqueal y la realización de traqueotomías. La traqueomalacia, entidad cada vez más reconocida, también es una causa importante. Otras causas menos comunes son las enfermedades inflamatorias crónicas (amiloidosis, sarcoidosis y policondritis recidivante), las enfermedades infecciosas (tuberculosis y el rinoescleroma) y las enfermedades colágeno-vasculares (granulomatosis con poliangitis o enfermedad de Wegener y el lupus). Los pacientes trasplantados de pulmón pueden presentar estenosis o malacia a nivel de la anastomosis, la cual puede ser sintomática. Finalmente, si no existe una causa específica, se hablaría de una estenosis traqueal idiopática2,3. Existen otras causas de obstrucción, como la compresión extrínseca por linfadenopatías o masas cervicales, la obstrucción por tumoraciones endoluminales benignas (fig. 1, imágenes 8, 9 y 10), la lesión por radiación e inhalación, y la aspiración de cuerpos extraños, que no serán revisadas en este manuscrito.
Condiciones asociadas con obstrucción no maligna de la vía aérea central
| Linfadenopatías |
| Infecciosas |
| Enfermedades inflamatoriasSarcoidosisEnfermedad de WegenerVasculares |
| Anillos |
| Variantes anatómicas |
| Tejido de granulación |
| Tubos endotraqueales |
| Tubos de traqueostomía |
| Stents de vía aérea |
| Cuerpos extraños |
| Anastomosis quirúrgicas |
| Granulomatosis de Wegener |
| Seudotumor |
| Hamartomas |
| Amiloide |
| Papilomatosis |
| HiperdinámicasTraqueobroncomalaciaColapso excesivo de la pared membranosa |
| Idiopáticas |
| Tuberculosis |
| Sarcoidosis |
| Otras |
| Bocio |
| Tapón de moco |
| Parálisis de cuerdas vocales |
| Epiglotitis |
| Coágulo de sangre |
Imágenes de diferentes tipos de patología obstructiva no maligna de la vía aérea. 1) Estenosis postintubación. 2) Tejido de granulación secundario a stent de silicona. 3) Traqueobroncomalacia. 4) Estenosis secundaria a granulomatosis de Wegener. 5) Estenosis secundaria a tuberculosis. 6) Traqueobroncopatía osteocondroplástica. 7) Estenosis idiopática. 8) Hamartoma. 9) Papiloma solitario. 10) Papilomatosis.
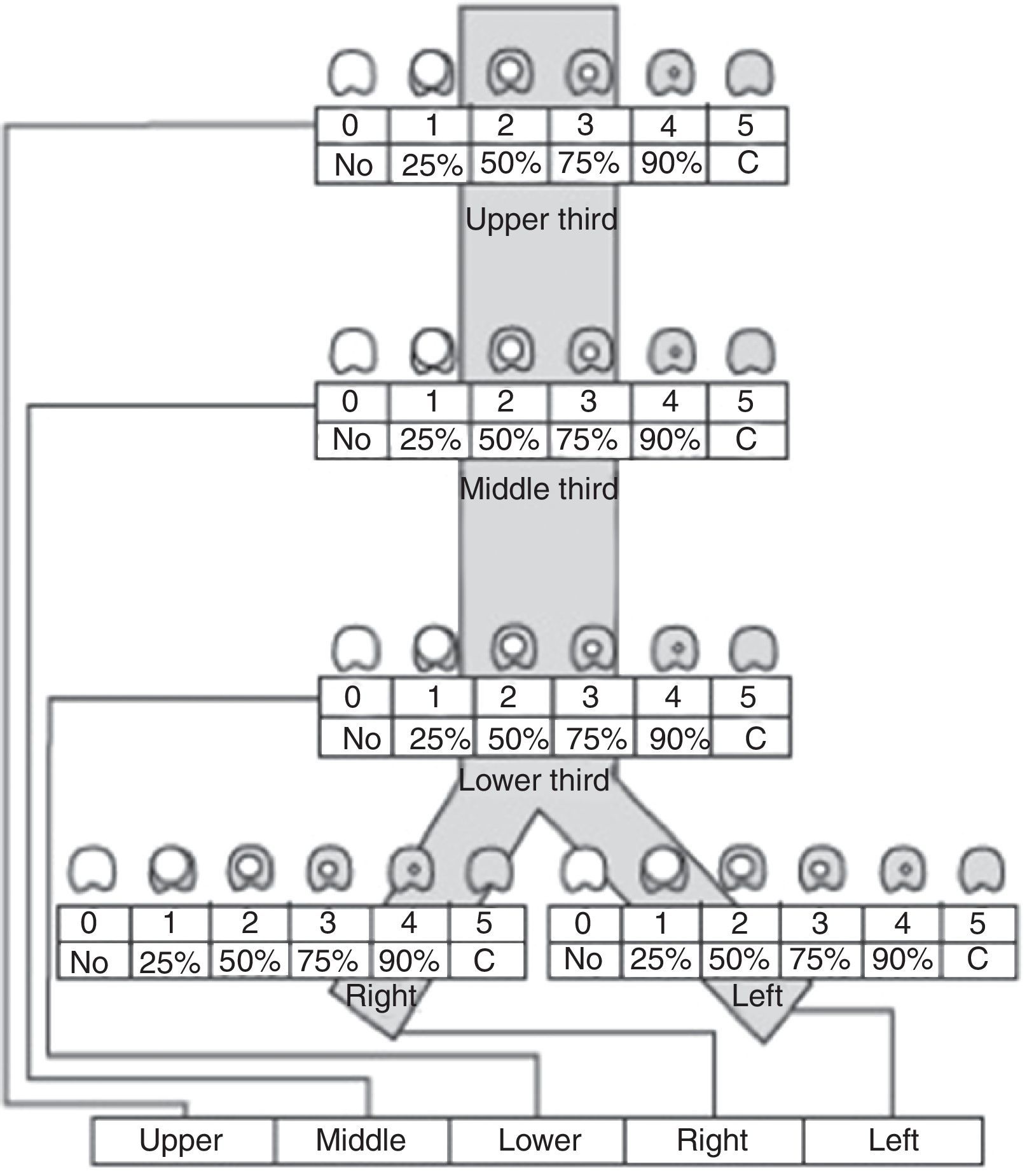
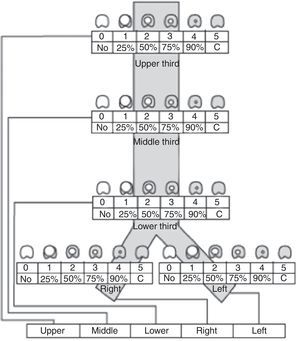
Recientemente Freitag et al.4 han publicado una clasificación de las estenosis que pretende llevar a cabo una división desde un punto de vista fundamentalmente dinámico y estructural, añadiendo también el grado de estenosis y su localización. Desafortunadamente esta clasificación es compleja y no ha logrado obtener acogida universal (fig. 2).
Esquema de clasificación de las estenosis según la localización, grado y tipo de estenosis, propuesto por Freitag et al.4.
Consideramos que lo más importante es diferenciar las estenosis simples de las complejas, puesto que esto determina el éxito o fracaso de la intervención endoscópica. Definimos una estenosis compleja como aquella que presenta una o varias de las siguientes características: larga (>10mm), tortuosa, con presencia de contracciones o daño cartilaginoso asociado a malacia. Todas estas situaciones dificultan el tratamiento endoscópico, siendo la cirugía el método terapéutico de elección.
Presentación clínicaDisnea y tos en grado variable, estridor y sibilancias, son el espectro clínico de esta entidad. La presentación clínica dependerá no solo de la enfermedad subyacente sino también de la localización de la lesión, del grado de estrechamiento de la luz y de la velocidad de progresión de esta. Otros factores como el estado previo de salud del paciente parecen desempeñar un papel importante en el desarrollo y resultado final del proceso. Hasta un 54% de los pacientes con estenosis traqueal comienzan con un distrés respiratorio5 debido a que previamente a la aparición de los síntomas se ha producido una importante y progresiva pérdida del diámetro de la luz de la vía aérea. La mayoría de los pacientes, durante un tiempo variable, son erróneamente diagnosticados de asma de control difícil o bronquitis crónica recurrente debido a la similitud de los síntomas y a la mejoría parcial de estos con la administración de corticoides, broncodilatadores y antibióticos. La persistencia de los síntomas a pesar del tratamiento junto con una alta sospecha clínica debe facilitar el diagnóstico correcto.
Evaluación diagnósticaLos estudios diagnósticos más frecuentemente utilizados son las pruebas de función pulmonar, la tomografía axial computarizada (TAC) y la broncoscopia6.
Las pruebas de función pulmonar son útiles tanto para el diagnóstico como para el seguimiento tras una intervención. Ante una estenosis traqueal se observa una tendencia al aplanamiento de la curva flujo-volumen, tanto inspiratoria como espiratoria, lo que depende de la localización y de las características de la lesión7. Normalmente esta alteración no es evidente hasta que la luz traqueal es menor de 10mm. Así como las obstrucciones extratorácicas variables presentan un aplanamiento en la curva inspiratoria, las obstrucciones intratorácicas muestran un aplanamiento en la curva espiratoria. Finalmente, las obstrucciones fijas presentan un aplanamiento en ambas curvas.
Con la TAC multidetector se adquieren cortes axiales extremadamente finos que permiten hacer reconstrucciones en 3 dimensiones, de gran utilidad en el diagnóstico, planificación de procedimientos y seguimiento de estos pacientes. Por otra parte, la TAC dinámica ha resultado ser un método de imagen efectivo y no invasivo para el diagnóstico de la TBM8–11.
Tanto la broncoscopia flexible como la rígida facilitan una visión directa de la lesión, permitiendo evaluar el grado de estrechamiento de la luz, el estado de la mucosa, la longitud, la forma, y la distancia de la estenosis con respecto a las cuerdas vocales y a la carina principal. Además permiten la toma de muestras para cultivo microbiológico, estudio citológico y anatomopatológico6,12.
En muchos casos es importante descartar la enfermedad por reflujo gastroesofágico (ERGE) mediante el uso de pH-metría, puesto que se ha establecido la relación entre esta y la estenosis laringotraqueal. La ERGE tiene un papel importante en su desarrollo y en el fallo persistente de su tratamiento, así como en la formas idiopáticas de estenosis traqueal13,14.
Estenosis traqueal postintubación y postraqueotomíaLa incidencia de estenosis traqueal postintubación (ETPI) y postraqueotomía (ETPT) oscila entre el 10-22%15,16, pero solo el 1-2% requiere tratamiento17. Hoy, la ETPI y ETPT, son entidades reconocidas con una incidencia de 4,9 casos por millón de habitantes18.
La ETPI ocurre en el lugar de asentamiento del manguito del tubo en un tercio de los casos16(fig. 1, imagen 1). La principal causa parece ser la pérdida de flujo sanguíneo en dicha región debido a la presión ejercida por el manguito. Dicha isquemia empieza en las primeras horas tras la intubación y se resuelve a modo de banda fibrosa en unas 3-6 semanas19,20. Afortunadamente la aparición de manguitos de baja presión y la monitorización rutinaria de esta han reducido su incidencia21. El tipo de estenosis en banda es el más frecuentemente encontrado22.
Por el contrario, la ETPT se produce como consecuencia de un proceso anormal de reparación tisular con formación de excesivo tejido de granulación alrededor del estoma (fig. 1, imagen 2), e incluso sobre o a través del cartílago previamente dañado durante el procedimiento sobre la pared anterior de la tráquea16. Las formas de estenosis encontradas son muy variadas, incluyendo en forma de «A», circunferencial y tejido de granulación, entre otras22. Además, muchas veces se asocian a traqueomalacia focal (fig. 1, imagen 3).
Otros factores que se han relacionado con el desarrollo de ETPI y ETPT son la altura del estoma de traqueotomía, la intubación prolongada, una intubación traumática, historia de intubación o traqueotomía previa, altas dosis de corticoides, edad avanzada, sexo femenino, fallo respiratorio severo, ERGE severa, enfermedades autoinmunes asociadas, síndrome de apnea-hipopnea del sueño y radioterapia local23. En este sentido, todavía no existe consenso respecto al momento en que un paciente con intubación orotraqueal y conectado a ventilación mecánica debe ser sometido a una traqueotomía. Así, Stauffer et al. afirman que una intubación inferior a 20 días no se relaciona con complicaciones o secuelas laringotraqueales, asociando las posibles complicaciones a una mala técnica24. Por el contrario, Whited no recomienda que la intubación exceda de los 5 días, habiendo encontrado por encima de este tiempo una elevada incidencia de lesiones laringotraqueales25. En nuestra opinión, a aquellos pacientes que requieran ventilación mecánica prolongada se les debe realizar una traqueotomía entre el día 7-14 para minimizar las complicaciones secundarias a la intubación.
Si se compara la longitud de estas lesiones se aprecia que las estenosis postintubación presentan una longitud media de 2,6cm, mientras que las postraqueotomía son de 1,2cm26.
El perfil típico del paciente con ETPI o ETPT es el de una mujer fumadora, obesa, con diabetes mellitus, hipertensión arterial y enfermedad cardiovascular. La obesidad se relaciona con un aumento de la circunferencia del cuello, incrementando el riesgo de trauma y fractura del cartílago durante la traqueotomía. Los pacientes con diabetes mellitus y enfermedad cardiovascular tendrían oclusión microvascular que contribuiría a la isquemia causada por la presión del manguito durante la intubación27,28.
El abordaje de las estenosis en este tipo de pacientes varía dependiendo de la presentación clínica, la localización de la lesión, la gravedad y el tipo de estenosis, el mecanismo por el que se haya producido y la presencia de comorbilidades. Todas estas variables, junto con la experiencia del cirujano y el endoscopista, determinarán la opción terapéutica más adecuada.
Las medidas terapéuticas endoscópicas actualmente más empleadas son la dilatación mecánica con balón neumático, la aplicación de láser CO2 o NdYAG y la colocación de prótesis endoluminales29.
De la misma forma que el mecanismo patogénico de la ETPI y el de la ETPT son distintos, también se defiende un tratamiento diferente. Zias et al. postulan que el tratamiento óptimo de las estenosis postintubación se realiza mediante la aplicación de incisiones radiales de láser con la ayuda asociada de dilataciones con balón. Por el contrario defienden el uso del láser como herramienta debridadora del excesivo tejido de granulación que tiene lugar en las estenosis postraqueotomía22.
La cirugía abierta desempeña un papel importante en el tratamiento de las estenosis de tipo compleja y recurrentes, donde se lleva a cabo la resección quirúrgica del segmento estenosado y la posterior unión término-terminal. No existe consenso pero se aboga por un tratamiento individualizado en centros de referencia con una gran experiencia. Grillo y Mathisen30 encontraron una mortalidad quirúrgica del 1,8%, pero otros han hallado unas tasas cercanas al 5%. Las complicaciones llegan al 14% y están en relación con la reestenosis, granulomas en el sitio de sutura, infecciones, hemorragias y enfisema subcutáneo31,32.
Para aquellos pacientes con estenosis complejas que no son susceptibles de tratamiento quirúrgico, o bien esta opción es fallida, se recomienda la utilización de stents de silicona, concretamente los de tipo Dumon33,34.
En pacientes con severas comorbilidades o en pacientes con estenosis de tipo simple los procedimientos endoscópicos pueden servir como puente hacia la cirugía, pero más importante, pueden ser curativos35. De hecho hoy en día se están convirtiendo en el tratamiento inicial de elección. Galluccio et al. demostraron poder tratar de forma definitiva el 96% de las estenosis simples y el 69% de las complejas, solo mediante técnicas broncoscópicas36.
La dilatación endoscópica efectuada mediante el uso de un balón emplea únicamente fuerzas radiales para reducir al mínimo el daño mecánico en la mucosa, al tiempo que permite un mejor control visual del procedimiento. Está indicada como ayuda a otras técnicas endoscópicas a distintos niveles de la vía aérea o de forma aislada ante estenosis simples, cortas, y que no obstruyen por completo la luz de la vía aérea, con suficiente aval por la literatura científica37.
La aplicación de láser solo será útil en lesiones pequeñas, estrechas, de longitud craneocaudal reducida y esqueleto cartilaginoso estable, aunque su uso se ha extendido y generalizado, presentando igualmente buenos resultados y bajo riesgo ante lesiones mayores. Proporciona un elevado porcentaje de decanulación con un reducido tiempo operatorio y una estancia hospitalaria baja38. Para estenosis en banda, existe una variante de la técnica que consiste en realizar cortes radiales con láser o con el cuchillo del electrocauterio a las 3, 9 y 12′ del campo antes de la dilatación38–40.
El microdebridador ha demostrado ser efectivo en las lesiones con excesivo tejido de granulación41–43.
La colocación de stents está indicada en pacientes que no responden a la dilatación endoscópica y a su vez no son candidatos para resección quirúrgica. Es importante recordar que los stents indicados para este tipo de lesiones deben ser fácilmente extraíbles, siendo actualmente los stents de silicona los más utilizados. Otra alternativa son los stents híbridos (AERO) de nitinol, completamente cubiertos de poliuretano, autoexpandibles y que se pueden retirar, los cuales no requieren de la broncoscopia rígida para su colocación44,45. La pérdida de soporte cartilaginoso y la ausencia de compresión extrínseca hacen que los stents situados en la región subglótica o tráquea proximal migren. En estos casos se puede considerar la fijación externa percutánea de dichos stents. Son potenciales complicaciones las infecciones cutáneas en torno al botón de fijación46,47. La reestenosis como consecuencia del propio proceso de reparación y obstrucción de los stents son las principales causas de reintervención23,39.
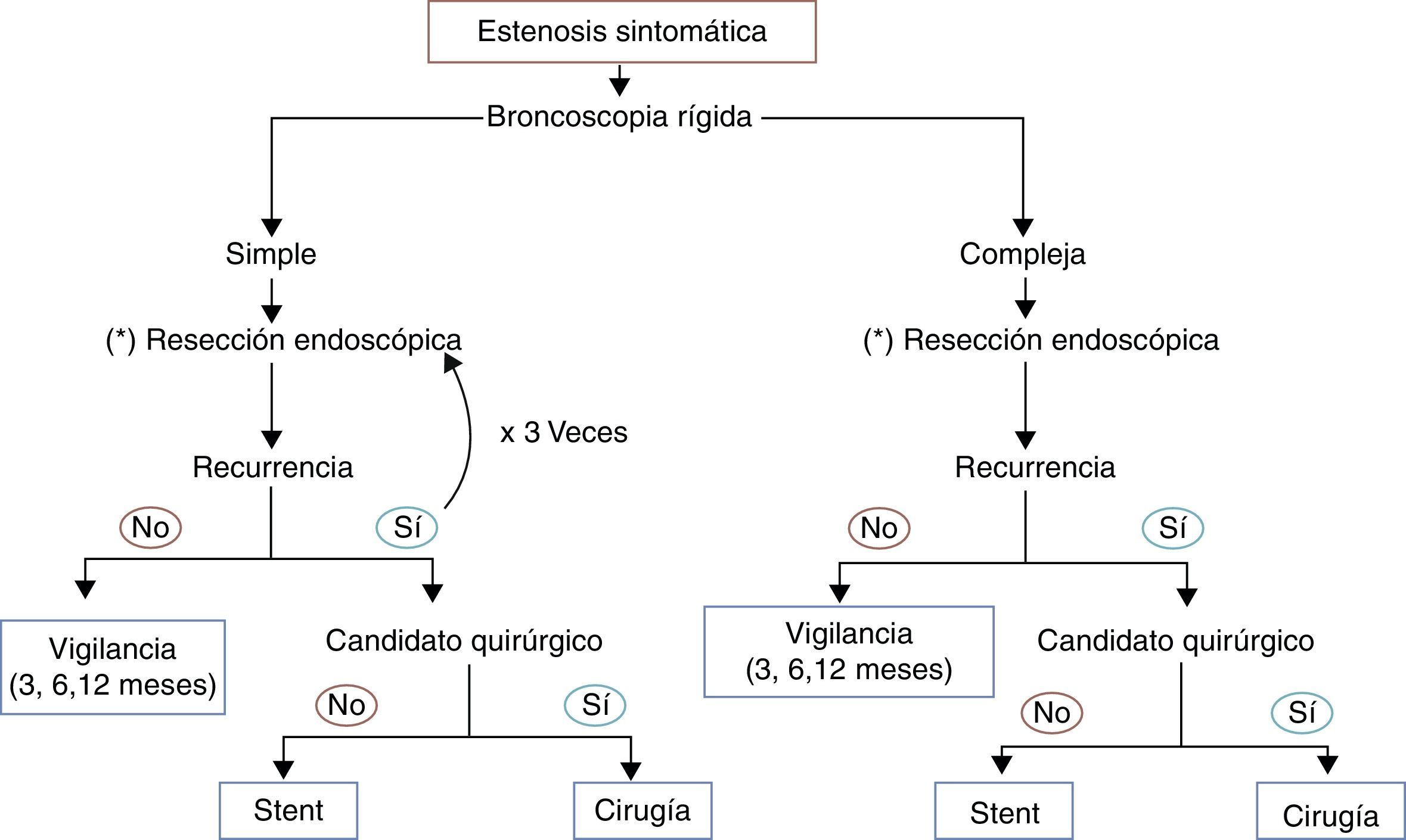
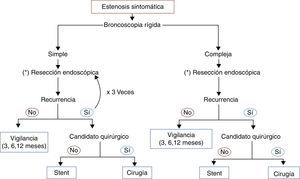
El uso de mitomicina tópica es controvertido, pero junto con las incisiones radiales con láser y la dilatación con balón, tiene cierto efecto beneficioso comparado con placebo a 2-3 años48–50 (fig. 3).
Merece una especial mención la localización subglótica de las estenosis, cuya principal causa es la intubación. El espacio subglótico se refiere a la porción de la vía aérea entre las cuerdas vocales y la fracción inferior del cartílago cricoides, siendo la parte más estrecha de la laringe y la única rodeada por un anillo cartilaginoso completo. Su diámetro estrecho, la inextensibilidad de los tejidos circundantes, la fragilidad del tejido de revestimiento y la pobre vascularización, la hacen más susceptible al trauma por intubación, a la reestenosis y al fracaso de la decanulación51. Se ha documentado que la incidencia de estenosis subglótica secundaria a intubación prolongada entre niños y adultos varía desde el 0,9% hasta el 8,3%52. El manejo es un reto que involucra diversas estrategias que deben ser individualizadas para cada paciente. Para las estenosis de consistencia blanda, membranosas, con adecuado soporte cartilaginoso, con longitudes en torno al centímetro, no concéntricas, que corresponden a los grados i y ii de Cotton-Myer se utilizan las técnicas endoscópicas ya descritas, destacando la utilización del láser; presentan una tasa de éxito variable según la literatura, entre el 40-94%53. Los grados iii y iv, estenosis complejas, de consistencia dura y mayor longitud, si bien inicialmente se pueden tratar con técnicas endoscópicas, la mayoría de las veces requerirán cirugía abierta reconstructiva (resección quirúrgica del segmento estenosado, englobando diversos anillos traqueales y el anillo anterior del cricoides además de la mitad caudal del la mucosa del sello cricoideo, con posterior unión término-terminal)53,54.
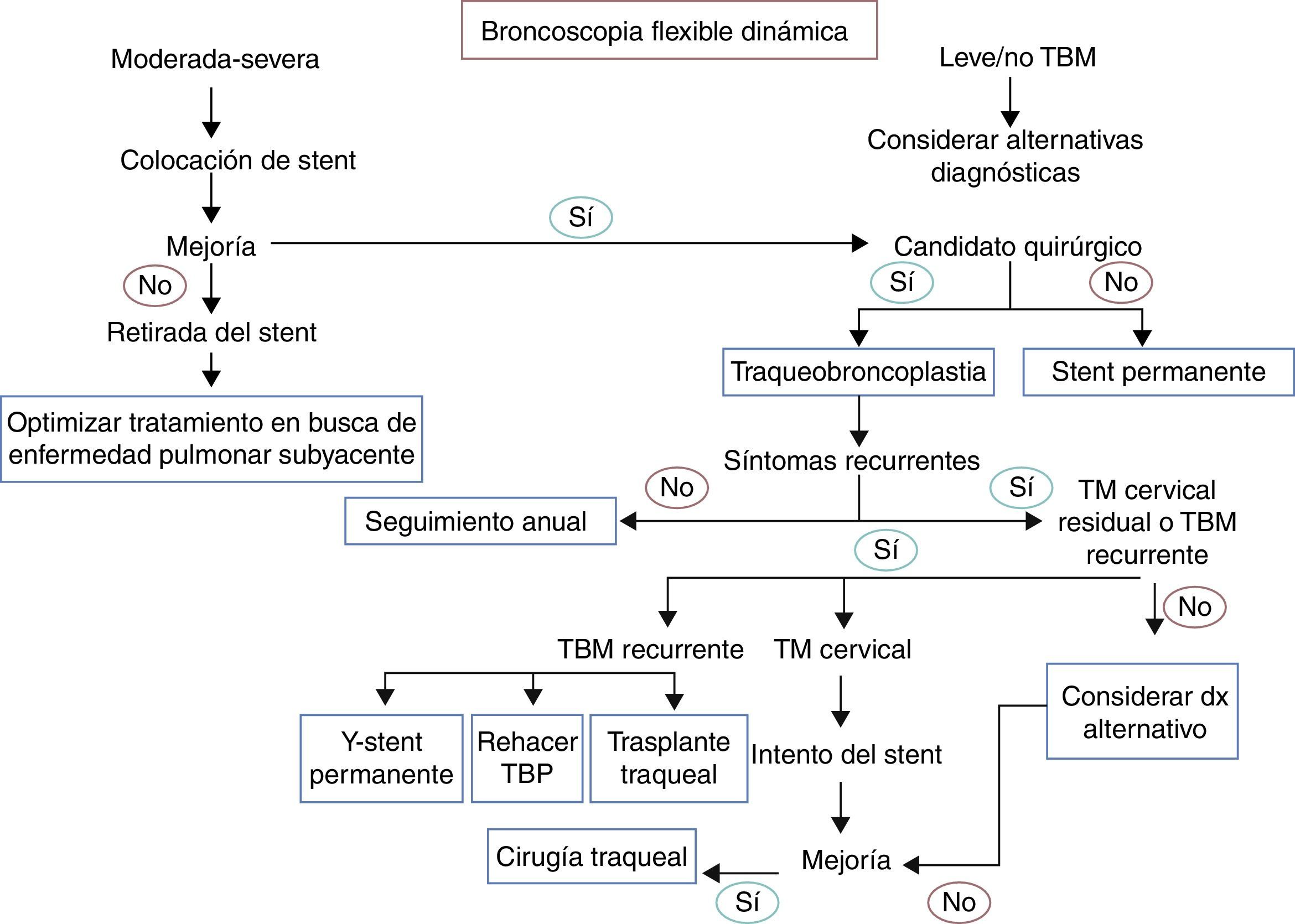
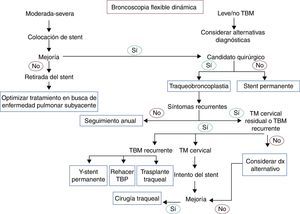
Obstrucción dinámica de la vía aérea: traqueobroncomalacia y colapso excesivo de la pars membranosaLa traqueobroncomalacia (TBM) y el colapso excesivo de la pars membranosa representan 2 patologías con una prevalencia estimada en torno al 12% de los pacientes con enfermedades respiratorias55. En la TBM se produce una disminución entre la proporción de cartílago y tejidos blandos, siendo este de 2:1 (normalmente 5:1), mientras que en el colapso excesivo de la pars membranosa se produce atrofia y disminución del número de fibras mioelásticas56. Son varias las causas que pueden dar lugar a TBM, tanto en su forma localizada como difusa57,58 (tabla 2). Existen diferentes formas de clasificar la enfermedad, siendo la clasificación funcional (FEMOS) la más completa59. La TBM puede no dar síntomas aunque frecuentemente es causa de tos, sibilancias, estridor, disnea, infecciones recurrentes y, en ocasiones, fallo respiratorio60. Exige, por ello, un diagnóstico diferencial con procesos patológicos como la enfermedad pulmonar obstructiva crónica, el asma y las bronquiectasias61. Las pruebas de función respiratoria pueden facilitar el diagnóstico de enfermedad pulmonar obstructiva concomitante, pero tienen limitaciones para el diagnóstico de TBM, puesto que hasta en un 21% son normales62. Por ello generalmente se requiere de la tomografía dinámica del tórax y de la broncoscopia dinámica flexible para su diagnóstico62,63 (fig. 1, imagen 3). Mediante la realización de maniobras dinámicas en inhalación y exhalación se puede diagnosticar fácilmente esta enfermedad. En pacientes con TBM difusa se debe realizar una prueba diagnóstica mediante la colocación de un stent de silicona61,64, junto con el tratamiento de las comorbilidades. Para aquellos pacientes que experimenten mejoría en los síntomas, el stent es retirado en preparación para la reconstrucción quirúrgica mediante traqueobroncoplastia65. Para aquellos pacientes a los que no se les pueda intervenir por sus comorbilidades, el tratamiento será una combinación entre el tratamiento sintomático y la posibilidad de un stent con carácter definitivo (fig. 4).
Clasificación de las causas más frecuentes de traqueobroncomalacia en adultos
| Primaria |
| Genética |
| Idiopática |
| Taqueobroncomegalia (síndrome de Mounier-Kuhn) |
| Secundaria |
| Postraumática |
| Postintubación |
| Postraqueotomía |
| Trauma torácico |
| Postrasplante de pulmón |
| Enfisema (EPOC) |
| Infecciones tipo bronquitis crónica |
| Inflamación crónica |
| Policondritis recidivante |
| Compresión extrínseca de la tráquea |
| Tumores benignos |
| Tumores malignos |
| Quistes |
| Abscesos |
| Aneurismas aórticos |
| Anillos o anomalías vasculares |
Diagrama de flujo para el manejo de la traqueobroncomalacia. dx: diagnóstico; TBM: traqueobroncomalacia; TBP: traqueobroncoplastia; TM: traqueomalacia. Seguimiento anual: tomografía axial computarizada dinámica, broncoscopia dinámica, pruebas de función pulmonar. Diagnóstico alternativo: asma, enfermedad por reflujo gastroesofágico, disfunción de cuerdas vocales, inmunodeficiencias.
Si bien se ha propuesto la ventilación mecánica no invasiva como posible tratamiento de la TBM, su papel parece quedar relegado al manejo de la insuficiencia respiratoria aguda en la TBM postintubación ya que mantiene abierta la vía aérea y facilita el drenaje de las secreciones. En este sentido, recientemente Murgu y Colt proponen la realización de una broncoscopia diagnóstica, a través de la mascarilla de CPAP y siempre y cuando el paciente no esté en situación crítica, con la intención de determinar si efectivamente el paciente respondería y se beneficiaría de presión positiva en la vía aérea66. En situación de estabilidad, la presión nasal intermitente se recomienda durante el día y la forma continua durante la noche. Estabiliza la vía aérea del paciente y actúa de puente hacia tratamientos más específicos y definitivos como la colocación de stents o la cirugía (traqueobroncoplastia)67. La CPAP parece evitar traqueotomías o intubaciones prolongadas en casos de TBM leve-moderada68.
La tráquea humana es un órgano único y complejo que requiere de un soporte rígido para resistir el ciclo respiratorio, de un adecuado aporte vascular para su mantenimiento y de un epitelio que le haga resistente al agresivo medioambiente externo. En este sentido, dentro del diagrama de flujo para el manejo de la TBM persistente tras la realización de una traqueobroncoplastia, comentamos la posibilidad de realizar un trasplante traqueal. Se trata de una modalidad terapéutica novedosa, todavía en estudio y con resultados inciertos, que cuenta con pocas series de casos y que está relegada para situaciones muy concretas que exijan solventar problemas posquirúrgicos (como sería este caso) o planteen la alternativa a la propia cirugía. Aunque no en el contexto de TBM, Delaere propone la realización de un alotrasplante traqueal con inmunosupresión temporal consistente en la implantación de tráquea procedente de un donante cadáver, previamente revascularizada de forma heterotópica durante 3 meses en el antebrazo del receptor, sobre la que finalmente se sustituye el epitelio traqueal por mucosa oral con el fin de evitar el rechazo y poder plantear la retirada definitiva del tratamiento inmunosupresor69.
Estenosis traqueobronquial en la granulomatosis con poliangitis (enfermedad de Wegener)La afectación de la vía aérea se presenta en un 15-55% de los casos70–72. Hasta en un 25% de los pacientes esta es la única manifestación73, pudiendo ser incluso irreversible. Las manifestaciones respiratorias incluyen obstrucción y/o necrosis del cartílago nasal, estenosis subglótica, estenosis traqueal y bronquial, malacia, formación de membranas; nódulos y masas, infiltrados alveolares y cavitaciones74,75 (fig. 1, imagen 4). Usualmente son pacientes jóvenes, por debajo de los 30 años, y con predominio del sexo femenino76,77. Los principales síntomas son: tos, sibilancias, disnea, estridor y hemoptisis72,78. La afectación de la pared posterior de la tráquea es frecuente a diferencia de otras patologías como la policondritis recidivante o la traqueobroncopatía osteocondroplásica79. La estenosis subglótica es la manifestación endobronquial más frecuente en la enfermedad de Wegener80,81 y usualmente no hay correlación entre la actividad inflamatoria en la vía aérea (demostrable por biopsia) con la positividad de los c-ANCA82–86.
El tratamiento endoscópico incluye inyección intralesional de corticoides, dilatación con balón neumático y terapias termoablativas. Se debe evitar el uso de stents o la realización de una traqueotomía, puesto que tienen sus propias complicaciones. Generalmente la resección quirúrgica con reanastomosis se utiliza en casos muy seleccionados78,79,87–92.
La aplicación intralesional de corticoides de larga acción (60-80mg de acetato de metilprednisolona), junto con la dilatación endoscópica, parece ser una terapia efectiva93–95.
Estenosis traqueobronquial en la amiloidosisLa obstrucción subglótica es la forma más común (el 0,5% de todas las lesiones sintomáticas en el árbol traqueobronquial y el 23% de todas las lesiones sintomáticas benignas). Es infrecuente la afectación simultánea del parénquima y del árbol traqueobronquial96.
En la mucosa traqueal, la amiloidosis puede producir desde lesiones difusas hasta masas que simulan tumores97. El diagnóstico se realiza mediante la biopsia de la lesión, demostrando la presencia de material rojo Congo positivo con birrefringencia verde bajo luz polarizada. Endoscópicamente se puede observar estrechamiento irregular de la luz, engrosamiento de la pared y calcificaciones irregulares96. Algunos pacientes pueden presentar obstrucción de la vía aérea o hemoptisis; en estos casos, la terapia con láser es el tratamiento de elección98–100. En pacientes con enfermedad difusa, Kurrus et al. documentaron la regresión de los depósitos endobronquiales de amiloide con radioterapia tras 10 sesiones de 20Gy101.
Estenosis traqueobronquial por tuberculosisEntre el 10 y el 40% de la tuberculosis pulmonar activa tiene componente endobronquial102,103, afectando los bronquios principales en el 60-95% de los casos104. Se observan más frecuentemente cuando hay un retraso en el diagnóstico y en el tratamiento105,106. La causa más probable es la afectación de nódulos linfáticos con posterior fistulización hacia los bronquios adyacentes107. La tuberculosis endobronquial puede presentarse como una lesión caseosa-edematosa, hiperémica, fibroestenótica, granular, tumoral o ulcerativa105,108. Frecuentemente vemos una lesión blanca, gelatinosa y polipoidea (fig. 1, imagen 5).
La terapia endoscópica incluye tratamiento termoablativo y dilataciones seriadas con balón. En lesiones sintomáticas cicatriciales irreversibles o compresión extrínseca de la vía aérea se puede considerar la colocación de un stent109.
Estenosis traqueobronquial en la traqueobroncopatía osteocondroplásticaLa traqueobroncopatía osteocondroplástica es una rara enfermedad, no tumoral, que afecta la tráquea y en menor porcentaje los bronquios principales, en la que nódulos submucosos de origen cartilaginoso u óseo se proyectan sobre la luz de la vía aérea110–113. Estos nódulos pueden ser de diferentes tamaños, normalmente entre 1-3mm y se localizan en la pared anterolateral de la tráquea respetando la pared posterior114. Estos pueden causar deformidad y estrechamiento de la tráquea, aunque superando más del 50% de la luz en menos del 10% de los casos110.
Se postula que pueda ser el resultado de metaplasia del tejido conectivo mesenquimal adyacente a la submucosa, teniendo en cuenta la presencia de determinadas citocinas (BMP-2, TGF-B1) en mayor cantidad de la habitual115.
Esta enfermedad no tiene asociación con el tabaquismo y su prevalencia es similar en ambos sexos, siendo la mayor parte de los casos personas de mediana edad en el momento del diagnóstico116,117.
La TAC demostrará nódulos submucosos densamente calcificados protruyendo en la luz de la vía aérea, en su pared anterolateral110,112,114. Estos mismos hallazgos se confirmarán mediante la visión broncoscópica (fig. 1, imagen 6). Si el aspecto es típico, la biopsia no es necesaria. En caso de realizarla se encuentra hueso o calcificación de la submucosa bronquial110. La traqueobroncopatía osteocondroplástica es una enfermedad de curso benigno y lento en la que raras veces se producen complicaciones como neumonías postobstructivas o fallo respiratorio116.En el caso de presentar síntomas obstructivos, la mayoría de los pacientes se tratan mediante el desbridamiento endoscópico junto con el uso de láser y stents110,113,116 e infrecuentemente se requiere de la resección quirúrgica.
Estenosis traqueal idiopáticaEn la mayoría de los casos este tipo de estenosis se localiza en la región subglótica o en el tercio superior de la tráquea118–120. Con predominio femenino, parece que los estrógenos pueden desempeñar un importante papel118–121. Otros autores sugieren que pueda estar en relación con la ERGE122,123.
Si bien su diagnóstico se sospecha mediante la evaluación de la curva flujo-volumen, la TAC multicorte y la broncoscopia (fig. 1, imagen 7) son esenciales para confirmar el diagnóstico124–126.
Las muestras histológicas recogidas durante la broncoscopia muestran una densa fibrosis y un moderado infiltrado inflamatorio con importante cantidad de fibroblastos127.
Mientras la cirugía sigue siendo el tratamiento definitivo48,128–129, lesiones menores de 1cm son tratadas exitosamente por medio de técnicas endoscópicas con incisiones radiales seguidas por dilatación con balón y la aplicación tópica de mitomicina C. El uso de stents extraíbles es considerado en pacientes con lesiones recurrentes que no son candidatos a cirugía o como puente hacia la misma. En caso de estenosis simples, se sugiere al menos 3 sesiones broncoscópicas antes de considerar el tratamiento quirúrgico. La inyección intralesional de esteroides o la aplicación de mitomicina C ha sido usada para prevenir la reestenosis tras tratamientos endoscópicos48,120,130. En caso de lesiones estenóticas complejas la resección quirúrgica es el tratamiento de elección.
Estenosis traqueobronquial en la policondritis recidivanteLa policondritis recidivante es una enfermedad multisistémica autoinmune con episodios recurrentes de inflamación que afecta estructuras cartilaginosas como las orejas, nariz, articulaciones periféricas, laringe y árbol traqueobronquial131,132. Es más frecuente entre la cuarta y la quinta década de la vida, sin existir predominio de ningún sexo131.
Aproximadamente la mitad de los pacientes que sufren esta enfermedad tendrán afectación pulmonar y de la vía aérea en su curso, como estenosis subglótica, malacia focal o difusa y estenosis traqueobronquial. La TAC dinámica del tórax, con cortes en inspiración y espiración forzada, será la prueba de imagen de elección. Observaremos estenosis focales, engrosamiento de la pared traqueal con o sin calcificaciones y colapso espiratorio asociado a malacia de tipo concéntrico133. La PET puede servir de ayuda para el diagnóstico y la valoración de la respuesta al tratamiento134,135.
Algunos de estos pacientes requieren medidas intervencionistas como dilatación con balón, stents o traqueotomía. En aquellos en los que se sobreañada traqueobroncomalacia se podrá utilizar CPAP intermitente, expectorantes y válvula de flutter para evitar la mucostasia y la sobreinfección. El tratamiento médico generalmente consiste en terapia antiinflamatoria con corticoesteroides en combinación con metrotexato, azatioprina o ciclofosfamida131. Existen estudios que apoyan el uso de nuevas terapias inmunomoduladoras como el etanercept, el infliximab y el rituximab136–140.
Estenosis traqueobronquial en sarcoidosisLa afectación de la vía aérea puede ocurrir incluso en ausencia de afectación parenquimatosa141–143.
La formación de granulomas le da a la mucosa un aspecto en empedrado141. Otras formas de afectación son el eritema, el edema y la formación de placas. El estrechamiento de la vía aérea secundario a estenosis cicatricial o a compresión extrínseca por adenopatías mediastínicas es raro144.
La tos es la manifestación clínica más frecuente de esta enfermedad cuando afecta a la vía aérea principal141,145–149. Los hallazgos endoscópicos varían desde estenosis únicas o múltiples hasta estrechamientos difusos de la vía aérea141,150,151.
En aquellos pacientes con síntomas leves, la terapia inhalada con corticoides debería ser suficiente, pudiendo añadir corticoides sistémicos141. En algunos casos es necesario procedimiento broncoscópicos, como dilatación neumática y terapias termoablativas sumado a intentos con corticoides intralesionales.
Estenosis bronquial postrasplante pulmonarLas estenosis bronquiales postrasplante representan una importante fuente de morbimortalidad y son consecuencia del proceso de reparación de las anastomosis. Su incidencia oscila entre el 16-33%152, y la mortalidad entre el 2-4%153–159.
Estas son vulnerables a la isquemia ya que la circulación de las arterias bronquiales no es normalmente restablecida y la perfusión depende del flujo retrógrado procedente de la arteria pulmonar hasta que se establezca un flujo colateral, pasadas 2-4 semanas160. Otros factores como el rechazo, la terapia inmunosupresora, las infecciones o una inadecuada preservación del órgano han sido implicados en la alteración del proceso de reparación161,162. Debido a que dos tercios de estos pacientes presentan broncomalacia asociada, la dilatación con balón neumático suele ser una solución transitoria, requiriendo el uso de stents en la mayoría de los casos163–166. De Gracia et al. describen que la utilización de stents es necesaria solo en la mitad de los casos167. Stents de silicona o híbridos166 deben utilizarse únicamente ante estenosis recurrentes que no han respondido a 3-4 dilataciones con balón o en aquellos casos de malacia focal severa sintomática165.
Recientemente Dutau et al., en una serie de 17 casos, proponen la utilización de stents de silicona argumentando la resolución de la estenosis y la curación de la anastomosis en la mayoría de los pacientes, con menos efectos secundarios que los habituales stents metálicos autoexpandibles utilizados, permitiendo su retirada168. Unos de los principales problemas que se plantea es la localización de las suturas de las anastomosis, que generalmente representa una dificultad para la adaptación anatómica del stent, con la consiguiente migración y/o la obstrucción de la embocadura de los lóbulos superiores. Estas complicaciones, sobre todo en el caso de las estenosis del bronquio intermediario, parecen resolverse con la utilización de un tubo en T de Montgomery modificado, situando el brazo de traqueotomía del tubo en la entrada del lóbulo superior derecho, manteniendo su luz permeable169.
ConclusiónLas lesiones no malignas de la vía aérea central son una causa frecuente de procedimientos broncoscópicos terapéuticos. El abordaje de estas patologías requiere estabilización inmediata, evaluación detallada, planificación meticulosa y tratamiento individualizado. Cada lesión necesita de una evaluación que entienda la fisiopatología e historia natural de la enfermedad. El tratamiento debe ser planificado por un equipo multidisciplinario que involucre a neumólogos intervencionistas, cirujanos de tórax, anestesistas, otorrinolaringólogos y radiólogos. En la práctica, la relación entre la broncoscopia terapéutica y la cirugía traqueal están entrelazadas y son complementarias.
Conflicto de interesesNinguno.
FinanciaciónNinguna.
AgradecimientosNinguno.