La última clasificación tumor, ganglio, metástasis (TNM), elaborada por la Asociación Internacional para el Estudio del Cáncer de Pulmón (IASLC) y basada en el análisis de pacientes procedentes de todo el mundo, introduce cambios en los descriptores, especialmente en lo referente al tamaño del tumor, y propone una nueva agrupación de estadios. También ha elaborado un nuevo mapa ganglionar que pretende facilitar la clasificación del componente «N». SEPAR recomienda utilizar esta nueva clasificación. En cuanto a los procedimientos recomendados para la estadificación, además del uso generalizado de la tomografía computarizada (TC), se señala el papel de la tomografía de emisión de positrones (PET) o los métodos de fusión de imágenes (PET/TC), que permiten una mejor evaluación del mediastino y de las metástasis extratorácicas. Se recomienda la incorporación de la ecobroncoscopia (EBUS) y de la ultrasonografía esofágica (EUS), para la obtención de muestra citohistológica, en el algoritmo de estadificación y se destaca la importancia de una reestadificación precisa después del tratamiento de inducción para tomar nuevas decisiones terapéuticas. Se comenta la previsible incorporación en el futuro próximo de la estadificación molecular y se recomienda la disección ganglionar sistemática con vistas a una más exacta clasificación quirúrgico-patológica.
The latest tumour, lymph node and metastasis (TNM) classification by the International Association for the Study of Lung Cancer (IASLC), based on the analysis of patients from all over the world, has incorporated changes in the descriptors, especially those regarding tumor size, while proposing new group staging. A new lymph node map has also been developed with the intention of facilitating the classification of the “N” component. SEPAR recommends using this new classification. As for the procedures recommended for staging, in addition to the generalized use of computed tomography (CT), it points to the role of positron emission tomography (PET) or image fusion methods (PET/CT), which provide a better evaluation of the mediastinum and extrathoracic metastases. Endobronchial ultrasound (EBUS) and esophageal ultrasound (EUS) for obtaining cytohistological samples have been incorporated in the staging algorithm, and it emphasizes the importance of precise re-staging after induction treatment in order to make new therapeutic decisions. Comment is made on the foreseeable incorporation in the near future of molecular staging, and systematic lymph node dissection is recommended with the intention of making a more exact surgical-pathological classification.
Han transcurrido más de 10 años desde la última publicación de la Normativa SEPAR sobre Diagnóstico y Estadificación del Cáncer de Pulmón (CP)1. Durante estos años se han incorporado a la práctica clínica nuevos procedimientos, entre los que cabe destacar la tomografía de emisión de positrones, aislada (PET) o integrada con la tomografía computarizada (PET/TC), y los nuevos métodos endoscópicos para la obtención de muestras ganglionares o de otros órganos: ultrasonografía endobronquial (EBUS) y esofágica (EUS). Además, recientemente, la Asociación Internacional para el Estudio del Cáncer de Pulmón (International Association for the Study of Lung Cancer [IASLC]) ha elaborado una nueva edición de la clasificación según el grado de extensión anatómica (clasificación TNM), basada en el análisis detallado de miles de pacientes con CP procedentes de muy diversas regiones del mundo2, clasificación que está siendo adoptada rápidamente por la práctica totalidad de las sociedades interesadas en el estudio del CP.
Por todo ello, creemos justificado actualizar las recomendaciones de la SEPAR sobre este importante apartado, aunque, por razones de espacio, nos limitaremos a los aspectos de estadificación, sin incluir el diagnóstico propiamente dicho. Por la misma razón, tampoco se comentarán los aspectos específicos de la estadificación del carcinoma microcítico de pulmón (CPM), si bien cabe mencionar que en la última edición de la clasificación TNM se recomienda su aplicación a dicha estirpe.
Estadificación actual del cáncer de pulmónLa clasificación anatómica TNM-estadios permite una descripción estandarizada de los tumores pulmonares, la comparación de resultados entre distintos estudios clínicos y encuadrar a los pacientes en estadios dentro de los cuales el pronóstico y la estrategia terapéutica sean similares. El sistema de estadificación internacional de 1997 (5.a edición) no experimentó cambios en 2002 (6.a edición) y ha permanecido vigente hasta 2009. Se ha empleado ampliamente en los carcinomas no microcíticos (CPNM) y en menor medida en los CPM, pero su metodología ha sido criticada. Dicho sistema procede del análisis de la base de datos de una sola institución y región geográfica, constituida entre 1975 y 1988, cuando no se empleaban muchas de las técnicas de imagen ni las terapias actuales, y compuesta por 5.319 pacientes tratados quirúrgicamente. Todos los tumores disponían de estadificación clínica y patológica, pero ninguno de los descriptores T, N o M había sido validado interna ni externamente.
Clasificación IASLC 2009: TNM 7.a ediciónPara actualizar y mejorar la 6.a edición, la IASLC, de acuerdo con la International Union Against Cancer (UICC) y el American Joint Committee on Cancer (AJCC) creó un Comité Internacional de Estadificación que recogió retrospectivamente los datos de 100.869 pacientes. Fueron diagnosticados entre 1990 y 2000, seguidos clínicamente al menos durante 5 años y procedían de 45 fuentes distintas (registros, ensayos clínicos, series quirúrgicas y hospitalarias) de 20 países. Cumplieron suficientes criterios de calidad para que 68.463 fueran analizados con CPNM y 13.032 con CPM; en total, 81.495 que recibieron los siguientes tratamientos: cirugía 41%, quimioterapia 23%, radioterapia 11%, y el 25%, combinaciones de los anteriores. Los hallazgos del estudio que pudieran constituir recomendaciones para cambiar algún componente T, N o M fueron validados internamente (por región geográfica y tipo de base de datos) y externamente con enfermos del registro Surveillance, Epidemiology and End Results (SEER) estadounidense.
Carcinomas no microcíticosComponente TSe evaluaron los pacientes que carecían de metástasis, y aunque contaban con información sobre diversos aspectos del componente T, solo se pudo analizar con detalle el tamaño tumoral, la existencia de nódulos acompañantes y la diseminación pleural3. El valor pronóstico del tamaño tumoral se estudió en los enfermos con tumores T1 y T2 N0 M0 patológicos completamente resecados y que no hubieran recibido terapia neoadyuvante. Los cálculos estadísticos determinaron tres puntos de corte en 2, 5 y 7cm, que, añadidos al valor de 3cm, frontera entre T1 y T2, dieron lugar a 5 grupos de tumores con supervivencia significativamente peor a medida que se hacía mayor el diámetro tumoral. Los grupos y sus tasas de supervivencia a los 5 años fueron: T1 ≤2cm, 77%; T1 >2cm y ≤3cm, 71%; T2 >3cm y ≤5cm, 58%; T2 >5cm y ≤7cm, 49%, y T2 >7cm, 35%. Esta graduación pronóstica se mantuvo cuando se evaluaron poblaciones de pacientes menos seleccionados: estadificación clínica, resección incompleta y diferente afectación ganglionar. Con tales argumentos se decidió subdividir los tumores T1 en T1a (≤2cm) y T1b (>2cm y ≤3cm), y los T2, en T2a (>3cm y ≤5cm) y T2b (>5cm y ≤7cm). Se comparó, así mismo, la supervivencia a 5 años de los pacientes con tumores T2 >7cm frente a la de los de tumores T3. Se encontraron cifras similares en las diferentes poblaciones, excepto en los casos N0 con resección completa, en los cuales se comprobó que la supervivencia era incluso superior en los T3 (41%) que en los T2>7cm (35%), por lo que se decidió reclasificar a estos últimos como T3 (tabla 1). Cuando se analizaron los tumores que, con estadificación patológica, presentaban nódulos adicionales pudo apreciarse: a) que la supervivencia a los 5 años era en los T3 (31%) similar a la de los T4 clasificados como tal por la existencia de nódulo/os adicional/es en el mismo lóbulo del tumor primario (28%); b) que los T4 por otros factores tenían la misma supervivencia que los clasificados como M1 por nódulo/os adicional/es en un lóbulo homolateral diferente al del tumor primario (22%), y c) que los T4 por diseminación pleural tenían un pronóstico claramente peor (11% de supervivencia a los 5 años). Se aconsejó, por tanto, para la nueva clasificación, considerar T3 a los tumores con nódulo/s adicional/es en el mismo lóbulo del tumor primario, considerar T4 a los tumores con nódulo/os adicional/es en un lóbulo homolateral diferente al del tumor primario, e incluir en la categoría M a los tumores con diseminación pleural (tabla 1).
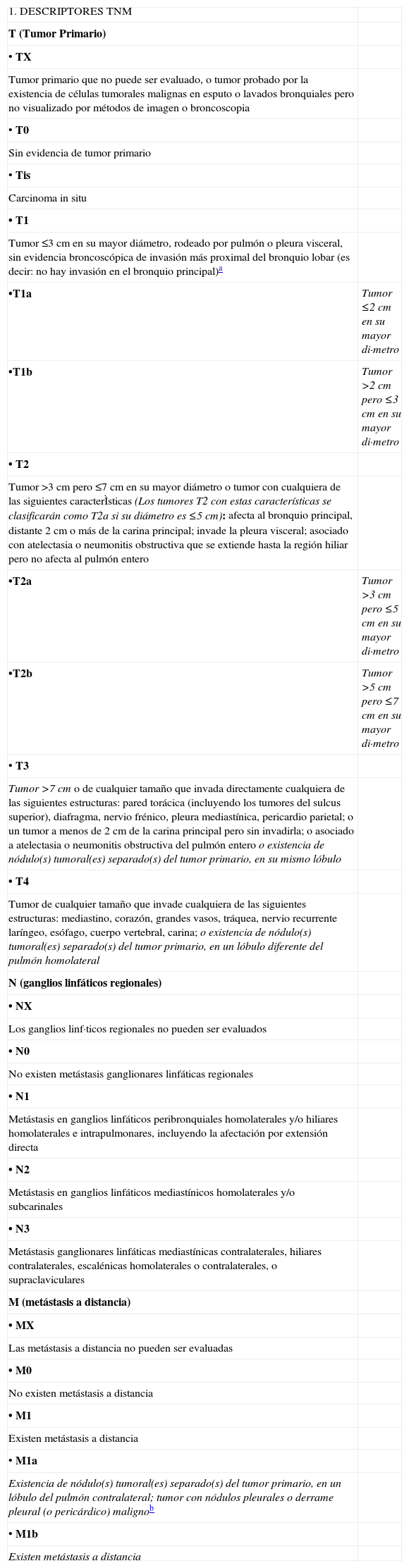
Sistema internacional de estadificación TNM-estadios 2009 (7.a edición)
| 1. DESCRIPTORES TNM | |
| T (Tumor Primario) | |
| • TX | |
| Tumor primario que no puede ser evaluado, o tumor probado por la existencia de células tumorales malignas en esputo o lavados bronquiales pero no visualizado por métodos de imagen o broncoscopia | |
| • T0 | |
| Sin evidencia de tumor primario | |
| • Tis | |
| Carcinoma in situ | |
| • T1 | |
| Tumor ≤3cm en su mayor diámetro, rodeado por pulmón o pleura visceral, sin evidencia broncoscópica de invasión más proximal del bronquio lobar (es decir: no hay invasión en el bronquio principal)a | |
| •T1a | Tumor ≤2cm en su mayor di·metro |
| •T1b | Tumor >2cm pero ≤3cm en su mayor di·metro |
| • T2 | |
| Tumor >3cm pero ≤7cm en su mayor diámetro o tumor con cualquiera de las siguientes caracterÌsticas (Los tumores T2 con estas características se clasificarán como T2a si su diámetro es ≤5cm): afecta al bronquio principal, distante 2 cm o más de la carina principal; invade la pleura visceral; asociado con atelectasia o neumonitis obstructiva que se extiende hasta la región hiliar pero no afecta al pulmón entero | |
| •T2a | Tumor >3cm pero ≤5cm en su mayor di·metro |
| •T2b | Tumor >5cm pero ≤7cm en su mayor di·metro |
| • T3 | |
| Tumor >7cm o de cualquier tamaño que invada directamente cualquiera de las siguientes estructuras: pared torácica (incluyendo los tumores del sulcus superior), diafragma, nervio frénico, pleura mediastínica, pericardio parietal; o un tumor a menos de 2cm de la carina principal pero sin invadirla; o asociado a atelectasia o neumonitis obstructiva del pulmón entero o existencia de nódulo(s) tumoral(es) separado(s) del tumor primario, en su mismo lóbulo | |
| • T4 | |
| Tumor de cualquier tamaño que invade cualquiera de las siguientes estructuras: mediastino, corazón, grandes vasos, tráquea, nervio recurrente laríngeo, esófago, cuerpo vertebral, carina; o existencia de nódulo(s) tumoral(es) separado(s) del tumor primario, en un lóbulo diferente del pulmón homolateral | |
| N (ganglios linfáticos regionales) | |
| • NX | |
| Los ganglios linf·ticos regionales no pueden ser evaluados | |
| • N0 | |
| No existen metástasis ganglionares linfáticas regionales | |
| • N1 | |
| Metástasis en ganglios linfáticos peribronquiales homolaterales y/o hiliares homolaterales e intrapulmonares, incluyendo la afectación por extensión directa | |
| • N2 | |
| Metástasis en ganglios linfáticos mediastínicos homolaterales y/o subcarinales | |
| • N3 | |
| Metástasis ganglionares linfáticas mediastínicas contralaterales, hiliares contralaterales, escalénicas homolaterales o contralaterales, o supraclaviculares | |
| M (metástasis a distancia) | |
| • MX | |
| Las metástasis a distancia no pueden ser evaluadas | |
| • M0 | |
| No existen metástasis a distancia | |
| • M1 | |
| Existen metástasis a distancia | |
| • M1a | |
| Existencia de nódulo(s) tumoral(es) separado(s) del tumor primario, en un lóbulo del pulmón contralateral; tumor con nódulos pleurales o derrame pleural (o pericárdico) malignob | |
| • M1b | |
| Existen metástasis a distancia |
| 2. Estadios | |||
| Carcinoma oculto | TX | N0 | M0 |
| Estadio 0 | Tis | N0 | M0 |
| Estadio IA | T1 a,b | N0 | M0 |
| Estadio IB | T2a | N0 | M0 |
| Estadio IIA | T1 a,b | N1 | M0 |
| T2a | N1 | M0 | |
| T2b | N0 | M0 | |
| Estadio IIB | T2b | N1 | M0 |
| T3 | N0 | M0 | |
| Estadio IIIA | T1,T2 | N2 | M0 |
| T3 | N1,N2 | M0 | |
| T4 | N0,N1 | M0 | |
| Estadio IIIB | T4 | N2 | M0 |
| Cualquier T | N3 | M0 | |
| Estadio IV | Cualquier T | Cualquier N | M1a,b |
Nota: Se destacan en cursiva los cambios con respecto a la clasificaciÛn TNM previa.
La poco frecuente diseminación superficial de un tumor de cualquier tamaño con su componente invasivo limitado a la pared bronquial, el cual puede extenderse proximalmente hasta el bronquio principal, se clasifica también como T1.
La mayoría de los derrames pleurales (y pericárdicos) asociados al cáncer de pulmón son debidos al tumor. Sin embargo, hay algunos pacientes en quienes múltiples estudios citopatológicos del líquido pleural (o pericárdico) son negativos para tumor, el líquido no es hemático y no es un exudado. Cuando estos elementos y el juicio clínico indiquen que el derrame no está relacionado con el tumor, el derrame debe ser excluido como elemento de estadificación y el paciente debe ser clasificado como T1, T2, T3 o T4.
Se confirmó la esperada disminución de la supervivencia a medida que aumentaba la afectación ganglionar, encontrándose también diferencias significativas en la supervivencia a los 5 años en tres grandes grupos de enfermos: a) con afectación de una sola zona N1 patológica (48%); b) de múltiples zonas N1 patológicas (35%) o una sola N2 patológica (34%), y c) múltiples zonas N2 patológicas (20%). Pero estos hallazgos no pudieron ser validados por áreas geográficas ni categorías T, por lo que no se recomendaron cambios relativos al componente N para la nueva clasificación4.
Debe tenerse en cuenta que estos datos proceden de pacientes intervenidos cuyo estado adenopático se evidenció por disección ganglionar sistemática, lo que, por el momento, en la estadificación clínica, solo es posible realizando video-assisted mediastinoscopic lymphadenectomy (VAMLA) o transcervical extended mediastinal lymphadenectomy (TEMLA) (véase, más adelante, «Procedimientos de estadificación mediante técnicas quirúrgicas»).
Componente MLos pacientes estudiados presentaron las siguientes tasas de supervivencia respectivamente a 1 y 5 años: T4 cualquier N M0, 53 y 16%; diseminación pleural, 45 y 6%; nódulo/s pulmonar/es contralateral/es, 46 y 3%, y metástasis a distancia, 22 y 1%; en este último caso, con unas cifras de supervivencia significativamente inferiores a las de los previamente citados5. Con tales referencias se decidió subdividir el componente M en M1a (presencia de diseminación pleural o nódulo/s pulmonar/es contralateral/es) y M1b (metástasis a distancia) (tabla 1).
Agrupación de estadiosConocidos los argumentos previos para reordenar algunos apartados de los componentes T y M, se llevó a cabo un sofisticado estudio estadístico con los 17.726 pacientes cuyos tumores estaban mejor estadificados2. Se obtuvieron las diferentes curvas de supervivencia de cada estadio, que, sin solaparse entre ellas, presentaban peores cifras a medida que aumentaba la extensión tumoral. Se confirma así la nueva agrupación de estadios (tabla 1), cuyas supervivencias a los 5 años, para cada estadio, fueron, según la estadificación clínica y la patológica, respectivamente, las siguientes: IA, 50 y 73%; IB, 43 y 58%; IIA, 36 y 46%; IIB, 25 y 36%; IIIA, 19 y 24%; IIIB, 7 y 9%, y IV, 2 y 13%.
Carcinomas de células pequeñas (CPM) y tumores carcinoidesEl Comité Internacional de Estadificación de la IASLC ha constatado que la supervivencia de los pacientes con CPM empeoraba a medida que las categorías T y N eran más altas6. También se comprobó que, excepto en el estadio IIA, que contaba solo con 55 pacientes para análisis, la supervivencia a 5 años empeoraba cuando progresaba el estadio: IA, 38%; IB, 21%; IIA, 38%; IIB, 18%; IIIA, 13%; IIIB, 9%, y IV, 1%. En base a ello se ha confirmado la propuesta de emplear el sistema TNM para estadificar los CPM.
A pesar de que la 6.ª clasificación TNM especificaba que no era aplicable a los tumores carcinoides, diversos estudios la han empleado, encontrando diferencias pronósticas entre los estadios. También la IASLC ha comprobado que los clasificados en el estadio I vivían significativamente más que los del estadio II, y estos, significativamente más que los de los estadios III/IV, por lo que se recomienda la nueva clasificación TNM de 2009 para describir la extensión de estos tumores7.
Limitaciones de la clasificación TNM de 2009Las principales limitaciones derivan del carácter retrospectivo de unas bases de datos que no fueron diseñadas para estudiar dicha clasificación TNM y que carecen de detalles anatómicos precisos sobre la extensión tumoral, el número y estaciones ganglionares afectadas o las diferencias entre las diversas formas de enfermedad M1. Por este motivo, la propia IASLC ha puesto en marcha un proyecto prospectivo encaminado a actualizar de nuevo la clasificación TNM en 2016, validando todos los descriptores T, N y M, especialmente los que no lo han sido hasta ahora. Para ello se está constituyendo una gran base internacional que, corrigiendo las omisiones geográficas y desproporciones en las modalidades terapéuticas, incluya pacientes con tumores no microcíticos, microcíticos y otros subtipos neuroendocrinos.
Nuevo mapa ganglionarLa IASLC ha propuesto un nuevo mapa ganglionar8, consensuado internacionalmente y de forma multidisciplinar, que reconcilia las diferencias entre el mapa de Naruke y el de la Japan Lung Cancer Society, y el mapa de Mountain y Dresler. El mapa de la IASLC mantiene las estaciones ganglionares de los otros mapas, pero también agrupa las anatómicamente próximas en zonas ganglionares para facilitar la clasificación ganglionar, especialmente en los pacientes que no serán intervenidos. En este mapa, todas las estaciones ganglionares están definidas por límites anatómicos precisos, fáciles de reconocer por técnicas de imagen y por inspección durante las exploraciones invasivas o la toracotomía. Las innovaciones de este mapa ganglionar son:
- •
La creación de una zona ganglionar supraclavicular que incluye los ganglios supraclaviculares, los cervicales bajos (caudales al borde inferior del cartílago cricoides) y los de la fosa supraesternal. Si estos ganglios están invadidos por tumor, se clasifican como N3, independientemente del lado del tumor.
- •
La ampliación de la estación ganglionar subcarínica. Ahora incluye todos los ganglios desde la bifurcación traqueal hasta el borde superior del bronquio lobar inferior izquierdo y el borde inferior del bronquio intermediario. Si están afectados por tumor, estos ganglios se clasifican como N2. En esta nueva estación subcarínica se incluyen ganglios que antes, al menos según el mapa japonés, eran hiliares (adyacentes a las caras inferiores de los bronquios principales), que podían clasificarse como N1 o N3, dependiendo del lado del tumor. La ampliación de la estación subcarínica supondrá un incremento de tumores N2 en detrimento de los N1 y N3.
- •
La incorporación de límites precisos para la estación número 10, la hiliar, que facilitará la recogida prospectiva de datos de cara a dilucidar el papel pronóstico de esta estación, cuya ubicación en los otros mapas siempre ha sido controvertida.
- •
La traslación de la línea media del mediastino superior desde la línea media anatómica traqueal al margen paratraqueal izquierdo. Esto afecta exclusivamente a las estaciones paratraqueales superiores e inferiores derechas e izquierdas. Esta modificación implica que los ganglios afectados que estén a la izquierda de la línea media anatómica, pero a la derecha de la nueva línea paratraqueal izquierda, serán N2 para tumores del pulmón derecho, pero N3 para los del pulmón izquierdo.
Aunque no se describirán con detalle, sí es útil recordar su utilidad con vistas a la estadificación. La anamnesis y la exploración física detalladas pueden aportar datos de gran valor sobre el grado de extensión de la enfermedad, que permitirían una simplificación sustancial de las pruebas a realizar posteriormente: así, la disfonía, el síndrome compresivo de la vena cava superior, el síndrome de Horner o el dolor torácico a menudo reflejan la invasión de estructuras anatómicas adyacentes al pulmón que suelen contraindicar un tratamiento quirúrgico. Igualmente, los síntomas neurológicos o el dolor óseo intenso y persistente deben hacer sospechar la existencia de metástasis a distancia, que tendrían implicaciones pronósticas y terapéuticas relevantes. La radiografía de tórax es habitualmente la primera prueba que permite sospechar con alta probabilidad la existencia de un CP. Además de su valor diagnóstico, la detección de derrame pleural, de destrucción de vértebras o costillas, de invasión mediastínica, etc., puede ser decisiva para establecer el grado de extensión y simplificar notablemente el proceso de estadificación.
Tomografía computarizada (TC) de tóraxDespués de la radiografía de tórax, la TC suele ser la siguiente prueba de imagen que proporciona información relevante en el proceso de estadificación. Su rendimiento y limitaciones en el diagnóstico del CP han sido ampliamente estudiados y conocidos9,10 (tabla 2). En relación con el tumor primario (T), la TC sigue siendo el mejor método para el estudio anatómico global del tórax. Permite obtener una información detallada sobre el tamaño, la localización, las relaciones anatómicas con estructuras vecinas y puede detectar nódulos de muy pequeño tamaño, habitualmente no detectables mediante radiografía de tórax. Con respecto a la invasión de la pared torácica, se han referido cifras de sensibilidad (S) del 83% y de especificidad (E) del 80%, pero el único signo verdaderamente fiable de invasión es la destrucción ósea9. En cuanto a la invasión del mediastino por el tumor, algunos criterios permitirían predecir la resecabilidad, como una distancia de contacto entre la masa y el mediastino≤3cm, la visualización de un plano graso entre ambas estructuras o un ángulo de contacto entre la masa y la aorta menor de 90°. Por el contrario, los signos radiológicos sugerentes de invasión de estructuras mediastínicas que implicarían irresecabilidad son poco fiables, y no es aceptable rechazar la cirugía sobre la base de tales hallazgos9.
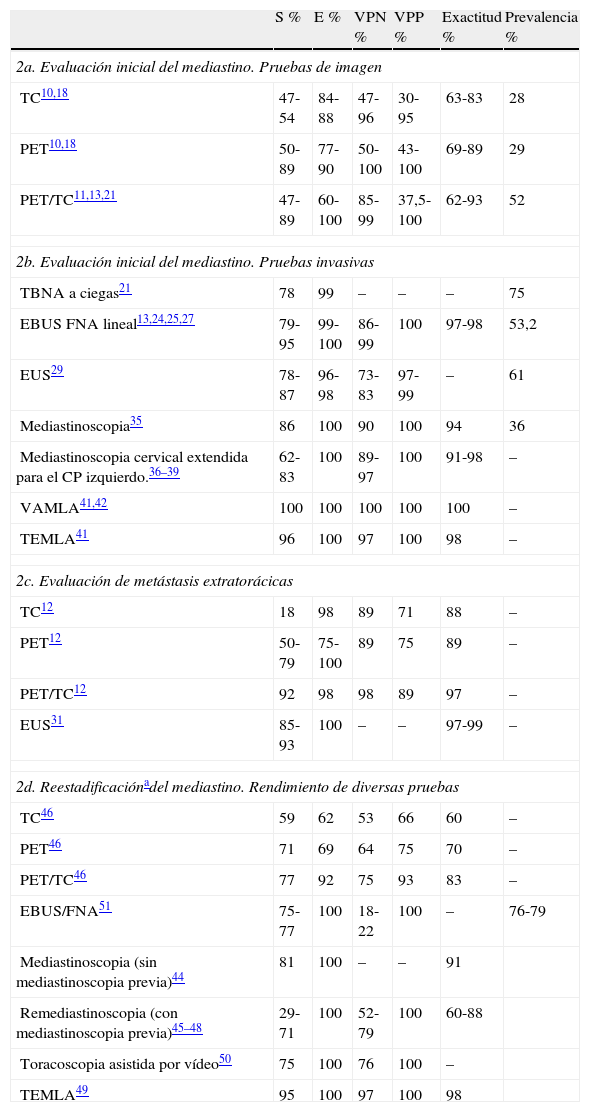
Rendimiento diagnóstico de diversas pruebas en la estadificación del CP
| S % | E % | VPN % | VPP % | Exactitud % | Prevalencia % | |
| 2a. Evaluación inicial del mediastino. Pruebas de imagen | ||||||
| TC10,18 | 47-54 | 84-88 | 47-96 | 30-95 | 63-83 | 28 |
| PET10,18 | 50-89 | 77-90 | 50-100 | 43-100 | 69-89 | 29 |
| PET/TC11,13,21 | 47-89 | 60-100 | 85-99 | 37,5-100 | 62-93 | 52 |
| 2b. Evaluación inicial del mediastino. Pruebas invasivas | ||||||
| TBNA a ciegas21 | 78 | 99 | – | – | – | 75 |
| EBUS FNA lineal13,24,25,27 | 79-95 | 99-100 | 86-99 | 100 | 97-98 | 53,2 |
| EUS29 | 78-87 | 96-98 | 73-83 | 97-99 | – | 61 |
| Mediastinoscopia35 | 86 | 100 | 90 | 100 | 94 | 36 |
| Mediastinoscopia cervical extendida para el CP izquierdo.36–39 | 62-83 | 100 | 89-97 | 100 | 91-98 | – |
| VAMLA41,42 | 100 | 100 | 100 | 100 | 100 | – |
| TEMLA41 | 96 | 100 | 97 | 100 | 98 | – |
| 2c. Evaluación de metástasis extratorácicas | ||||||
| TC12 | 18 | 98 | 89 | 71 | 88 | – |
| PET12 | 50-79 | 75-100 | 89 | 75 | 89 | – |
| PET/TC12 | 92 | 98 | 98 | 89 | 97 | – |
| EUS31 | 85-93 | 100 | – | – | 97-99 | – |
| 2d. Reestadificaciónadel mediastino. Rendimiento de diversas pruebas | ||||||
| TC46 | 59 | 62 | 53 | 66 | 60 | – |
| PET46 | 71 | 69 | 64 | 75 | 70 | – |
| PET/TC46 | 77 | 92 | 75 | 93 | 83 | – |
| EBUS/FNA51 | 75-77 | 100 | 18-22 | 100 | – | 76-79 |
| Mediastinoscopia (sin mediastinoscopia previa)44 | 81 | 100 | – | – | 91 | |
| Remediastinoscopia (con mediastinoscopia previa)45–48 | 29-71 | 100 | 52-79 | 100 | 60-88 | |
| Toracoscopia asistida por vídeo50 | 75 | 100 | 76 | 100 | – | |
| TEMLA49 | 95 | 100 | 97 | 100 | 98 | |
TC: tomografía computarizada; PET: tomografía de emisión de positrones; TBNA: punción-aspiración transbronquial con aguja. EBUS FNA: ultrasonografía endobronquial y aspiración con aguja fina; EUS: ultrasonografía esofágica; VAMLA: linfadenectomía mediastínica asistida por vídeo; TEMLA: linfadenectomía mediastínica transcervical extendida.
En general, se acepta el tamaño de 1cm en el diámetro más corto como el límite superior de la normalidad, aunque este criterio no es útil para discernir entre ganglios malignos y benignos9,10. Alrededor del 40% de los ganglios mediastínicos sugestivos de malignidad según la TC son benignos, y el 20% de los aparentemente benignos finalmente no lo son. Incluso entre pacientes con estadio clínico 1A, el 5-15% mostrarán afectación ganglionar en el examen quirúrgico-patológico10. Estas limitaciones en el rendimiento diagnóstico (tabla 2) obligan a confirmar los hallazgos de la TC mediante otras pruebas más fiables.
Metástasis a distancia (M)Hígado y suprarrenales. Las metástasis hepáticas aisladas no son frecuentes en el CPNM, pero sí en el CPM. Las suprarrenales son frecuente lugar de metástasis, aunque su diferenciación con adenomas benignos a menudo exige la obtención de muestra citohistológica. Por ello, se suelen realizar en una misma exploración la TC de tórax y abdomen superior. En cuanto a la búsqueda de posibles metástasis extratorácicas, las recomendaciones se comentan más adelante.
Tomografía de emisión de positrones. (PET y PET/TC)La PET, modalidad diagnóstica basada en la mayor actividad metabólica de las células neoplásicas, aporta información de interés sobre la biología tumoral, pero su capacidad de resolución espacial es menor que la de la TC. En cuanto al umbral de normalidad para el denominado valor de captación estándar (SUV), cada centro deberá establecer su propio punto de corte. El desarrollo de la PET/TC, que integra en una única exploración las imágenes de ambos procedimientos, mejora la eficacia diagnóstica11,12. Para la evaluación del mediastino, dicha eficacia es superior a la de la TC (tabla 2), aunque varía según la estirpe: así, para el adenocarcinoma, el VPP de la PET/TC es del 50%, y el VPN, del 77,8%, mientras que para el carcinoma escamoso dichas cifras son del 23,1 y del 96,3%, respectivamente13.
Sin embargo, la captación elevada de glucosa en procesos benignos, como granulomas, infecciones, etc. ocasiona una tasa de resultados falsos positivos (FP) del 20-25%, por lo que se aconseja la confirmación de tales hallazgos mediante la obtención de muestra citohistológica antes de rechazar la opción quirúrgica en un paciente potencialmente candidato. Por el contrario, ante un resultado negativo de la PET en la evaluación mediastínica, se considera aceptable proceder a la intervención sin pruebas invasivas previas, con las excepciones siguientes: a) tumores de localización central, habitualmente en contacto con el mediastino; b) tumores de baja actividad metabólica; c) aparente afectación N1, o d) cuando se han detectado en la TC ganglios con cuyo menor diámetro es >15mm; en esta última situación, un metaanálisis reveló una probabilidad post-test de afectación tumoral del 21%14,15.
Los resultados de la PET, o de la PET/TC, dada su elevada S para detectar metástasis a distancia, pueden ser relevantes para modificar el plan terapéutico, especialmente para evitar toracotomías innecesarias16. Por otro lado, en pacientes candidatos a radioterapia, la PET/TC permite una mejor delimitación de la zona a irradiar17. Por ello se recomienda su uso en pacientes con estadio clínico 1A-IIIA, provisionalmente subsidiarios de tratamiento radical, si bien su utilidad en el estadio IA es menos evidente10.
Búsqueda de metástasis extratorácicasUna evaluación clínica cuidadosa continúa siendo el mejor método para la predicción de metástasis. Síntomas inespecíficos, como pérdida de peso, astenia, dolores osteomusculares u otros más específicos, como cambios sutiles del humor o leve pérdida de fuerza en un miembro, así como alteraciones bioquímicas o hematológicas no explicadas por otro motivo (hipercalcemia, hipoalbuminemia, elevación de LDH, anemia, etc.), se asocian con la presencia de metástasis. Las pruebas de imagen para diagnósitco estarán dirigidas por la localización de los síntomas o signos presentes. Así, el dolor óseo justifica la realización de una gammagrafía, que tiene una S del 87% y una E del 67% para detectar metástasis óseas10. Dada la frecuente existencia de lesiones degenerativas o postraumáticas, no es raro encontrar imágenes dudosas, en cuyo caso la PET puede ser de utilidad, ya que tiene una elevada exactitud, con S, E, VPP y VPN superiores al 90%9. La PET, o la PET/TC, son más resolutivas que la TC para discernir lesiones hepáticas o suprarrenales, especialmente cuando son grandes, en cuyo caso la exactitud se aproxima al 100%. En lesiones con diámetro <15mm el rendimiento es mucho menor. Además de su mayor eficacia diagnóstica en las localizaciones habituales, la PET puede detectar metástasis u otros tumores primarios en lugares insospechados, como el tracto gastrointestinal, la vejiga, los tejidos blandos, etc. Publicaciones recientes demuestran que la PET/TC mejora el rendimiento de la PET o la TC aisladas, aunque el 15% de las imágenes anormales son clasificadas como indeterminadas12,18.
La tabla 2 resume algunos resultados de dichos estudios, si bien las cifras de VPN podrían estar sobreestimadas por limitaciones de seguimiento derivadas del escaso tiempo transcurrido desde la introducción de la PET/TC. La práctica sistemática de esta prueba mejora la estadificación, al detectar metástasis a distancia ocultas tras una estadificación convencional (desde el 8% en pacientes en estadio I provisional, hasta el 24% en estadio III, mediante PET/TC), reduciendo así el número de toracotomías inútiles16.
Pero no está exenta de inconvenientes, pues la existencia de resultados falsos positivos (FP) a menudo exige realizar procedimientos de riesgo para obtener confirmación citohistológica de una lesión que finalmente resulta benigna. En general, salvo evidencia clínica y radiográfica abrumadora, los hallazgos de imágenes sugestivas de metástasis, especialmente cuando se trata de un foco único de hipercaptación, no deben conducir a excluir a los pacientes de tratamientos potencialmente curativos si no se obtiene confirmación histológica de malignidad18. Por otro lado, hay que recordar que, en algunos casos, la comprobación de una metástasis única (suprarrenal o cerebral) no implica necesariamente renunciar al tratamiento quirúrgico del tumor primario, ya que aquella podría ser también extirpada8.
En cuanto al diagnóstico de metástasis cerebrales, se debe realizar una TC o resonancia magnética (RM) craneal ante cualquier síntoma o signo neurológico sospechoso, así como en pacientes con estadio III asintomáticos en los que se considere la posibilidad de tratamiento agresivo (cirugía o radioterapia torácica)19. En estadios más tempranos la indicación es más discutible, aunque dada la mayor incidencia en las estirpes no escamosas (incluso del 20%), parece aconsejable su realización.
RM torácicaSe recomienda su uso solo en algunas circunstancias especiales, como en los tumores del sulcus superior por su superioridad sobre la TC para evaluar la invasión del plexo braquial, los vasos mediastínicos o el cuerpo vertebral, de modo que la exactitud diagnóstica para evaluar la extensión del tumor puede llegar hasta el 94%, frente al 63% de la TAC9.
Procedimientos de estadificación invasivos no quirúrgicosLa exploración endoscópica, tanto digestiva como respiratoria, permite obtener muestra citohistológica de los ganglios mediastínicos a partir de la punción aspirativa con aguja fina (PAAF). La punción transbronquial puede realizarse de dos formas: a ciegas (transbronchial needle aspiration [TBNA]) o bien ecodirigida en tiempo real (endobronchial ultrasonograhy [EBUS]). Con la punción transbronquial se pueden alcanzar las estaciones mediastínicas altas (2, 3p y 4), la subcarínica (7) y las intrapulmonares hiliares (10) y las lobares (11). La PAAF transesofágica (EUS-PAAF) se realiza con control ultrasonográfico en tiempo real y permite alcanzar las estaciones paratraqueal inferior izquierda (4L), con frecuencia la subaórtica (5) y todas las mediastínicas bajas (7, 8 y 9). En algunas ocasiones, si la adenopatía se localiza relativamente posterior, es posible acceder también a la 4R, la 2R y la 2L. La EBUS y EUS-PAAF de lesiones mediastínicas son procedimientos seguros que pueden practicarse en régimen ambulatorio. No se han descrito complicaciones importantes en la punción de adenopatías mediastínicas20.
Aunque no existe un consenso sobre cuál debe ser el estándar de una exploración ecoendoscópica, sería recomendable: 1) explorar y puncionar todos los ganglios sospechosos en la PET-TC, descartando de forma secuencial N3, N2 y N1, y 2) explorar las estaciones ganglionares N3 en todos los casos con intención curativa radical y puncionar los ganglios ≥5mm de diámetro. Estudios recientes indican que deberíamos considerar negativo el resultado de la ecoendoscopia cuando no se evidencie malignidad después de 3 punciones con presencia de linfocitos en el examen citológico peroperatorio. Asimismo, si la muestra está contaminada, es necrótica, insuficiente o hemática, debería considerarse como indeterminada, y la negatividad para células malignas habría de confirmarse mediante técnicas quirúrgicas.
Punción transbronquial a ciegas (TBNA)En una revisión sistemática de 17 estudios se establece que la TBNA posee una S del 78%, una E del 100% y una tasa de FN del 28%21. La eficacia diagnóstica solo se aproxima a la punción orientada por ecografía en la estación subcarínica; en el resto, su rendimiento es inferior (58% vs 84%)22. Si se introducen criterios de coste-efectividad, la TBNA es menos recomendable que las técnicas ecoendoscópicas y la mediastinoscopia (MED) cuando la prevalencia de afectación ganglionar mediastínica es superior al 25%23.
Ultrasonografía endoscópica respiratoria (EBUS)En un metaanálisis centrado en la estadificación del CP por EBUS se revisaron un total de 11 estudios, que incluían 1.299 pacientes24. La S global fue del 93% y la E global del 100%, con una prevalencia media de 53,2%. El análisis por subgrupos destaca que la selección de pacientes con ganglios anormales por TC o PET, así como la disponibilidad de diagnóstico citopatológico inmediato, son factores independientes que incrementan la S global hasta valores de 94 y del 97%, respectivamente. En ausencia de diagnóstico citohistológico inmediato, el rendimiento diagnóstico está en función del número de punciones aspirativas que se realizan por ganglio. La S es del 69,8, del 83.7 y del 95,3% para la primera, la segunda y la tercera punción, mientras que el VPN es del 86,5, del 92,2 y del 97,6%, respectivamente25.
La alta precisión diagnóstica de la EBUS para la estadificación ganglionar mediastínica puede mantenerse incluso en ganglios de diámetro <1cm. En un estudio de 100 pacientes con ganglios normales por TC (diámetro menor entre 5 y 10mm; media, 8,1mm) se obtuvo una S del 92,3% y una E del 100%, con un VPN del 96,3%26. En todos se realizó control quirúrgico, mediante toracotomía (85%) o MED (15%). Incluso, en un segundo estudio con 100 pacientes con CP y PET con un mediastino morfometabólicamente normal, la EBUS-PAAF tuvo una S del 89%, una E del 100% y un VPN del 98,9% en la detección de metástasis ganglionares27.
No se han publicado datos respecto a análisis de coste-efectividad, aunque su realización puede ahorrar entre un 30 y un 56% de mediastinoscopias28.
Ultrasonografía endoscópica digestiva (EUS)En un metaanálisis que agrupa 18 estudios se concluye que la S global de la técnica es del 83% y la E global, del 97%. Cuando la exploración se realiza en pacientes con TC patológico, la S aumenta al 90%, con una E del 97%29. Es posible puncionar ganglios en pacientes con mediastino normal por TC (diámetro <1cm), con una S entre 50 y 61% y una E entre 98 y 100%30.
La EUS-PAAF permite además detectar metástasis subdiafragmáticas (glándula suprarrenal izquierda, ganglios del tronco celíaco e hígado)31, así como valorar la presencia de invasión mediastínica por parte del tumor (T4) con mucha más precisión que las técnicas radiológicas (S, 98%; E, 98%; FN, 1%, y FP, 30%)32.
En un estudio aleatorizado comparativo entre MED y EUS- PAAF sistemática en 104 pacientes candidatos a cirugía, se demuestra que esta última alternativa reduce el número de toracotomías innecesarias del 25 al 9%33.
Exploración ultrasonográfica mediastínica globalLa combinación de EUS-PAAF y EBUS-PAAF permite un acceso complementario a todas las estaciones ganglionares mediastínicas, excepto la 6. La S de esta combinación es del 93%, con un VPN del 97%. En un modelo de análisis de costes, del año 2007, según los baremos de las aseguradoras médicas americanas, se estima que la combinación de EBUS y EUS es coste-efectiva respecto a la MED con prevalencia de ganglios afectados superior al 32,9%. Por debajo de esta cifra, la aproximación más coste-efectiva es la EUS23.
Procedimientos de estadificación mediante técnicas quirúrgicasMediastinoscopia (MED), mediastinotomía (MEDTM), mediastinoscopia cervical extendida (MEDCE) y videotoracoscopiaLas dos guías de práctica clínica más recientes13,21 sobre estadificación clínica del CP coinciden en recomendar, con un grado de recomendación 1B21, la confirmación citohistológica de las alteraciones radiológicas o metabólicas que sugieran afectación ganglionar mediastínica. Ambas guías, elaboradas antes de publicaciones recientes sobre el rendimiento de la EBUS27 y la EUS29, también recomiendan una técnica quirúrgica mínimamente invasiva si esta confirmación se ha realizado con una técnica endoscópica y el resultado del estudio citohistológico de la muestra ha sido negativo para malignidad o no concluyente.
La técnica quirúrgica más utilizada en estos casos es la MED. Permite explorar las estaciones ganglionares paratraqueales derechas e izquierdas, superiores e inferiores, y la estación subcarínica. El requerimiento mínimo aceptable para la MED es la biopsia de, al menos, un ganglio de las estaciones paratraqueales inferiores, derechas e izquierdas, y de la subcarínica13. Si el tumor es izquierdo, se precisa ampliar la exploración a las estaciones ganglionares subaórtica y paraaórtica, sobre todo si el tumor es hiliar o del lóbulo superior. Tanto la MEDTM paraesternal izquierda como la MEDCE dan acceso a estas dos estaciones ganglionares. La experiencia con 739 MEDTM sistemáticas para estadificación del CP izquierdo pone de manifiesto el aumento de exploraciones positivas cuando se combina con la MED (un 28% de las exploraciones), y la toma de muestra sistemática de la grasa mediastínica cuando no se encuentran adenopatías en estos niveles revela infiltración neoplásica en el 6% de los casos34. Realizadas en combinación de forma sistemática en pacientes candidatos a la resección pulmonar, la MED y la MEDTM paraesternal izquierda o la MEDCE alcanzan los siguientes resultados: S, 86%; E, 100%; exactitud diagnóstica, 94%; VPP, 100%, y VPN, 90%35. Cuando estas exploraciones son negativas, la posibilidad de encontrar ganglios metastatizados en las estaciones ganglionares mediastínicas inferiores es muy baja (1,2% de los casos)35, por lo que su exploración sistemática con toracoscopia o punción transesofágica guiada por ultrasonidos, cuando las técnicas de imagen son normales, no estaría indicada. La tasa de complicaciones de estas exploraciones se sitúa alrededor del 3%, y la de mortalidad, sobre el 0,1%.
Hay pocas publicaciones sobre la MEDCE en sustitución de la MEDTM paraesternal izquierda para estadificación del CP izquierdo, pero sus resultados son muy homogéneos36-39. Es una alternativa válida a la MEDTM paraesternal izquierda sin complicaciones específicas asociadas. Su elevado VPN es relevante para indicar la resección pulmonar sin necesidad de tratamiento de inducción.
La toracoscopia, con o sin asistencia de vídeo, permite una exploración completa de la cavidad pleural y del mediastino ipsilateral, si no hay adherencias pleurales que lo impidan. En condiciones ideales, permite el acceso a las estaciones ganglionares paratraqueales inferiores derechas e hiliares, subcarínicas, paraesofágicas y del ligamento pulmonar inferior en ambos lados, así como a las estaciones subaórticas y paraaórticas en el lado izquierdo. Comparada con la MED, tiene el inconveniente de que es una exploración unilateral, por lo que no puede descartar afectación N3, salvo que se exploren ambos hemitórax. Es útil en el estudio de los derrames pleurales acompañantes, para confirmar o descartar la afectación pleural, y en el diagnóstico de nódulos pulmonares si su localización periférica permite biopsiarlos o extirparlos mediante resección pulmonar atípica. Su utilización antes de la toracotomía, asociada a pericardioscopia, puede identificar causas de irresecabilidad y evitar toracotomías exploradoras en el 10% de los pacientes40.
La adaptación de una cámara de vídeo al mediastinoscopio ha hecho evolucionar la técnica de una forma insospechada. Se han descrito dos formas de linfadenectomía mediastínica por vídeo-MED que son equivalentes a la disección ganglionar mediastínica realizada por toracotomía. Se trata de la linfadenectomía mediastínica asistida por vídeo (VAMLA, video-assisted mediastinoscopic lymphadenectomy[VAMLA])41,42 y de la linfadenectomía mediastínica transcervical extendida (TEMLA, transcervical extended mediastinal lymphadenectomy)43 (tabla 2). Es de interés destacar que, en las últimas 150 TEMLA, todos los parámetros diagnósticos fueron del 100%.
Todas estas técnicas también son útiles para la reestadificación, indicada en la valoración preoperatoria de segundos tumores primarios, en tumores recidivados y, con mayor frecuencia en el momento actual, en la valoración de la respuesta tumoral después de tratamiento de inducción en casos de CP localmente avanzados. Para esta última indicación, la tabla 2 resume los resultados de la MED de reestadificación sin MED previa44, de la remediastinoscopia (REMED)45-48, de la TEMLA49 y de la videotoracoscopia50. En el caso de la MED de reestadificación sin MED previa, es lógico que los valores sean superiores a los de la REMED, ya que el mediastino superior no se ve alterado por las adherencias del primer procedimiento quirúrgico. Los resultados de la REMED son muy homogéneos cuando se ha realizado de forma sistemática. Solo una serie destaca por su baja S y bajo VPN. Sin embargo, en esa serie, en más del 60% de los pacientes, en la REMED no se biopsiaron los ganglios subcarínicos, que son los más afectados junto con los paratraqueales derechos inferiores. La TEMLA tiene los mejores valores de reestadificación, pero hay que tener en cuenta que, en estos casos, la estadificación se hizo mediante EBUS. Por tanto, no había adherencias mediastínicas, que son las que más dificultan la REMED. Por último, la videotoracoscopia se ha utilizado poco en la reestadificación, pero los resultados de este único estudio multicéntrico50 indican que pueden ser equiparables a los de la REMED.
ReestadificaciónAunque la combinación de quimioterapia y radioterapia torácica (RTT) es el tratamiento indicado en la mayoría de pacientes con afectación tumoral mediastínica, N2, algunos con circunstancias favorables y previsiblemente subsidiarios de lobectomía pueden beneficiarse de la resección quirúrgica, siempre que el tratamiento de inducción consiga una remisión completa histológica de las adenopatías mediastínicas. La persistencia de tumor en dichas adenopatías es generalmente considerada contraindicación de la cirugía. De ahí la importancia crucial de una evaluación precisa de la respuesta ganglionar al tratamiento de inducción. La TC puede detectar cambios en el tamaño tumoral que tienen lugar después del tratamiento de inducción, pero incluso en caso de gran reducción de volumen tumoral post-quimioterapia a menudo persisten clones de células malignas viables, y, por otro lado, también se sabe que masas residuales de considerable volumen pueden estar constituidas solo por tejido fibrótico. A este respecto, la PET y la PET/TC han demostrado recientemente mayor exactitud en la evaluación de la respuesta al tratamiento, aunque el rendimiento diagnóstico es sustancialmente menor que en la estadificación inicial (tabla 2). Por tanto, es esencial obtener una muestra citohistológica de los ganglios mediastínicos después del tratamiento de inducción. La EBUS tiene una S del 76% y una E del 100% para analizar la respuesta a la quimioterapia de inducción. Sin embargo su VPN es del 20%, lo que obliga a comprobación quirúrgica51. Stigt et al, en un grupo de 26 pacientes a los que se les realiza quimioterapia de inducción y comprobación por EUS, obtuvo un VPN es del 91,6%52. Hasta la fecha, no existen estudios de reestadificación endoscópica combinada.
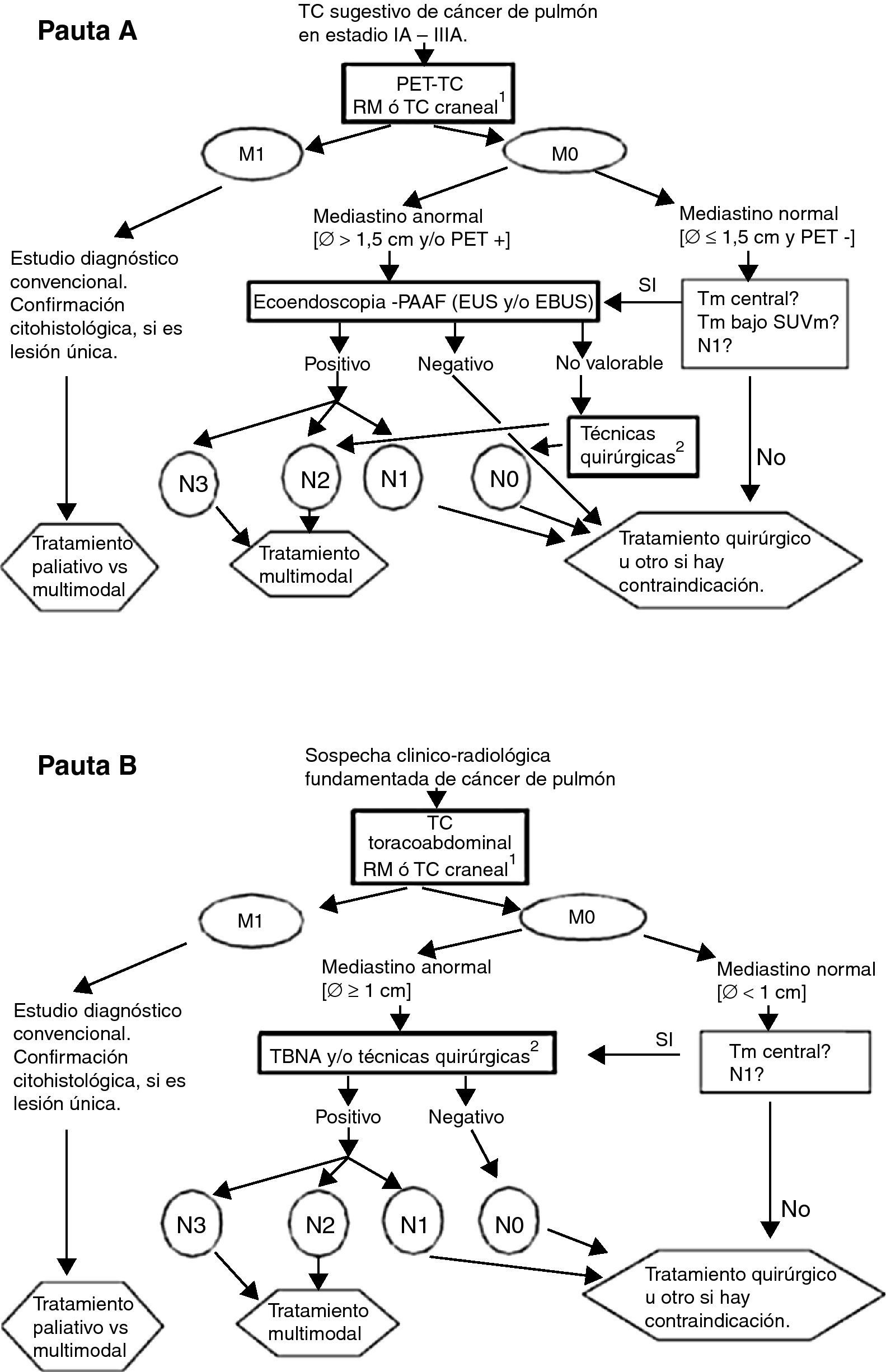
Después de evaluar la información reciente sobre el rendimiento de diversas pruebas, en la figura 1 se recomiendan pautas de actuación adaptadas a los medios disponibles. La B, aunque no óptima, puede ser aún la única opción disponible en algunos centros.
Pautas de estadificación del cáncer de pulmón. A) RM craneal para pacientes candidatos a tratamiento radical en estadio III. B)Técnicas quirúrgicas: se incluyen mediastinoscopia, mediastinotomía, mediastinoscopia cervical extendida, toracoscopia, linfadenectomía mediastínica transcervical extendida (TEMLA) y linfadenectomía mediastínica videoasistida (VAMLA).
Notas: a) Se considerará negativo el resultado de la EBUS solo si, después de al menos tres punciones con presencia de linfocitos, no se observan células malignas. b) La pauta B puede ser aceptable en los centros sin accesibilidad a PET, EBUS ni EUS. c) El límite de 1,5cm para el tamaño de los ganglios mediastínicos en la pauta A se fundamenta en un metaanálisis (ver texto y referencia 14), El límite de 1cm (pauta B) es el empleado tradicionalmente.
Una correcta clasificación patológica tumoral y ganglionar es muy importante para proporcionar un pronóstico, indicar el tratamiento adyuvante y llevar a cabo comparaciones en estudios clínicos.
Estadificación patológica quirúrgicaEvaluación de la afectación tumoral TDurante la cirugía se deben tomar muestras histológicas de las estructuras anatómicas que macroscópicamente sean sospechosas de invasión tumoral y que modifiquen la clasificación T del tumor. El estudio se efectuará intraoperatoriamente, y en caso de ser positivo, puede variar la extensión de la resección necesaria. Aunque estas situaciones deben evaluarse preoperatoriamente, en determinadas afectaciones T4 puede conseguirse una resección completa del tumor, de la carina traqueal, del nervio laríngeo o del cuerpo vertebral.
En estos casos debe excluirse la afectación N2 también de forma intraoperatoria53. En pacientes con un nódulo satélite en el mismo lóbulo de un CP diagnosticado no se requiere investigación intraoperatoria54. Finalmente, si durante la cirugía se encuentra otro tumor en un lóbulo diferente, se debe realizar el tratamiento de ambos tumores una vez excluida la afectación N2 también de forma intraoperatoria54.
Evaluación de la afectación ganglionar NLa mejor forma de clasificar la resección pulmonar es la estadificación ganglionar intraoperatoria. El impacto de la afectación ganglionar en el pronóstico facilita la toma de decisiones sobre la indicación de tratamientos adyuvantes. Se considera un elemento clave para considerar una cirugía completa y un requerimiento esencial en el control de calidad de la cirugía55. Las técnicas utilizadas van desde la simple inspección hasta la linfadenectomía bilateral en bloque. La extensión de la evaluación ganglionar dependerá de las implicaciones pronósticas, de la posible inclusión en tratamientos complementarios, incluso de la posibilidad de recidiva local de la enfermedad. El balance entre el riesgo de una exploración exhaustiva y extensa, con la morbilidad asociada, y la correcta clasificación de la afectación ganglionar debe guiar la toma de decisiones.
El ensayo clínico del American College of Surgery Oncology Group (ACOSOG Z0030)54 diseñado para determinar el efecto de la linfadenectomía sobre la supervivencia, en pacientes operados por CP, no demostró diferencias de morbimortalidad entre la linfadenectomía y el muestreo ganglionar. Aunque los resultados de este estudio sobre la supervivencia están por comunicar, un metaanálisis llevado a cabo por Wright et al56 sobre 3 ensayos clínicos, con pocos pacientes e importantes limitaciones metodológicas, sugiere que la linfadenectomía mejora la supervivencia, comparada con el muestreo ganglionar.
Aunque la afectación multiestación, tanto N1 como N2, parece tener peor pronóstico que una sola4, no hay evidencias para modificar las recomendaciones de evaluación.
La guía de evaluación intraoperatoria de la ESTS57 propone las siguientes definiciones sobre los métodos de evaluación ganglionar durante la cirugía:
- 1.
Biopsia ganglionar selectiva. Consiste en biopsiar uno o varios ganglios de aspecto sospechoso. Estaría justificado solo para demostrar la afectación N1 o N2 cuando la resección no es posible (toracotomía exploradora).
- 2.
Muestreo. Es la exploración mediante extirpación de ganglios de un número preestablecido de estaciones ganglionares pulmonares y mediastínicas con un fin concreto. Muestreo sistemático: resección de estaciones predeterminadas por el cirujano.
- 3.
Disección ganglionar sistemática. Resección sistemática de todo el tejido mediastínico, incluyendo las adenopatías entre los límites anatómicos. En los tumores del lado izquierdo, para poder acceder a las estaciones paratraqueales altas y bajas se debe liberar el ligamento arterioso para poder movilizar el arco aórtico. Se requiere un mínimo de 3 estaciones ganglionares (incluyendo siempre la subcarínica). Los ganglios deben identificarse y ser analizados histológicamente de forma separada. Además, se deben disecar las adenopatías hiliares e intrapulmonares.
- 4.
Disección ganglionar sistemática lóbulo-específica. Resección sistemática de todo el tejido mediastínico, incluyendo las adenopatías, dependiendo del lóbulo donde se localice el tumor. Este tipo de disección selectiva es aplicable a carcinomas escamosos T1. Las áreas a explorar según el lóbulo afectado, siguiendo las descripciones de Naruke58 y de Ichinose59 y las normas del Grupo Cooperativo de Carcinoma Broncogénico de SEPAR55, son: disección y examen histológico de los ganglios hiliares e intrapulmonares (lobares, interlobares y segmentarios) y al menos tres de las siguientes estaciones ganglionares mediastínicas, según la localización lobar del tumor primario: a) lóbulo superior derecho y lóbulo medio: áreas 2R, 4R y 7; b) lóbulo inferior derecho: áreas 4R, 7, 8 y 9; c) lóbulo superior izquierdo: áreas 5, 6 y 7; d) lóbulo inferior izquierdo: áreas 7, 8 y 9. En total debería incluir 6 ganglios.
- 5.
Disección ganglionar extendida. Se define como la de los ganglios pulmonares y mediastínicos contralaterales, como complemento a la disección ganglionar sistemática ipsilateral al tumor. Incluye la disección cervical y generalmente se realiza mediante esternotomía media.
En pacientes con tumores en estadio I o II y que pueden tolerar una resección pulmonar, el procedimiento mínimo recomendado es la lobectomía60. En pacientes con estadio I y que pueden tolerar una intervención quirúrgica pero no una lobectomía, la resección sublobar (segmentectomía reglada o atípica) es preferible al tratamiento no quirúrgico60. En el estadio I el abordaje mediante cirugía mínimamente invasiva es tan recomendable como la toracotomía estándar61. En pacientes con tumores centrales o localmente avanzados, así como en aquellos con N1, la resección completa mediante técnicas broncoplásticas ofrece mejores resultados que la neumonectomía62.
Definición de resección tumoral completa. La IASLC define como resección tumoral completa63 la que cumple los siguientes criterios:
- a)
Márgenes de resección libres demostrados microscópicamente. Estos márgenes deben incluir los muñones de arterias, venas y bronquios, los tejidos blandos peribronquiales y cualquier margen periférico cercano al tumor o al resto del tejido resecado.
- b)
Disección ganglionar sistemática en su forma más amplia, o bien disección ganglionar sistemática lóbulo-específica (tal como se describe más arriba). Las muestras deben incluir, al menos, seis ganglios, tres de las estaciones intrapulmonares y/o hiliares y tres de las mediastínicas, una de las cuales debe ser la subcarínica.
- c)
No debe haber extensión extracapsular del tumor en los ganglios resecados de manera aislada o en los localizados en el margen del principal tumor pulmonar.
- d)
El ganglio mediastínico extirpado más alto debe ser negativo.
Procesado y estudio macroscópico. La pieza se fijará óptimamente insuflando la vía aérea con formol, que es el fijador de rutina. Las medidas de la pieza y el tumor se toman una vez fijada la pieza.
La valoración del tumor debe incluir: a) localización parenquimatosa o endobronquial (si el bronquio es principal, lobar o segmentario) y su relación con la pleura; b) diámetro mayor; c) descripción (forma, color, delimitación, cavitación); d) extensión anatómica: afectación bronquial, invasión vascular, invasión pleural visceral o la menor distancia a la pleura visceral (la IASLC recomienda el uso de tinciones para la capa elástica de la pleura visceral, cuya afectación define la invasión de la pleura visceral, en los casos en que las tinciones normales con hematoxilina y eosina son dudosas)64,65, extensión a cisuras interlobares y tejidos adheridos; e) relación con márgenes, especificando la distancia menor (bronquial, vascular, superficie del parénquima resecado, tejidos adheridos), y f) presencia de otros nódulos tumorales. Los carcinomas primarios sincrónicos se estadifican independientemente.
Valoración del parénquima circundante. Normal o anormal, especificando la patología.
Ganglios linfáticos de la pieza operatoria. Localización, número y tamaño.
Ganglios linfáticos remitidos separados de la pieza. Con especificación de cada estación ganglionar, número y tamaño.
Estadificación molecular del cáncer de pulmónLa presencia de metástasis ganglionares es uno de los factores pronósticos más importantes en el CPNM. Entre el 30-40% de los pacientes sin afectación ganglionar aparente en el momento de la cirugía presentan recidiva tumoral y fallecen por este motivo. Esta subestadificación probablemente resulte de la existencia de células tumorales ocultas imposible de detectar por los métodos de imagen o histopatológicos habituales.
Se acepta el término micrometástasis como un foco de células tumorales entre 0,2 y 2mm de diámetro, siendo habitualmente solo detectable mediante inmunohistoquímica. En el CP se buscan proteínas asociadas a células epiteliales, como las citoqueratinas. Los distintos estudios concuerdan que la presencia de micrometástasis se asocia de forma fehaciente a un menor periodo libre de enfermedad y a una peor supervivencia global.
La estadificación molecular se refiere a la determinación de biomarcadores tumorales en el tejido linfático, como indicador de presencia de células neoplásicas. La detección y cuantificación de ARN mensajero que codifica proteínas propias de tumor o célula epitelial es posible mediante la quantitative reverse-transciptase-polimerase chain reaction (qRT-PCR).
También es posible analizar mutaciones específicas o alteraciones epigenéticas tumorales en el ADN extraído del ganglio linfático. La necesidad de mínima cantidad de tejido, una mayor sensibilidad de detección y menores costes son algunas de las ventajas del uso de qRT-PCR frente a la inmunohistoquímica.
Diversos estudios analizan el valor de distintos biomarcadores en muestras de ganglios extraídos quirúrgicamente66,67. También es posible estudiar la presencia de biomarcadores en ganglios mediastínicos mediante técnicas de punción ecoendoscópica, aunque los trabajos publicados al respecto son escasos68,69. La presencia de metilación o de ciertas mutaciones en los genes estudiados está relacionada con mayor frecuencia con recidiva tumoral y con menor supervivencia global y libre de enfermedad, pero no hay todavía series largas de pacientes con seguimientos prolongados, ni estudios aleatorizados que permitan afirmar con rotundidad que la estadificación molecular tenga relevancia clínica y pronóstica. Sin embargo, identificar a este grupo de pacientes en un futuro próximo va a permitir beneficiarse de algún tipo de quimioterapia u otros fármacos para así reducir el riesgo de recidiva.
Resumen de recomendaciones- 1.
La Sociedad Española de Neumología y Cirugía Torácica (SEPAR) acepta y recomienda emplear la 7.a edición de la clasificación TNM propuesta por la IASLC en 2009 y el nuevo mapa ganglionar de la IASLC para la estadificación del CPNM, del CPM y de los tumores carcinoides.
- 2.
Se debe realizar una TC de tórax y abdomen superior a todo paciente con sospecha o diagnóstico de CP que pueda ser susceptible de tratamiento. Grado de recomendación (Gr. R): consistente; Evidencia (Ev): moderada.
- 3.
En pacientes con estadio clínico IA- IIIA potencialmente candidatos a tratamiento radical, está indicada la realización de PET o PET/TC para la evaluación del mediastino y detección de posibles metástasis extratorácicas. Gr. R.: consistente; Ev: moderada (débil en estadio IA). En ausencia de M1, si la PET muestra hipermetabolismo en los ganglios mediastínicos, es necesaria la confirmación citohistológica (GrR: alta/Ev: alta). Si la PET es negativa, puede procederse directamente a la cirugía, salvo en las circunstancias siguientes: a) ganglios mediastínicos de cuyo menor diámetro es>15mm por TC con contraste; b) se trata de un tumor central (1/3 medial del hemitórax), habitualmente en contacto con el mediastino; c) el tumor tiene bajo SUVmax (como algunos adenocarcinomas), o d) existe sospecha de N1. En estas circunstancias se recomienda confirmación citohistológica de los ganglios mediastínicos previa a la intervención (GrR: consistente/Ev: moderada). La combinación de EBUS y EUS es el abordaje endoscópico de mayor rendimiento diagnóstico (GrR: consistente/Ev: alta).
- 4.
Un resultado negativo de una punción aspirativa debería ser confirmado mediante mediastinoscopia (GrR: débil/Ev: alta) cuando no se han realizado 3 pases en ausencia de diagnóstico citopatológico inmediato, o bien si el diagnóstico citopatológico no confirma presencia de tejido linfático normal.
- 5.
Se recomienda realizar una TC o RM craneal, ante cualquier síntoma o signo neurológico sospechoso, y en pacientes neurológicamente asintomáticos con estadio III en los que se considere la posibilidad de tratamiento radical (cirugía o radioterapia torácica). Gr. R.: consistente; Ev: moderada. En estadios más tempranos y estirpe no epidermoide parece útil, aunque la evidencia es menor.
- 6.
El hallazgo de una imagen anormal sugestiva de metástasis única debe confirmarse con muestra citohistológica de la lesión antes de excluir a los pacientes de tratamientos potencialmente curativos. Gr. R.: consistente; Ev: moderada.
- 7.
Cuando se prevea la posibilidad de cirugía tras tratamiento de inducción (estadio IIIA- N2), se recomienda reestadificar las lesiones mediastínicas mediante obtención de muestra citohistológica. Si el procedimiento utilizado ha sido una punción y el resultado es negativo, se recomienda una técnica quirúrgica de comprobación. Gr. R.: consistente; Ev: elevada.
- 8.
Entre los diversos abordajes posibles (TBNA, EUS-PAAF, EBUS-PAAF, MED, MEDTM, VAMLA o TEMLA) para la obtención de muestra citohistológica, se escogerá la técnica en función de la propia experiencia, prevaleciendo siempre la más coste-efectiva, menos invasora y con menor demora. Cada centro debería planificar la secuencia de posibles pruebas a realizar en función de su disponibilidad local, de modo que el comienzo del tratamiento se demore lo menos posible. Gr. R.: consistente; Ev: débil.
- 9.
La disección ganglionar sistemática es la evaluación ganglionar intraoperatoria recomendada: asegura una correcta estadificación que permite indicar el tratamiento adyuvante adecuado, no aumenta la morbimortalidad en relación con el muestreo ganglionar y parece que se asocia a un mejor pronóstico Gr. R.: consistente; Ev: elevada.