La artritis reumatoide (AR) es una causa importante de morbimortalidad en los países desarrollados, con una prevalencia entre el 0,5-1%, y una incidencia entre 5-50 personas por 100.000 habitantes. La nodulosis es la manifestación extraarticular más frecuente y se frecuenta en el 25% de los pacientes con AR1,2. Las manifestaciones pulmonares son variadas e incluyen nódulos necrobióticos, infecciones, lesión pulmonar inducida por fármacos, bronquiolitis obliterante, enfermedad pulmonar intersticial, bronquiectasias y tumores.
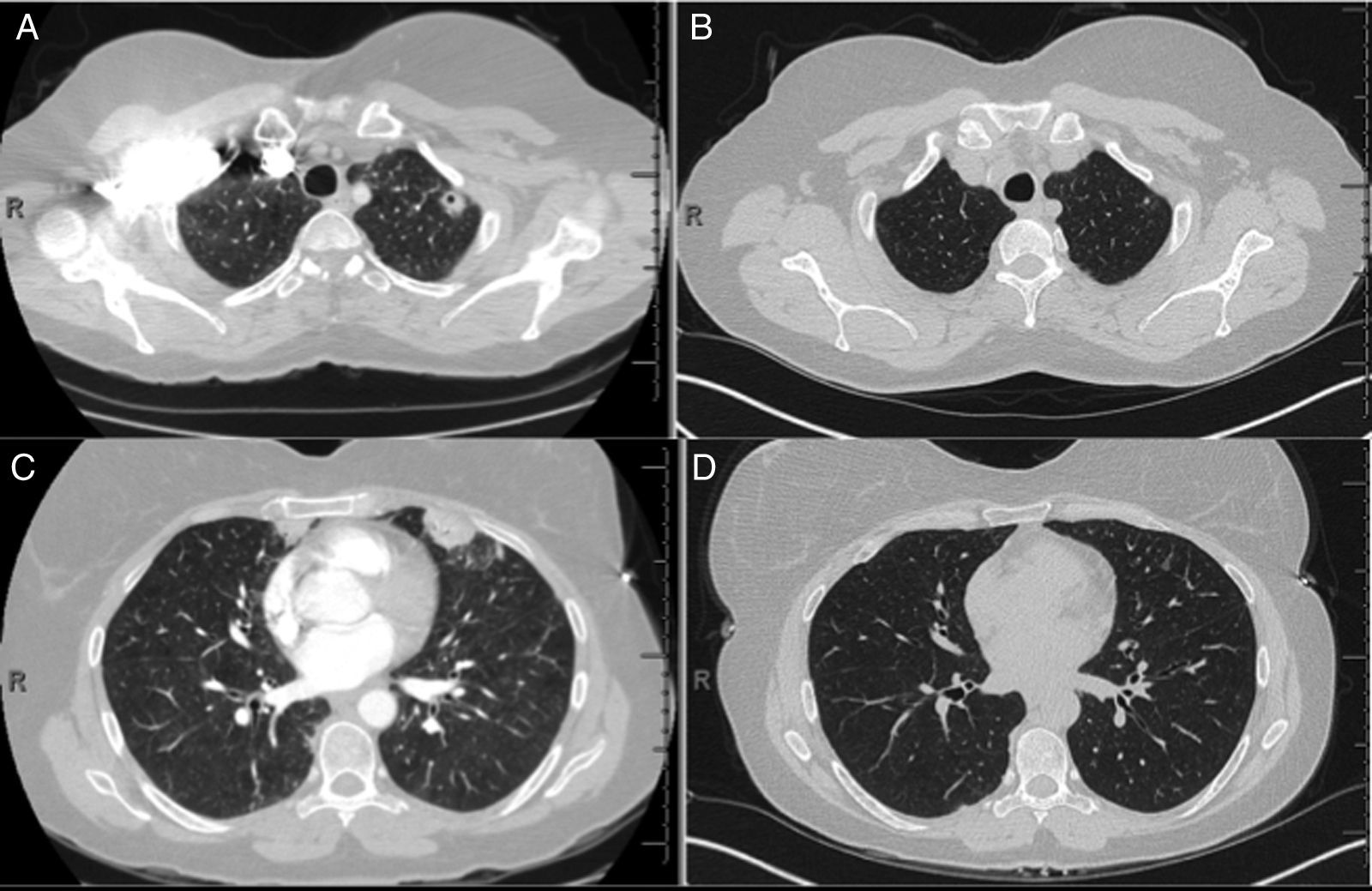
El factor de necrosis tumoral (TNF) es una citocina proinflamatoria sobreexpresada en los pacientes con AR. El American College of Rheumatology cuenta con recomendaciones oficiales sobre el uso de agentes biológicos anti-TNF en pacientes con AR con factores de mal pronóstico. Presentamos el caso de una mujer de 50 años que desarrolló consolidaciones nodulares multifocales, con y sin cavitación (figs. 1A y C), un mes tras iniciar tratamiento con etanercept. Se suspendieron los medicamentos inmunosupresores y el lavado broncoalveolar del lóbulo superior izquierdo y la língula fue negativo para etiología infecciosa. Al no haber confirmación de una infección, se reinició el tratamiento para la AR, exceptuando el etanercept. Una serie de estudios de tomografía computarizada (TC) mostraron la regresión de los nódulos en el intervalo. Se observaron cambios radiográficos en la TC de la visita de seguimiento a los 2 meses y ya no se han visto cambios a los 9 meses (figs. 1B y C).
TC torácica. A) La TC inicial muestra un nódulo en el lóbulo superior izquierdo con cavitación; B) La TC con mayor resolución del nódulo en el lóbulo superior izquierdo tras 9 meses de seguimiento; C) La TC inicial muestra el nódulo periférico en la língula; D) La TC con mayor resolución del nódulo periférico en la língula tras 9 meses de seguimiento.
La descripción de casos de enfermedad nodular asociada a etanercept ha sido variada, incluyendo desde nódulos pulmonares nuevos con histopatología típica de nódulos pulmonares de AR, a histopatología compatible con sarcoidosis o histopatología de infiltrados linfohistiocitarios no típicos de las anteriores3,4. Los tratamientos para nódulos pulmonares asociados al etanercept han variado, pero normalmente consisten en la administración de esteroides y la retirada del fármaco. También se han publicado 2 casos que destacan la evolución de los nódulos manteniendo el tratamiento con etanercept, bien ilustrando la regresión de los nódulos, o bien su estabilización, sin progresar a pesar de mantener el tratamiento con etanercept5.
Este caso es un ejemplo de que una proteína de fusión recombinante del receptor humano de TNF puede contribuir a la aparición contraintuitiva de enfermedad granulomatosa y nodulosis pulmonar. Se han propuesto diversos mecanismos para la aparición de nodulosis pulmonar, pero actualmente se desconoce el mecanismo exacto. Se ha propuesto que el crecimiento o la formación de nódulos pulmonares pueden estar relacionados con el aumento de tamaño de los núcleos necróticos, un resultado de la reducción de los niveles de TNF soluble, que estaría produciendo un efecto exagerado o alterado sobre otras vías inflamatorias. También se ha relacionado directamente con la progresión de la AR y no con el agente terapéutico1,4.
En conclusión, observamos que la aparición de nódulos pulmonares no es infrecuente en los pacientes con AR, pero recomendamos que su posible relación con el etanercept se tenga en cuenta en el diagnóstico diferencial. El lavado broncoalveolar debe continuar siendo parte integral de la evaluación pero, si el resultado no es determinante, sería razonable suspender el tratamiento con etanercept y hacer un seguimiento con una serie de estudios de imagen a las 6-8 semanas. Si los nódulos son estables o experimentan regresión, la serie de estudios de imagen habrá sido un abordaje razonable. Si la enfermedad progresa, se debe profundizar.
Considerar el etanercept como posible etiología de nódulos pulmonares nuevos puede disminuir la morbilidad asociada a procedimientos diagnósticos invasivos utilizados en el estudio de nódulos pulmonares, que serían innecesarios.