El diagnóstico de las lesiones pulmonares periféricas (LPP) constituye un verdadero reto para los neumólogos. La ecografía endobronquial radial (R-EBUS) es una técnica que se ha desarrollado para mejorar el rendimiento diagnóstico. El objetivo de este estudio fue evaluar la efectividad de la R-EBUS en el diagnóstico de las LPP.
MétodosSe llevó a cabo un estudio retrospectivo en 174 pacientes a los que se habían diagnosticado LPP y a los que se practicó una broncoscopia bajo guía de EBUS. Para el diagnóstico se evaluó el examen histológico de las muestras obtenidas mediante biopsia pulmonar transbronquial (BPTB) y los exámenes citológicos del frotis de cepillado, líquido de irrigación del cepillado y líquido de lavado broncoalveolar (LLBA).
ResultadosEl diámetro medio de las LPP fue de 25,1±10,7mm. Los diagnósticos finales fueron 129 enfermedades malignas y 45 lesiones benignas. El rendimiento diagnóstico global de la broncoscopia bajo guía de EBUS fue del 79,9%. Ni el tamaño ni la etiología de las LPP mostraron influencia alguna en el rendimiento diagnóstico de la broncoscopia bajo guía de EBUS (82,9% frente al 74,6% para las LPP de tamaño >20mm y las LPP de tamaño ≤20mm; p=0,19, y 82,9% frente al 71,1% para las enfermedades malignas y benignas; p=0,09). La BPTB fue la que obtuvo el máximo rendimiento de entre estas diversas muestras (69,0, 50,6, 42,0 y 44,3% para las muestras de BPTB, frotis de cepillado, líquido de irrigación de cepillado y LLBA, respectivamente; p<0,001). La combinación de BPTB, frotis de cepillado y LLBA aportó el máximo rendimiento diagnóstico, mientras que el líquido de irrigación de cepillado no añadió una mejora adicional de los resultados.
ConclusiónLa broncoscopia bajo guía de R-EBUS es una técnica útil en el diagnóstico de las LPP. Para alcanzar el máximo rendimiento diagnóstico deben utilizarse conjuntamente la BPTB, el frotis de cepillado y el lavado broncoalveolar.
The diagnosis of peripheral pulmonary lesions (PPLs) is a challenging task for pulmonologists. Radial probe endobronchial ultrasound (R-EBUS) has been developed to enhance diagnostic yield. The objective of this study was to evaluate the effectiveness of R-EBUS in the diagnosis of PPLs.
MethodsA retrospective study was conducted on 174 patients diagnosed with PPLs who underwent EBUS-guided bronchoscopy. Histological examination of specimens obtained by transbronchial lung biopsy (TBLB) and cytological examinations of brushing smear, brush rinse fluid and bronchoalveolar lavage fluid (BALF) were evaluated for the diagnosis.
ResultsThe mean diameter of the PPLs was 25.1±10.7mm. The final diagnoses included 129 malignancies and 45 benign lesions. The overall diagnostic yield of EBUS-guided bronchoscopy was 79.9%. Neither size nor etiology of the PPLs influenced the diagnostic performance of EBUS-guided bronchoscopy (82.9% vs. 74.6% for PPLs>20mm and PPLs≤20mm; p=0.19, and 82.9% vs. 71.1% for malignancy and benign diseases; p=0.09). TBLB rendered the highest yield among these specimens (69.0%, 50.6%, 42.0%, and 44.3% for TBLB, brushing smear, brush rinse fluid, and BALF, respectively; p<0.001). The combination of TBLB, brush smear, and BALF provided the greatest diagnostic yield, while brush rinse fluid did not add benefits to the outcomes.
ConclusionR-EBUS-guided bronchoscopy is a useful technique in the diagnosis of PPLs. To achieve the highest diagnostic performance, TBLB, brushing smear and bronchoalveolar lavage should be performed together.
La fibrobroncoscopia (FB) bajo guía fluoroscópica se ha venido utilizando desde la década de 1970 y ha pasado a ser una práctica estándar en el diagnóstico de las lesiones pulmonares periféricas (LPP)1,2. Los instrumentos de obtención de muestras, como cepillos o pinzas de biopsia, se introducen en el bronquio adecuado y se confirma su posición en el objetivo antes de la obtención de las muestras bajo control fluoroscópico. Lamentablemente, este abordaje broncoscópico tiene limitaciones en la evaluación de las LPP de pequeño tamaño. Para las LPP de un tamaño <2cm la técnica de broncoscopia citada tiene un rendimiento diagnóstico bastante bajo, que oscila entre el 11 y el 42%3,4.
La ecografía endobronquial radial (R-EBUS) es una técnica que se ha desarrollado para mejorar el rendimiento diagnóstico en las LPP desde la década de 1990. Desde entonces ha sido ampliamente aceptada por los neumólogos intervencionistas, dado su excelente rendimiento diagnóstico en las LPP de pequeño tamaño, sobre todo las <20mm5. La ventaja de la R-EBUS respecto a la fluoroscopia no está tan solo en la identificación de la localización anatómica, sino también en que informa de la estructura interna de las LPP. En consecuencia, resulta útil al broncoscopista para obtener una muestra de tejido adecuada del interior de la lesión. El rendimiento diagnóstico combinado en los cánceres de pulmón periférico fue del 73%, según lo indicado por un metaanálisis de 16 estudios publicados entre 2002 y 20096.
En nuestro centro, la broncoscopia guiada por R-EBUS para el diagnóstico de las LPP se utilizó por primera vez en junio de 2009. El objetivo de este estudio fue evaluar retrospectivamente la efectividad de la R-EBUS en el diagnóstico de las LPP. El objetivo secundario fue identificar la técnica de muestreo broncoscópico que alcanzaba un mayor rendimiento diagnóstico para reducir el coste de las muestras obtenidas.
Material y métodosHemos llevado a cabo una revisión retrospectiva de 174 pacientes a los que se diagnosticaron LPP y que fueron examinados mediante broncoscopia bajo guía de R-EBUS entre junio de 2009 y mayo de 2013 en el Hospital Ramathibodi, un centro de referencia universitario de nivel terciario de Bangkok (Tailandia). Este estudio retrospectivo fue aprobado por el Comité de Ética de Experimentación Humana del Hospital Ramathibodi, Facultad de Medicina, Universidad de Mahidol. La LPP se definió como una lesión del pulmón que está rodeada de parénquima pulmonar y que no es visible endoscópicamente mediante broncoscopia. Se realizó una tomografía computarizada (TC) de tórax en todos los casos, y se eligió un bronquio subsegmentario correspondiente a la LPP antes de realizar el procedimiento broncoscópico. Se registró el tamaño de la lesión mediante su diámetro máximo en la TC. Se obtuvo el consentimiento informado por escrito de todos los pacientes antes del inicio del procedimiento broncoscópico.
La broncoscopia mediante FB (BF-P180; Olympus, Tokio: diámetro externo, 4,9mm; diámetro del canal, 2,0mm) se llevó a cabo por vía transnasal y bajo anestesia local. Se examinó broncoscópicamente todo el árbol bronquial hasta el nivel de los bronquios subsegmentarios. A continuación se introdujo una sonda de R-EBUS con cubierta de vaina guía (VG) (UM-S20-17S; Olympus, Tokio) a través del canal de trabajo del FB y se hizo avanzar hasta el bronquio subsegmentario pretendido. Se examinaron las imágenes de EBUS y de fluoroscopia para confirmar que la sonda y la VG habían llegado a las lesiones a evaluar. A continuación se desplazó la sonda de R-EBUS dentro de la lesión para examinar el área más sospechosa, con objeto de obtener muestras de tejido bajo visión fluoroscópica7. Tras la localización adecuada, se mantuvo en su lugar la VG mientras se retiraba la sonda bajo fluoroscopia. Se introdujeron unas pinzas de biopsia y un cepillo bronquial a través de la VG para obtener muestras en la localización marcada bajo guía fluoroscópica. En general, el número de intentos de obtención de muestras de cepillado y de biopsia fue de 5 de cada8. Finalmente, se retiró la VG y se realizó un lavado broncoalveolar mediante la instilación de 50ml de solución salina normal y la posterior aspiración del mismo. Se repitió la instilación de 50ml de solución salina normal hasta alcanzar un total de 100-150ml para poder recoger al menos 50ml de líquido recuperado, lo cual se consideró un lavado adecuado.
Las muestras obtenidas mediante biopsia pulmonar transbronquial (BPTB) se reunieron en un tubo de micropipeta que se llenó con 0,5ml de solución salina normal. Después de finalizada la intervención de BPTB, se llenó el tubo con 1ml de formol al 10% y se centrifugó a 6.000 revoluciones por minuto durante 5min. A continuación se procesó el sedimento como bloque de células para la evaluación anatomopatológica. Con la muestra de cepillado bronquial se preparó un frotis en un portaobjetos y se fijó de inmediato en un frasco con alcohol al 95%, y se tiñó utilizando el método de Papanicolaou. El cepillado bronquial se irrigó con 3ml de solución salina normal estéril para la obtención de nuevas muestras. Además, se utilizó 1ml de solución salina normal estéril para irrigar la muestra que quedaba dentro de la VG arrastrándola hacia el líquido de irrigación del cepillado. Este líquido se envió al laboratorio para la centrifugación y tinción con el método de Papanicolaou. El líquido de lavado broncoalveolar (LLBA) se procesó para el examen citológico, la tinción de Gram, la tinción para bacilos acidorresistentes modificada y la tinción de Giemsa, y para la realización de cultivos.
Análisis estadísticoLas variables continuas se expresaron en forma de media±desviación estándar (DE) y las variables discretas se presentaron en forma de porcentajes. Para ilustrar la asociación existente entre las variables independientes y el rendimiento diagnóstico, las variables continuas se analizaron con la prueba de t de Student bilateral, y las variables discretas se evaluaron con la prueba de χ2. Se comparó el rendimiento diagnóstico de cada una de las técnicas de obtención de muestras mediante la prueba Q de Cochran. Si se alcanzaba la significación estadística, se calculaba la prueba de McNemar para comparar las diversas técnicas. Todas las pruebas estadísticas fueron bilaterales, y se consideró estadísticamente significativo un valor de p<0,05. Todos los datos se analizaron con el programa SPSS v16.0 para Windows (SPSS Inc., Chicago, IL, EE.UU.).
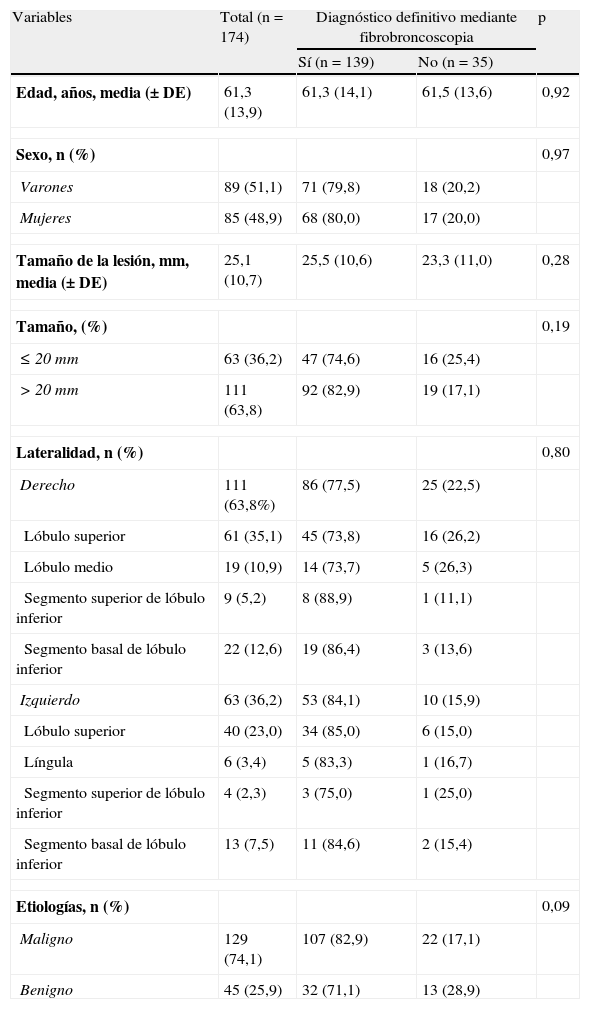
ResultadosSe examinaron retrospectivamente un total de 174 pacientes (89 varones y 85 mujeres). Los diagnósticos finales se presentan en la tabla 1. La media (±DE) de edad fue de 61,3±13,9años. La media (±DE) de diámetro de las LPP fue de 25,1±10,7mm. El rendimiento diagnóstico global de la broncoscopia bajo guía de EBUS fue del 79,9%. En la tabla 2 se resumen las características basales de los pacientes y los factores relacionados con el rendimiento diagnóstico de la FB bajo guía de R-EBUS. Ni el tamaño ni la etiología de las LPP mostraron influencia alguna en el rendimiento diagnóstico de la FB bajo guía de EBUS.
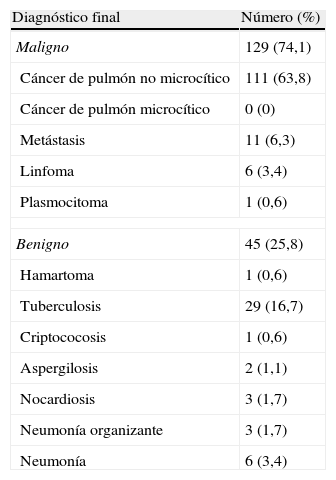
Diagnósticos finales de las lesiones pulmonares periféricas en 174 pacientes
| Diagnóstico final | Número (%) |
| Maligno | 129 (74,1) |
| Cáncer de pulmón no microcítico | 111 (63,8) |
| Cáncer de pulmón microcítico | 0 (0) |
| Metástasis | 11 (6,3) |
| Linfoma | 6 (3,4) |
| Plasmocitoma | 1 (0,6) |
| Benigno | 45 (25,8) |
| Hamartoma | 1 (0,6) |
| Tuberculosis | 29 (16,7) |
| Criptococosis | 1 (0,6) |
| Aspergilosis | 2 (1,1) |
| Nocardiosis | 3 (1,7) |
| Neumonía organizante | 3 (1,7) |
| Neumonía | 6 (3,4) |
Características basales y efectos sobre el rendimiento diagnóstico de la fibrobroncoscopia
| Variables | Total (n=174) | Diagnóstico definitivo mediante fibrobroncoscopia | p | |
| Sí (n=139) | No (n=35) | |||
| Edad, años, media (±DE) | 61,3 (13,9) | 61,3 (14,1) | 61,5 (13,6) | 0,92 |
| Sexo, n (%) | 0,97 | |||
| Varones | 89 (51,1) | 71 (79,8) | 18 (20,2) | |
| Mujeres | 85 (48,9) | 68 (80,0) | 17 (20,0) | |
| Tamaño de la lesión, mm, media (±DE) | 25,1 (10,7) | 25,5 (10,6) | 23,3 (11,0) | 0,28 |
| Tamaño, (%) | 0,19 | |||
| ≤ 20mm | 63 (36,2) | 47 (74,6) | 16 (25,4) | |
| > 20mm | 111 (63,8) | 92 (82,9) | 19 (17,1) | |
| Lateralidad, n (%) | 0,80 | |||
| Derecho | 111 (63,8%) | 86 (77,5) | 25 (22,5) | |
| Lóbulo superior | 61 (35,1) | 45 (73,8) | 16 (26,2) | |
| Lóbulo medio | 19 (10,9) | 14 (73,7) | 5 (26,3) | |
| Segmento superior de lóbulo inferior | 9 (5,2) | 8 (88,9) | 1 (11,1) | |
| Segmento basal de lóbulo inferior | 22 (12,6) | 19 (86,4) | 3 (13,6) | |
| Izquierdo | 63 (36,2) | 53 (84,1) | 10 (15,9) | |
| Lóbulo superior | 40 (23,0) | 34 (85,0) | 6 (15,0) | |
| Língula | 6 (3,4) | 5 (83,3) | 1 (16,7) | |
| Segmento superior de lóbulo inferior | 4 (2,3) | 3 (75,0) | 1 (25,0) | |
| Segmento basal de lóbulo inferior | 13 (7,5) | 11 (84,6) | 2 (15,4) | |
| Etiologías, n (%) | 0,09 | |||
| Maligno | 129 (74,1) | 107 (82,9) | 22 (17,1) | |
| Benigno | 45 (25,9) | 32 (71,1) | 13 (28,9) | |
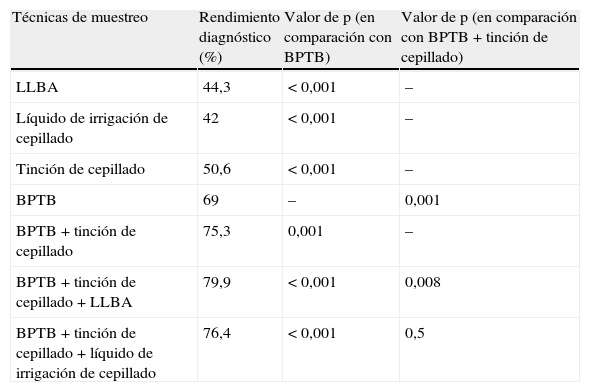
En la tabla 3 se muestra el rendimiento diagnóstico de diferentes técnicas de obtención de muestras mediante broncoscopia. De entre ellas, la BPTB fue la que obtuvo un rendimiento diagnóstico más alto (p<0,001, prueba Q de Cochran). La combinación de la BPTB con un frotis de cepillado proporcionó un rendimiento diagnóstico superior al de la BPTB sola (p=0,001). Además, al combinar el LLBA con la combinación de BPTB y frotis de cepillado se alcanzó el máximo rendimiento diagnóstico (p=0,008), mientras que el líquido de irrigación del cepillado no aportó un beneficio adicional a los resultados clínicos obtenidos con esa combinación (p=0,5).
Rendimiento diagnóstico de diferentes técnicas de obtención de muestras mediante broncoscopia
| Técnicas de muestreo | Rendimiento diagnóstico (%) | Valor de p (en comparación con BPTB) | Valor de p (en comparación con BPTB+tinción de cepillado) |
| LLBA | 44,3 | < 0,001 | – |
| Líquido de irrigación de cepillado | 42 | < 0,001 | – |
| Tinción de cepillado | 50,6 | < 0,001 | – |
| BPTB | 69 | – | 0,001 |
| BPTB+tinción de cepillado | 75,3 | 0,001 | – |
| BPTB+tinción de cepillado+LLBA | 79,9 | < 0,001 | 0,008 |
| BPTB+tinción de cepillado+líquido de irrigación de cepillado | 76,4 | < 0,001 | 0,5 |
BPTB: biopsia pulmonar transbronquial; LLBA: líquido de lavado broncoalveolar.
En nuestro estudio, ninguno de los pacientes presentó una hemorragia importante que requiriera intervención. Además, no se observaron efectos adversos importantes, como neumotórax o dificultad respiratoria, durante este periodo de estudio.
DiscusiónEl rendimiento diagnóstico de la R-EBUS en las LPP fue muy diverso, con valores que iban del 46 al 84%9. En el periodo inicial de uso de la R-EBUS se esperaba que su combinación con la guía fluoroscópica fuera innecesaria dada la preocupación existente por la exposición a la radiación. Sin embargo, el rendimiento diagnóstico de este enfoque fue inferior al de la R-EBUS con fluoroscopia6. Esto se explicaba por el movimiento de las LPP durante la respiración, el deslizamiento de la VG respecto a la diana a examinar, y el acortamiento o alargamiento de la VG tras la realización de exámenes y obtenciones de muestras repetidas10,11. En la actualidad, la combinación de R-EBUS con una guía fluoroscópica es ampliamente aceptada como procedimiento estándar.
Kurimoto et al.5 introdujeron una VG específica dedicada a la R-EBUS en 2004. Lleva un marcaje en la punta de la VG que la hace visible fluoroscópicamente y facilita la confirmación de si la VG continúa estando en la posición adecuada tras la retirada de la R-EBUS. Las ventajas de la VG incluyen la posibilidad de repetir el acceso a la lesión para la obtención de muestras, la evitación del colapso de las ramas bronquiales pequeñas tras la obtención de las muestras, y la posibilidad de aplicar una cuña a la lesión como protección frente al sangrado del lugar de biopsia hacia el bronquio proximal.
Las características de las LPP afectan también al rendimiento diagnóstico de la FB bajo guía de R-EBUS. En muchos estudios se ha puesto de manifiesto que el tamaño de la lesión es un factor significativo que influye en el rendimiento diagnóstico de la R-EBUS5,6,12-14. En nuestro estudio, aunque el rendimiento diagnóstico en las LPP de tamaño >20mm fue superior al obtenido para las que tenían un tamaño <20mm, esto no alcanzó significación estadística. Una posible causa de esta observación podría ser la presencia de un signo de bronquio en la TC que puede indicar la posición de la sonda en relación con la lesión. El tamaño de la lesión fue un factor significativo en la predicción de la visibilidad de las LPP en la R-EBUS14. Huang et al.14 observaron que la visibilidad en las LPP de tamaño <20mm es de tan solo el 48,6%. En los casos que no eran visibles en la R-EBUS, los resultados no fueron diagnósticos. En nuestro estudio retrospectivo los datos procedían de la práctica clínica habitual, y ello podía comportar un sesgo de selección inevitable a la hora de elegir el abordaje diagnóstico a utilizar para las LPP. En el caso de que no hubiera ningún bronquio del que dependiera la LPP que pudiera identificarse en la TC, se optaba por otros enfoques diagnósticos como la aspiración mediante punción transtorácica. Solamente los pacientes en los que se identificaron bronquios de los que dependían las lesiones, con independencia de su tamaño, fueron seleccionados para el uso de la FB bajo guía de R-EBUS, y ello permitió obtener una visibilidad de imagen de R-EBUS en la mayoría de los casos. En consecuencia, el tamaño no influyó de manera estadísticamente significativa en nuestra serie. Esto fue observado también por Yamada et al.8, que indicaron que tan solo la posición de la sonda en relación con la lesión, y no así su tamaño, predecían el rendimiento diagnóstico en su análisis multivariante. Nuestro rendimiento diagnóstico fue del 79,9%, lo cual es comparable a lo observado en los pacientes con imágenes de R-EBUS positivas en otros estudios8,10,13,14.
La etiología fue también un factor significativo que influyó en el rendimiento diagnóstico5,12,14. Aunque en el presente estudio el rendimiento diagnóstico en las lesiones malignas resultó superior al obtenido en las enfermedades benignas, no hubo diferencias estadísticamente significativas entre ellas. La baja prevalencia de las enfermedades benignas y el bajo número de pacientes fueron probablemente las causas de esta diferencia en los resultados.
La técnica de muestreo es otro motivo de preocupación por lo que respecta al rendimiento diagnóstico de la FB. Se demostró que la BPTB era la técnica más eficaz para obtener el diagnóstico5,8, y que el número apropiado de muestras de biopsia8 debía ser como mínimo de 5.
Las muestras obtenidas mediante el empleo de pinzas de biopsia a través de la VG son de menor tamaño que las obtenidas con pinzas de biopsia estándares. Así pues, reunimos todas las muestras de biopsia de cada paciente en el tubo de micropipeta y procesamos el tejido para el examen histológico mediante preparación de bloques de células. Las ventajas de la técnica de bloques de células frente a la preparación anatomopatológica convencional no se han investigado y deberán ser objeto de estudio en el futuro.
La combinación de otras técnicas de obtención de muestras diagnósticas y de muestras de BPTB puede aumentar el rendimiento diagnóstico. Nosotros observamos que la adición de los resultados diagnósticos del LLBA a la combinación de BPTB y frotis de cepillado puede elevar el rendimiento diagnóstico total, y que ello hizo que esta combinación alcanzara el máximo resultado diagnóstico. En cambio, el líquido de irrigación del cepillado obtenido a partir del cepillado bronquial y la VG, con el que se preparó un frotis para un examen citológico adicional, no aumentó el rendimiento diagnóstico. En consecuencia, podría descartarse su uso, ya que su realización comporta unos costes desproporcionados.
En conclusión, hemos demostrado que la FB bajo guía de R-EBUS es una técnica útil para el diagnóstico de las LPP. Por lo que respecta a las técnicas de obtención de muestras, para alcanzar el máximo rendimiento diagnóstico deben utilizarse conjuntamente la BPTB, el frotis de cepillado y el lavado broncoalveolar.
Consideraciones éticasEste protocolo de estudio retrospectivo fue aprobado por el Comité de Ética de Experimentación Humana del Hospital Ramathibodi, Facultad de Medicina, Universidad de Mahidol.
FinanciaciónNinguna.
AutoríaViboon Boonsarngsuk diseñó y llevó a cabo el estudio, realizó la broncoscopia bajo guía de R-EBUS, analizó los datos, preparó y revisó el manuscrito.
Wasana Kanoksil procesó y revisó la citología y la histología.
Sarangrat Laungdamerongchai realizó el estudio, colaboró en la broncoscopia bajo guía de R-EBUS.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Los autores dan las gracias al Dr. Pensupa Raweelert por sus sugerencias constructivas y su corrección del inglés.