La hemoptisis es una manifestación sintomática de una enfermedad torácica que puede ser grave y poner en peligro la vida, y requiere una evaluación y tratamiento urgentes. El objetivo del presente estudio fue evaluar la eficacia hemostásica de la aplicación endobronquial de la solución Ankaferd Blood Stopper® (ABS) en pacientes con hemoptisis.
Este estudio retrospectivo se realizó en 20 pacientes con hemoptisis en los que se aplicó ABS endobronquial mediante 25broncoscopias.
La aplicación endobronquial de ABS tuvo éxito en 23 de las 25broncoscopias. Se repitió la aplicación de ABS a causa de una recidiva hemorrágica en 4pacientes.
Esta es la primera serie de casos que describe el uso de la aplicación endobronquial de ABS, un nuevo agente hemostásico que constituye un método eficaz para el tratamiento de la hemorragia, sobre todo en lesiones malignas endobronquiales locales. Pensamos que la aplicación broncoscópica de ABS puede ser un método terapéutico alternativo y de apoyo en casos de hemoptisis no controlada.
Hemoptysis is symptomatic of potentially serious and life-threatening chest disease and requires urgent evaluation and treatment. The aim of this study was to evaluate the hemostatic efficacy of endobronchial application of Ankaferd Blood Stopper® (ABS) solution in patients with hemoptysis.
This retrospective study included 20patients with hemoptysis in whom endobronchial ABS was applied in 25bronchoscopic procedures.
Endobronchial application of ABS was successful in 23 of the 25 bronchoscopic procedures. ABS application was repeated due to recurrent bleeding in 4patients.
This is the first case series demonstrating the endobronchial application of ABS, a novel hemostatic agent, effective in the management of bleeding, especially in local endobronchial malignant lesions. Bronchoscopic ABS application may be an alternative supportive therapeutic method in cases of uncontrolled hemoptysis.
El hemostásico Ankaferd (Ankaferd Blood Stopper® [ABS]) es un peculiar extracto de plantas medicinales populares que se utilizó anteriormente en la medicina tradicional turca como agente hemostásico. Está formado por una mezcla estándar de plantas, todas ellas con actividad antitrombínica, antiplaquetaria, antioxidante, antiaterosclerótica y antitumoral. El mecanismo de acción básico de ABS es la formación de una red proteica encapsulada que proporciona un foco para la agregación eritrocitaria vital1. Las acciones paradójicas antitrombóticas de un producto antihemorrágico se han explicado por sus acciones sobre el fibrinógeno gamma observadas en análisis de proteómica funcional2. ABC ha sido registrado recientemente para el tratamiento de las hemorragias clínicas cuando los métodos convencionales de control de la hemorragia son ineficaces. El objetivo del presente estudio fue evaluar de manera retrospectiva la eficacia de la aplicación endobronquial del producto hemostásico ABS en el tratamiento de la hemoptisis.
Pacientes y métodosSe utilizó ABS en 20pacientes (18varones y 2mujeres) en los que se realizaron 25broncoscopias localmente mediante un broncoscopio de fibra óptica flexible (Olympus® BF XT20, BF-1T160 y Pentax® 18P). Se obtuvo el consentimiento informado de todos los pacientes antes de la broncoscopia. La indicación principal para el uso de ABS fue el control de la hemorragia originada en el árbol bronquial que persistía a pesar del lavado con solución salina helada del segmento afectado y/o la instilación de adrenalina en el lugar de la hemorragia. En 7casos el sangrado se inició después de una intervención de biopsia endobronquial o transbronquial, y en los otros 13 fue un sangrado endobronquial difuso o local. Si la lesión sangrante era visible, el ABS se aplicaba directamente en el lugar del sangrado mediante la sonda broncoscópica. La aplicación de ABS se realizó a través de un catéter de lavado broncoalveolar desde la carina principal si había un sangrado difuso de un segmento del pulmón. Se repitió la dosis de 2ml si la respuesta era insuficiente. Según la cantidad de sangrado diario (gravedad de la hemoptisis), se clasificó a los pacientes en los 4grupos siguientes3: «leve»: tan solo estrías hemáticas en el esputo; «moderada»: 30-100cm3; «grave»: 100-600cm3; «masiva»: >600cm3. El éxito en el control de la hemorragia tras la aplicación de ABS se definió como el cese del sangrado durante la intervención broncoscópica y la ausencia de recidivas hemorrágicas durante un periodo de 24h.
ResultadosLa media de edad de los pacientes fue de 58años (rango, 25-81años). La hemoptisis fue el síntoma de presentación en 13pacientes y el sangrado se inició tras una biopsia broncoscópica en 7pacientes. ABS permitió controlar el sangrado en unos segundos tras la instilación en el foco hemorrágico en 23 de las intervenciones; sin embargo, resultó ineficaz en 2casos. Se repitió la aplicación de ABS a causa de una recidiva hemorrágica en 4pacientes en los que la hemoptisis reapareció al menos 24h después de la primera intervención. Las características clínicas de los pacientes se presentan en la tabla 1.
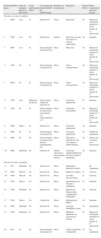
Características clínicas de los pacientes en los que se ha aplicado ABS endobronquial para el tratamiento de la hemoptisis
| Paciente número | Edad/Sexo | Grado de hemoptisis antes de la intervención | Lesión endobronquial (Sí/No) | Vía de aplicación (directaa/catéterb) del ABS/Posología: | Resultados de la intervención | Diagnóstico | Recidiva (Sí/No) | Última evaluación del estado del paciente |
| Pacientes con cáncer de pulmón | ||||||||
| 1 | 69/M | Leve | Sí | Directa/2ml | Eficaz | Microcítico | No | Muerte por enfermedad progresiva 4 meses después de la intervención |
| 2 | 79/M | Leve | No | Directa/2ml | Ineficaz | Microcítico (erosión de la mucosa a causa de radioterapia) | No | Remisión |
| 3 | 68/M | Leve | Sí | Directa (después de biopsia)/2ml | Eficaz | Microcítico | No | Muerte por enfermedad progresiva 3 meses después de la intervención |
| 4 | 74/M | No | Sí | Directa (después de biopsia)/2ml | Eficaz | Tumor neuroendocrino | No | Muerte por enfermedad progresiva 3 meses después de la intervención |
| 5 | 68/M | No | Sí | Directa (después de biopsia)/2ml | Eficaz | Tumor neuroendocrino | No | Muerte por enfermedad progresiva 3 meses después de la intervención |
| 6 | 73/M | Leve | Infiltración de mucosa | Directa (antes y después de biopsia)/2ml | Eficaz | Carcinoma epidermoide | Sí | Remisión |
| 7c | 75/M | No | Sí | Directa (después de reducción de masa tumoral con electrocauterio)/2ml | Eficaz | Carcinoma sarcomatoide | No | Muerte por enfermedad progresiva 5 meses después de la intervención |
| 8 | 64/M | Masiva | Sí | Directa/2ml | Eficaz | Carcinoma epidermoide | No | Remisión |
| 9 | 58/M | No | Sí | Directa(después de biopsia)/2ml | Eficaz | Carcinoma epidermoide | No | Pérdida del seguimiento |
| 10 | 59/M | No | No | Directa (después de aspiración por punción transtraqueal)/2mL | Eficaz | Microcítico+síndrome de vena cava superior+trombocitopenia | No | Muerte a las 2 semanas de la intervención |
| 11d | 60/M | Moderada | Síe | Directa/2ml | Primera intervención eficaz/segunda ineficaz | Carcinoma epidermoide/Erosión de mucosa debida a radioterapia | No | Remisión |
| Pacientes sin cáncer de pulmón | ||||||||
| 12 | 75/F | Moderada | No | Directa/2ml | Eficaz | Enfermedad pulmonar cavitaria | En seguimiento | |
| 13f | 25/M | Masivag | No | Directa/2ml | Eficaz | Pulmón de soldador | Sí | Curación |
| 14h | 55/M | Masivag | No | Directa/2ml | Eficaz | Vasculitis leucocitoclástica | Sí | Curación |
| 15 | 53/M | Masiva | No | Directa/2ml | Eficaz | Granulomatosis de Wegener+aspergiloma | Sí | Remisión |
| 16 | 53/M | Moderada | No | Directa/2ml | Eficaz | Inducida por fármaco (ácido acetilsalicílico y clopidogrel) | No | Curación |
| 17 | 35/M | Masiva | No | Catéter/4ml | Eficaz | Enfermedad de Behçet | No | Remisión |
| 18 | 40/M | Moderada | No | Directa/4ml | Eficaz | Leucemia mieloblástica aguda | No | Seguimiento |
| 19 | 81/M | Moderada | Sí | Directa/2ml | Eficaz | Metástasis pulmonares de carcinoma de próstata | Sí | Muerte por enfermedad metastásica 6 meses después de la intervención |
| 20 | 45/F | No | No | Directa (después de biopsia)/2ml | Eficaz | Artritis reumatoide+Bronquiolitis | No | En seguimiento |
ABS: Ankaferd Blood Stopper®; F: mujer; M: varón.
Hubo lesiones endobronquiales hemorrágicas debidas a cáncer de pulmón en 8pacientes, y una infiltración tumoral de la mucosa en un paciente. El sangrado se inició después de una biopsia transbronquial en un paciente, y después de una aspiración por punción transtraqueal en otro.
En 9 de los pacientes hubo causas no malignas de la hemoptisis (tabla 1). Se produjo un sangrado masivo en 6 de los pacientes (5 en el grupo de causa no maligna y uno en el grupo de causa maligna). La vasculitis fue la etiología más frecuente de los sangrados masivos.
DiscusiónEl presente estudio puede mostrar una opción terapéutica alternativa en situaciones de urgencia mediante la aplicación endobronquial de ABS. Observamos que la aplicación endobronquial de ABS a una dosis de 2-4ml resultó eficaz en la mayor parte de las situaciones. ABS tiene una acción muy rápida que permite controlar la hemorragia en unos pocos segundos tras la aplicación. El fármaco resultó especialmente eficaz en las lesiones hemorrágicas locales. Tan solo se ha descrito un caso de aplicación endobronquial de ABS para el control de una hemorragia profusa debida a una lesión endobronquial neoplásica4. Sin embargo, la administración tópica de ABS se ha ensayado con éxito en muchas situaciones hemorrágicas diferentes, como hemorragia digestiva, epistaxis, hemorragias de pacientes hemofílicos, sangrado dental y sangrado tras una amigdalectomía5. El cáncer de pulmón fue la causa de la mayor parte de casos de nuestra serie (11pacientes), y el sangrado se inició después de la biopsia en 7 de estos casos. La aplicación endobronquial de ABS detuvo la hemorragia en todos los casos, con lo que evitó retrasos diagnósticos y curativos innecesarios en el tratamiento. En el presente estudio hubo 5casos de hemoptisis masiva en el grupo de pacientes sin cáncer. En todos estos pacientes, ABS resultó eficaz en el tratamiento del sangrado pulmonar. Además, el tratamiento inmunosupresor en los casos de vasculitis y el tratamiento de apoyo en los casos de hemoptisis debida a humos de soldadura mejoraron los resultados clínicos y radiológicos.
En conclusión, esta es la primera serie de casos que describe el uso de la aplicación endobronquial de ABS, un nuevo agente hemostásico que constituye un método eficaz para el tratamiento de la hemorragia, sobre todo en lesiones malignas endobronquiales locales. En consecuencia, la aplicación broncoscópica de ABS puede ser un método terapéutico alternativo y de apoyo en los casos de hemoptisis no controlada. Serán necesarios otros estudios clínicos controlados y prospectivos para identificar plenamente la seguridad, la posología y la eficacia del uso tópico de ABS en pacientes con hemoptisis.