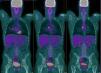
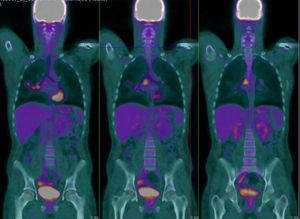
Presentamos el caso de un varón de 20 años de edad, con antecedentes de sarcoma de Ewing humeral izquierdo, diagnosticado a los 15 años, y en seguimiento por oncología médica desde entonces. Tras el diagnóstico recibió quimioterapia neoadyuvante según esquema VAC/ifosfamida-VP-16×5 ciclos, con posterior realización de cirugía radical con resultado anatomopatológico de respuesta patológica completa. El paciente completa de forma adyuvante 12 ciclos con el mismo esquema y pasa a revisiones periódicas. Tras 2 años de periodo libre de enfermedad se diagnostica de probable recidiva pleuro-pulmonar por PET-TAC, describiéndose focos hipermetabólicos en cisura mayor de pulmón derecho y a nivel adenopático subcarinal e hiliar derecho, si bien estas últimas se describían como de probable naturaleza inflamatoria inespecífica, y recomendándose control estrecho por prueba de imagen. Sin alergias medicamentosas conocidas. Sin hábitos tóxicos ni exposiciones ocupacionales. Estudiante; sin antecedentes familiares de interés. Acude a consulta externa de servicio de neumología derivado desde al servicio de oncología médica por presencia de adenopatías mediastínicas sospechosas de recidiva tumoral en PET-TAC. Clínicamente presenta cierta astenia, sin otra sintomatología acompañante. Examen físico dentro de la normalidad. Las pruebas de laboratorio revelaron una bioquímica, hemograma y coagulación estrictamente normales. Se realizó tomografía axial computarizada de tórax, abdomen y pelvis, por parte de oncología médica, evidenciándose conglomerado adenopático en el espacio subcarinal, y adenopatías hiliares bilaterales, sin otros hallazgos a nivel de tórax, abdomen ni pelvis. A la vista de los anteriores hallazgos, se solicitó PET-TAC que destacó la presencia de focos hipermetabólicos sobre pulmón derecho y adenopatías subcarinales e hilio pulmonar derecho, con aumento de intensidad metabólica respecto a PET-TAC previo de revisión (fig. 1). Se realizó ecobroncoscopia bajo sedación profunda controlada por anestesista, objetivándose a nivel subcarinal adenopatía de 12mm, con forma redondeada, bordes bien delimitados, ecoestructura homogénea y ausencia de estructura hiliar central ni signos de necrosis, que se puncionó con citopatólogo in situ en sala de exploración en 3 ocasiones, con obtención de material adecuado para realización de estudios posteriores, llegándose al diagnóstico anatomopatológico de metástasis de sarcoma de Ewing. Tras el diagnóstico, el paciente recibió 4 ciclos de quimioterapia según esquema ciclofosfamida-topotecán, con buena tolerancia y respuesta metabólica completa, y posteriormente se realizó trasplante autógeno de sangre periférica (TASPE), con persistencia de respuesta metabólica completa en revisiones posteriores.
El sarcoma de Ewing es el segundo tumor óseo maligno más frecuente en la edad pediátrica. Aproximadamente el 90% de los casos se da en la segunda década de la vida, con un pico de edad de 13 años, y es extremadamente raro en menores de 5 años, tiene una mayor prevalencia masculina con una relación 1,5-2:1. La forma de presentación clínica habitual es dolor y tumefacción de la región afectada, que pueden acompañarse de masa palpable1. Ocasionalmente (más común cuando existe enfermedad metastásica) asocian manifestaciones sistémicas como fiebre, astenia, pérdida de peso, leucocitosis, anemia y aumento de la velocidad de sedimentación, que pueden conducir a un diagnóstico erróneo de osteomielitis aguda2. Las localizaciones más frecuentes son: las diáfisis de los huesos largos y la pelvis (70-75% de los casos), también presenta especial predilección por la escápula, y menor por las costillas y vértebras; aunque puede afectar a cualquier hueso. Un 15-20% de los pacientes presentan metástasis pulmonares al diagnóstico, en su progresión también puede presentar metástasis óseas y adenopáticas3. La quimioterapia estándar actual para el sarcoma de Ewing incluye entre 4 y 6 ciclos de vincristina, doxorrubicina (adriamicina) y ciclofosfamida, alternando con ifosfamida y etopósido (VDC/IE)4.
El pronóstico del sarcoma de Ewing está determinado por diferentes parámetros, que constituyen el índice pronóstico: edad >18 años, localización extraósea, tamaño mayor o igual a 8cm, metástasis a distancia (20%), histología postherapyI, IIA o IIB, traslocación EWS-FLI1 tipo 2 y niveles elevados de LDH, confieren mal pronóstico. En nuestro caso, el paciente presentaba datos de mal pronóstico (como la presencia de metástasis a distancia de localización mediastínica, confirmada citológicamente mediante EBUS y pleuropulmonar evidenciada por PET-TAC, sin embargo, la estrategia terapéutica multidisciplinar óptima ha hecho que el paciente se haya beneficiado de un correcto tratamiento5. El diagnóstico de los casos de sarcoma de Ewing con afectación pulmonar descritos en la literatura se realiza, en la inmensa mayoría de los casos, por biopsia transtorácica de lesiones pulmonares accesibles, siendo fundamental el adecuado abordaje de lesiones mediastínicas mediante ecobroncoscopia, de ahí el interés del presente caso, al ser una técnica mínimamente invasiva, de alta rentabilidad diagnóstica y permitiéndonos establecer un diagnóstico diferencial con otras entidades.