La neumonía organizada es una entidad clinicohistológica que suele manifestarse de forma subaguda con clínica respiratoria e infiltrados pulmonares. Puede ser de causa desconocida (criptogenética) o estar asociada a distintas enfermedades, infecciones o fármacos. Presentamos el caso de una paciente de 60 años con antecedentes de una neoplasia de mama, motivo por el cual seguía tratamiento con trastuzumab, un anticuerpo monoclonal anti-HER2, a quien se detectó de forma casual un infiltrado pulmonar, cuya biopsia transbronquial fue diagnóstica de neumonía organizada. Tras la retirada del fármaco desapareció el infiltrado pulmonar. Debido a la creciente utilización de la terapia biológica en diferentes campos de la clínica, nos parece de interés comunicar esta forma de afectación pulmonar atribuible al anticuerpo monoclonal trastuzumab.
Organizing pneumonia is a clinical and histological condition in which the onset is usually subacute with respiratory symptoms and pulmonary infiltrates. It may be unknown origin (cryptogenic) or associated with other illnesses, infectious diseases or drugs. We present a 60 year-old female patient with a previous history of breast cancer, who was being treated with trastuzumab, an antiHER2 monoclonal antibody. She was diagnosed with casual pulmonary infiltrates that had histological changes compatible with organizing pneumonia. The pulmonary infiltrates disappeared on withdrawing trastuzumab treatment. Due to the increasing use of biological therapies in different medical areas, we believe it is of interest to report this pulmonary involvement attributed to the monoclonal antibody trastuzumab.
La neumonía organizada es una entidad clinicohistológica que puede presentarse en relación con la administración de algunos fármacos. El trastuzumab (Herceptin®) es un anticuerpo monoclonal dirigido contra el dominio extracelular de la proteína HER2, que es responsable de la actividad tirosincinasa y está sobreexpresada en hasta un 25% de los carcinomas infiltrantes de mama. En el caso que presentamos a continuación pudimos demostrar la asociación entre el tratamiento con trastuzumab y la aparición de neumonía organizada, en una paciente con el antecedente de neoplasia de mama.
Observación clínicaMujer de 60 años, sin alergias medicamentosas conocidas ni hábitos tóxicos, con antecedentes de hipertensión arterial, dislipemia y asma bronquial. Tras el diagnóstico en octubre del 2006 de una neoplasia de mama derecha, se le realizó tumorectomía y linfadenectomía axilar. El resultado de la anatomía patológica fue de carcinoma ductal infiltrante de 15×11×10mm, grado 2, con un único ganglio axilar afectado de los 15 aislados. El estudio inmunohistoquímico mostró receptores de estrógeno y progesterona positivos, y amplificación y polisomía de HER2 por hibridación in situ fluorescente. Tras el estudio de extensión se clasificó como un pT1c pN0 M0, y se consideró a la paciente tributaria de realizar tratamiento adyuvante. Entre los meses de noviembre y marzo de 2007 recibió 6 ciclos de tratamiento citostático intravenoso según el esquema docetaxel+adriamicina+ciclofosfamida cada 21 días. Posteriormente, entre abril y junio de 2007 recibió irradiación sobre la mama derecha con fotones de 6Mv, a un fraccionamiento de 2Gy por sesión, hasta llegar a una dosis total de 48Gy, más sobreimpresión en lecho quirúrgico hasta un total de 68Gy; la única complicación que presentó fue una dermatitis grado 2, resuelta con tratamiento tópico. En agosto de 2007 inició tratamiento con trastuzumab a una dosis inicial de 8mg/kg, y posteriormente de 6mg/kg cada 21 días. En enero de 2008, al presentar una clínica sugestiva de infección bronquial, se le realizó una radiografía de tórax en la que se observó un nódulo de 17mm en el lóbulo superior del pulmón derecho, que con posterioridad se confirmó mediante tomografía computarizada (TAC) de tórax. Aproximadamente un mes después se repitió la radiología simple de tórax, y más tarde la TAC torácica (fig. 1), que mostró una condensación periférica, con pequeñas áreas de cavitación, rodeada de opacidades en vidrio deslustrado y tractos pleuropulmonares de aspecto fibrótico, todo ello indicativo de una neumonía organizada. La paciente se encontraba asintomática en ese momento. La fibrobroncoscopia mostró normalidad endobronquial, los cultivos microbiológicos para bacterias y micobacterias fueron negativos y las citologías no mostraron células malignas; en el lavado broncoalveolar se informó de un 59% de linfocitos–con un predominio de CD4 (71%)–y de un 10% de neutrófilos, y en la biopsia transbronquial se observó proliferación fibroblástica intraalveolar, que era indicativa de un patrón histológico de neumonía organizada (fig. 2). Ante la sospecha de neumonía organizada secundaria a trastuzumab, se decidió suspender dicho tratamiento después de que la paciente hubiera recibido 11 ciclos durante 7 meses. Tras la retirada del fármaco, el infiltrado pulmonar experimentó una reducción progresiva hasta su completa resolución en mayo de 2008. Después de 14 meses de seguimiento la paciente se encuentra asintomática y sin evidencia de enfermedad neoplásica ni afectación parenquimatosa pulmonar. La lesión nodular, cuyo estudio condujo a estos hallazgos, no presentaba captación en la tomografía por emisión de positrones, y se pudo constatar que ya existía en radiografías previas al diagnóstico de la neoplasia de mama.
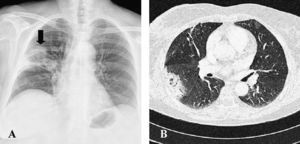
A: radiología simple de tórax (proyección posteroanterior) que muestra un nódulo pulmonar solitario y un área de consolidación en el lóbulo superior derecho (flecha). B: sección axial de tomografía computarizada de tórax en ventana de pulmón, que muestra condensación periférica, con pequeñas áreas de cavitación, rodeada de opacidades en vidrio deslustrado.
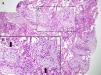
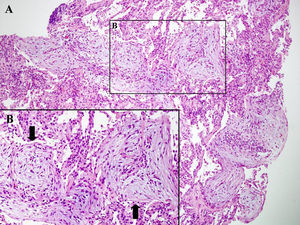
Biopsia transbronquial obtenida mediante fibrobroncoscopia, donde se puede observar parénquima pulmonar peribronquial con proliferación fibroblástica intraalveolar (flechas), indicativo de un patrón histológico de neumonía organizada. A: hematoxilina-eosina (×10 aumentos). B: hematoxilina-eosina (×20 aumentos).
La neumonía organizada (anteriormente conocida como bronquiolitis obliterante con neumonía organizada) se caracteriza por la presencia de manifestaciones clínicas subagudas (tos, disnea y fiebre), junto a infiltrados pulmonares alveolares y/o intersticiales (a veces migratorios e incluso recidivantes). Para establecer el diagnóstico de seguridad se requiere la demostración de focos de neumonía organizada en las muestras de biopsia transbronquial o quirúrgica, acompañado de un cuadro clinicorradiológico compatible. La neumonía organizada puede ser idiopática o estar asociada a colagenosis, infecciones, administración de fármacos (bleomicina, derivados ergóticos, nitrofurantoína, fenitoína, amiodarona, carbamacepina, ciclofosfamida, etc.) o radioterapia1–4. La radiografía de tórax muestra imágenes de consolidación unilaterales o bilaterales, en ocasiones migratorias y recidivantes, aunque en algunos casos las imágenes son nodulares o reticulonodulillares. El hallazgo en la TAC torácica de áreas de consolidación pulmonar de distribución subpleural o peribronquiolar y un lavado broncoalveolar con linfocitosis, a menudo asociada a neutrofilia y/o eosinofilia, junto con una inversión del cociente de linfocitos T CD4+/CD8+, orientan al diagnóstico1.
En la actualidad, el arsenal terapéutico utilizado en el cáncer de mama incluye la cirugía, la quimioterapia, la radioterapia, el tratamiento hormonal y la terapia biológica. El tratamiento dirigido utilizando anticuerpos monoclonales contra el receptor de membrana HER2 ha demostrado importantes beneficios en pacientes con una elevada expresión de este receptor.
HER2 pertenece a una familia de 4 receptores transmembrana con actividad tirosincinasa que regulan la proliferación, diferenciación y supervivencia celulares5,6. La sobreexpresión de la proteína HER2 o la amplificación del gen HER2/neu ocurre en un 20–25% de los carcinomas infiltrantes de mama7,8 y se asocia a un comportamiento tumoral más agresivo, con una mayor tasa de recurrencia y un menor intervalo libre de recaída tras la quimioterapia adyuvante7. El trastuzumab (Herceptin®) es un anticuerpo monoclonal humanizado dirigido contra el dominio extracelular de la proteína HER2. La unión al receptor HER2 evita la dimerización del receptor y bloquea la activación de las vías de señalización, con lo que se inhiben la proliferación y la supervivencia celulares. El uso de trastuzumab se ha extendido a la población HER2 positiva tanto en enfermedad metastásica como en adyuvancia y neoadyuvancia, y mejora tanto la supervivencia global como la supervivencia libre de recaída. El trastuzumab es en general un fármaco bien tolerado, pero no exento de efectos secundarios. La toxicidad más importante descrita es la cardíaca, principalmente en forma de insuficiencia cardíaca congestiva, que revierte al retirar el fármaco; ocurre en alrededor de un 4,5% de los casos y obliga a un seguimiento de la función cardíaca antes y durante el tratamiento. También se ha descrito toxicidad pulmonar, aunque es excepcional8. En 2003 se describió el primer caso de neumonía organizada asociada a tratamiento con trastuzumab9, y hasta la fecha no nos consta la publicación de ningún otro.
En nuestro caso, la afectación pulmonar que presentó la paciente, de acuerdo con los criterios clásicos para considerar reacción adversa a un fármaco, se hallaría en un nivel de certeza probable, pues para definir la reacción como segura se precisaría la reaparición de la neumonía organizada tras la reexposición al medicamento10, hecho que no se contempló por consideraciones éticas. El rituximab, otro anticuerpo monoclonal, también se ha asociado a neumonía organizada, como se describe en artículos de reciente aparición11,12. En cuanto al posible papel de la radioterapia en el desarrollo de neumonía organizada, esta complicación se halla documentada en la literatura médica13. En el caso que describimos, los meses transcurridos entre su finalización y la aparición de las lesiones permiten descartar razonablemente la radioterapia como causante de la afectación pulmonar.
Dada la creciente utilización del tratamiento biológico en diferentes ámbitos de la clínica, no sería de extrañar que en los próximos años se notificaran más casos en la literatura médica, por lo que nos parece relevante comunicar esta reacción adversa pulmonar en forma de neumonía organizada.