Algunas de las investigaciones a que se aluden en la sección de "Perspectivas futuras de la toracoscopia médica" están siendo financiadas por la Red Respira-ISCIII-RTIC-03/11
Introducción
La toracoscopia fue descrita por primera vez, en 1910, por Jacobaeus, profesor de medicina en Estocolmo, quien expuso sus hallazgos endoscópicos en 2 casos de pleuritis tuberculosa1. Aunque en los siguientes 40 años esta técnica se orientó casi exclusivamente al tratamiento de las lesiones tuberculosas pulmonares cavitadas (inducción de neumotórax tras la sección de las adherencias pleuropulmonares mediante la aplicación de electrocauterio, "colapsoterapia" u "operación de Jacobaeus"), el mismo Jacobaeus expuso 15 años más tarde sus posibilidades diagnósticas y terapéuticas en una amplia revisión de su experiencia titulada "Toracoscopia y su importancia práctica"2.
Una vez conseguido el control de la tuberculosis a través del tratamiento farmacológico, evitando así la necesidad de intervención directa o indirecta sobre las cavidades pulmonares en la mayoría de los casos, a finales de la década de los setenta surgió un renovado interés por las posibilidades de la toracoscopia, la cual se desarrolló principalmente a partir de centros con muy dilatada experiencia en los Países Bajos3, Alemania4 y Francia5. En España, Cantó es el maestro indiscutible de muchos de nosotros6, y el libro de Sebatián Quetglás et al7 sobre la toracoscopia compite en calidad con los mejores de los grupos europeos mencionados anteriormente.
A mediados de los años ochenta se empezaron a diseñar instrumentos que, además de la toma de biopsias, permitieran intervenir sobre las estructuras intratorácicas. Cuando a finales de esa década se desarrollaron las videocámaras adaptables a los endoscopios surgió el acrónimo VATS (video-assisted thoracic surgery)8,9, con el término cirugía videotoracoscópica (CVT) como equivalente en español, la cual se encuadra plenamente dentro de las tendencias modernas hacia una medicina mínimamente invasiva10.
Con el desarrollo de todas estas técnicas queda cada vez más claro que hay que distinguir entre una indicación "primitiva" de la toracoscopia, que se orienta a explorar y tratar fundamentalmente los derrames pleurales, y la CVT, más compleja e intervencionista. Mientras que la primera puede llevarse a cabo bajo anestesia local y con una sola entrada, la CVT requiere varios puntos de entrada y anestesia general. Para clarificar las diferencias frente a la denominada en principio "toracoscopia quirúrgica"11, se propuso hace años el término "toracoscopia médica" para la primera de estas 2 modalidades12, quizá con la intención de subrayar el hecho de que pueden realizarla no sólo por cirujanos torácicos, sino también neumólogos bien entrenados13.
Técnica de la "toracoscopia médica"
Antes de realizar la exploración es necesario explicar al paciente en qué consiste la técnica y qué sensaciones puede experimentar durante la ejecución de las distintas maniobras. De este modo la toracoscopia puede tolerarse muy bien con sólo anestesia local y la aplicación moderada de analgésicos por vía intravenosa. Es importante valorar el estado general antes de indicar la exploración, prestando atención a la presencia de hipoproteinemia o debilidad extrema del paciente, edemas generalizados o infiltración de la pared del hemitórax a explorar, y especialmente se debe ser muy cuidadoso con la presencia de tos intensa, ya que ésta puede dificultar mucho la exploración y favorecer la aparición de enfisema subcutáneo.
Siempre se debe hacer un estudio de coagulación con recuento de plaquetas (se requiere una cifra superior a 60.000/µl), además de los controles habituales de coagulación. En nuestra experiencia los pacientes más peligrosos son los inmunodeprimidos --en quienes el recuento de plaquetas puede no ser reflejo claro del deterioro de su función-- y también los que presentan cirrosis hepática. No obstante, los problemas hemorrágicos más graves durante una toracoscopia suelen deberse más a un accidente (rotura de un vaso por la pinza de biopsia) que a una coagulopatía.
El mayor problema técnico para la realización de una toracoscopia con anestesia local y en un medio no estrictamente quirúrgico es la presencia de adherencias extensas entre el pulmón y la pared torácica. En estos casos, la introducción del trocar puede ser muy difícil y peligrosa. Por ello, es recomendable usar una cánula de Veress para inducir neumotórax --similar a las usadas para inducir neumoperitoneo-- cuando se sospeche que el pulmón está adherido a la pared en la zona en que vamos a introducir el toracoscopio. La tomografía computarizada puede ser de gran ayuda en estos casos. Nosotros hemos encontrado una clara relación entre las concentraciones de lactatodeshidrogenasa en el líquido pleural y las adherencias, de modo que una cifra superior a 1.500 U/l hace presagiar la presencia de importantes adherencias, las cuales serán con gran probabilidad muy conflictivas si los valores de lactatodeshidrogenasa superan las 3.000 U/l.
Aunque no constituya en sí una contraindicación absoluta, el mal estado general del paciente, sobre todo si presenta una neoplasia avanzada, constituye una contraindicación relativa para la toracoscopia. Nos parece difícilmente aceptable someter a cualquier tipo de exploración invasiva a un paciente al que presumiblemente quedan sólo unas semanas de vida, y en este sentido hemos de tener en cuenta datos como el índice de Karnofsky y otros parámetros clínicos, incluido el valor del pH en el líquido pleural, que habitualmente se asocia a mal resultado de la pleurodesis y corta supervivencia --en especial en los carcinomas pleurales metastáticos-- si es inferior a 7,2014. Tampoco consideramos prudente hacer una toracoscopia si el paciente presenta grave insuficiencia respiratoria, y particularmente si tiene hipercapnia y/o afectación del hemitórax contralateral al de la exploración.
Como ya se especificó más arriba, la CVT requiere anestesia general, intubación traqueal y, habitualmente, bloqueo unipulmonar mediante tubo de doble luz. Se necesitan además varias puertas de entrada en el tórax que permitan la introducción del instrumental óptico y operatorio, el cual se ha de adecuar a su vez al tipo de intervención que se va a realizar. Por el contrario, la "toracoscopia médica" puede realizarse sin mayores problemas usando una anestesia local cuidadosa apoyada en ligera analgesia/sedación intravenosa, y con un único trocar de 7 o 10 mm de diámetro (dependiendo de la amplitud de los espacios intercostales). Cuando se prefiere usar instrumental más fino (hoy día se dispone de toracoscopios de menos de 3 mm), se hace necesaria la doble entrada: se introduce por una puerta de entrada la óptica y por la otra la pinza de biopsia.
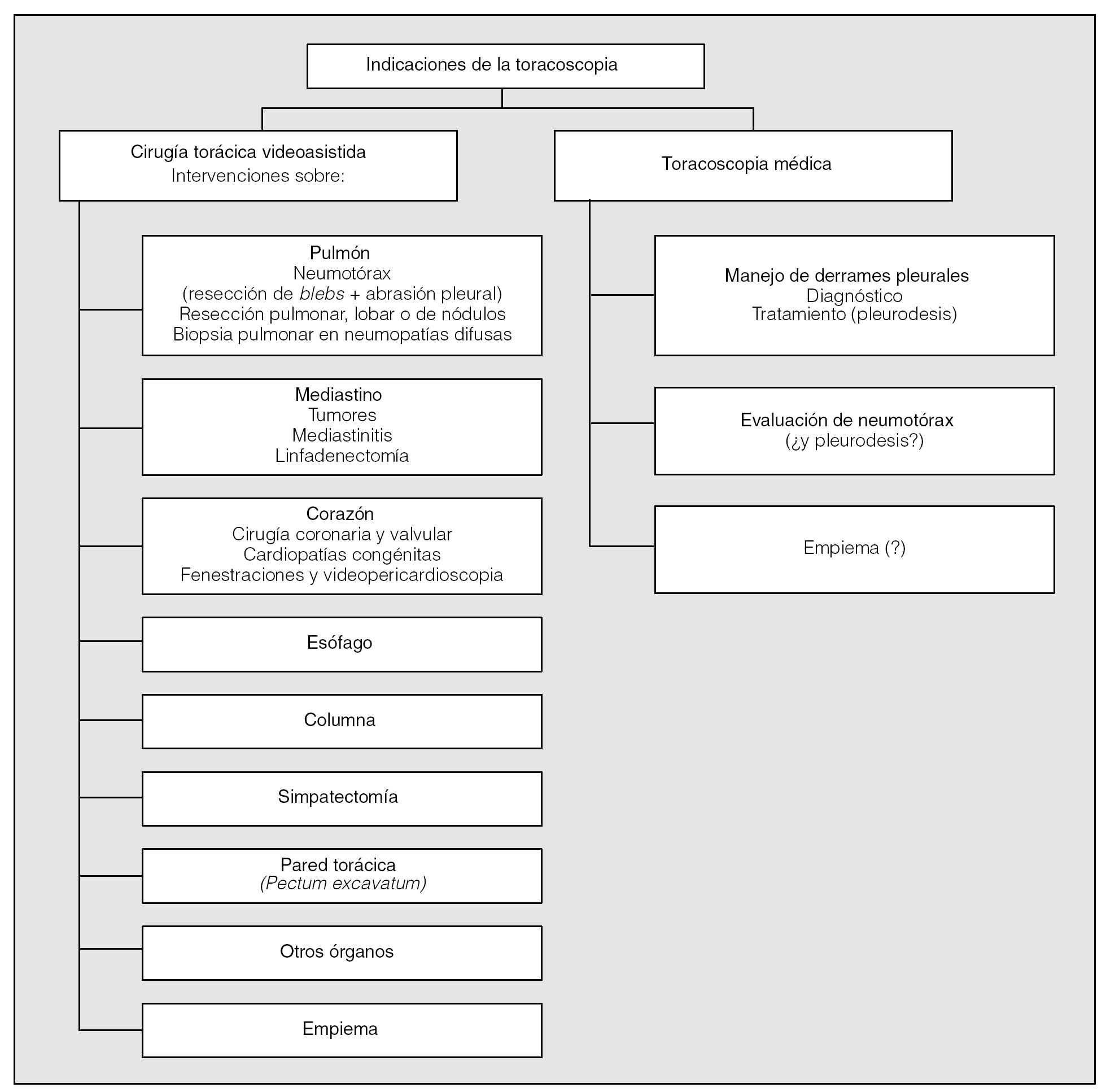
Indicaciones de la toracoscopia (fig. 1)
Fig. 1. Indicaciones de la toracoscopia.
Las indicaciones de la CVT se han extendido de un modo impensable en los últimos años, a medida que se ha ido desarrollando y perfeccionando un impresionante arsenal de instrumentos adaptados para todo tipo de intervenciones endoscópicas15. Actualmente permite la realización de intervenciones de pulmón16-18, afecciones mediastínicas19-21, corazón22-25, esófago26, columna vertebral27,28, simpático paravertebral29-32, pared torácica33, cualquier otro órgano accesible desde una entrada torácica34, y también se ha mostrado eficaz para el manejo del empiema35,36, especialmente cuando aparece tras neumonectomía37. La CVT se está adoptando también como técnica de elección, frente a la esternotomía38, en los casos en que se indica cirugía de reducción de volumen pulmonar. Uno de los avances más fascinantes en los últimos años radica en la posibilidad de realizar intervenciones endoscópicas con la ayuda de robots39-42.
Las indicaciones de la "toracoscopia médica" (o pleuroscopia), especialmente si se realiza con anestesia local y por neumólogos, se concentran en el estudio de derrames pleurales de causa inexplicada y en el tratamiento de los derrames malignos recidivantes mediante la realización de pleurodesis. Otras indicaciones del pasado, tales como la biopsia pulmonar en neumopatías intersticiales difusas o el tratamiento de los empiemas, caen en mi opinión más adecuadamente dentro del ámbito de la CVT, que permite su realización con mayor facilidad y seguridad para el paciente.
Toracoscopia en el neumotórax
El control del neumotórax espontáneo mediante CVT se ha comparado con el rendimiento de la toracotomía axilar, con resultados similares, lo que apoyaría el uso de aquella como primera opción siempre que sea posible43,44.
Aunque en el manejo actual del neumotórax se incluye habitualmente la resección de ampollas o blebs (pequeñas formaciones ampollosas subpleurales) mediante técnicas endoscópicas propias de la CVT, hay también grupos que otorgan un papel prioritario a la realización de pleurodesis en neumotórax espontáneo, con o sin resección de tejido pulmonar acompañante45,46, y esto puede tener especial relevancia en pacientes con enfermedad pulmonar obstructiva crónica avanzada, que difícilmente tolerarían una técnica endoscópica más agresiva. Para delimitar de forma más clara la necesidad o no de resecar los blebs se ha propuesto recientemente el uso de fluoresceína inhalada durante la toracoscopia, lo que permitiría detectar defectos pulmonares microscópicos y hacer así una buena demarcación de los territorios subpleurales dañados en el pulmón47.
Toracoscopia en el manejo de los derrames pleurales
Exceptuando algunas indicaciones anecdóticas, la "toracoscopia médica" queda confinada en la actualidad básicamente al manejo de los derrames pleurales y, pese a las dificultades en el entrenamiento técnico, éste es un campo irrenunciable para el neumólogo, retomando el punto de vista de Jacobaeus, quien expresaba en 1910 que "el examen de las cavidades pleurales [mediante toracoscopia] es de particular interés, en buena parte debido a las limitaciones que la cirugía tiene [en aquella época] para actuar sobre esta región del cuerpo". Es obvio que en nuestro tiempo la cirugía no tiene esas limitaciones, pero también lo es que el cirujano se encuentra más confortablemente instalado en el quirófano y con el paciente anestesiado por completo o profundamente sedado, lo cual rara vez es necesario para el manejo de un derrame pleural en nuestra experiencia. En consecuencia, y aunque de ningún modo se proponga aquí la realización de toracoscopias de forma temeraria, creo que la simplificación que habitualmente entraña la "toracoscopia médica" (sin listas de espera para obtener quirófano ni necesidad de anestesia general e intubación traqueal en pacientes que en ocasiones las tolerarían difícilmente) es un argumento de peso a favor del manejo de los derrames pleurales dentro de un ámbito neumológico, siempre que se adquiera la necesaria preparación y se adopten las imprescindibles precauciones de seguridad. También es obvio que la toracoscopia requiere intenso entrenamiento, tanto en su vertiente "médica" como "quirúrgica", y cuando se aboga por un dominio netamente quirúrgico de todas sus variantes se suele argumentar que el control de algunas de las complicaciones más graves que se pueden presentar requiere el concurso de la cirugía. Aunque esta afirmación es en esencia cierta, su peso real dependerá de la incidencia real de esas complicaciones graves, las cuales son muy escasas en la bibliografía48, y en nuestra experiencia, con cerca de 600 toracoscopias realizadas, nunca hemos requerido asistencia quirúrgica de emergencia49.
En el estudio de cualquier derrame pleural de más de 2 semanas de evolución y causa desconocida se ha de plantear siempre la realización de una técnica biópsica, ya sea mediante aguja o por toracoscopia. No obstante, y a diferencia de la toracoscopia, la biopsia ciega está desprovista de cualquier implicación terapéutica, por lo que la elección de una u otra técnica se condiciona en gran medida por su disponibilidad en el ámbito en que la actividad clínica se desenvuelve y por la agresividad clínica del derrame. Así, la biopsia pleural con aguja se puede realizar en régimen ambulatorio sin mayores problemas50, mientras que la toracoscopia requiere ingreso del paciente y es bastante más complicada en su realización.
En líneas generales, y dada la prevalencia de tuberculosis en nuestro país, es aconsejable el uso de biopsia pleural con aguja para el estudio de derrames de más de 2 semanas de evolución en pacientes jóvenes, y se reservaría la toracoscopia para los mayores de 40 años, en los que la neoplasia es más probable. Si la biopsia con aguja no es diagnóstica, nuestra opción sería acudir a la toracoscopia antes que a una segunda biopsia ciega.
Si la toracoscopia ha conseguido explorar la mayor parte de la cavidad pleural y no resulta diagnóstica, cabe optar por un seguimiento clínico del paciente, en el que se puede llegar a detectar una neoplasia en aproximadamente la cuarta parte de los casos. Si la toracoscopia consiguió sólo una exploración parcial de la cavidad pleural (en la mayoría de los casos por presencia de adherencias firmes) y la situación clínica del paciente es aceptable, sería preferible acudir a la toracotomía para lograr un diagnóstico definitivo, especialmente si sospechamos la existencia de mesotelioma o de un tumor que pudiera beneficiarse de radio o quimioterapia.
Hay ocasiones en que se debe considerar la realización de una segunda toracoscopia cuando la primera no ha sido diagnóstica, especialmente en los pacientes en que el derrame recidiva y requiere su control mediante tratamiento sinfisante. En este caso es importante hacer un completo "mapeo" de la cavidad pleural, tomando abundantes biopsias, y no es excepcional que se detecte así un mesotelioma que había pasado inadvertido en la primera exploración.
"Toracoscopia médica" con finalidad terapéutica
La pleurodesis mediante pulverización de talco constituye la indicación principal para la toracoscopia terapéutica, y proporciona una buena difusión del agente sinfisante por toda la cavidad pleural, lo que contribuye a unos resultados mejores que los que se consiguen con talco en suspensión inyectado a través del drenaje (slurry). Aunque la pleurodesis es en la mayoría de los casos un complemento necesario en el manejo del neumotórax, su principal indicación es el control de los derrames pleurales malignos recidivantes. Hay casos en que no hay duda sobre la necesidad de realizarla, sobre todo cuando el derrame pleural es masivo y provoca desplazamiento contralateral del mediastino. Sin embargo, hay otras ocasiones en que la indicación de pleurodesis es dudosa o incluso está formalmente contraindicada:
1. Cuando se sospecha la existencia de un "pulmón atrapado" por tumor o fibrina es altamente improbable que se consiga una reexpansión pulmonar completa.
2. Cuando hay una grave afectación del pulmón contralateral al derrame pleural o la tomografía computarizada muestra un patrón muy indicativo de linfangitis carcinomatosa, hay que plantear opciones alternativas a la pleurodesis, como la corticoterapia, las toracocentesis repetidas o la colocación de un catéter pleural conectado a algún sistema colector del líquido pleural.
3. Si el derrame pleural coexiste con ascitis, es poco probable que la pleurodesis sea eficaz, y en estos casos es absolutamente necesario controlar la ascitis antes de intentar realizarla.
4. No se debe intentar la realización de una pleurodesis en un paciente en que se sospecha obstrucción bronquial proximal. En estos casos hay que practicar una broncoscopia, con eventual aplicación de láser y colocación de prótesis endobronquial, antes de cualquier intento sinfisante de la pleura.
5. Es importante no demorar excesivamente la realización de pleurodesis en un paciente con derrame pleural recidivante no controlado por la quimioterapia, porque con toda probabilidad se producirá un grave atrapamiento del pulmón, que conducirá a un fracaso de la técnica sinfisante y provocará mayores complicaciones.
Cuando la pleurodesis está contraindicada, otras posibles alternativas son la implantación de un shunt pleuroperitoneal o de un catéter intrapleural conectado a un frasco de vacío o bolsa de colostomía.
Una indicación controvertida para el uso de la "toracoscopia médica" es el empiema. Aunque esta técnica permite resolver en ocasiones el problema mediante el lavado de la cavidad pleural, la sección de adherencias y la colocación de un tubo de drenaje en la posición adecuada, desde mi punto de vista esta exploración es tediosa en la mayoría de las ocasiones, y consigue una completa resolución del problema sólo a veces y siempre que la actuación se haga tempranamente y en empiemas no demasiado complejos. En estos casos, el empleo de fibrinolíticos intrapleurales puede ser igual o incluso más efectivo que la toracoscopia. En casos más complicados podría estar indicada la CVT, que permite el uso de un instrumental más adecuado para limpiar la cavidad pleural de detritos y placas de fibrina, y parece haber algunas evidencias actuales de que en estos casos es preferible recurrir a la CVT como primera opción51.
Perspectivas futuras de la "toracoscopia médica"
Sin pretender ser exhaustivo, creo que en este apartado habría que ocuparse de 3 aspectos relevantes que se comentan a continuación.
Modificaciones técnicas
La base de esta exploración por parte de los neumólogos radica en su ejecución con la mayor simplicidad posible, y cualquier modificación técnica que contribuya a esta simplificación ayudará, por consiguiente, a la extensión de su uso. En este sentido convendría considerar 2 aspectos:
1. ¿Toracoscopio flexible? Es frecuente oír preguntas o comentarios respecto al posible uso del broncofibroscopio para explorar la cavidad pleural, y obviamente este interés está basado en la mayor familiaridad que el neumólogo tiene con este instrumento. No obstante, su uso no puede recomendarse con esta finalidad, dada su poca potencia de iluminación en el interior de una cavidad tan grande como la pleural, la facilidad con que el explorador se puede desorientar y la dificultad para tomar biopsias sin un apoyo sólido. En los últimos años se ha desarrollado un toracoscopio semiflexible, que puede usarse satisfactoriamente en cualquier unidad de endoscopia respiratoria52. Este instrumento ha mejorado sobremanera la facilidad para explorar la cavidad pleural, aunque es costoso y sigue teniendo todavía algunos de los inconvenientes del broncoscopio flexible.
2. ¿Toracoscopio de pequeño calibre? Con el rápido avance de la técnica de fibra óptica, los endoscopistas estamos asistiendo en los últimos años a la presentación de broncofibroscopios cada vez más finos y con un canal de trabajo aceptable, y la toracoscopia no es ajena a este desarrollo, sin que se pierda calidad de visión. Por ello creo que el uso de toracoscopios con calibre menor de 10 mm se irá extendiendo en los próximos años, hecho que facilitará de algún modo que los neumólogos, que por otra parte están habituados a introducir agujas de biopsia en la cavidad pleural con técnica ciega, pierdan el miedo a introducir un toracoscopio, el cual les ayudará enormemente a mejorar su rendimiento en el estudio de las enfermedades pleurales. Nosotros hemos demostrado que no hay pérdida significativa en el rendimiento diagnóstico cuando se usa un toracoscopio de 7 mm en lugar del habitual de 10 mm, y recientemente se han presentado buenos resultados usando toracoscopios extremadamente finos, resultados en gran medida comparables con los obtenidos con los toracoscopios convencionales, más gruesos53.
Formación y práctica de la toracoscopia por parte de los neumólogos
Uno de los problemas relacionados con la toracoscopia radica en su lenta curva de aprendizaje, de modo que se requiere la realización de una importante cantidad de exploraciones antes de considerar que el entrenamiento ha sido adecuado. Así, nuestro rendimiento en la toma de biopsias con valor diagnóstico aumentó desde un 70% en la primera época (con 96 pacientes neoplásicos) hasta un 91% en la segunda (con 174 pacientes añadidos sobre la primera serie). Esto implica que, a medida que adquirimos más confianza en el manejo de la técnica, tomamos mayores y mejores biopsias, sin por ello aumentar el índice de complicaciones. Mi percepción personal es que, dejándose llevar por la facilidad de encomendar al cirujano torácico la realización de la técnica en numerosos hospitales, muchos neumólogos se han acomodado en los últimos años a renunciar a esta exploración, a veces incluso cuando en ese centro en cuestión había una tradición de realización de pleuroscopias desde muchos años atrás. Sin que obviamente se trate de emprender ningún tipo de cruzada en favor de la "toracoscopia médica", creo que, dada la experiencia de quienes hemos estado realizándola durante bastantes años sin grandes complicaciones, se debería incentivar y planificar una formación continuada y reglada para las nuevas generaciones de neumólogos. Una de las posibilidades de entrenar a los residentes en esta materia sería la realización de toracoscopia en los pacientes con neumotórax, en quienes la toracoscopia permitiría efectuar una completa evaluación de la situación pleuropulmonar antes de tomar decisiones terapéuticas. Esta práctica está bien establecida en algunos países europeos, especialmente escandinavos, y proporciona una excelente oportunidad para entrenar a los principiantes en toracoscopia, ya que el pulmón se encuentra ya colapsado y el riesgo de provocar complicaciones al introducir el trocar es escaso54.
La toracoscopia como instrumento de investigación
Ésta es una posibilidad muy poco explorada, pero que a nosotros nos está produciendo grandes satisfacciones en los últimos años, y básicamente en 3 campos concretos:
1. Estadificación de los tumores pleurales (especialmente mesotelioma), que nos ayuda en la toma de decisiones terapéuticas e incluso nos orienta sobre la eficacia de determinados tratamientos (quimioterapia u otros tratamientos intrapleurales) en muchos casos.
2. Estudios a realizar sobre biopsias pleurales, que nos permiten investigar la agresividad de un determinado tumor y la presencia en sus células de determinados receptores o marcadores, y que en un futuro nos podrían permitir investigar su sensibilidad a algunos de los tratamientos que pretendamos aplicar.
3. Otros estudios permiten establecer una estrecha correlación entre determinados marcadores o sustancias presentes en el líquido pleural y su correspondencia histológica en el tejido, lo que nos ayuda a conseguir un mejor conocimiento de la fisiopatología de la cavidad pleural, cuya actividad metabólica es intensa y que, en mi opinión, está muy lejos de ser un simple espacio virtual sin funcionalidad aparente55.