Se recomienda la tromboprofilaxis con heparina de bajo peso molecular a dosis fijas en pacientes médicos agudos que requieran ingreso hospitalario. El objetivo de este estudio ha sido determinar si la actividad antifactor Xa de la enoxaparina depende del peso corporal cuando se administra a pacientes hospitalizados por un proceso respiratorio agudo como profilaxis de la enfermedad tromboembólica venosa.
Pacientes y métodosSe incluyó prospectivamente en el estudio a todos los pacientes ingresados en el Servicio de Neumología entre enero y diciembre de 2006 por un proceso respiratorio agudo con indicación de tromboprofilaxis farmacológica. Se determinó la actividad anti-Xa 4 h después de la administración de la enoxaparina, en el tercer día de ingreso hospitalario. El criterio de evaluación principal fue la actividad anti-Xa en función del índice de masa corporal (IMC).
ResultadosSe incluyó a 112 pacientes en el estudio. La actividad anti-Xa media disminuyó a medida que aumentaban los cuartiles de IMC (0,28, 0,23, 0,15 y 0,13 U/ml para los cuartiles 1, 2, 3 y 4, respectivamente). En el análisis multivariable, el IMC fue la única variable predictora de actividad anti-Xa insuficiente (odds ratio = 1,14; intervalo de confianza del 95%, 1,05-1,24; p < 0,002), después de ajustar por la edad, el sexo y la creatinina sérica. Hubo 2 episodios sintomáticos de trombosis venosa profunda proximal en el mes posterior al ingreso hospitalario, ambos en pacientes con actividad anti-Xa insuficiente.
ConclusionesLa actividad anti-Xa de la enoxaparina depende del IMC en los pacientes que reciben tromboprofilaxis por un proceso médico agudo que requiera hospitalización.
Thromboprophylaxis with a fixed dose of lowmolecular- weight heparin is recommended for hospitalized acutely ill medical patients. The purpose of this study was to assess whether the anti-factor Xa (anti-Xa) activity of enoxaparin prescribed for venous thromboembolism prophylaxis depends on body mass index (BMI) in patients hospitalized for an acute respiratory disease.
Patients and methodsAll patients admitted to the respiratory medicine department (January-December 2006) for an acute respiratory disease, and for whom pharmacologic thromboprophylaxis was indicated, were included in the study. Anti-Xa activity was measured 4 hours after administration of enoxaparin on the third day of hospitalization. The primary outcome was anti-Xa activity in relation to BMI.
ResultsOne hundred twelve patients were enrolled. Mean anti-Xa activity decreased with each BMI quartile (0.28, 0.23, 0.15, and 0.13 U/mL for quartiles 1, 2, 3, and 4, respectively). In the multivariate analysis, BMI was the only predictor of inadequate anti-Xa activity (odds ratio, 1.14; 95% confidence interval, 10.5-1.24; P<.002) after adjustment for age, sex, and serum creatinine levels. Two episodes of symptomatic proximal deep vein thrombosis were diagnosed in the month after hospitalization; both occurred in patients who had inadequate anti-Xa activity.
ConclusionsAnti-Xa activity is dependent on BMI in hospitalized acute medical patients receiving enoxaparin for thromboprophylaxis.
Las heparinas de bajo peso molecular (HBPM) se han convertido en el tratamiento de elección de los pacientes con enfermedad tromboembólica venosa (ETEV)1. El pico de actividad antifactor Xa se produce de 3 a 5h después de una inyección subcutánea y, a diferencia de la heparina no fraccionada, su eficacia y seguridad se basan en su acción predecible cuando se utilizan dosis ajustadas al peso del paciente2.
Dos ensayos clínicos han demostrado que los pacientes médicos con enfermedad aguda que requieren ingreso hospitalario presentan un riesgo de ETEV no despreciable y que la administración de una dosis fija de HBPM (independiente del peso) reduce de manera significativa este riesgo3,4. En ambos estudios el beneficio de la tromboprofilaxis farmacológica no se mantuvo en el subgrupo de pacientes obesos5,6. Aunque una proporción significativa de pacientes médicos no recibe tromboprofilaxis7, la mayoría de los episodios trombóticos se producen en pacientes en quienes fracasa la tromboprofilaxis8.
Las HBPM tienen un efecto limitado en la prolongación del tiempo de tromboplastina parcial activado9–11, y no se recomienda el uso de éste para el seguimiento de su actividad. El método recomendado para comprobar la respuesta anticoagulante de las HBPM es la medición de la actividad anti-Xa12. Se ha propuesto realizar el seguimiento de estos valores en los pacientes obesos, en aquéllos con insuficiencia renal y en las embarazadas13–16.
Éste es el motivo por el que hemos realizado un estudio farmacocinético en pacientes con enfermedad respiratoria ingresados a los que se administró enoxaparina como tromboprofilaxis, para estimar tanto la actividad anti-Xa como su variabilidad en función del peso e identificar los factores responsables de dicha variabilidad.
Pacientes y métodosDiseño, pacientes y criterios de selecciónSe trata de un estudio prospectivo de cohorte, realizado en un hospital terciario universitario entre enero y diciembre de 2006. Se incluyó en él a todos los pacientes ingresados en el Servicio de Neumología por una enfermedad respiratoria aguda que requirieron enoxaparina para profilaxis de ETEV17. Se excluyó a aquéllos con indicación de tratamiento anticoagulante curativo o con cualquier contraindicación para el uso de dosis profilácticas de HBPM (hemorragia activa o riesgo alto de hemorragia). El estudio fue aprobado por el Comité Ético del hospital y todos los pacientes dieron su consentimiento para participar en él.
IntervencionesSe administró a los pacientes enoxaparina subcutánea (Clexane®, Sanofi-Aventis, España) en dosis de 40mg al día durante una media ± desviación estándar de 10 ± 4 días. La actividad anti-Xa se determinó 4h después de la administración de la enoxaparina10 el tercer día de ingreso hospitalario. No se realizó ningún ajuste de dosis en función de los valores de anti-Xa.
Actividad anti-XaLas muestras de sangre se recogieron en un tubo citratado, se centrifugaron a 2.000g durante 20min y se almacenaron a −20°C. La actividad anti-Xa se midió con el reactivo Berichrom® (Dade-Behring, Liederbach, Alemania). Se estableció como rango de actividad anti-Xa profiláctica entre 0,2 y 0,6 U/ml, y como rango de actividad terapéutica entre 0,6 y 1,0 U/ml18–20.
Episodios analizadosSe definió como parámetro de valoración principal la actividad anti-Xa en función del índice de masa corporal (IMC). El parámetro secundario fueron los episodios trombóticos sintomáticos que se confirmaron objetivamente y las hemorragias mayores en el mes posterior al ingreso hospitalario.
A nálisis estadísticoLas variables continuas se expresaron como media ± desviación estándar y se compararon con el test de la t de Student para datos emparejados y no emparejados. Las variables categóricas, que se expresaron como porcentajes, se compararon con la prueba de la χ2, o bien con el test exacto de Fisher en caso necesario. En el análisis multivariado se utilizó un modelo de regresión logística que incluyó el IMC, la edad, el sexo y los valores de creatinina sérica. Los valores de p < 0,05 se consideraron estadísticamente significativos. El análisis estadístico se realizó con el paquete estadístico SPSS para Windows, versión 13 (SPSS Inc., Chicago, Illinois, EE.UU.).
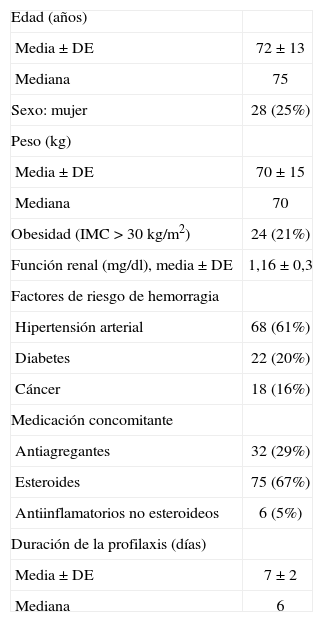
ResultadosPacientesSe incluyó en el estudio a 112 pacientes con indicación de tromboprofilaxis farmacológica por enfermedad respiratoria aguda que ingresaron en el Servicio de Neumología del Hospital Ramón y Cajal entre enero y diciembre de 2006. Sus características basales se recogen en la tabla I. La edad media de los pacientes era de 72 años y un 25% tenía más de 80 años. La mayoría eran varones. El 21% presentaba obesidad y el 9% insuficiencia renal (concentración de creatinina sérica > 1,5mg/dl) en el momento del ingreso. La duración media de la tromboprofilaxis fue de 7 días.
Características basales de los 112 pacientes estudiados
| Edad (años) | |
| Media ± DE | 72 ± 13 |
| Mediana | 75 |
| Sexo: mujer | 28 (25%) |
| Peso (kg) | |
| Media ± DE | 70 ± 15 |
| Mediana | 70 |
| Obesidad (IMC > 30kg/m2) | 24 (21%) |
| Función renal (mg/dl), media ± DE | 1,16 ± 0,3 |
| Factores de riesgo de hemorragia | |
| Hipertensión arterial | 68 (61%) |
| Diabetes | 22 (20%) |
| Cáncer | 18 (16%) |
| Medicación concomitante | |
| Antiagregantes | 32 (29%) |
| Esteroides | 75 (67%) |
| Antiinflamatorios no esteroideos | 6 (5%) |
| Duración de la profilaxis (días) | |
| Media ± DE | 7 ± 2 |
| Mediana | 6 |
DE: desviación estándar; IMC: índice de masa corporal.
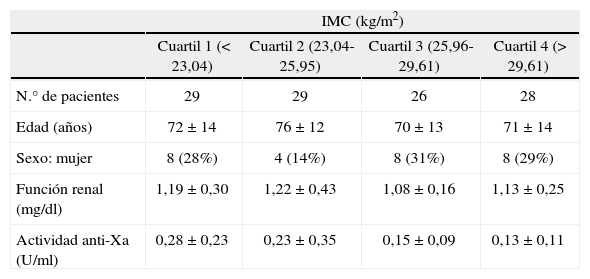
De los 112 pacientes, 62 (55%) presentaban una actividad anti-Xa inferior a la adecuada para tromboprofilaxis. La actividad anti-Xa media (tabla II) fue significativamente inferior en el cuartil de los pacientes con mayor IMC (p < 0,001). Esta relación se mantuvo cuando la cohorte se dividió en deciles de IMC, sin evidenciarse una relación en forma de U (fig. 1).
Actividad anti-Xa media en función de los cuartiles de índice de masa corporal (IMC)
| IMC (kg/m2) | ||||
| Cuartil 1 (< 23,04) | Cuartil 2 (23,04-25,95) | Cuartil 3 (25,96-29,61) | Cuartil 4 (> 29,61) | |
| N.° de pacientes | 29 | 29 | 26 | 28 |
| Edad (años) | 72 ± 14 | 76 ± 12 | 70 ± 13 | 71 ± 14 |
| Sexo: mujer | 8 (28%) | 4 (14%) | 8 (31%) | 8 (29%) |
| Función renal (mg/dl) | 1,19 ± 0,30 | 1,22 ± 0,43 | 1,08 ± 0,16 | 1,13 ± 0,25 |
| Actividad anti-Xa (U/ml) | 0,28 ± 0,23 | 0,23 ± 0,35 | 0,15 ± 0,09 | 0,13 ± 0,11 |
Valores expresados como media ± desviación estándar o número de pacientes (porcentaje).
Únicamente el IMC se asoció de forma estadísticamente significativa a la actividad anti-Xa (odds ratio = 1,14; intervalo de confianza del 95%, 1,05-1,24; p < 0,002), una vez ajustado en función de la edad, el sexo y la creatinina sérica.
Episodios trombóticos y hemorrágicosNo se produjo ninguna hemorragia mayor durante el período de seguimiento. Se registraron 2 episodios sintomáticos de trombosis venosa profunda proximal en el mes posterior al ingreso hospitalario, ambos en pacientes con actividad anti-Xa insuficiente.
DiscusiónDe este estudio se derivan 2 hallazgos fundamentales. En primer lugar, la actividad anti-Xa de la enoxaparina está inversamente relacionada con el IMC de los pacientes que reciben tromboprofilaxis por un proceso respiratorio agudo. En segundo lugar, la actividad anti-Xa es inferior a la que se considera profiláctica cuando el IMC está por encima de 26kg/m2.
La relación entre los parámetros farmacocinéticos de las HBPM y el peso corporal ya era conocida en el tratamiento de la ETEV20. Sin embargo, esta relación se ha estudiado menos en los pacientes médicos que reciben tromboprofilaxis farmacológica. Nuestros resultados indican que la actividad anti-Xa de la enoxaparina administrada como profilaxis antitrombótica a los pacientes médicos ingresados depende del peso corporal. Estos resultados son similares a los de 2 estudios publicados previamente sobre profilaxis de pacientes quirúrgicos obesos21 y de pacientes ingresados en unidades de cuidados intensivos22. Sin embargo, esta correlación estadísticamente significativa no se traduce necesariamente en un efecto clínico relevante.
Los estudios clínicos han mostrado resultados contradictorios sobre la correlación de la actividad anti-Xa y los eventos clínicos de los pacientes en quienes se han empleado HBPM para la profilaxis o el tratamiento de la ETEV23–28. Levine et al27 encontraron una asociación significativa entre la actividad anti-Xa y la incidencia de trombosis venosa profunda, detectada por venografía, o hematomas de la herida quirúrgica en pacientes a los que se administró tromboprofilaxis por cirugía de prótesis de cadera. Otros autores han demostrado asociaciones más débiles en la profilaxis de cirugía general25,26, y en algunos estudios no se ha encontrado ninguna correlación23,29.
Nuestro estudio presenta algunas limitaciones que deben tenerse en cuenta. Los rangos de actividad anti-Xa de la enoxaparina para profilaxis y tratamiento de la ETEV no se han validado en estudios prospectivos. Además, la serie estudiada fue pequeña y se produjeron pocos eventos clínicos. En este sentido, no pudo determinarse si la menor actividad anti-Xa en pacientes obesos se traduce en un aumento del riesgo trombótico en estos pacientes. Finalmente, en la mayoría de los pacientes del estudio la función renal era normal, y nuestros resultados no son generalizables para pacientes con disminución del aclaramiento de creatinina.
En conclusión, la actividad anti-Xa de la enoxaparina depende del IMC en los pacientes que reciben tromboprofilaxis por un proceso médico agudo. Se requieren estudios bien diseñados para analizar si este hallazgo implica un aumento de la incidencia de episodios trombóticos en este grupo de pacientes.
Trabajo financiado con una beca de la Sociedad Neumomadrid.