Introducción
La aparición de fibrilación auricular (FA) en el postoperatorio de cualquier intervención quirúrgica no es infrecuente. La asociación entre FA y cirugía sobre órganos torácicos, excepto el corazón, se sitúa entre el 3,8 y el 37%1. La frecuencia de aparición de FA en caso de lobectomías se encuentra establecida en un 10-20% y es cercana al 40% cuando se trata de neumonectomías2.
La presencia de FA se relaciona con una mayor morbilidad, mayor riesgo de accidente cerebrovascular, incremento de la estancia hospitalaria y, por tanto, un mayor coste hospitalario, además de un aumento de la mortalidad perioperatoria y un peor pronóstico de supervivencia a largo plazo3,4.
Se han identificado varios factores de riesgo que hacen que en el postoperatorio de la cirugía torácica sea más frecuente el desarrollo de FA: la edad avanzada, enfermedad cardíaca previa, enfermedad pulmonar obstructiva crónica (EPOC)5, antecedente de arritmias y tipo de cirugía realizada1,3.
El objetivo del presente estudio ha sido evaluar la hipótesis de que el desarrollo postoperatorio de FA en cirugía pulmonar anatómica depende significativamente de factores de comorbilidad preoperatoria e identificar estos factores y el exceso de riesgo.
Pacientes y método
Entre enero de 2002 y diciembre de 2003 se realizaron en nuestro servicio 149 resecciones anatómicas pulmonares. Se recogieron prospectivamente las características clínicas, quirúrgicas, bioquímicas y oncológicas de todos los pacientes intervenidos en nuestro servicio. Se excluyeron de este estudio todas aquellas intervenciones no anatómicas y toracotomías exploradoras, así como a los pacientes con FA diagnosticada previa a la cirugía. Todas las intervenciones se realizaron por toracotomía según la técnica clásica. No se efectuó disección mediastínica de forma sistemática, de manera que ésta se practicó en unos pacientes mientras que otros se sometieron a muestreo ganglionar según decidiera el cirujano responsable en cada caso particular. La valoración de la función pulmonar se llevó a cabo según el protocolo del Grupo Cooperativo de Carcinoma Broncogénico de la Sociedad Española de Neumología y Cirugía Torácica (GCCB-S)6. Ningún paciente recibió tratamiento profiláctico para la evitar FA.
Las variables prospectivas analizadas fueron: edad, sexo, función respiratoria --volumen espiratorio forzado en el primer segundo (FEV1), absoluto y porcentaje; FEV1 postoperatorio calculado, y capacidad vital forzada (FVC), absoluto y porcentaje--, comorbilidad (EPOC, enfermedad cardíaca, diabetes mellitus, enfermedad vascular periférica), causa de la resección (carcinoma broncogénico y su estadificación patológica, enfermedad metastásica, tumor neuroendocrino pulmonar, aspergiloma pulmonar, patología benigna), tipo de resección, tipo de disección mediastínica, tratamiento quimioterápico previo, aparición de FA y día en que se presentó, estancia hospitalaria y mortalidad y sus causas a los 30 días.
Se consideró enfermedad cardíaca previa la afección cardíaca en cualquier momento de la vida, incluidas arritmias no tratadas, infarto de miocardio antiguo, fiebre reumática con afectación valvular e insuficiencia cardíaca de cualquier etiología. La enfermedad vascular periférica se definió según los criterios establecidos en el protocolo del GCCB-S6. Se consideró EPOC cuando el FEV1 era menor del 80% del teórico y el FEV1/FVC menor del 70%. Se registró la variable quimioterapia previa cuando ésta se había administrado en los 3 meses previos a la cirugía tanto para el tratamiento oncológico de las metástasis a distancia como para tratamiento de inducción previo a la cirugía del carcinoma broncogénico.
Se calculó el FEV1 postoperatorio según la fórmula descrita por Juhl y Frost7.
Todos los pacientes permanecieron las primeras 24 h postoperatorias en la unidad de reanimación. En esta unidad se realiza monitorización continua del electrocardiograma y de la saturación de oxígeno mediante pulsioximetría. Posteriormente se trasladó a los pacientes a la unidad de cirugía torácica, donde durante los siguientes días se les monitorizó mediante pulsioximetría y se les realizó un electrocardiograma a diario. Todos los casos de FA se confirmaron electrocardiográficamente. Todos los pacientes recibieron la visita del fisioterapeuta y realizaron ejercicios respiratorios con espirómetro incentivado.
La FA se trató en todos los pacientes y los fármacos empleados fueron digoxina y antiarrítmicos, amiodarona o propafenona, en función de los antecedentes cardiológicos previos.
Análisis estadístico
El análisis estadístico de los datos se realizó con el programa SPSS versión 11.5. Las variables cualitativas se compararon con la prueba estadística de la χ² o test exacto de Fisher cuando era apropiado. Las variables cuantitativas se compararon con la prueba de la t de Student para variables independientes. Se estimaron los excesos de riesgo con la prueba de Mantel-Haenszel. El nivel de confianza se estableció en p < 0,05.
Resultados
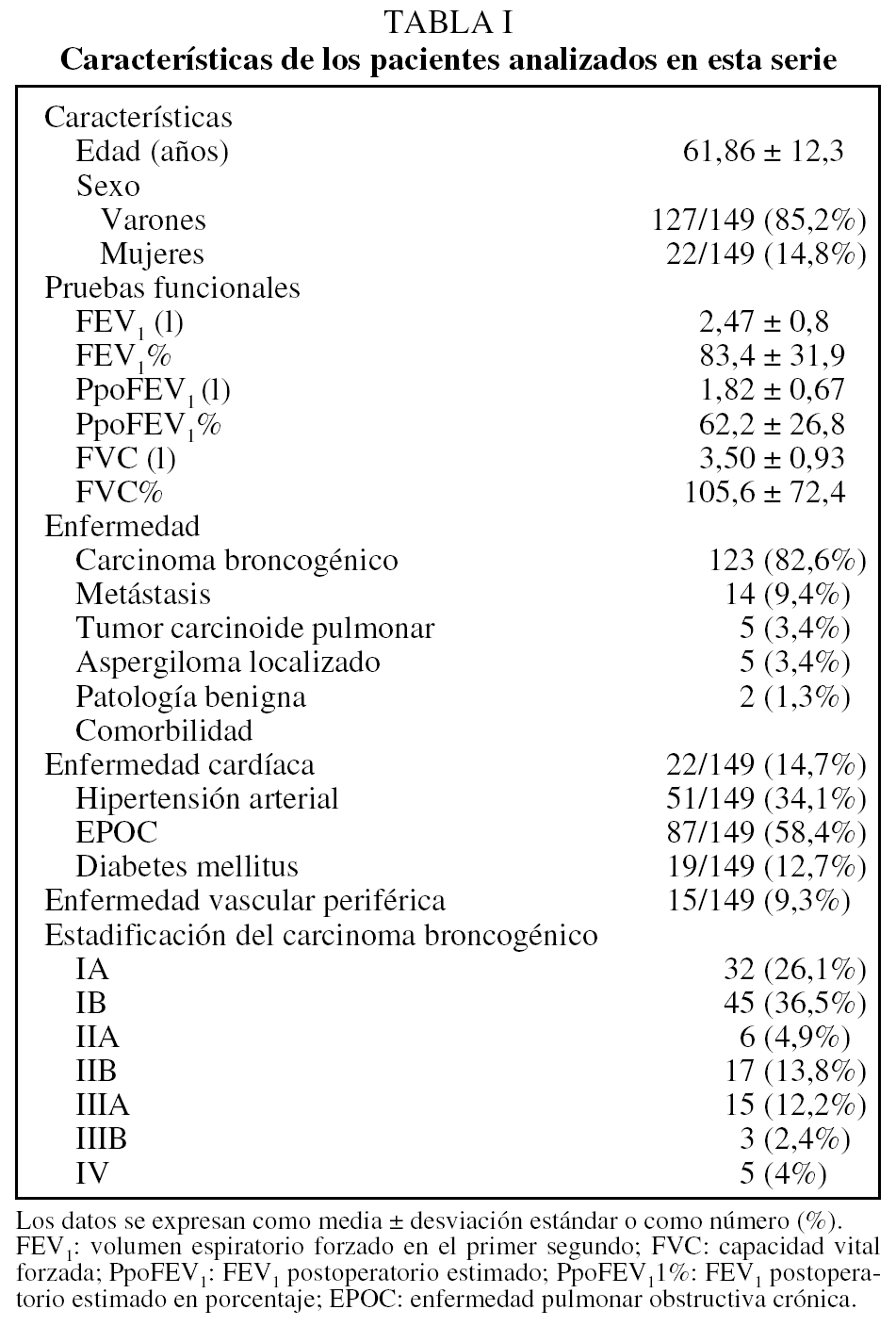
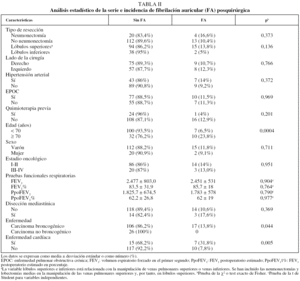
La edad media (± desviación estándar) de los pacientes operados --127 varones (85,2%) y 22 mujeres (14,8%)-- fue de 61,8 ± 12,3 años (rango: 17-79). Las características clínicas, oncológicas y funcionales más importantes de estos pacientes están recogidas en la tabla I. La estancia media postoperatoria fue de 9,9 ± 5,9 días. La mortalidad fue del 8,1% (12 pacientes). Las causas de mortalidad fueron neumonía (4 casos), infarto agudo de miocardio (un caso), fístula bronquial (3 casos), síndrome de distrés respiratorio del adulto (3 casos) y tromboembolia pulmonar (un caso).
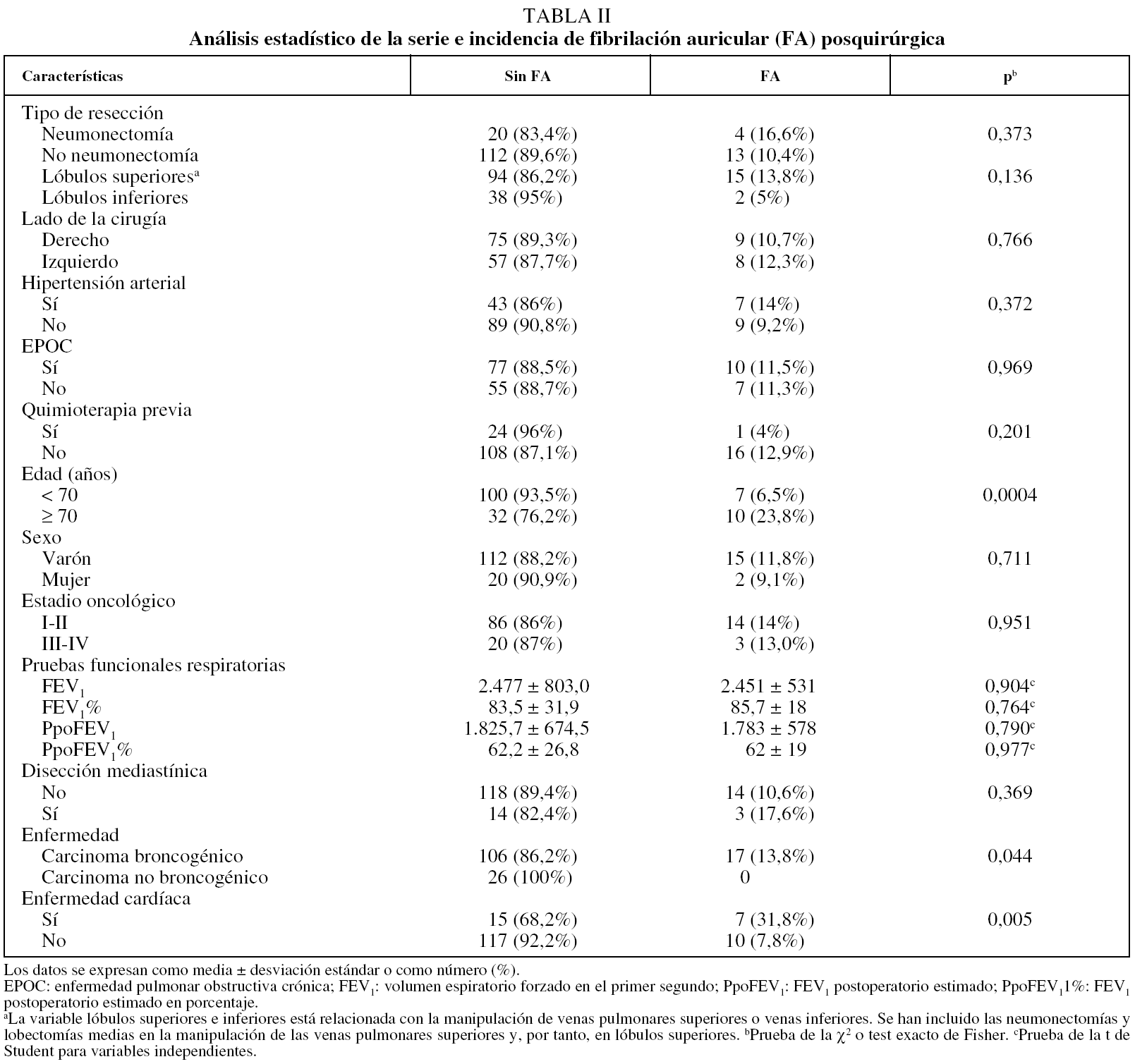
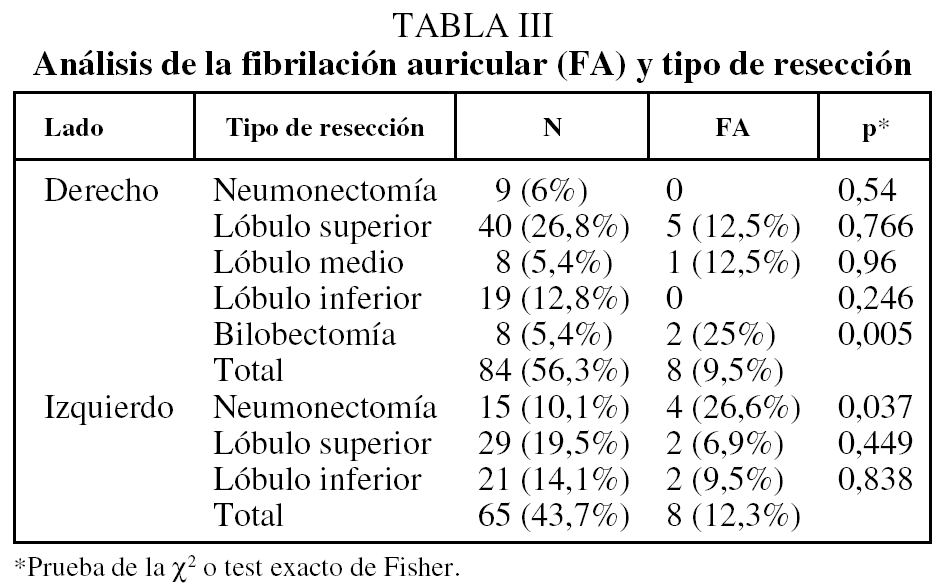
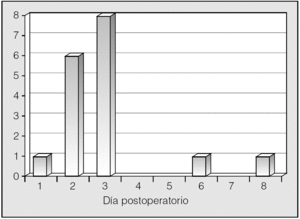
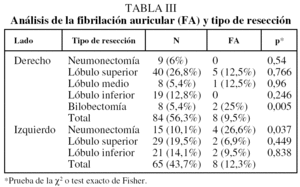
Se detectó FA en el postoperatorio en 17 pacientes (11,4%). Su aparición se produjo en los días 2-3 del postoperatorio en 14 (82,3%) de los 17 pacientes (fig. 1). Se consiguió reversión a ritmo sinusal en 15 (88,2%). Sólo fallecieron 2 pacientes que habían desarrollado FA, dato que no es estadísticamente significativo. Las variables estudiadas más importantes y los resultados estadísticos se recogen en la tabla II. El tipo de intervención y la incidencia de FA se indican en la tabla III. Se identificaron los siguientes factores de riesgo: edad ≥ 70 años (p < 0,0004), enfermedad cardíaca previa (p < 0,005), pacientes operados por carcinoma broncogénico (p < 0,04) y tipo de resección bilobectomía derecha (p < 0,05) y neumonectomía izquierda (p < 0,03). El exceso de riesgo respecto a las variables positivas se recoge en la tabla IV. No fueron factores de riesgo la presencia de hipertensión arterial, EPOC, estadio del carcinoma broncogénico, disección mediastínica sistemática ni otro tipo de resección pulmonar distinta, ni ninguna otra característica estudiada.
Fig. 1. Día de aparición de la fibrilación auricular.
Discusión
La aparición de FA durante el postoperatorio de la cirugía torácica es frecuente, ya que a la intervención y la manipulación se suman frecuentemente factores predisponentes de origen multifactorial como son la hipoxia, hipovolemia, sepsis, desequilibrios electrolíticos, aumento de actividad vagal o el incremento de precarga cardíaca1,8. Según otros estudios, la edad avanzada, el sexo masculino, una historia de enfermedad cardíaca previa y las transfusiones intraoperatorias también hacen que aumente el riesgo de FA3.
La FA es causa de morbilidad porque supone más riesgo de accidente cerebrovascular o embolia periférica, además de aumentar la estancia hospitalaria y alargar la estancia en unidades de cuidados intensivos2,9.
La incidencia registrada en nuestra serie (11,4%) es similar a las de otras series publicadas3,8,10,11. El factor de riesgo con mayor fuerza identificado, tanto en los estudios publicados en la bibliografía como en nuestra serie, ha sido la edad9. Aunque cabría pensar que la edad pudiera ser un factor de confusión entre la presencia de FA y el aumento de estancia hospitalaria y morbilidad asociada, el hecho es que es un factor importante teniendo en cuenta el incremento de la edad media de los pacientes intervenidos en los servicios de cirugía torácica. El sexo varón también se ha relacionado con un mayor riesgo de desarrollar esta arritmia2,3.
No hemos encontrado una relación significativa clara de los valores del FEV1 pre y postoperatorio estimado, tanto en valores absolutos como en porcentaje, con la aparición de FA. Sin embargo, la bibliografía refleja una relación entre la gravedad de la EPOC y un mayor riesgo de FA5. Asimismo, el hecho de presentar hipoxemia tanto en el preoperatorio como en el postoperatorio se ha relacionado también con esta arritmia2,12. La enfermedad cardíaca previa se ha identificado como factor de riesgo en diversos estudios, sobre todo la enfermedad isquémica y la insuficiencia cardíaca congestiva de diversas etiologías13.
El mecanismo de producción podría estar relacionado con una estimulación del área auricular en la zona de la sutura de resección en la vena pulmonar, zona que se ha identificado en varios estudios prestigiosos como zona de gatillo. Esto ocurre hasta en un 94% de los casos sobre todo en las venas pulmonares superiores, concretamente en los 2-4 cm centrales, donde se originaría la actividad ectópica14. En ciertos estudios aparece una mayor incidencia en neumonectomías15,16 y en estos casos podría estar relacionado con la disección a veces intrapericárdica de dichas venas superiores12. Otros estudios no encuentran relación entre el tipo de resección pulmonar y esta arritmia17. En nuestra serie esta asociación no ha sido significativa, aunque también es cierto que en nuestra práctica somos muy restrictivos en la realización de neumonectomías derechas en pacientes mayores de 70 años. Tampoco hemos constatado una relación mayor con la realización de resecciones pulmonares de lóbulos superiores y, por consiguiente, una manipulación más evidente de las venas pulmonares superiores3, donde electrofisiológicamente podrían estar dichas zonas de gatillo con más frecuencia14. Ésta sería la razón fundamental para la gran diferencia de incidencia de FA entre las resecciones pulmonares anatómicas y no anatómicas, en las que normalmente no existe manipulación de las estructuras periauriculares ni pericárdicas12.
En ningún estudio, por lo que sabemos, ha sido un factor determinante el estadio tumoral5. Sí lo han sido el tipo de resección pulmonar y la disección mediastínica llevada a cabo. Por tanto, la realización de disección mediastínica sistemática también aparece en la bibliografía como factor de riesgo del desarrollo de FA12. Esto podría relacionarse con la lesión de las ramas nerviosas vagales, que se lesionan al extirpar el tejido linfograso de las áreas mediastínicas y peripulmonares, que son imprescindibles para la adecuada estadificación de certeza del carcinoma broncogénico.
La aparición de FA en el postoperatorio puede causar un aumento de la comorbilidad. Con el fin de evitar este riesgo, se ha contemplado la posibilidad de utilizar profilácticamente ciertos fármacos para prevenirla o disminuir su incidencia. Algunos de ellos son la digoxina18, los bloqueadores beta, la amiodarona19,20 y el diltiazem21. En pacientes de alto riesgo21 tan sólo los 2 últimos han demostrado tener valor profiláctico en el desarrollo de FA20. La amiodarona se considera el antiarrítmico más seguro y eficaz para su tratamiento22. Estos estudios no demostraron, sin embargo, una disminución de los costes o la estancia hospitalaria.
En conclusión, la aparición de FA después de una resección pulmonar anatómica es una complicación frecuente que se asocia a edad avanzada, antecedentes de cardiopatía, intervención por carcinoma broncogénico, neumonectomía izquierda y bilobectomía derecha. La identificación de estos factores de riesgo puede ser de utilidad para iniciar estudios prospectivos encaminados a valorar el uso de fármacos antiarrítmicos para prevenir esta complicación.
Correspondencia: Dr. A. Gómez-Caro.
Servicio de Cirugía Torácica. Hospital Universitario 12 de Octubre.
Ctra. de Andalucía, Km 5,400. 28041Madrid. España.
Correo electrónico: abelitov@yahoo.es
Recibido: 28-2-2005; aceptado para su publicación: 3-5-2005.