Introducción
Las guías clínicas describen la limitación al flujo aéreo que se registra en la enfermedad pulmonar obstructiva crónica (EPOC) como un fenómeno progresivo, es decir, como un trastorno que evoluciona negativamente en el curso de la enfermedad, con las consecuencias nefastas que se derivan de este fenómeno1. La EPOC es progresiva y cambiante, 2 rasgos que la definen, la caracterizan y ponen también de manifiesto las dificultades que plantea su posible control.
Tradicionalmente, la evolución de la EPOC se ha considerado en función de la tasa acelerada de deterioro del volumen espiratorio forzado en el primer segundo (FEV1), que se observó originalmente en datos procedentes de un estudio de Fletcher y Peto2. Los datos de este trabajo mostraron la existencia de un descenso progresivo del valor del FEV1 a partir de la conjunción de datos transversales, recogidos en diferentes grupos de edad, y longitudinales, mediante el seguimiento de 8 años. Siguiendo este esquema se sabía también que el abandono del tabaquismo era la única intervención capaz de reducir la tasa de descenso del FEV1 en pacientes con EPOC. Los datos del Nacional Health Study3 corroboraron los hallazgos de Fletcher y Peto2, y pusieron de manifiesto que ninguna intervención farmacológica de las disponibles en ese momento podía influir en dicha caída.
En los últimos años, el renovado interés por la EPOC ha hecho posible que nuevos parámetros de valoración se hayan añadido al FEV1 en una búsqueda por cambiar su curso clínico4. Es necesario recordar que la historia natural de la pérdida de función respiratoria es paralela a la de la evolución clínica, pero no idéntica5. La modificación de la evolución de la enfermedad, concepto que alude a la posibilidad de variar su curso natural, se ha convertido en un objetivo prioritario del abordaje de la EPOC. En este sentido, al igual que se hace en otras enfermedades crónicas como la artritis reumatoide o la esclerosis múltiple, se ha incluido la valoración de una serie de parámetros centrados en el paciente como un componente de la definición. En la EPOC, modificar la enfermedad pasa por detener el ritmo creciente de empeoramiento funcional y sistémico que se encuentra asociado a ella.
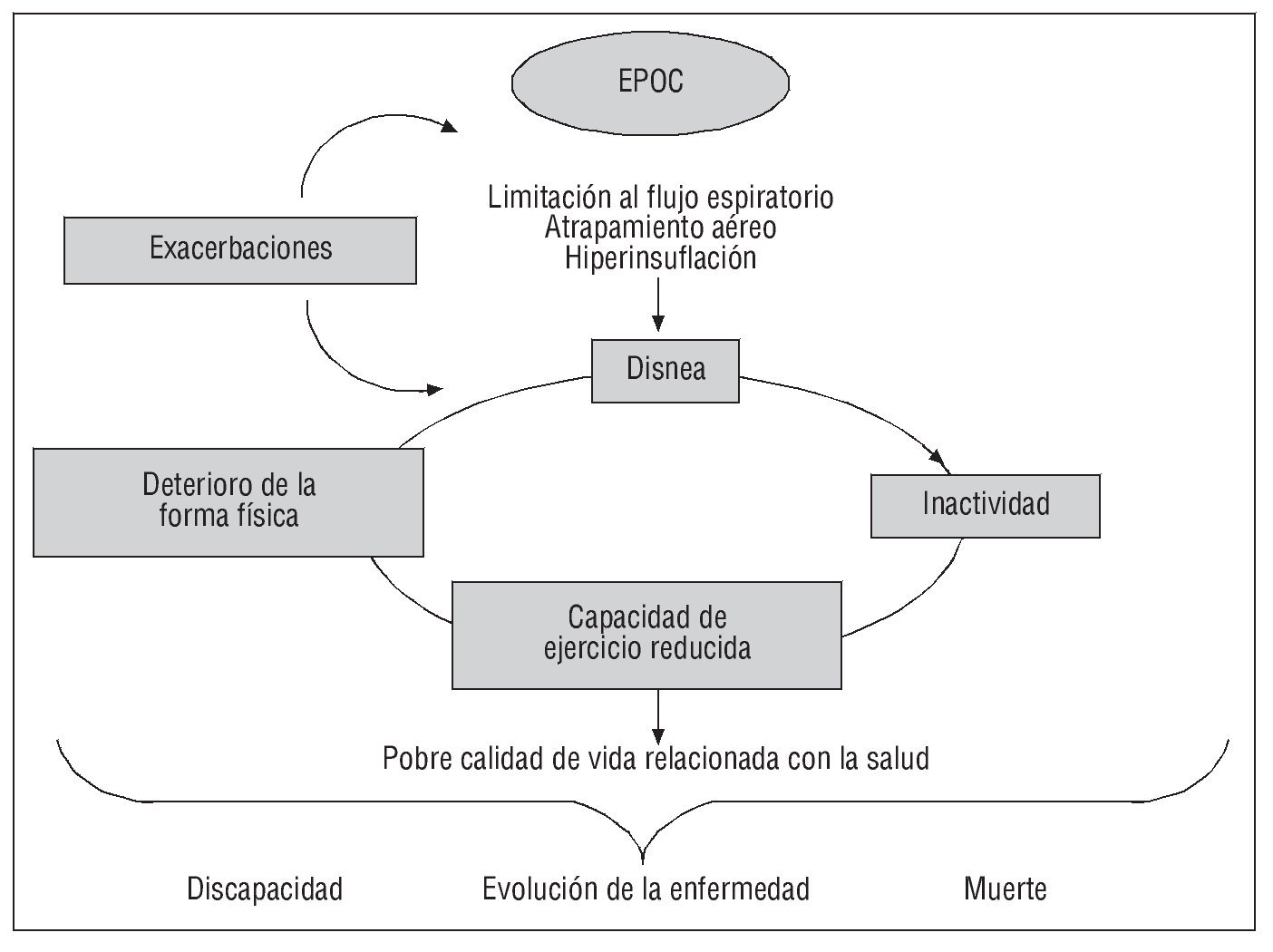
Los componentes esenciales que caracterizan el deterioro fisiológico en la EPOC son la limitación al flujo espiratorio, el atrapamiento aéreo y la hiperinsuflación. Estas anomalías fisiológicas dan lugar al síntoma más relevante e invalidante de la enfermedad, que es la disnea, la cual limita la actividad física del paciente. Como respuesta a este trastorno, los pacientes se vuelven inactivos y tratan de evitar situaciones que exigen cierta actividad física o incluso actividades de la vida diaria, lo que lleva a la pérdida de capacidad física y a la discapacidad. Este círculo vicioso conduce a un empeoramiento de la enfermedad, con una disminución de la calidad de vida relacionada con la salud, y da lugar a discapacidad, progresión de la enfermedad y muerte prematura. Por otro lado, para terminar de agravar las cosas, la EPOC suele asociarse a exacerbaciones agudas de los síntomas. Las exacerbaciones son más frecuentes y/o graves a medida que empeora la EPOC y contribuirán al impacto a largo plazo y a una mortalidad prematura6 (fig. 1).
Fig. 1. Círculo vicioso de la enfermedad pulmonar obstructiva crónica (EPOC) y las posibilidades de intervención para modificar la evolución de la enfermedad.
Cuando se pretende hacer una modificación positiva de la enfermedad, es preciso tener en cuenta todos estos aspectos de la fisiopatología de la EPOC y actuar sobre la capacidad pulmonar, el atrapamiento aéreo, las exacerbaciones, la disnea y la tolerancia al ejercicio. En los últimos años se han llevado a cabo importante estudios a medio y largo plazo en los que se han analizado diferentes tipos de intervenciones farmacológicas, muchas de las cuales se ha demostrado que son capaces de inducir beneficios significativos en la evolución de la enfermedad. En este sentido, el desarrollo del tiotropio ha sido todo un ejemplo a seguir de estudios bien diseñados que han ido estudiando el impacto de este anticolinérgico de acción prolongada en la modificación de la EPOC. Se ha demostrado que el tiotropio puede influir en el curso clínico de la EPOC al incidir positivamente en todas las variables de valoración mencionadas más arriba7-20 (tabla I). Así, el tratamiento de mantenimiento con tiotropio es capaz de reducir la limitación al flujo de aire y mejorar el atrapamiento aéreo y la hiperinsuflación, aportando una permeabilidad ininterrumpida durante 24 h de las vías aéreas a través del bloqueo colinérgico y la relajación del músculo liso de las vías aéreas. La atenuación resultante de la disnea puede brindar la oportunidad de que mejore la resistencia física (reacondicionamiento) y el paciente retome las actividades de la vida diaria. Por último, la disminución de las exacerbaciones, junto con los otros efectos funcionales ya descritos, hace que puedan mejorar la calidad de vida y el estado de salud. En resumen, la modificación de la enfermedad en la EPOC es un concepto evolutivo y en la actualidad se acepta que, junto con el deterioro de la función pulmonar, los parámetros antes comentados también empeoran con la progresión de la enfermedad. La aceptación de este hecho es clave para comprender la evolución y la historia natural de la EPOC.
En la primera parte de este artículo se realiza una puesta al día del presente del tiotropio, para lo cual se revisan los estudios más importantes que sustentan las evidencias actuales sobre los efectos positivos que este broncodilatador proporciona en los parámetros centrados en el paciente. En la segunda parte se analizan el diseño, la situación actual y las perspectivas futuras que pueden abrirse cuando se conozcan los resultados del ambicioso estudio UPLIFT (Understanding Potential Long-term Impacts on Function with Tiotropium), cuyo objetivo principal ha sido evaluar el efecto del tiotropio en la progresión de la enfermedad en el marco de un ensayo de 4 años de duración en el que han participado casi 6.000 pacientes con EPOC (tabla II).
Tiotropio: evidencias actuales
Desde antes de la comercialización del tiotropio, hace ya 5 años, ha aparecido un importante número de estudios que, cumpliendo con los postulados de la evidencia científica, avalan su eficacia en el tratamiento de la EPOC21. Estos estudios muestran una serie de aspectos beneficiosos del tiotropio, como su efecto en la función pulmonar y la disnea, las exacerbaciones, el ejercicio y la calidad de vida (tabla I y fig. 1).
Tiotropio y función pulmonar
El objetivo principal de los primeros estudios fue la evolución del FEV1 y de la capacidad vital forzada (FVC) durante un año de seguimiento, comparando el tiotropio con placebo y con ipratropio. En una segunda fase se diseñaron estudios para conocer su impacto en la hiperinsuflación pulmonar, tanto en condiciones estáticas como dinámicas (durante el ejercicio).
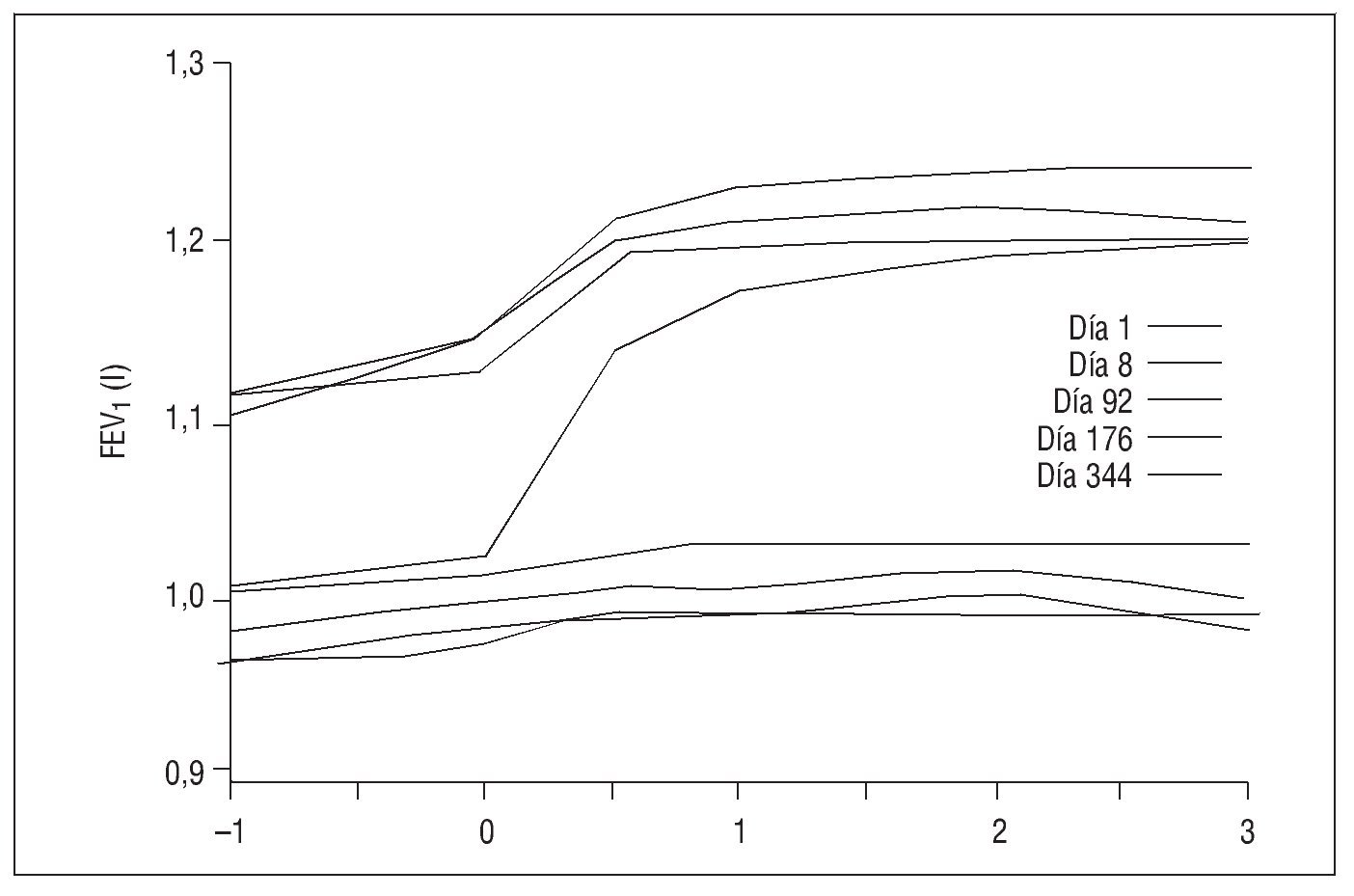
Volumen espiratorio forzado en el primer segundo y capacidad vital forzada. Casaburi et al8, en un estudio de un año de duración, evaluaron el efecto broncodilatador del tiotropio comparado con placebo. El beneficio del tiotropio en el FEV1, tanto valle como pico, llegó hasta 220 ml, y el de la FVC hasta los 510 ml. Los efectos favorables, evidentes ya desde el inicio del estudio, se mantuvieron durante el período de tratamiento (12 meses) y no se observaron signos de taquifilaxia (fig. 2). Los estudios que han comparado el tiotropio con otros broncodilatadores ofrecen una visión de la efectividad broncodilatadora relativa de este fármaco y de su valor añadido. Van Noord et al22 compararon, en 288 pacientes con EPOC, la administración de una única dosis diaria de 18 μg de tiotropio frente a 40 μg de ipratropio cada 6 h. En este estudio el tiotropio produjo un incremento del pico de flujo espiratorio tanto matutino como nocturno, del FEV1 y de la FVC, así como una menor necesidad de salbutamol de rescate, todo ello con una tasa de efectos secundarios similar. Posteriormente Vincken et al9, en un estudio de un año de duración, demostraron la superioridad del tiotropio tanto en la mejoría del FEV1 como de la FVC, que además se mantuvieron por encima de los valores basales (el 9, el 6 y el 11,6%, respectivamente), lo que no ocurrió con el ipratropio. La mejoría de la FVC puede indicar que, además del efecto broncodilatador de los anticolinérgicos en las vías respiratorias centrales, éstos podrían contribuir a la disminución del efecto de atrapamiento aéreo secundario al cierre tardío de las vías respiratorias de pequeño calibre10. Dado que el efecto farmacológico de ambos medicamentos es similar, las razones de esta superioridad posiblemente haya que buscarlas en la vida media más prolongada del tiotropio y en la facilidad para cumplir con el tratamiento, de modo que los pacientes consiguen más fácilmente la dosis adecuada. Donohue et al10 demostraron que el tiotropio consiguió una mejoría del FEV1 estadísticamente significativa frente al salmeterol en un estudio de 6 meses. Años después, Brusasco23 analizó la eficacia y tolerabilidad del tiotropio comparado con salmeterol inhalado, y observó que ambos fueron superiores al placebo y que el efecto del tiotropio fue significativamente mayor que el del salmeterol. La asociación de ambos fármacos también ha demostrado un efecto broncodilatador superior al de cada uno por separado cuando se administran junto a fluticasona inhalada24. El mismo efecto broncodilatador superior se ha demostrado frente al formoterol25. En 71 pacientes con EPOC, el tiotropio produjo una mejoría del FEV1 significativamente mayor que el formoterol en la media diurna y sin diferencias en la media nocturna. Con la asociación de ambos fármacos administrados una y 2 veces al día, respectivamente, se conseguían los mejores efectos, que eran incluso superiores al efecto de cada uno administrado por separado. Con posterioridad el mismo grupo de Van Noord et al14, en 95 pacientes con EPOC moderada-grave en fase estable, compararon la monoterapia con tiotropio frente a la asociación del tiotropio y formoterol (1-2 veces al día), y encontraron mayor beneficio con dicha asociación no sólo por lo que se refería al FEV1, sino también a la FVC y la capacidad inspiratoria, al tiempo que disminuía la necesidad del uso de broncodilatadores de rescate en estos pacientes. Estos hallazgos ya se habían descrito en estudios previos de Cazolla et al26,27.
Fig. 2. Cambios en el volumen espiratorio forzado en el primer segundo (FEV1) valle y pico en los grupos de tiotropio y placebo del estudio de Casaburi et al8, de un año de duración.
Volúmenes pulmonares estáticos y dinámicos. La mejoría de la disnea y de la tolerancia al esfuerzo no siempre se correlaciona con cambios de la misma magnitud en el FEV1. La mejoría en la hiperinsuflación y en el atrapamiento aéreo tanto en situación estática como dinámica (volúmenes operativos) parece ser uno de los mecanismos más importantes que se encuentran detrás de estos cambios favorables28. En esta línea, se han realizado 4 estudios (Celli et al15, O'Donnell et al13, Maltais et al17 y Verkindre et al16) que muestran mejorías estadísticamente significativas de los volúmenes pulmonares del grupo tratado con tiotropio frente al grupo placebo. Celli et al15 demostraron que en pacientes con EPOC estable e hiperinsuflación, tras 4 semanas de tratamiento con tiotropio, la capacidad inspiratoria aumentó significativamente frente a placebo (entre 220 y 350 ml). O'Donnell et al13 compararon el tiotropio con placebo en 187 pacientes con EPOC moderada-grave e hiperinsuflación -capacidad residual funcional (FRC) > 120% del valor teórico- evaluando múltiples variables: tolerancia al ejercicio, hiperinsuflación tanto estática como dinámica e intensidad de la disnea con el ejercicio. Se observó una reducción significativa de la FRC tanto en reposo como en ejercicio, además de una mejoría de la tolerancia al ejercicio, que persistió tras las 6 semanas de tratamiento. Esto se traduce en una mejora de la disnea, de la tolerancia al ejercicio y del estado de salud29. Así, al final del estudio (día 42), los pacientes con EPOC que recibieron tiotropio podían hacer ejercicio durante una media de 10,5 min, frente a los 8 min del grupo placebo. Comparados con los valores basales, la FRC disminuyó y la capacidad inspiratoria y el volumen de reserva inspiratorio aumentaron, lo que demuestra que el tiotropio disminuyó los volúmenes pulmonares operativos y alargó el tiempo de esfuerzo. Los estudios de Maltais et al17 con medidas en reposo y tras ejercicio (diseño muy similar al de O'Donnell et al13) y de Verkindre et al16 arrojaron resultados parecidos en capacidad inspiratoria y FRC y en capacidad inspiratoria, respectivamente. Por último, en los 2 ensayos que valoraron la mejoría del volumen residual, el tiotropio proporcionó una mejoría estadísticamente significativa respecto a placebo13,15.
El análisis global de todos estos datos indica que el tiotropio disminuyó la hiperinsuflación en reposo y durante el esfuerzo en pacientes con EPOC, lo que hace posible que aumente la duración del esfuerzo. Esta mejoría permite a los pacientes con EPOC aumentar sus actividades diarias y así revertir el ciclo de inactividad crónica y discapacidad física.
Tiotropio y exacerbaciones
Las exacerbaciones agudas de la EPOC (EA-EPOC) son un factor negativo en la morbilidad y mortalidad de la enfermedad6, además de suponer un coste económico importante, ya que la mayor carga económica que ocasionan los pacientes con EPOC deriva del ingreso hospitalario por EA-EPOC. Por lo tanto, las intervenciones que disminuyan la tasa de exacerbaciones o su gravedad son esenciales en el manejo global de la enfermedad. En los primeros trabajos publicados, como los de Brusasco et al11 y Tashkin y Kesten12, se encontró una reducción del número de EA-EPOC por paciente y año de hasta un 28% en los que utilizaban tiotropio, junto con un aumento significativo del tiempo hasta la primera EA-EPOC, en comparación con placebo, aunque la diferencia entre el tiotropio y el salmeterol no fue significativa. En los estudios del tiotropio de un año y de 6 meses de duración8,9, el porcentaje de pacientes con al menos una exacerbación fue una variable de valoración secundaria. En estos estudios el número de pacientes que experimentaron una o varias exacerbaciones fue menor en el grupo tratado con tiotropio que en los grupos tratados con placebo o ipratropio. Las diferencias fueron estadísticamente significativas entre los grupos tratados con placebo y con tiotropio (diferencia del 14%), y entre los grupos tratados con ipratropio y con tiotropio (diferencia del 24%), en los ensayos de un año. Estos resultados siguen confirmándose en estudios que tienen como objetivo principal de valoración las exacerbaciones, como el de Niewoehner et al18 (Veteran's Health Administration), de 6 meses de duración, en el que se permitió a los pacientes utilizar todos los medicamentos con acción respiratoria, excepto los anti-colinérgicos inhalados. En este estudio el tiotropio redujo de forma significativa el porcentaje de pacientes que experimentaron una o varias exacerbaciones al compararlo con placebo (un 27,9 frente aun 32,3%, respectivamente; p = 0,037). Los pacientes tratados con tiotropio presentaron un número significativamente menor (-19%) de exacerbaciones que los pacientes tratados con placebo. Menos pacientes tratados con tiotropio fueron hospitalizados por exacerbaciones de la EPOC (un 7,0 frente a un 9,5%, respectivamente; p = 0,056). En el grupo de tiotropio se retrasó la aparición de la primera EA y se redujo el uso de recursos sanitarios (hospitalización, visitas médicas no programadas y días de antibióticos).
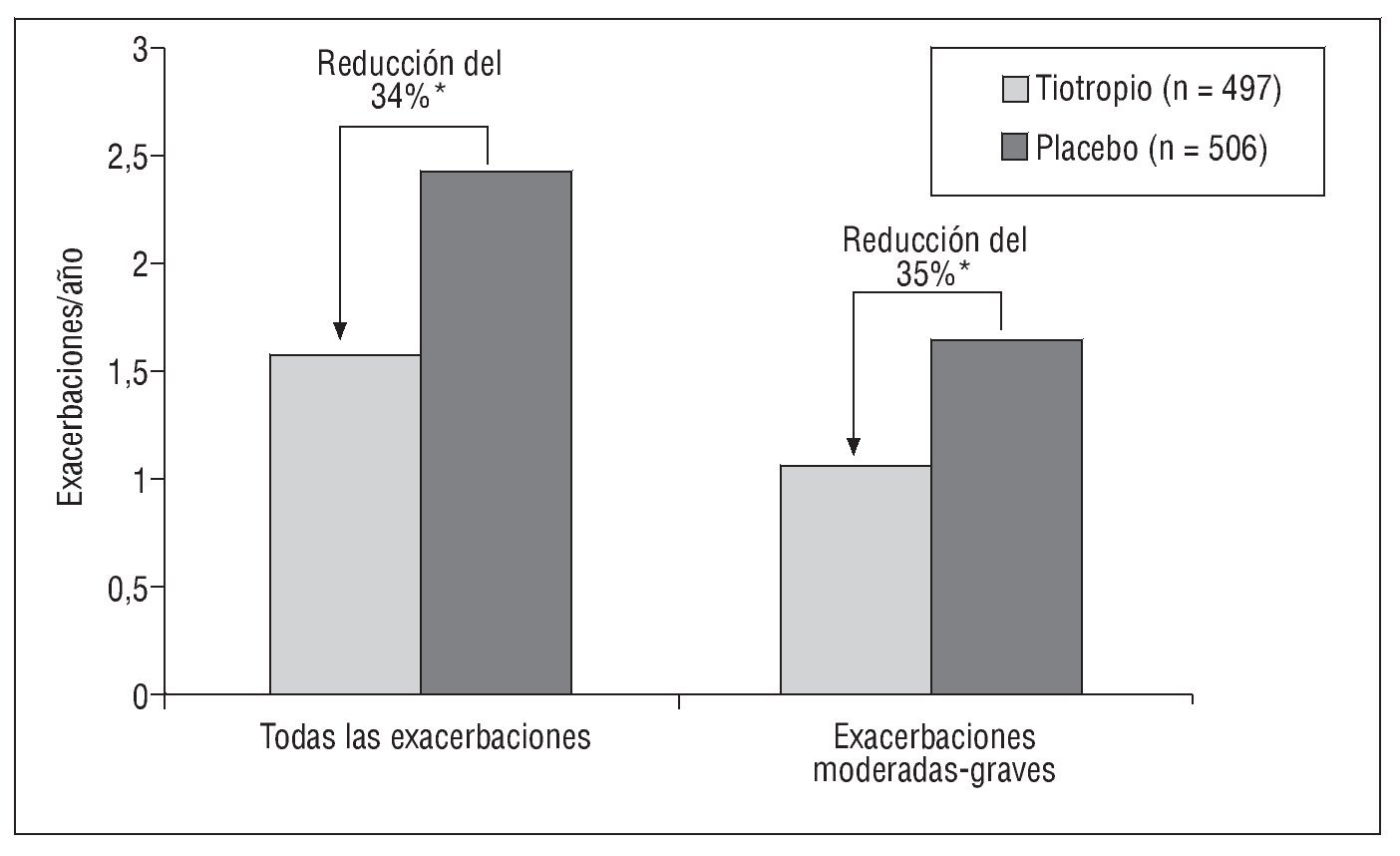
Por último, el estudio MISTRAL19 (Mesure de l'Influence de SPIRIVA®sur les Troubles Respiratoires Aigus à Long terme), en el que se recogieron también las exacerbaciones leves, muestra los resultados de un amplio estudio aleatorizado con tiotropio controlado con placebo, de un año de duración. En este trabajo el empleo del tiotropio producía un retraso de 100 días hasta la primera EA-EPOC, una reducción del 17% en el grupo de pacientes con más de una EA-EPOC, una disminución del 35% en el número de exacerbaciones que precisaban tratamiento con esteroides y/o antibióticos sistémicos (exacerbaciones moderadas) o que precisaban hospitalización (exacerbaciones graves). Comparados con los pacientes tratados con placebo, los tratados con tiotropio experimentaron un 34% menos de exacerbaciones de cualquier grado de gravedad, así como una reducción significativa de los días de exacerbación (fig. 3). Además, el uso de este fármaco se asoció a un menor empleo de medicación respiratoria concomitante (antibióticos y esteroides orales) y también disminuyó el número de visitas médicas no programadas, lo que implicaría un importante ahorro en los recursos sanitarios.
Fig. 3. Estudio MISTRAL19: disminución del número de exacerbaciones por efecto del tratamiento con tiotropio. *p < 0,01.
En un controvertido metaanálisis de Salpeter et al30, que revisaron un total de 22 ensayos con un total de 15.276 participantes, el uso de anticolinérgicos inhalados en pacientes con EPOC reducía significativamente las EA-EPOC graves (riesgo relativo = 0,67; intervalo de confianza del 95%, 0,53-0,86) y las muertes de causa respiratoria (riesgo relativo = 0,27; intervalo de confianza del 95%, 0,09-0,81), en comparación con placebo y agonistas β2.
Tiotropio, disnea y calidad de vida relacionada con la salud
La EPOC se considera en la actualidad una enfermedad sistémica, de forma que la pérdida de tolerancia al ejercicio y la disnea, junto a otros síntomas generales, determinan el estado de salud y la calidad de vida de los pacientes. Los trabajos publicados8,17 han demostrado que el tiotropio se asocia con mejoras significativas y clínicamente relevantes de diversos parámetros clínicos, como la disnea valorada mediante distintos cuestionarios -índice transicional de disnea (TDI), escala de Borg-, la tolerancia al ejercicio y el estado de salud. Tashkin y Kesten12 demostraron mejoras significativas en la disnea y el estado de salud incluso en pacientes con escasa reversibilidad inicial con el tiotropio, definida como un incremento del FEV1 menor del 12% o de 200 ml con respecto al valor basal tras la primera dosis de tiotropio. Vincken et al9 encuentran que el tiotropio mejora significativamente la puntuación final del TDI y los dominios físicos del cuestionario genérico de salud SF-36 en comparación con el ipratropio, aunque esta mejoría no alcanzó el intervalo de relevancia clínica. En el estudio de Donohue et al10, donde se analizaron parámetros de calidad de vida y estado de salud, el tiotropio fue superior al salmeterol en la mejoría de la disnea medida por el TDI. Sin embargo, Brusasco et al11 encontraron que el tiotropio y el salmeterol producían mejorías significativas en el TDI comparados con placebo, pero muy similares si se comparaban los 2 fármacos entre sí.
Tiotropio y ejercicio (actividad física)
Aunque el hecho fisiopatológico determinante de la EPOC es la limitación del flujo espiratorio, el FEV1 no siempre está relacionado con la intensidad de la disnea y la tolerancia al ejercicio de los pacientes que la presentan31. El atrapamiento aéreo resultante del retraso en el vaciamiento del pulmón y el aumento del volumen pulmonar al final de la espiración se agravan con el ejercicio e impiden satisfacer las demandas ventilatorias incrementadas. La intensidad de la disnea aumenta y sólo puede alcanzarse un posterior incremento de la ventilación por medio de un incremento de la frecuencia respiratoria. Esto ocasiona un círculo vicioso al provocar mayor hiperinsuflación, que obliga a la reducción de la actividad física, que a su vez se traduce en discapacidad muscular y empeoramiento de la enfermedad7,32. Uno de los beneficios más importantes que cabe esperar de los broncodilatadores en la EPOC parte de su capacidad para disminuir la hiperinsuflación reduciendo la disnea durante el ejercicio y mejorando la tolerancia a éste. La mejora en la actividad física está avalada por los resultados de 2 ensayos clínicos aleatorizados, a doble ciego y controlados con placebo, de 42 días de duración, realizados en pacientes con EPOC e hiperinsuflación (FRC ≥ 120% de los valores teóricos de referencia), en quienes se utilizó un cicloergómetro con carga de trabajo constante (ésta se fijó en el 75% de la carga de trabajo determinada en una prueba de cicloergometría incremental anterior). En ambos estudios se demuestra que las mejorías del flujo de aire, atrapamiento aéreo e hiperinsuflación logradas con el tiotropio se traducen en una menor disnea y en un aumento de la resistencia al esfuerzo, con una mayor duración de éste13,17. En el estudio de O'Donnell et al13, al final del período de seguimiento la diferencia media en la duración del esfuerzo fue de 105 s -diferencia del 21% (p < 0,01) respecto a placebo-. En el trabajo de Maltais et al17, los pacientes tratados con tiotropio presentaron una mejoría progresiva de la duración del esfuerzo durante el tratamiento, de forma que al final del estudio la diferencia media en la duración del esfuerzo fue de 236 s -diferencia del 42% (p < 0,0001) respecto a placebo.
En otro estudio aleatorizado, doble ciego y controlado con placebo, de 12 semanas de duración, se evaluó el efecto del tiotropio en la prueba de la marcha de carga progresiva (shuttle walking test). La distancia recorrida por el grupo tratado con placebo el día 1 no experimentó cambios importantes respecto a los valores basales durante el seguimiento, mientras que la mejoría media en la distancia recorrida por el grupo tratado con tiotropio fue de 33 m (día 42) y 36 m (día 84) en comparación con placebo (p < 0,05).
Avanzando en los beneficios que el tiotropio proporciona en la tolerancia al ejercicio, Casaburi et al20 diseñaron un estudio para conocer el efecto del tiotropio sumado a un programa de rehabilitación. Los pacientes recibieron el fármaco en estudio o placebo durante 4 semanas, sin instrucciones sobre la realización de ejercicio, seguidas de 8 semanas de rehabilitación pulmonar formal, y luego otras 12 semanas de seguimiento. La variable de valoración principal fue la duración de la prueba de esfuerzo en tapiz rodante con carga de trabajo constante. Durante todo el período de estudio el grupo tratado con tiotropio obtuvo resultados superiores al grupo tratado con placebo. La diferencia media en la duración del esfuerzo después de 13 semanas (fin de la rehabilitación pulmonar) fue de 5,35 min (un 32% más que con placebo; p < 0,05). A las 25 semanas (12 semanas después de interrumpir la rehabilitación pulmonar) la mejoría de la duración del esfuerzo se mantenía en el grupo tratado con tiotropio. En resumen, los resultados favorables de diferentes estudios que, utilizando métodos distintos, han valorado el impacto del tiotropio en la duración del esfuerzo demuestran la reproducibilidad del efecto del tiotropio en la resistencia y la tolerancia al esfuerzo, y que la disminución de la hiperinsuflación dinámica parece ser el mecanismo fisiopatológico fundamental que explica estos cambios33.
Mirando al futuro próximo: el estudio UPLIFT
Cuando aparezca publicado este artículo, faltarán muy pocas semanas para conocer los primeros resultados de este importante estudio (Congreso de la European Respiratory Society, que se celebrará en Berlín en octubre de 2008). El último paciente finalizó su período de tratamiento hace unos meses y en la actualidad estamos inmersos en la fase de análisis de datos y de elaboración de los resultados.
Fundamentos
La tasa anual de reducción del FEV1 se ha utilizado como medida indirecta para el estudio de la evolución natural de la EPOC2,3,5. En todos los individuos se produce una pérdida natural del FEV1 que empieza después de que este parámetro alcance un máximo, lo que ocurre en torno a los 25 años de edad. El ritmo normal de esta pérdida es entre 20 y 50 ml al año. Los pacientes que presentan una mayor susceptibilidad al humo del cigarrillo y que desarrollan EPOC pueden experimentar una pérdida anual del FEV1 que oscila entre 40 y 80 ml al año, aunque hay diferencias significativas entre diversos estudios sobre la rapidez de este descenso34. Si bien el curso clínico y la tasa de disminución de la función pulmonar pueden presentar cierta variación, existe una correlación entre el FEV1 y diversos parámetros de evolución clínica, como la disnea, la calidad de vida relacionada con la salud, las exacerbaciones graves y la mortalidad. La ventaja de estudiar el FEV1 de manera seriada a lo largo del tiempo (estudios longitudinales) es la objetividad documentada, la reproducibilidad y la validez de la medida. Los inconvenientes derivan de que la correlación entre los valores del FEV1 y parámetros de evolución clínica como disnea, estado de salud y capacidad de ejercicio, aunque existente, es en muchos casos débil.
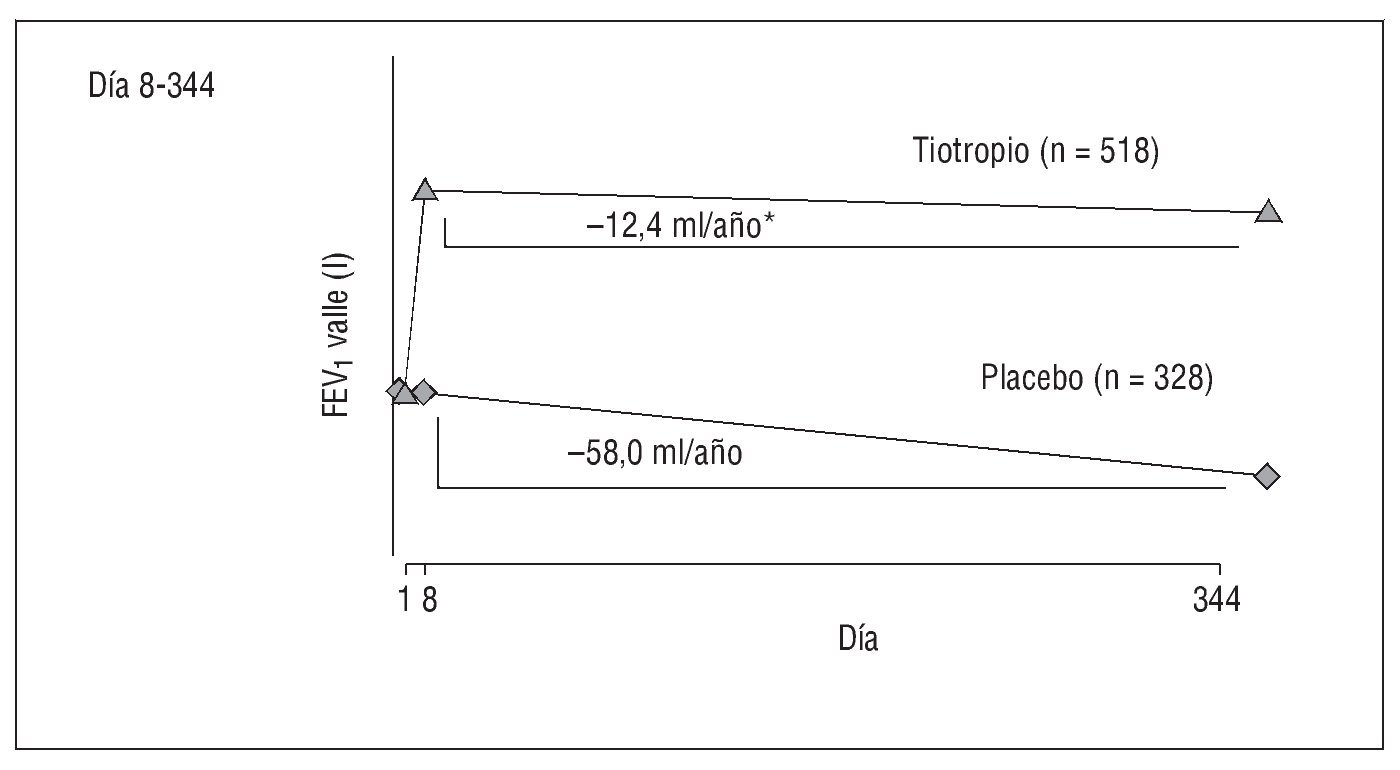
Como ya se ha descrito en los apartados anteriores, los estudios realizados con tiotropio de 6 meses y de un año de duración han puesto de manifiesto que este fármaco puede mejorar la función pulmonar y el estado de salud, así como reducir la dificultad respiratoria y el número y la gravedad de las exacerbaciones8,9. En un análisis post hoc realizado por Anzueto et al35 de los estudios controlados de un año de duración, la reducción anual del FEV1 matutino antes de la administración del tiotropio fue considerablemente inferior a la disminución observada con placebo (-0,01 frente a -0,04 l desde el día 8 al día 344; p < 0,05) (fig. 4). Otros estudios han mostrado que el tiotropio reduce la hiperinsuflación y la disnea provocada por el ejercicio, al tiempo que prolonga la capacidad de ejercicio36.
Fig. 4. Análisis post hoc35 de la variación media del volumen espiratorio forzado en el primer segundo valle (ml/año) en los grupos de tiotropio y placebo, los días 8 a 344. *p < 0,005, tiotropio frente a placebo (pendientes de regresión media).
Todas estas observaciones han conducido a plantear nuevas hipótesis respecto a la evolución clínica que se produce cuando se mantiene el tratamiento más de un año, y abren la posibilidad de que el tiotropio ejerza una influencia a largo plazo en la tasa anual de pérdida de la función pulmonar y modifique así la evolución natural de la enfermedad. Para aclarar estas hipótesis se diseñó un ambicioso estudio de 4 años de duración denominado UPLIFT, que intenta evaluar la influencia del tiotropio en la evolución natural de la EPOC.
Objetivo (tabla II)
El objetivo principal del estudio UPLIFT consiste en determinar si el tratamiento con tiotropio (18 μg) una vez al día, administrado con el dispositivo HandiHaler, reduce la disminución del FEV1 a lo largo del tiempo en pacientes con EPOC. Las variables de valoración han sido: a) la disminución anual del FEV1 matinal previo a la administración del fármaco (FEV1 valle) a partir del día 30 (fase de equilibrio estable) y hasta la finalización del tratamiento doble ciego, y b) la tasa anual de reducción del FEV1 tras la administración del broncodilatador, también desde el día 30 hasta el final. Con el objeto de asegurar una broncodilatación máxima, se determinan los valores del FEV1 y de la FVC después de la administración secuencial de salbutamol y de bromuro de ipratropio, que elimina todo el tono del músculo liso de las vías aéreas. Por lo tanto, la velocidad de deterioro se determina 24 h después de la dosis anterior del fármaco en estudio y tras la broncodilatación máxima; los cambios en la última presumiblemente reflejan sólo cambios estructurales en las vías aéreas.
Los objetivos secundarios del estudio UPLIFT incluyen la evaluación de la tasa anual media de reducción, observada antes y después de la administración del broncodilatador, del FEV1, la FVC y la capacidad vital lenta a partir del día 1 y hasta completar el ensayo, y la tasa anual media de reducción de los valores de la FVC y la capacidad vital lenta previos y posteriores al broncodilatador a partir del día 30 y hasta completar el tratamiento doble ciego. Otros objetivos del estudio han sido la medida de la evolución del estado de salud (mediante el St. George's Respiratory Questionnaire), las exacerbaciones y hospitalizaciones a consecuencia de éstas, y la mortalidad tanto de origen respiratorio como por todas las causas37.
Diseño
UPLIFT es un ensayo clínico de 4 años de duración, multicéntrico (475 centros participantes), multinacional (37 países de Europa, Asia, África, Australia y América), de grupos paralelos, controlado con placebo, aleatorizado (se incluyó a 8.019 pacientes, de los que finalmente se aleatorizó a 5.993) y doble ciego. El primer paciente se aleatorizó en junio de 2003; en marzo de 2004 se completó el reclutamiento, y el último paciente finalizó el estudio en abril de 2008. Los pacientes se distribuyeron al azar en una relación 1:1 para recibir tiotropio o placebo más su tratamiento habitual. Se les permitió utilizar agonistas β2 (de acción corta y prolongada), teofilinas y esteroides inhalados. Los otros fármacos anticolinérgicos fueron el único tratamiento respiratorio concomitante prohibido durante el ensayo. Este hecho hace que sea un estudio que refleja el tipo de pacientes vistos en la práctica clínica habitual, lo que por un lado dará un mayor valor a sus resultados, aunque por otro presenta el inconveniente de que la formación de demasiados grupos puede hacer que se pierda potencia estadística.
En un estudio de estas características, asegurar la correcta calidad de las espirometrías ha sido básico. Las exploraciones funcionales se han realizado en todos los casos con el mismo modelo de espirómetro, han estado centralizadas y se han seguido unos controles estrictos, como lo prueba el hecho de que el 89,6% se han considerado espirometrías de buena calidad y menos del 1% no han cumplido los mínimos exigidos38.
Criterios de inclusión
En el estudio UPLIFT se ha incluido a varones y mujeres con historia de consumo de tabaco superior a 10 paquetes al año y con un FEV1 tras la administración de broncodilatador, en las visitas 1 y 2, igual o inferior al 70% del valor teórico de referencia (FEV1/FVC% < 70%). Los pacientes debían referir estabilidad en la medicación respiratoria en al menos las 6 semanas previas a su inclusión. Es importante señalar que el criterio de reversibilidad no fue excluyente. De hecho, más del 65% de los pacientes presentaron reversibilidad significativa después de la administración de dosis que pueden considerarse óptimas de salbutamol e ipratropio39.
Características de los pacientes
De los datos ya publicados y de las comunicaciones presentadas en congresos sabemos que la edad media de los pacientes que han participado en el estudio es de 64,5 años, que el 75% son varones y que el FEV1 medio es de 1,1 l (39,3%). El grado de tabaquismo acumulado por estos pacientes es de 49 paquetes/año y el 31% era fumador activo. El primer síntoma de consulta médica por EPOC fue la disnea (70%), seguido de la tos (21%). Un estudio de los patrones de prescripción mostró que, a pesar de las recomendaciones de las guías clínicas40, la utilización de broncodilatadores de acción prolongada sigue siendo muy baja (más del 25% de los pacientes con estadios avanzados no los tienen prescritos) y que un porcentaje importante de pacientes que se encuentran en estadios más leves reciben tratamiento con esteroides inhalados41 (un 45% en estadio II). Estos datos se repiten de forma constante en la mayoría de los estudios publicados que analizan el grado de adecuación del tratamiento de la EPOC a las normativas42 y deben ser objeto de análisis y servir para instaurar medidas correctoras.
Perspectivas
Si del estudio UPLIFT, como es de desear y es previsible por los resultados de estudios preliminares, se derivaran resultados positivos, sería la primera vez que una medida farmacológica es capaz de modificar la tasa de caída del FEV1, lo que implicaría que la enfermedad subyacente está siendo verdaderamente modificada. Los datos positivos del UPLIFT apoyarían que, junto al abandono del hábito tabáquico, se debería iniciar en cualquier estadio de la EPOC tratamiento con tiotropio, ya que ambas medidas habrían demostrado ser capaces de modificar la evolución natural de la enfermedad. La probabilidad de demostrar el mantenimiento de la broncodilatación, así como el mantenimiento en el tiempo de la disminución del número y de la gravedad de las exacerbaciones encontrada en los estudios a un año, abre la puerta a un auténtico cambio en los datos conocidos hasta ahora sobre la evolución natural de la EPOC. Asimismo, es posible que las modificaciones en el FEV1 y en las exacerbaciones puedan conducir a mejorías mantenidas a largo plazo en la calidad de vida relacionada con la salud y posiblemente en la mortalidad por causa respiratoria. Por último, la exposición de miles de pacientes a tiotropio, en el seno de un ensayo controlado, conllevará un estudio en profundidad sobre la seguridad de este fármaco anticolinérgico.
En resumen, el análisis conjunto de distintos estudios que han comparado el tiotropio con placebo revelan que su administración no sólo se asocia a una mejoría del FEV1, sino que además ofrece beneficios adicionales en los principales parámetros de eficacia clínica centrados en el paciente, como la disnea, la capacidad de ejercicio, la presencia de exacerbaciones y la calidad de vida. Estos resultados uniformes, junto con la acumulación de otros datos procedentes de estudios aislados, llevaron a plantear la puesta en marcha de un ambicioso estudio prospectivo: el UPLIFT. Este estudio, ya finalizado y con los resultados a punto de ser conocidos, se ha planteado el reto de comprender el efecto potencial que el tiotropio ejerce a largo plazo en la función pulmonar. Sus resultados favorables permitirán avanzar en la modificación de la historia natural de la EPOC.
Declaración de conflicto de intereses
Los autores han declarado no tener ningún conflicto de intereses.
Correspondencia:
Dr. J.M. Rodríguez González-Moro.
Servicio de Neumología. Hospital General Universitario Gregorio Marañón. Dr. Esquerdo, 46. 28007 Madrid. España.
Correo electrónico: jrodriguezgo.hgugm@salud.madrid.org