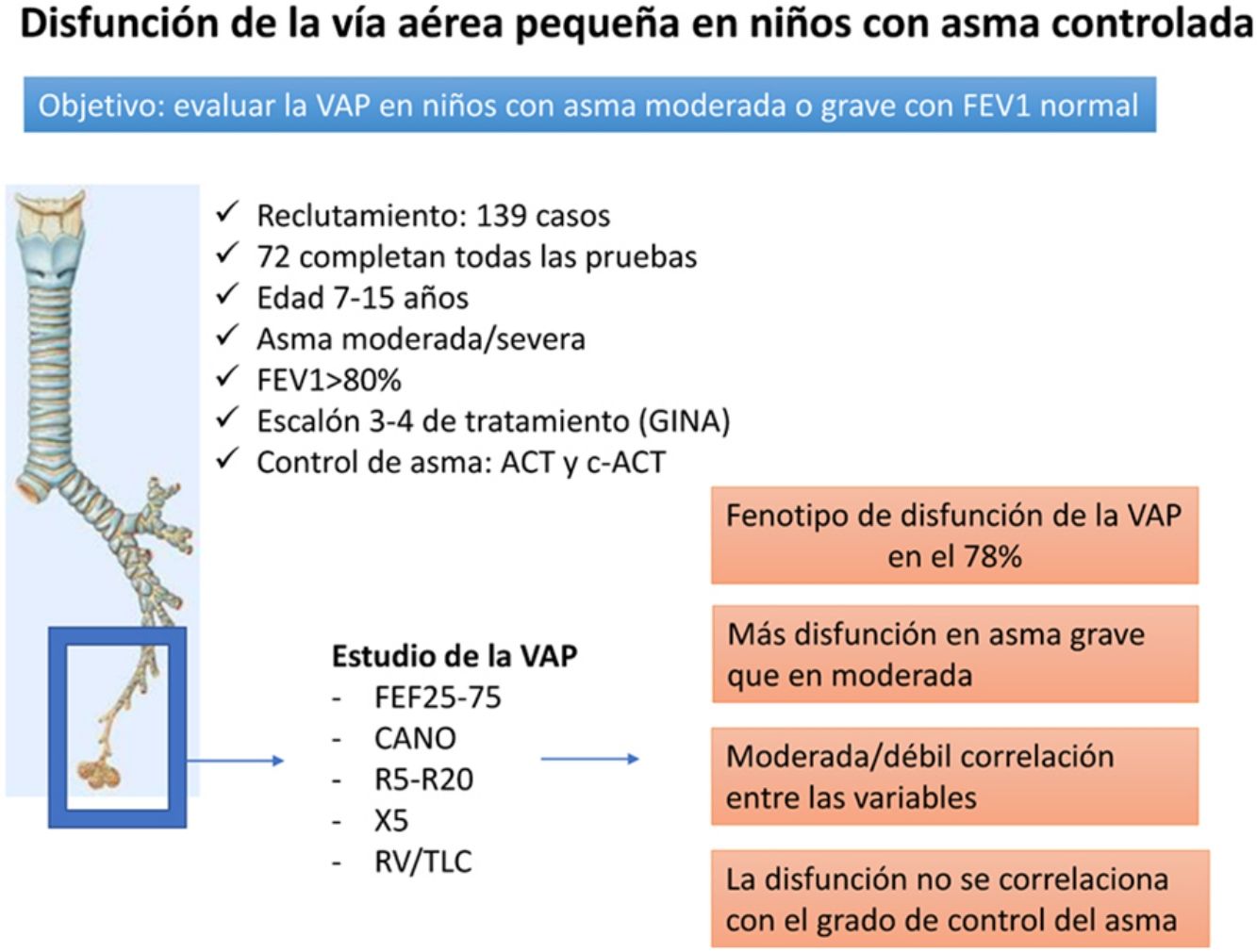
El asma se caracteriza por una inflamación crónica de las vías respiratorias centrales y distales. El objetivo de este estudio ha sido evaluar la vía aérea pequeña (VAP) en niños con asma moderada y/o grave con FEV1 normal.
MétodosEstudio abierto, prospectivo, observacional y transversal con inclusión consecutiva de casos con asma moderada o grave, bajo tratamiento clínico habitual con FEV1 basal normal. Se ha determinado la FEno a flujos múltiples (CAno), resistencias y reactancia oscilatorias (R5-R20, X5), espirometría forzada (FEV1, FEF25-75), pletismografía corporal total (RV/TLC) y prueba de broncodilatación. La afectación de la VAP se definió por: CAno>4,5ppb, R5-R20>0,147kPa/L/s, X5<−0,18kPa/L, FEF25-75<−1,65 z-score, RV/TLC>33%. El mal control de asma se definió por≤19 puntos en el cuestionario ACT o≤20 en c-ACT.
ResultadosCohorte de 100 casos, 76 con asma moderada y 24 con asma grave, 71 niños clasificados como mal controlados y 29 bien controlados. El 77,78% del grupo con todas las determinaciones correctas (n=72) mostró≥1 parámetro alterado de VAP y el 48,61%≥2 parámetros. No hubo diferencias entre los casos bien y mal controlados.
ConclusionesLos niños con asma moderada y grave, con el FEV1 preservado, muestran un fenotipo de VAP disfuncionante. En nuestra muestra, la evaluación de la VAP mediante las técnicas descritas, no aporta información sobre el control habitual de la enfermedad.
Asthma is characterized by chronic inflammation of the central and distal airways. The aim of this study was to assess the small airway (SA) of children with moderate-severe asthma with normal FEV1.
MethodsThis was an open-label, prospective, observational, cross-sectional study with consecutive inclusion of patients with moderate-severe asthma, receiving standard clinical treatment, with normal baseline FEV1. We determined multiflow FEno (CAno), oscillatory resistance and reactance (R5-R20, X5), forced spirometry (FEV1, FEF25-75), total body plethysmography (RV/TLC) and bronchodilation test. SA involvement was defined as: CAno>4.5 ppb, R5-R20>0.147kPa/L/s, X5<−0.18kPa/L, FEF25-75<−1.65 z-score, RV/TLC>33%. Poor asthma control was defined as ≤ 19 points on the ACT questionnaire or ≤ 20 on the c-ACT.
ResultsIn a cohort of 100 cases, 76 had moderate asthma and 24 had severe asthma; 71 children were classified as poorly controlled and 29 were well-controlled. In total, 77.78% of the group with all the correct determinations (n=72) showed ≥ 1 altered SA parameter and 48.61% ≥ 2 parameters. There were no differences between well-controlled or poorly controlled cases.
ConclusionsChildren with moderate-severe asthma, with normal FEV1, show a phenotype of dysfunctional SA. In our series, the evaluation of SA using the techniques described above did not provide information on disease control.
El asma es una enfermedad caracterizada por una inflamación crónica de las vías respiratorias que afecta a todo el tracto respiratorio, desde las vías aéreas centrales hasta las más periféricas1. Algunos investigadores señalan que la inflamación y la remodelación de la vía aérea pequeña (VAP) está presente en humanos y en modelos experimentales2 y que esta afectación de la VAP está asociada a un aumento de los síntomas de asma y a un peor control de la enfermedad. En la infancia, el flujo espiratorio máximo 25-75% se considera un marcador indirecto de la VAP3. El aumento de las resistencias oscilatorias y la disminución de la reactancia determinada por oscilometría se asocian con un peor estado de salud y con mal control de la enfermedad en niños4 y en adultos5. Otros trabajos indican que la afectación de los mesoflujos también se asocia a peor control de la enfermedad6,7. El atrapamiento aéreo, determinado de manera indirecta mediante la pletismografía corporal, se ha relacionado con exacerbaciones más graves8, más hospitalizaciones por asma9, incluso con peor calidad de vida relacionada con la salud10. Además, otros autores han comunicado que una mayor concentración alveolar de óxido nítrico (CAno) se asocia con presencia de síntomas y peor control del asma en la infancia11. La disfunción de la VAP es evidente en pacientes con asma grave12,13.
El objetivo principal de este estudio ha sido evaluar la VAP en niños con asma en la práctica clínica habitual con volumen espiratorio forzado en el primer segundo (FEV1) normal, para conocer su posible utilidad en el manejo del asma.
MétodosEl estudio fue aprobado por el Comité de Ética y de Investigación del centro hospitalario. En todos los casos hubo consentimiento informado de los padres (y del niño en el caso de mayores de 11 años) y permiso para la explotación de los datos, en cumplimiento de las normas legales vigentes.
Estudio prospectivo, observacional y transversal con pacientes entre 7 y 15 años, diagnosticados de asma y clasificados como moderada o grave según GINA 20161, situados en el escalón 3 o superior de tratamiento (glucocorticoides inhalados asociados a agonistas-β2-adrenérgicos de acción prolongada) durante al menos los 4 últimos meses, en el ámbito de las consultas externas de Neumología Infantil de un hospital terciario. El periodo de reclutamiento fue de 1 de enero a 30 de junio del 2015.
Fueron excluidos los sujetos que presentaban un FEV1 inferior al 80% del valor teórico, mala técnica inhalatoria del tratamiento de base, pobre adherencia al mismo (<80% de la dosis prescritas)14, los que habían presentado una crisis asmática en los 7 últimos días, los tratados con glucocorticoides orales en los últimos 7 días, los que presentaban una infección respiratoria aguda y/o fiebre y los niños no colaboradores para las pruebas de función pulmonar.
Al no disponer de datos de prevalencia de disfunción de la VAP en niños con asma moderada o grave, se realizó un estudio piloto con los 30 primeros casos (23 asma moderada y 7 grave), para estimar el tamaño muestral. No se observaron diferencias entre ambos grupos. No hubo asociación ni entre las variables de medida resistencias entre 5 y 20 hercios (R5-R20), reactancia a 5 hercios (X5), CAno, relación entre volumen residual y capacidad pulmonar total (RV/TLC) y flujo espiratorio forzado entre el 25 y 75% de la capacidad vital forzada (FEF25-75). Con los puntos de corte utilizados, los parámetros de VAP alterados fueron los siguientes: CAno (n=4), R5-R20 (n=13), X5 (n=12), FEF25-75 (n=3) y RV/TLC (n=6). Se prosiguió el reclutamiento para disponer de un tamaño muestral teórico suficiente (n=100) para cumplir el objetivo del estudio.
En todos los casos se determinó la fracción exhalada de óxido nítrico a respiración única y a flujos múltiples (30, 150 y 250ml/s), utilizando el analizador de quimioluminiscencia estacionario Eco Medics CLD 88 SP® con adaptadores de flujo Denox 88, con el fin de obtener la CAno mediante la aplicación del modelo bicompartimental y la ecuación de Tsoukias y George15. A continuación, se realizó, en este orden, la oscilometría de impulsos (IOS) (MasterLab versión 5.1, Viasys®, Wuerzburg, Alemania), la espirometría forzada (MasterScreen v. 4.67, Viasys®, Alemania) y la pletismografía corporal total (MasterLab versión 5.1, Viasys®, Wuerzburg, Alemania). Tras estas pruebas basales, se practicó la prueba broncodilatadora (PBD), administrando salbutamol inhalado (400mcg) con cámara espaciadora Volumatic® y repitiendo 15minutos después la IOS, espirometría forzada y pletismografía. Todas estas técnicas se realizaron bajo las recomendaciones publicadas16–20.
Se utilizaron los valores de referencia de Lechtenbörger et al.21 para la IOS, Jaeger22 para las resistencias por pletismografía y las ecuaciones propuestas por Zapletal23 para la pletismografía y la espirometría forzada. Se consideró PBD positiva si el FEV1≥12% respecto al valor previo o≥9% respecto al valor teórico24.
Se consideró disfunción de VAP, si la CAno>4,5ppb25; R5-R20>0,147kPa/L/s4; X5<−0,18kPa/L4; FEF25-75<65% del teórico26; y/o RV/TLC>33%27.
Se calculó el z-score correspondiente al 65% del valor teórico del FEF25-75, mediante regresión logística en la muestra, siendo este (−1,65) el valor utilizado como punto de corte.
Todos los casos cumplimentaron el cuestionario de control de asma ACT en español para mayores de 12 años28 o su versión pediátrica c-ACT en el caso de los niños menores de 12 años29. Se consideró mal control de la enfermedad una puntuación≤19 puntos en el cuestionario ACT o≤20 en c-ACT.
Los datos se procesaron mediante el paquete estadístico Stata versión 14.1® (Stata Corp. Texas, EE. UU.) en una base de datos diseñada al efecto. Se consideró estadísticamente significativo un valor de p<0,05. Para las características demográficas y basales, se realizó un análisis descriptivo, que para las variables continuas incluyó el número de observaciones, media y desviación estándar de la media y para las variables categóricas, frecuencias. Las variables de distribución no normal se expresaron en mediana y rango, y el análisis se realizó mediante estadística no paramétrica (prueba de Kruskal-Wallis). Las diferencias entre 2 grupos, en el caso de variables continuas, se analizaron mediante la prueba de t de Student para muestras independientes y mediante el análisis de la varianza, y se utilizó la prueba de Ji cuadrado de Pearson o prueba exacta de Fisher, en el caso de variables categóricas. Se analizó la correlación y el grado de acuerdo de los diferentes parámetros que evalúan la VAP, mediante el coeficiente de correlación de Spearman y Kappa de Cohen.
ResultadosSe reclutaron 139 casos de modo consecutivo en el ámbito de la consulta externa de Neumología Infantil. Se excluyeron 39 casos por cumplir uno o más criterios de exclusión: 4, por medicación broncodilatadora; uno, no autorización; 11, no colaboradores en las pruebas funcionales; 3, tratamiento con glucocorticoides orales en los 7 últimos días; 3, infección respiratoria actual; 8, crisis asmática actual; 6, baja cuplimentación del tratamiento; y 3, FEV1 inferior al 80% del valor teórico.
La media de edad de los 100 casos incluidos fue 11,1±2,53 años (rango 7-15), predominando los varones (n=67). Se clasificaron 76 casos como asma moderada y 24 como asma grave; 71 casos mal controlados y 29 bien controlados, sin diferencias entre los grupos de asma moderada y grave (p=0,12).
Todos los casos (n=100) realizaron todas las pruebas y se incluyeron todas las variables, excepto en 28 casos donde las determinaciones de la fracción exhalada de óxido nítrico no siguieron el modelo lineal. No hubo diferencias significativas entre asma moderada y asma grave en las variables no dependientes de la VAP en las pruebas de óxido nítrico, espirometría y pletismografía, excepto en la IOS: los casos de asma grave tuvieron valores más elevados de R5 (p=0,02) y Z5 (p=0,02).
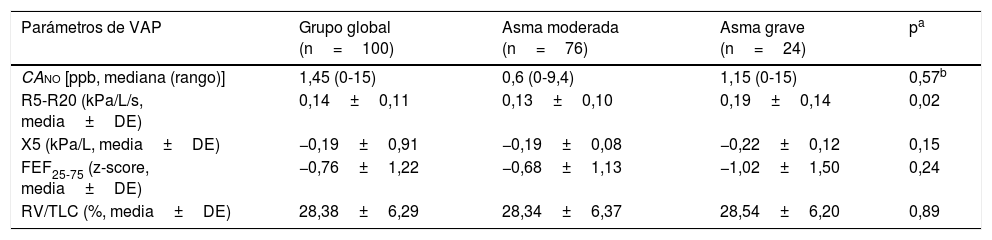
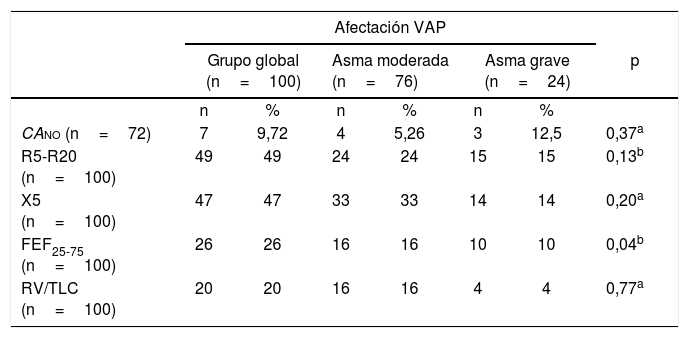
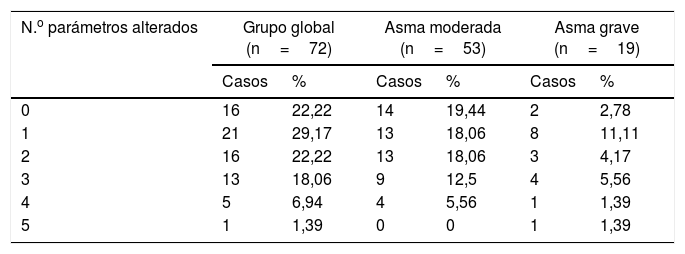
En las variables relacionadas con la VAP, los casos de asma grave mostraron valores más elevados de R5-R20 (p=0,02) (tabla 1). Los parámetros de VAP estuvieron alterados con las frecuencias que se muestran en la tabla 2. No hubo diferencias entre asma moderada y asma grave, salvo en el FEF25-75 alterado con mayor frecuencia en asma grave (p=0,04). De todos los casos con todas las pruebas válidas (n=72), el 77,78% presentaron uno o más parámetros alterados y el 48,61% 2 o más, sin diferencias significativas entre asma moderada y asma grave (p=0,27) (tabla 3).
Valores medios de los distintos parámetros indicativos de afectación de la vía aérea pequeña en el grupo global de niños asmáticos y en los subgrupos de asma moderada y asma grave
| Parámetros de VAP | Grupo global (n=100) | Asma moderada (n=76) | Asma grave (n=24) | pa |
|---|---|---|---|---|
| CAno [ppb, mediana (rango)] | 1,45 (0-15) | 0,6 (0-9,4) | 1,15 (0-15) | 0,57b |
| R5-R20 (kPa/L/s, media±DE) | 0,14±0,11 | 0,13±0,10 | 0,19±0,14 | 0,02 |
| X5 (kPa/L, media±DE) | −0,19±0,91 | −0,19±0,08 | −0,22±0,12 | 0,15 |
| FEF25-75 (z-score, media±DE) | −0,76±1,22 | −0,68±1,13 | −1,02±1,50 | 0,24 |
| RV/TLC (%, media±DE) | 28,38±6,29 | 28,34±6,37 | 28,54±6,20 | 0,89 |
CAno: concentración alveolar de óxido nítrico; DE: desviación estándar; FEF25-75: flujo espiratorio forzado entre el 25% y el 75% de la capacidad vital forzada; RV/TLC: relación volumen residual y capacidad pulmonar total; R5-R20: resistencia entre 5 y 20 hercios; VAP: vía aérea pequeña; X5: reactancia a 5 hercios; z-score: variable estandarizada para comparar datos.
Proporción de niños con afectación de los distintos parámetros indicativos de afectación de la vía aérea pequeña en el grupo global de niños asmáticos y en los subgrupos de asma moderada y asma grave
| Afectación VAP | |||||||
|---|---|---|---|---|---|---|---|
| Grupo global (n=100) | Asma moderada (n=76) | Asma grave (n=24) | p | ||||
| n | % | n | % | n | % | ||
| CAno (n=72) | 7 | 9,72 | 4 | 5,26 | 3 | 12,5 | 0,37a |
| R5-R20 (n=100) | 49 | 49 | 24 | 24 | 15 | 15 | 0,13b |
| X5 (n=100) | 47 | 47 | 33 | 33 | 14 | 14 | 0,20a |
| FEF25-75 (n=100) | 26 | 26 | 16 | 16 | 10 | 10 | 0,04b |
| RV/TLC (n=100) | 20 | 20 | 16 | 16 | 4 | 4 | 0,77a |
CAno: concentración alveolar de óxido nítrico; FEF25-75: flujo espiratorio forzado entre el 25% y el 75% de la capacidad vital forzada; RV/TLC: relación volumen residual y capacidad pulmonar total; R5-R20: resistencia entre 5 y 20 hercios; VAP: vía aérea pequeña; X5: reactancia a 5 hercios.
Número de parámetros indicativos de afectación de la vía aérea pequeña alterados en el grupo global de niños asmáticos y en los subgrupos de asma moderada y asma grave
| N.o parámetros alterados | Grupo global (n=72) | Asma moderada (n=53) | Asma grave (n=19) | |||
|---|---|---|---|---|---|---|
| Casos | % | Casos | % | Casos | % | |
| 0 | 16 | 22,22 | 14 | 19,44 | 2 | 2,78 |
| 1 | 21 | 29,17 | 13 | 18,06 | 8 | 11,11 |
| 2 | 16 | 22,22 | 13 | 18,06 | 3 | 4,17 |
| 3 | 13 | 18,06 | 9 | 12,5 | 4 | 5,56 |
| 4 | 5 | 6,94 | 4 | 5,56 | 1 | 1,39 |
| 5 | 1 | 1,39 | 0 | 0 | 1 | 1,39 |
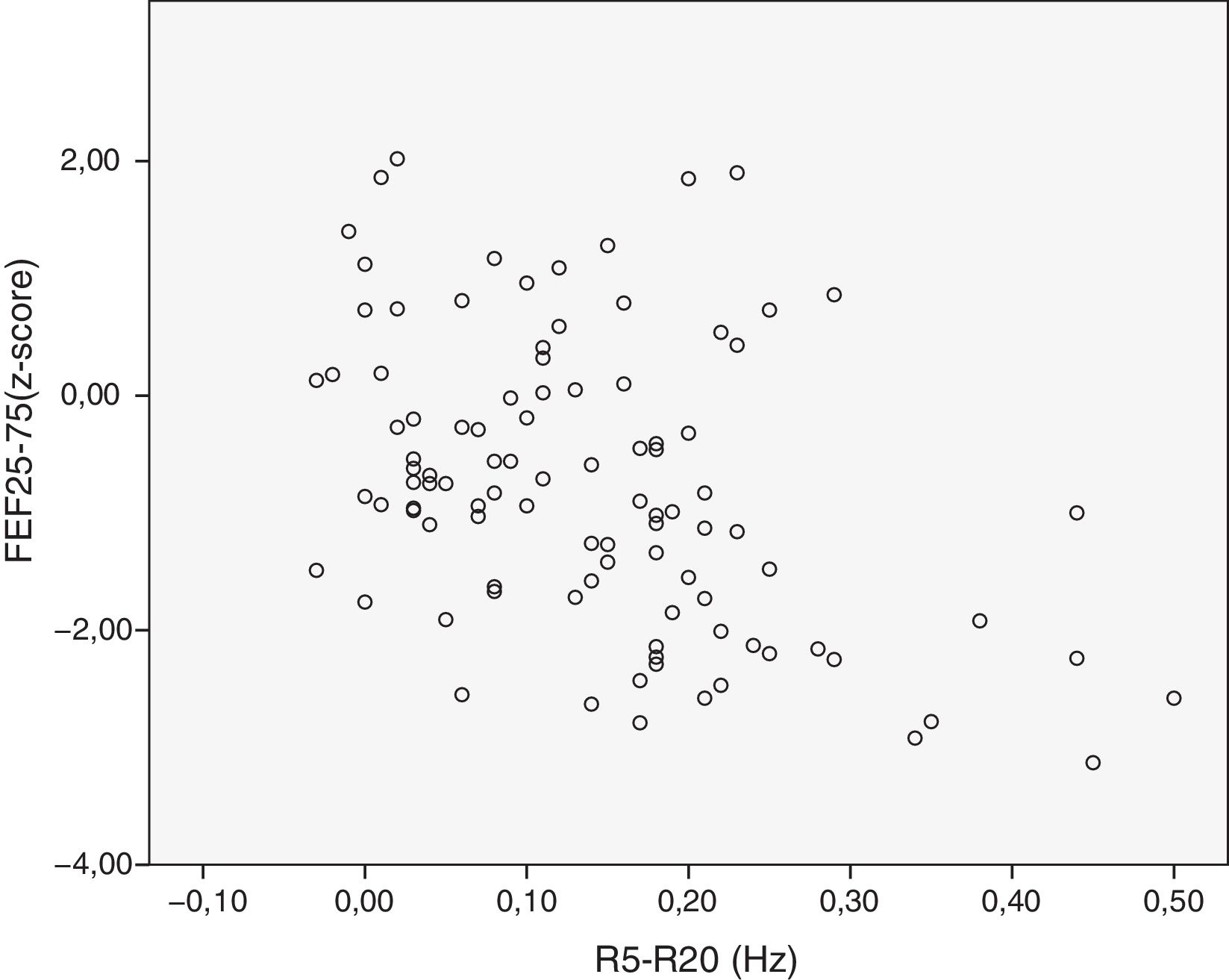
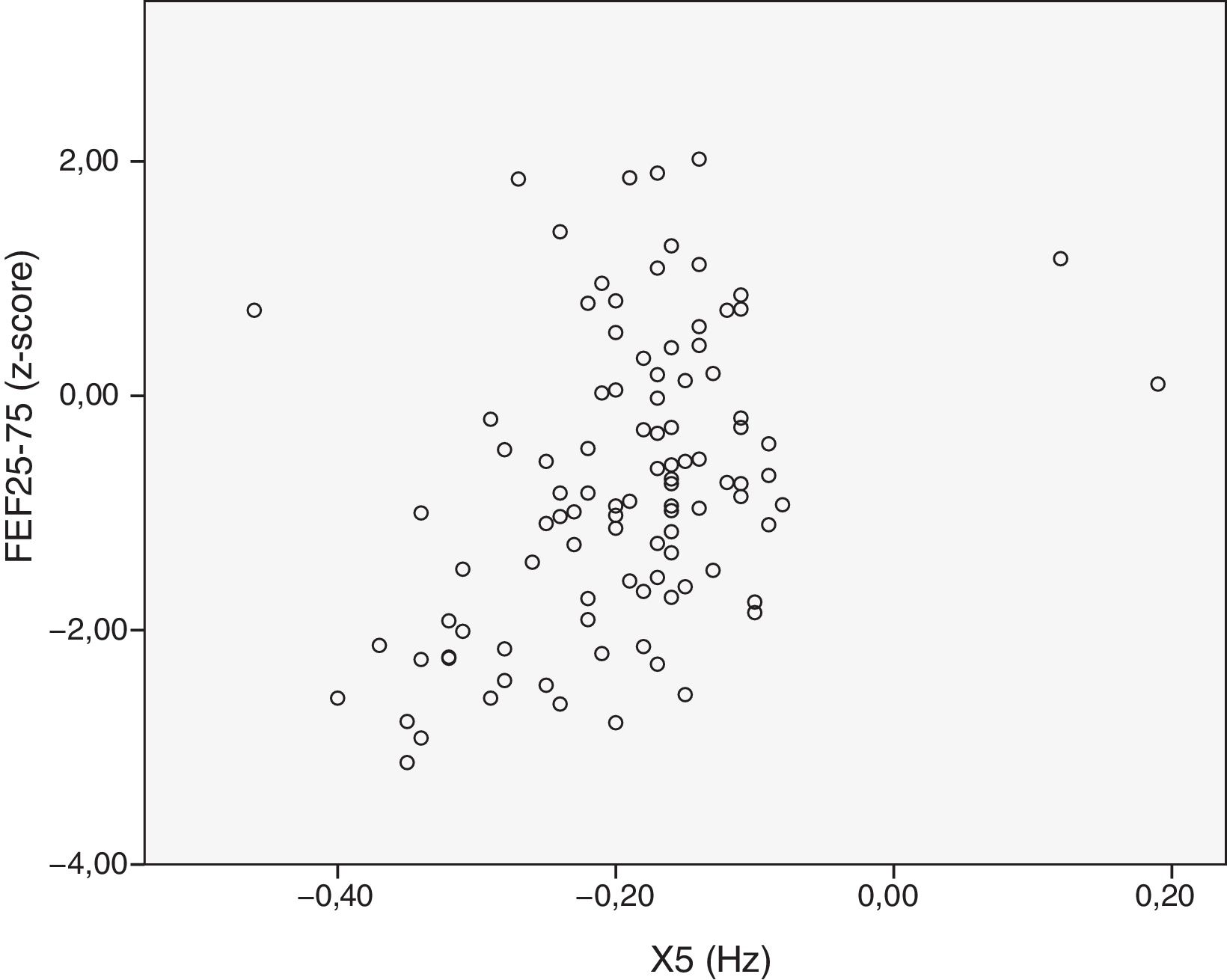
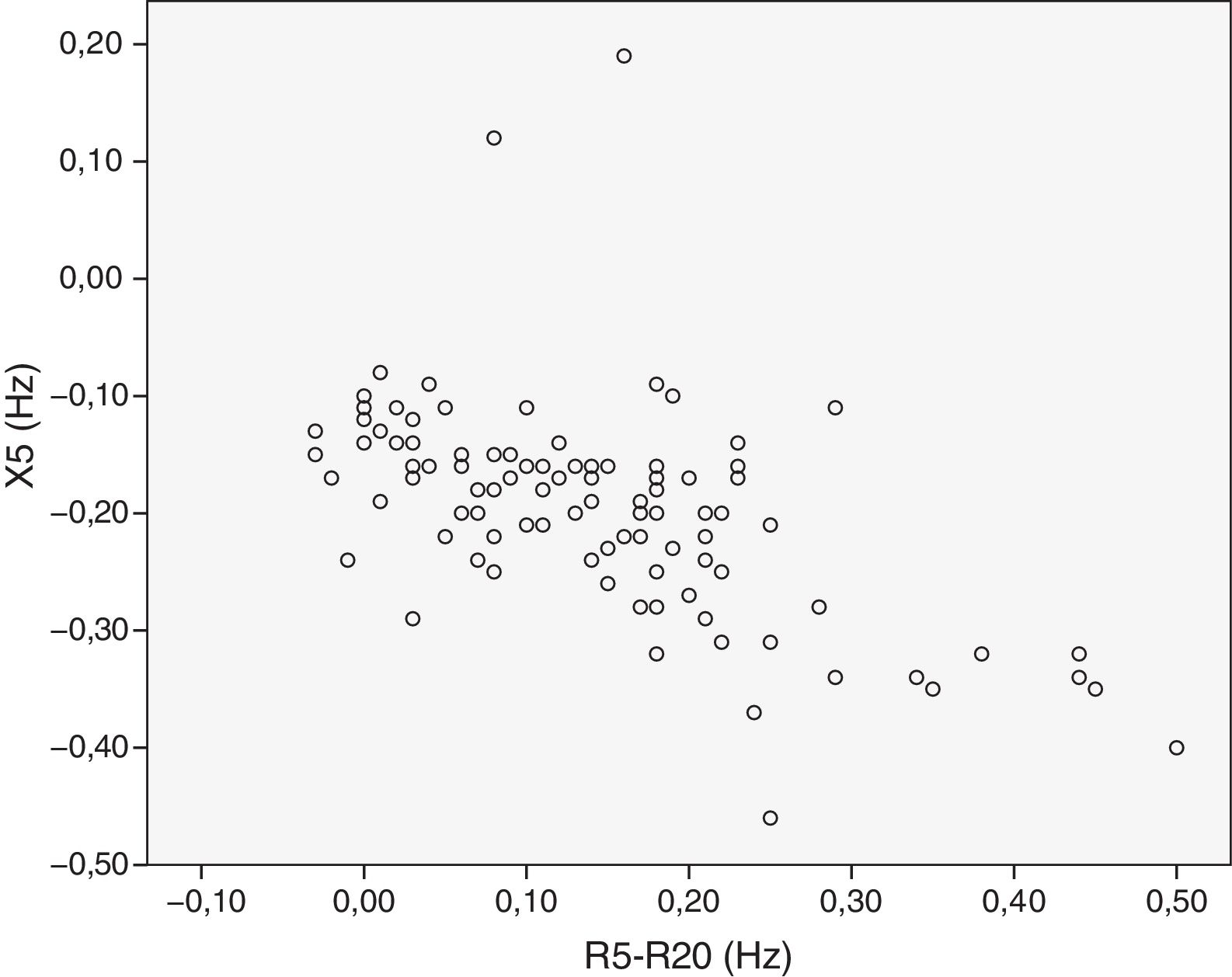
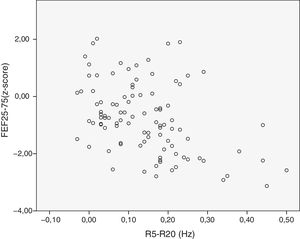
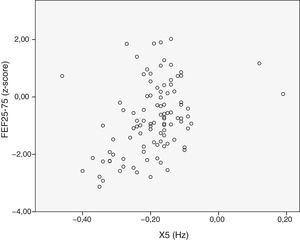
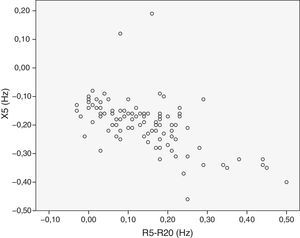
Se analizó la relación entre las variables dependientes de la VAP. Se observó una correlación moderada entre FEF25-75 y R5-R20 (r=−0,58) (fig. 1), entre FEF25-75 y X5 (r=0,57) (fig. 2) y entre R5-R20 y X5 (r=−0,58) (fig. 3). Hubo acuerdo moderado entre R5-R20 y X5 (κ=0,44; p<0,05) y acuerdo bajo entre R5-R20 y FEF25-75 (κ=0,29; p<0,05), X5 y FEF25-75 (κ=0,28; p=0,00) y RV/TLC y FEF25-75 (κ=0,27; p<0,05).
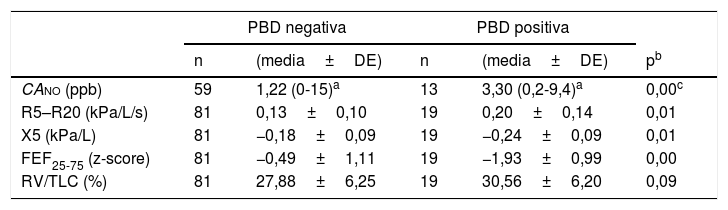
En 19 casos la PBD fue positiva. En este grupo no se encontraron diferencias entre asma moderada y asma grave, ni entre los subgrupos de buen y mal control. En este grupo con prueba de broncodilatación positiva se obtuvieron peores resultados que en el grupo con prueba de broncodilatación negativa (tabla 4).
Comparativos de los distintos parámetros indicativos de afectación de la vía aérea pequeña entre el grupo de niños asmáticos con prueba broncodilatadora positiva y negativa
| PBD negativa | PBD positiva | ||||
|---|---|---|---|---|---|
| n | (media±DE) | n | (media±DE) | pb | |
| CAno (ppb) | 59 | 1,22 (0-15)a | 13 | 3,30 (0,2-9,4)a | 0,00c |
| R5–R20 (kPa/L/s) | 81 | 0,13±0,10 | 19 | 0,20±0,14 | 0,01 |
| X5 (kPa/L) | 81 | −0,18±0,09 | 19 | −0,24±0,09 | 0,01 |
| FEF25-75 (z-score) | 81 | −0,49±1,11 | 19 | −1,93±0,99 | 0,00 |
| RV/TLC (%) | 81 | 27,88±6,25 | 19 | 30,56±6,20 | 0,09 |
CAno: concentración alveolar de óxido nítrico; DE: desviación estándar; FEF25-75: flujo espiratorio forzado entre el 25% y el 75% de la capacidad vital forzada; PBD: prueba broncodilatadora; RV/TLC: relación volumen residual y capacidad pulmonar total; R5-R20: resistencia entre 5 y 20 hercios; X5: reactancia a 5 hercios; z-score: variable estandarizada para comparar datos.
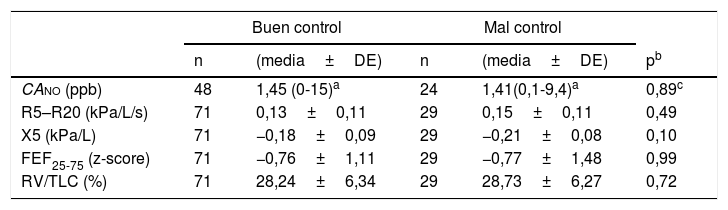
Se compararon los parámetros de VAP entre los grupos de buen y mal control de la enfermedad, sin obtener diferencias estadísticamente significativas en ninguna de las variables (tabla 5). Del mismo modo, la suma de diferentes parámetros alterados no fue indicativo de peor control de la enfermedad (p=0,07).
Valores medios de los distintos parámetros indicativos de afectación de la vía aérea pequeña en los grupos de niños con asma bien controlados y mal controlados
| Buen control | Mal control | ||||
|---|---|---|---|---|---|
| n | (media±DE) | n | (media±DE) | pb | |
| CAno (ppb) | 48 | 1,45 (0-15)a | 24 | 1,41(0,1-9,4)a | 0,89c |
| R5–R20 (kPa/L/s) | 71 | 0,13±0,11 | 29 | 0,15±0,11 | 0,49 |
| X5 (kPa/L) | 71 | −0,18±0,09 | 29 | −0,21±0,08 | 0,10 |
| FEF25-75 (z-score) | 71 | −0,76±1,11 | 29 | −0,77±1,48 | 0,99 |
| RV/TLC (%) | 71 | 28,24±6,34 | 29 | 28,73±6,27 | 0,72 |
CAno: concentración alveolar de óxido nítrico; DE: desviación estándar; FEF25-75: flujo espiratorio forzado entre el 25% y el 75% de la capacidad vital forzada; RV/TLC: relación volumen residual y capacidad pulmonar total; R5-R20: resistencia entre 5 y 20 hercios; X5: reactancia a 5 hercios; z-score: variable estandarizada para comparar datos..
Por último, el número de parámetros alterados de la VAP no se asocia a las hospitalizaciones por asma durante los 12 últimos meses (2 casos) (prueba exacta de Fisher, p=0,06)
DiscusiónEn este estudio se han incluido casos con FEV1 superior al 80% del valor predicho con el objetivo de valorar si con la vía aérea proximal preservada la disfunción de VAP pudiera ser el motivo de no alcanzar el control completo de la enfermedad.
Uno de los principales problemas para analizar y evaluar el grado de afectación de la VAP es la dificultad de acceso a la misma. Las diferentes maneras de estudiarla tienen sus limitaciones. La medida de la FEF25-75 es una de las más comúnmente citadas en lo que se refiere a afectación de la VAP, aun teniendo las limitaciones conocidas. En ausencia de limitación al flujo espiratorio, un incremento del RV podría atribuirse a un cierre prematuro de la VAP y dado que la TLC no suele modificarse en el asma, la afectación de la VAP podría manifestarse a través de un incremento del cociente RV/TLC, marcador de atrapamiento aéreo e hiperinsuflación pulmonar. En la IOS, la diferencia entre la resistencia total y la resistencia central [R (5Hz)−R (20Hz)] corresponde a la resistencia de la VAP, mientras que la reactancia pulmonar medida a 5Hz, representa las propiedades elásticas, capacitancia o el grado de obstrucción de las vías aéreas periféricas. Por otra parte, la CAno se interpreta como un marcador subrogado de la afectación inflamatoria de la VAP.
Uno de los principales hallazgos de este estudio fue que el 77,78% de los niños asmáticos moderados y graves con todas las pruebas realizadas de VAP (72 casos), tratados con la asociación de GCI a dosis medias o altas y agonistas-β2-adrenérgicos de acción prolongada, con el FEV1 normal y un número de hospitalizaciones durante el último año muy bajo (2 casos), tuvieron al menos un criterio de afectación de VAP, tal y como ha sido comunicado por Pisi et al.30 y Wagner et al.31 en asmáticos con valores normales de FEV1. Este hallazgo, que estimamos de interés, justifica que se realicen estudios longitudinales que evalúen su significado en el manejo y buen control del niño asmático32.
La afectación de la VAP se evidenció principalmente por IOS, tanto por R5-R20 (n=49) como por X5 (n=47). Sin embargo, FEF25-75, RV/TLC y CAno mostraron resultados anormales con menor frecuencia [n=26, n=20 y n=7 (9,72%), respectivamente], lo que indica que los puntos de corte utilizados para los parámetros de la IOS podrían ser demasiado sensibles a los cambios en la vía aérea periférica o poco específicos.
En cuanto a la CAno, el modelo bicompartimental de óxido nítrico no se pudo aplicar en el 28% de nuestros casos. Esta cifra es algo mayor que la comunicada por otros autores25,33 y podría explicarse por las diferencias en la ventilación y el patrón inflamatorio de los mismos. El punto de corte de normalidad se fijó en el límite superior calculado para el grupo de niños sanos en nuestra población (4,5ppb)25, que es similar a lo descrito por otros autores33,34 que han utilizado la misma metodología. En nuestra muestra no se encontraron concentraciones elevadas de óxido nítrico alveolar, lo que no descarta la afectación inflamatoria de la VAP, ya que tanto los niveles de la CAno como la concentración del óxido bronquial pueden verse afectados por el uso de glucocorticoides inhalados35. No hemos encontrado diferencias en cuanto a la CAno entre los grupos de asma moderada y asma grave, al igual que van Veen et al.36.
La evaluación de la VAP por IOS ha mostrado valores significativamente más elevados de R5-R20 en el grupo de niños con asma grave (0,19±0,14Hz), resultado concordante con publicaciones previas que hacen referencia a la disfunción de la VAP en el asma grave37. Para las variables dependientes de la IOS, no existen estudios en población pediátrica que determinen el punto de corte que establezca la afectación de VAP. Por este motivo, hemos utilizado los puntos de corte determinados por Shi et al.4 en el trabajo realizado para determinar la utilidad de la IOS en el control de la enfermedad en niños asmáticos, con las limitaciones que ello implica. De esta forma, casi la mitad de la cohorte estudiada mostró un aumento de resistencias de vía aérea periférica y una reactancia disminuida por lo que, aunque estos puntos de corte resultan muy sensibles para detectar cambios en la VAP, no son útiles para discriminar entre asma moderada y severa, y tampoco discriminan entre asma bien y mal controlada.
En lo que a la FEF25-75 se refiere, existe controversia para el estudio de la VAP por su dependencia de la FVC y su baja reproducibilidad38. La cohorte que hemos estudiado mostró un z-score medio de −0,76±1,22, muy lejos de poder ser considerado patológico, sin observarse diferencias entre los grupos de distinta severidad, probablemente por la gran variabilidad de este parámetro. El punto de corte del FEF25-75 lo elegimos en base a un estudio llevado a cabo en 700 niños con asma que tenía por objetivo definir el punto de corte del FEF25-7526. Posteriormente, calculamos el z-score correspondiente en nuestra muestra. En el análisis realizado con dicho punto de corte, la FEF25-75 fue el único parámetro de VAP que se mostró alterado y en mayor frecuencia y proporción en el grupo con asma grave (p=0,04). Aunque la FEF25-75 es el parámetro de mayor disponibilidad en la práctica clínica habitual, debe ser interpretado con cautela por las limitaciones comentadas previamente.
De manera similar a lo considerado por Sorkness et al.39, elegimos la relación RV/TLC como índice de hiperinsuflación (atrapamiento aéreo). Con el fin de identificar la hiperinsuflación con un nivel de confianza elevado, definimos valor de corte el percentil 95 de RV/TLC en niños, que es 0,3327. En nuestro estudio, el valor medio del RV/TLC fue de 28,38±6,29%, no observándose diferencias significativas entre los grupos con asma moderada y asma grave. En nuestra muestra, el 20% de los niños mostraron un valor de RV/TLC superior al 33%, en comparación con el 7-11% detectado en el estudio de Mahut el al.40, probablemente por tratarse de casos con asma de menor severidad.
Un total de 19 casos tuvieron una PBD positiva. Estos pacientes obtuvieron peores resultados en los marcadores de VAP que los pacientes del grupo de PBD negativa, por lo que podemos indicar que cierto grado de obstrucción de la vía aérea proximal no dificulta el análisis de la VAP. En este grupo de niños con PBD positiva, se analizaron las variables dependientes de la VAP posbroncodilatación mediante IOS, espirometría y pletismografía, y se observó una mejoría significativa en todos los indicadores de afectación de VAP.
Se analizó la utilidad del estudio de la VAP para conocer el grado de control de la enfermedad, sin que ninguna de las variables relacionadas con la VAP mostrase asociación con el grado de control de asma. De la misma manera, la suma de los diferentes parámetros alterados no se asoció a un peor control de la enfermedad. Este resultado está en la línea de un estudio realizado en adultos con asma modera o grave12, con la vía aérea proximal preservada, en el que no encontraron asociación entre la puntuación del cuestionario ACT y los diferentes parámetros de VAP en los 222 pacientes estudiados. Al parecer, c-ACT y ACT se correlacionan bien con los criterios de la GINA1 para predecir el riesgo de asma no controlada, pero los puntos de corte comúnmente utilizados para c-ACT y ACT parecen subestimar la proporción de los niños con asma no controlada como se ha definido por GINA41, lo que podría suponer un cambio en los resultados que hemos obtenido en cuanto la asociación entre disfunción de VAP y control de la enfermedad. Otra hipótesis posible para la falta de asociación entre la disfunción de la VAP y el control de la enfermedad sería el hecho de que, efectivamente, aquella no sea motivo de peor control de asma, sino que se trate de una característica más de la enfermedad o que se encuentre relacionada con otros factores como podrían ser la respuesta alérgica42, persistencia, evolución o pronóstico de la enfermedad.
La limitación principal de nuestro estudio es la inexistencia de valores de referencia que determinen la afectación de la VAP. Por otra parte, el diseño transversal imposibilita el estudio del comportamiento evolutivo de la VAP, en una enfermedad en la que la variabilidad a lo largo del tiempo es una característica definitoria de la misma. De la misma manera, la heterogeneidad del asma grave dificulta su estudio, por la variabilidad que puede mostrar dependiendo del momento en el que se realice. Por último, hay que señalar la falta de normativa técnica para determinar la CAno. Por todo ello, se necesitan estudios multicéntricos longitudinales que aclaren estas y otras dudas al respecto.
ConclusionesLa mayoría de los niños con asma moderada y grave situados en el escalón de tratamiento correspondiente con el FEV1 en rangos normales, tienen un fenotipo de VAP disfuncionante en términos de resistencia, reactancia, inflamación, limitación al flujo espiratorio o atrapamiento aéreo, con un grado de acuerdo moderado entre ellos. Esta disfunción de la VAP no se relaciona con el nivel de control del asma.
FinanciaciónEste Proyecto de Investigación no ha recibido ninguna financiación.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
A Jose I. Emparanza, MD, PhD, Unidad de Investigación Clínica del HU Donostia, por la realización del análisis estadístico.