Se desconoce la prevalencia de EPOC entre pacientes que acuden al sistema de salud en Latinoamérica. El estudio Prevalencia y práctica habitUal –diagnóstico y tratamiento– en población de riesgo de EPOC en Médicos generalistas de 4 países de América Latina (PUMA) evalúa prevalencia, diagnóstico y tratamiento de EPOC en pacientes en riesgo que acuden a atención primaria constituyéndose en detección de casos oportunista. El objetivo de esta publicación es describir la metodología del estudio.
MétodosEstudio multicéntrico, observacional, transversal, realizado en Argentina, Colombia, Uruguay y Venezuela. Participaron pacientes≥40 años, fumadores o ex fumadores y/o expuestos a combustión de biomasa que acudieron a consultas de atención primaria. Los pacientes elegibles realizaron espirometrías pre y posbroncodilatador y respondieron cuestionarios estandarizados sobre datos demográficos, hábito tabáquico, exposición a polución ambiental/doméstica, síntomas/antecedentes y manejo de enfermedades respiratorias, comorbilidades y uso de recursos sanitarios.
ResultadosParticiparon 57 centros en 4 países. Se reclutaron 1.907 pacientes, 1.743 completaron el Cuestionario PUMA y 1.540 pacientes realizaron espirometrías validadas.
ConclusionesDescribimos la metodología empleada en el estudio PUMA, primer estudio sistemático multicéntrico realizado en 4 países de Latinoamérica para detección de casos de EPOC confirmados por espirometría en atención primaria. Aproximadamente el 90% de los pacientes que realizaron el Cuestionario PUMA realizaron espirometrías válidas. Esto permite reflexionar sobre la factibilidad de realizar detección de casos oportunista en el primer nivel asistencial para encontrar pacientes en estadios tempranos o no diagnosticados y mejorar el diagnóstico y manejo de EPOC en atención primaria.
The prevalence of COPD among patients treated in the healthcare system in Latin America is unknown. The PUMA study (Prevalencia y práctica habitUal –diagnóstico y tratamiento– en población de riesgo de EPOC en Médicos generalistas de 4 países de América Latina) screened at-risk patients attending primary care centers to evaluate the prevalence, diagnosis and treatment of COPD in this setting. The aim of this report is to describe the study methodology.
MethodsMulticenter, observational, cross-sectional study conducted in Argentina, Colombia, Uruguay and Venezuela. Subjects were≥40 years, smokers, former smokers and/or exposed to fossil fuels attending primary care centers. Eligible patients underwent pre- and post- bronchodilator spirometry and completed standardized questionnaires on demographics, smoking, exposure to environmental/domestic pollution, symptoms/history and management of respiratory diseases, comorbidities, and use of healthcare resources.
ResultsA total of 57 centers in 4 countries participated; 1,907 patients were included, 1,743 completed the PUMA questionnaire and 1,540 patients underwent validated spirometry.
ConclusionsWe describe the methodology used in the PUMA study, the first systematic multicenter study in four Latin American countries aimed at detecting COPD cases confirmed by spirometry in primary care. Approximately 90% of patients who completed the PUMA questionnaire underwent valid spirometry tests. This gives room for reflection on the feasibility of opportunistic screening at the primary care level to detect patients in the early stages of COPD or with undiagnosed COPD, and improve the diagnosis and management of this disease.
La enfermedad pulmonar obstructiva crónica (EPOC) es una condición frecuente, prevenible y tratable caracterizada por la obstrucción progresiva y parcialmente reversible del flujo de aire, la cual puede estar acompañada por disnea, tos y producción de esputo1–3. El impacto global de la EPOC se incrementó en todo el mundo convirtiéndose en una de las principales causas de mortalidad, morbilidad, y pérdida de calidad de vida, y se encuentra asociada a costes sociales y médicos elevados4–6.
El diagnóstico temprano y el tratamiento adecuado son críticos para establecer las medidas preventivas minimizando la progresión de la EPOC y sus consecuencias2. Considerando que la EPOC puede ser asintomática en su etapa inicial y que su diagnóstico requiere la realización de la espirometría para confirmar la obstrucción al flujo aéreo, el subdiagnóstico y el diagnóstico erróneo son muy comunes, especialmente al comienzo de la enfermedad1–3,6.
Hay numerosos estudios de prevalencia de la EPOC de base poblacional (PLATINO, BOLD, EPISCAN) en distintos países del mundo, con cifras que oscilan alrededor del 10-15% de la población estudiada7–9. En el estudio Proyecto Latinoamericano de Investigación en Obstrucción Pulmonar (PLATINO), la prevalencia poblacional de la EPOC en 5 ciudades de América Latina fue, en promedio, del 14,3%7. En ese mismo estudio el 89% de los individuos diagnosticados con EPOC a través de la espirometría no tenían diagnóstico previo, el 64% de los individuos que manifestaban tener EPOC no tenían limitación al flujo aéreo en la espirometría y solo un 20% había realizado una espirometría en algún momento de su vida, lo cual indica que la subutilización de la espirometría es una limitación mayor a la hora de efectuar el diagnóstico de EPOC10.
Existe menos información sobre la prevalencia de EPOC en la población que acude al primer nivel de atención del sistema de salud. Los escasos datos disponibles en la bibliografía internacional sugieren cifras significativamente mayores que rondan el 20%11,12. En Latinoamérica hay un solo estudio realizado en 27 ciudades de México que arrojó una prevalencia de 20,6%13. Es en el primer nivel de atención donde resulta más probable encontrar pacientes en estadios tempranos o no diagnosticados. Por lo tanto el conocimiento de la prevalencia de la enfermedad en este escalón asistencial es fundamental para planear e implementar estrategias para la detección y manejo temprano de la enfermedad11,12. Los datos obtenidos en esta población complementan los obtenidos en estudios de prevalencia poblacional. Ambos son necesarios para un abordaje sanitario integral adecuado.
Por esta razón, planificamos realizar el estudio Prevalencia y práctica habitUal -diagnóstico y tratamiento- en población de riesgo de EPOC en Médicos generalistas de 4 países de América latina (PUMA) -clinicaltrials.gov identifier: NCT01493544. El mismo fue diseñado para estimar la prevalencia, factores determinantes del subdiagnóstico y diagnóstico erróneo así como el tratamiento de la EPOC entre los pacientes de alto riesgo que consultaron por cualquier motivo a un médico de atención primaria en Argentina, Colombia, Uruguay y Venezuela. El objetivo de esta publicación es describir la metodología utilizada.
MétodosDiseño y población de estudioEl estudio PUMA es un estudio multicéntrico, multinacional, transversal, no intervencionista. Para el diseño del protocolo y estandarización de la metodología se nombró un comité ejecutivo compuesto por expertos en epidemiología y medicina respiratoria de Latinoamérica. Se designó además un coordinador nacional por país también experto en neumología.
La selección de centros se realizó en cada país y debía reflejar la realidad de la práctica de atención primaria en cuanto a la distribución geográfica (urbana o rural), y sector de la práctica médica (pública o privada). Los centros participantes estuvieron constituidos por centros de atención primaria ambulatoria (médicos clínicos, familiares y/o generales), que no tuvieran contacto directo con especialistas en medicina respiratoria. El estudio fue aprobado por los comités de ética pertinentes para cada centro y todos los participantes otorgaron por escrito su consentimiento informado.
La población de estudio estuvo constituida por pacientes con alto riesgo de EPOC que asistieron a la consulta de atención primaria en los centros participantes de Argentina, Colombia, Uruguay y Venezuela. La concurrencia de los pacientes fue parte de las visitas regulares programadas o espontáneas y su cita médica no dependió del estudio. Se consideró alto riesgo de EPOC (criterios de inclusión) a los pacientes≥40 años, fumadores actuales o ex fumadores (≥10 paquetes/año, ≥50 pipas/año, o≥50 tabacos/año), y/o con antecedentes de exposición al humo procedente de la combustión de combustibles orgánicos, como la madera o el carbón, para cocinar o calentar (combustión de biomasa≥100 horas/leña/año).
Los criterios de exclusión fueron embarazo, pacientes con contraindicación para la espirometría (cirugía torácica, abdominal o neurológica; síndrome coronario agudo; desprendimiento de retina; hospitalización por cualquier problema cardíaco en los últimos 3 meses), frecuencia cardíaca ≥120lpm, incapacidad física o mental para completar los procedimientos del estudio, en fase de tratamiento por tuberculosis, o participantes actuales de un ensayo clínico.
Cada centro tuvo preasignado un número de pacientes a reclutar. El número de días de reclutamiento por centro dependió de la cantidad de pacientes con criterios de inclusión que concurrieran y completaran el estudio.
Los pacientes fueron seleccionados para participar del estudio en forma consecutiva según orden de llegada a la consulta médica. Aquellos que no cumplían con los criterios de inclusión continuaban con su consulta programada.
Capacitación del personalLos coordinadores nacionales estuvieron a cargo de la formación y de las certificaciones del personal involucrado en la cumplimentación de los cuestionarios y realización de espirometrías. Esto fue implementado en cada país utilizando formaciones y materiales de evaluación estandarizados que se diseñaron específicamente para este estudio, basados en las recomendaciones de la American Thoracic Society (ATS)14. Se realizaron reuniones de investigadores para asegurar la adherencia a los procedimientos y a los estándares de calidad. Se sistematizó la modalidad de informe espirométrico y la elaboración de los mismos estuvo a cargo de los coordinadores nacionales, quienes dieron seguimiento a la calidad de las maniobras realizadas. El personal de campo envió en forma electrónica las espirometrías al coordinador nacional dentro de 24 horas de realizadas, a fin de contar con su aprobación sobre la calidad técnica antes de finalizar el reclutamiento en un centro. Cada espirometría fue considerada válida solamente con el aval del coordinador. En caso contrario debió repetirse el estudio cuando fue posible o el mismo fue descartado.
Procedimientos del estudioLos médicos investigadores fueron responsables de la selección de la muestra corroborando los criterios de inclusión, exclusión y obtención del consentimiento informado. Se recogieron datos provenientes de los médicos y de los pacientes a través de cuestionarios estandarizados (tabla 1).
Cuestionarios y actividades realizadas en las visitas
| Visita de estudio | Visita 1 | Visita 2d |
| Consentimiento informado para pacientes | X | |
| Criterios de inclusión y exclusión | X | |
| Cuestionario al investigadora | X | |
| Cuestionario de datos mínimosb | X | |
| Cuestionario PUMA | X | |
| Cuestionario de antecedentes del pacientec | X | |
| Espirometría | X | X |
| Oximetría | X | X |
En el Cuestionario al Investigador cada médico informó sobre su edad y sexo, años de ejercicio de la medicina general, formación profesional, antecedentes de tabaquismo, media de pacientes atendidos al día, desempeño de actividad docente, ubicación del centro de estudio (urbano/rural), características de la práctica médica (público/privado), factores limitantes a la adopción de guías de EPOC, y recursos diagnósticos y terapéuticos disponibles.
En el Cuestionario de Antecedentes, los médicos recolectaron información registrada en la historia clínica, incluyendo espirometrías, diagnósticos y tratamientos previos así como presencia de comorbilidades.
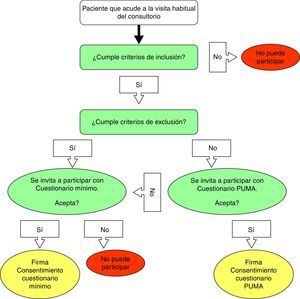
El médico corroboraba si el paciente podía realizar espirometría y oximetría en esa visita. Los pacientes eran luego remitidos al personal entrenado para realizar dichos estudios y completar el cuestionario correspondiente. El personal entrenado encuestaba directamente al paciente para completar el Cuestionario PUMA (versión modificada del cuestionario del estudio PLATINO). A los pacientes con criterios de inclusión pero con algún criterio de exclusión, se los invitó a participar con el Cuestionario de Información Mínima (información demográfica básica y de hábito tabáquico).
La variable de resultado primario fue el diagnóstico de EPOC basado en la espirometría. Los individuos con EPOC fueron definidos como aquellos con volumen espiratorio forzado en el primer segundo (VEF1) dividido por capacidad vital forzada (CVF) inferior a 0,7. De manera adicional, la prevalencia de EPOC también fue estimada en base a otros criterios espirométricos tales como la clasificación GOLD (http://www.goldcopd.org) y los criterios para el límite inferior del valor normal (LLN, por su sigla en inglés). Las variables independientes se obtuvieron a partir de los cuestionarios utilizados e incluyeron datos demográficos, hábito tabáquico, polución ambiental/doméstica, síntomas/antecedentes y manejo de enfermedades respiratorias, comorbilidades y uso de recursos de salud.
Ante la presencia de algún criterio temporal que impidiera la realización de la espirometría el paciente completaba el cuestionario y se coordinaba una segunda visita. Los criterios para diferimiento de la espirometría incluyeron el uso de broncodilatadores de acción corta en las últimas 3 horas, broncodilatadores beta-adrenérgicos de acción prolongada en las últimas 12 horas, medicamentos anticolinérgicos de acción prolongada en las últimas 24 horas, fumar cigarrillos, pipas u otros productos del tabaco en las últimas 2 horas, realización de ejercicio físico, incluyendo el uso del gimnasio, o caminar o trotar en la última hora y presencia de una infección respiratoria aguda en el momento de la visita.
Se obtuvieron datos antropométricos utilizando dispositivos de medición de altura y balanzas calibradas. Para la realización de las espirometrías se utilizó en todos los centros un espirómetro con tecnología ultrasónica (Easy One by NDD TECHNOPARK, Medical Technologies, Inc. Two Dundee Park, Andover, MA, EE. UU.), que reúne los requisitos de control de calidad de la ATS14.
Para la aceptabilidad y reproducibilidad de las espirometrías se usaron los criterios de la ATS (entre 150-200ml), con 8 maniobras, hasta un máximo de 15 permitidas, con el fin de obtener mediciones reproducibles. Las espirometrías se realizaron con los pacientes sentados utilizando una pinza nasal. Cada participante completó 2 pruebas espirométricas - examen de espirometría basal y una segunda prueba 15 minutos después de la administración de 400μg de salbutamol en aerosol aplicado con espaciador.
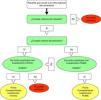
La oximetría se realizó con un oxímetro de pulso digital una vez que el paciente hubiera estado 5 minutos en reposo y antes de recibir el broncodilatador para la espirometría (Riestet–ri-foxN pulse Oximeter [Rudolf Riester GmbH - Bruckstrasse. 31, D-72417 Jungingen, Alemania] o NONIN Onyx 9500 Oximeter [Nonin Medical, Inc., 13700 1st Avenue, North Plymouth, MN, EE. UU.]). Se realizaron con los pacientes sentados y respirando aire ambiente con el oxímetro colocado en el dedo índice derecho. Se informó el promedio de 6 mediciones tomadas en intervalos de 10 segundos. También se recogió el valor de la frecuencia cardíaca que proporciona el dispositivo. El cuadro de flujo correspondiente a la selección de los pacientes puede observarse en la figura 1 y los procedimientos realizados durante la visita están descriptos en la tabla 1.
Análisis estadísticoEl tamaño original de la muestra se calculó para investigar la prevalencia de EPOC confirmada por espirometría en la población de estudio mencionada en cada país (estimada en un 20%) con un margen de error de 3,0 puntos porcentuales, llegando a una muestra requerida de 715 individuos por país. Solo Venezuela (n=721) alcanzó el número estimado de pacientes que completaron el cuestionario PUMA a la fecha de cierre de reclutamiento por lo que para Argentina (n=454) y Colombia (n=465), el margen de error de la prevalencia estimada es de 3,7 puntos porcentuales. Para incrementar el tamaño de la muestra para el análisis combinado, se incluyeron 103 pacientes de Uruguay.
Además de los análisis específicos por país, se llevarán a cabo algunas pruebas de factor de riesgo utilizando toda la muestra. En tales casos, el poder estadístico es igual o mayor a un 90% detectando índices de probabilidad de (a) 1,4 o mayor para las exposiciones que afectan a 20% de la población libre de enfermedad; (b) 1,6 o mayor para las exposiciones que afecta a 10% de la población libre de enfermedad. Para objetivos secundarios restringidos a los participantes con EPOC (n previsto=572), los márgenes de error para proporciones de 10, 20 y 50% son, respectivamente, 2,5, 3,5 y 4,2 puntos porcentuales.
Las estadísticas descriptivas incluirán cálculos de medias, medianas, desviaciones estándar y rangos para las variables continuas, y proporciones y sus respectivos intervalos de confianza del 95% para las variables categóricas. La prevalencia de EPOC y su manejo se estudiarán en cada país excepto en el caso de Uruguay debido al pequeño tamaño muestral. La mayoría de los análisis restantes utilizarán la muestra combinada, excepto cuando las pruebas por heterogeneidad sugieran la necesidad de análisis específicos del país. En los análisis bivariados, las proporciones se compararán mediante la prueba de chi-cuadrado para la heterogeneidad y tendencia lineal. Las diferencias en las medias se pondrán a prueba a través de T-test o análisis unidireccional de la varianza. Para los análisis multivariables, la regresión logística o lineal será empleada para los resultados categóricos y continuos, respectivamente. Los análisis estadísticos serán realizados utilizando Stata, versión 12 (www.stata.com).
ResultadosEl protocolo final se terminó en agosto 2011. Durante el tercer trimestre de 2011 y el primero de 2012, cada país participante obtuvo las aprobaciones del estudio por los comités de ética pertinentes y/o autoridades nacionales relevantes dependiendo de las regulaciones locales para este tipo de estudio. El tiempo requerido para este proceso fue variable en cada país y estas diferencias impactaron en el periodo de reclutamiento.
El primer paciente fue incluido en Argentina el 6 de febrero de 2012 y el último se registró en Colombia el 31 de octubre de 2012 (tabla 2). La base de datos se cerró el 30 de noviembre de 2012.
Recolección de muestras por país
| Argentina n (%) | Colombia n (%) | Uruguay n (%) | Venezuela n (%) | Total | |
| Tiempo para la recolección desde ingreso del primer paciente a ingreso del último paciente | 5 meses | 4 meses | 2 meses | 8 meses | 8 meses (máximo) |
| Tamaño de muestra final | 506 (26,5) | 476 (25,0) | 112 (5,9) | 813 (42,6) | 1.907 (100,0) |
El número de centros fue diferente entre los países participantes reflejando la práctica de atención primaria local, alcanzando un total de 57 centros involucrados.
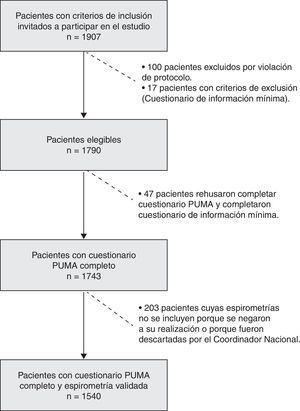
Se reclutaron 1.907 pacientes, de los cuales 1.790 fueron elegibles (reunieron todos los criterios de inclusión y ninguno de exclusión); 100 pacientes fueron excluidos por violación del protocolo respecto a los criterios de inclusión y 17 pacientes presentaron al menos un criterio de exclusión. Estos últimos completaron el Cuestionario de Información Mínima.
De los 1.790 pacientes elegibles, 47 se negaron a completar el Cuestionario PUMA y completaron el Cuestionario de Información Mínima. Así quedaron 1.743 pacientes con Cuestionario PUMA completo, de los cuales 1.540 pacientes tuvieron espirometrías aceptables según criterio de los coordinadores nacionales. Es decir, el 88,4% de los pacientes que completaron el Cuestionario PUMA tuvieron espirometrías válidas y constituyeron la muestra para evaluar la prevalencia de EPOC (tabla 3 y fig. 2).
Tasas de respuestas por país
| Argentina n (%) | Colombia n (%) | Uruguay n (%) | Venezuela n (%) | Total n (%) | |
| Pacientes elegibles | 491 (26,3) | 467 (26,1) | 104 (5,8) | 726 (40,6) | 1.790 (100,0) |
| Negativa a completar el Cuestionario PUMA con todos criterios de inclusión | 37 (7,5) | 2 (0,4) | 1 (1,0) | 5 (0,7) | 47 (2,5) |
| Cuestionario de Info mínima realizado | 42 (8,5) | 11 (2,3) | 2 (1,9) | 9 (1,2) | 64 (3,5) |
| Tasa de respuesta global de Cuestionario PUMA | 454 (91,5) | 465 (97,7) | 103 (98,1) | 721 (98,8) | 1.743 (96,5) |
| Espirometrías validadas | 446 (98,2) | 326 (70,1) | 103 (100,0) | 665 (92,2) | 1.540 (88,4) |
El estudio PUMA es un estudio observacional, multicéntrico, multinacional, transversal, desarrollado en una población de pacientes de alto riesgo de EPOC que asistió a una consulta médica de atención primaria. El estudio fue diseñado específicamente para evaluar la prevalencia de EPOC confirmada por espirometría en este grupo de pacientes y, por lo tanto, se constituye en un estudio de detección de casos oportunista.
La búsqueda de casos en estudios de atención primaria ha arrojado valores diferentes a los obtenidos en estudios poblacionales lo que subraya la importancia de tener resultados específicos en esta población para una adecuada planificación sanitaria. Laniado-Laborin et al. utilizaron una metodología de búsqueda de casos basada en médicos de atención primaria en 27 ciudades de México13. Encontraron una prevalencia de EPOC de 20,6% significativamente mayor a la obtenida en el estudio PLATINO para la ciudad de México (7,8%), en el EPI-SCAN para España (10,2%) y a la citada en un artículo de revisión de estudios epidemiológicos (4-10%), todos ellos de base poblacional7,9,15. Hill et al. encontraron también en un estudio que incluyó 3 sitios de atención primaria una prevalencia de 20,7% de los cuales solo un 32% conocía su diagnóstico previamente11.
Es una fortaleza de este estudio el uso de un protocolo estricto en una población predefinida con un método de estudio similar en todos los centros que incluyó cuestionarios validados y técnica espirométrica estandarizada con equipamiento similar, que permitirá comparar además los resultados empleando diferentes criterios espirométricos (GOLD, LLN)7,8.
El estudio de Laniado-Laborin evaluó pacientes previamente seleccionados por los médicos generales y no constituían una muestra randomizada con los sesgos potenciales que ello implica13. Para tratar de evitar estos inconvenientes, en el estudio PUMA se realizó una selección de centros basada en listas disponibles de médicos de atención primaria y los pacientes estudiados fueron los que concurrieron en forma espontánea. A pesar de los esfuerzos para que la muestra fuera representativa somos conscientes que la validez externa puede tener problemas de precisión pero el procedimiento empleado fue el más razonable en función de las posibilidades operativas de los distintos países.
El estudio PUMA clarificará la prevalencia de subdiagnóstico y diagnóstico erróneo de EPOC vinculados con la subutilización de la espirometría en esta población de 4 países de América Latina. El hecho de ser multicéntrico y multinacional es otro punto importante del estudio ya que permitirá tener un panorama comparativo de distintos países estudiados con igual metodología. En el análisis de los resultados y las variaciones entre países será importante incluir los problemas potenciales de validez externa ya mencionados.
A través del Cuestionario PUMA se recolectó una gran cantidad adicional de información que será útil para evaluar temas claves como la influencia demográfica y factores socioeconómicos, presencia de síntomas, exacerbaciones y manejo de enfermedades respiratorias y comorbilidades lo que influencia tanto la severidad de los síntomas y calidad de vida de los pacientes, como también el riesgo de hospitalización y, eventualmente, muerte15–17. La heterogeneidad de todos estos factores entre los países participantes será analizada.
A partir de este estudio se podrá estimar también el rol de los profesionales de atención primaria en la adecuada utilización de recursos sanitarios y terapéuticos. Esto posibilitará desarrollar estrategias para orientar a estos médicos en pos de mejorar el diagnóstico y manejo de la EPOC.
En el estudio PUMA casi el 90% de los pacientes que realizaron el Cuestionario PUMA constituyen la muestra del estudio con espirometrías válidas realizadas en el primer nivel de atención. Esto nos permite reflexionar sobre la factibilidad de realizar diagnósticos tempranos a través de la búsqueda de casos. Sin duda la precocidad del diagnóstico podría modificar el curso natural de una enfermedad que es frecuentemente subdiagnosticada y diagnosticada generalmente en estadios avanzados.
Número de palabras del cuerpo principal del manuscrito: 2.990.
FinanciaciónEl presente estudio observacional fue patrocinado por AstraZeneca América Latina.
El apoyo editorial para este manuscrito fue provisto por Flow Healthcare Consultancy, financiado por AstraZeneca.
Conflicto de interesesEduardo Schiavi ha recibido honorarios por impartir conferencias y/o por asesoría científica por parte de AstraZeneca, Boehringer Ingelheim y Takeda.
Roberto Stirbulov ha recibido honorarios por impartir conferencias y/o por asesoría científica por parte de Boehringer Ingelheim y Novartis.
Ramón Hernández era personal de AstraZeneca Latinoamérica al momento de diseño y desarrollo del estudio PUMA.
Sandra Mercurio es personal de AstraZeneca Argentina.
Valentina Di Boscio es personal de AstraZeneca Argentina.
Contribución de los autoresES contribuyó en la conceptualización y diseño de este estudio y participó en la redacción y revisión crítica de este manuscrito. RS contribuyó en la conceptualización y diseño de este estudio. RHV contribuyó en la conceptualización y diseño de este estudio. SM contribuyó en la conceptualización y diseño de este estudio y participó en la redacción y revisión crítica de este manuscrito. VDB contribuyó en la conceptualización y diseño de este estudio y participó en la redacción y revisión crítica de este manuscrito.
El Comité Ejecutivo estuvo compuesto por miembros de la Asociación Latinoamericana del Tórax (ALAT) de Argentina, Brasil, Colombia, México, Uruguay, y Venezuela.
Coordinadores nacionales: Gustavo Zabert (Argentina), Carlos Aguirre (Colombia), Alejandra Rey (Uruguay), y Dolores Moreno (Venezuela).
Comité Ejecutivo: María Montes de Oca (Venezuela), Alejandro Casas (Colombia), Eliseo Guallar (Estados Unidos), José Jardim (Brasil), María Victorina López Varela (Uruguay), Sandra Mercurio (Argentina), Alejandra Ramírez Venegas (México), Eduardo Schiavi (Argentina), Roberto Stirbulov (Brasil).
Nuestro reconocimiento a Pedro Hallal quien contribuyó con el análisis estadístico y a todos los investigadores y pacientes que participaron en el estudio PUMA.