El depósito de amiloide en el árbol traqueobronquial es una forma de presentación muy poco frecuente y supone alrededor del 1% de los tumores benignos de esta zona. Describimos aquí un caso de amiloidosis traqueobronquial primaria que obstruía casi por completo la parte distal de la tráquea y el bronquio principal izquierdo.
Se realizó con éxito la extirpación de la masa mediante resección mecánica y coagulación con láser Nd-YAG utilizando una broncoscopia rígida. Posteriormente se implantó una prótesis en Y autoexpansible de nueva generación, para restablecer la permeabilidad de la vía aérea. Cinco meses después, los exámenes radiológico y broncoscópico mostraron la presencia de la prótesis en el lugar adecuado, con una permeabilidad normal del árbol traqueobronquial.
Amyloid deposition in tracheobronchial tree is a rare presentation and counts about 1% of benign tumors in this area. Herein, we describe a case of primary tracheobronchial amyloidosis which obstructed almost completely the distal trachea and the main left bronchus.
The mass was successfully resected by mechanical resection and Nd-YAG laser coagulation during rigid bronchoscopy. Afterwards, a self-expanding Y-stent of new generation was inserted to restore airway patency. Five months later, radiological and bronchoscopic findings showed the stent in site, with normal patency of the tracheo-bronchial tree.
- •
El depósito de amiloide con oclusión casi completa del árbol traqueobronquial es excepcional.
- •
Se ha descrito su tratamiento con resección endoscópica, radioterapia o fotorresección con láser.
- •
La resección mecánica endoscópica con coagulación con láser Nd-YAG e implantación de una prótesis puede ser una intervención apropiada.
- •
La prótesis preserva la permeabilidad de la vía aérea y previene la recidiva del depósito de amiloide.
La amiloidosis se caracteriza por un depósito extracelular de proteínas fibrilares insolubles en órganos y tejidos. El depósito de amiloide en el árbol traqueobronquial es una forma de presentación muy poco frecuente y supone alrededor del 1% de los tumores benignos de esta zona1. Describimos un caso de amiloidosis traqueobronquial localizada que fue tratado con éxito mediante resección mecánica y coagulación con láser utilizando una broncoscopia rígida; a continuación se realizó una implantación de una prótesis en Y metálica recubierta, autoexpansible.
Caso clínicoUna mujer de 67años, no fumadora, fue ingresada en nuestro hospital por tos, dificultad respiratoria y hemoptisis. La paciente había apreciado los síntomas durante los últimos 7meses. La disnea había progresado hasta el punto de que solamente podía caminar una manzana sin detenerse. Durante este tiempo tuvo una tos productiva (anteriormente la tos no se acompañaba de producción de esputo) asociada ocasionalmente a pequeñas estrías de sangre en el esputo. Sin embargo, la hemoptisis no era masiva.
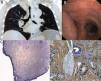
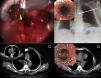
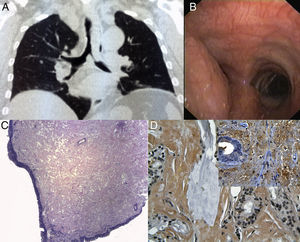
La paciente no refería ningún antecedente patológico de interés. Los análisis de laboratorio y de sangre estuvieron dentro de los límites normales. A la exploración se observó estridor y una reducción de la expansión del hemitórax izquierdo. La radiografía de tórax fue normal, pero la TC reveló una estenosis traqueobronquial grave (fig. 1A). El examen endoscópico mostró una masa que obstruía en un 80% la tráquea en la parte distal y casi en su totalidad el bronquio principal izquierdo. La mucosa estaba enrojecida y era frágil (fig. 1B). La masa remedaba una lesión neoplásica, pero las muestras de biopsia fueron diagnósticas de amiloidosis. La tinción de hematoxilina y eosina mostró la presencia de un material amorfo dentro del epitelio normal (fig. 1C) que se teñía selectivamente con rojo Congo (fig. 1D). Se consideró que el objetivo principal era el restablecimiento de la permeabilidad de la vía aérea. Se practicó a la paciente una broncoscopia rígida bajo sedación consciente, además de anestesia tópica con lidocaína; se extirpó la masa por completo mediante resección mecánica y coagulación con láser Nd-YAG (fig. 1A); a continuación de introdujo una prótesis en Y con recubrimiento, autoexpansible, de nueva generación (Micro-tech®, Nanjing, Co, Ltd., Shanghai, China). Se aseguró una colocación correcta mediante la introducción de una guía en cada bronquio principal (recuadro de la fig. 2A). La intervención fue bien tolerada y los síntomas respiratorios desaparecieron rápidamente. Los exámenes radiológico (fig. 2B) y endoscópico (recuadro de la fig. 2B) confirmaron la expansión completa del dispositivo.
La TC de tórax muestra: A) Una masa con una estenosis de la tráquea en la parte distal (longitud de 5cm) y del bronquio principal izquierdo. B) La visualización endoscópica muestra una masa que protruye de la pared lateral de la tráquea distal, causando una considerable oclusión de la tráquea y del orificio del bronquio principal izquierdo. C) La mucosa traqueal está engrosada por la presencia de una sustancia amorfa, a pesar de estar recubierta por un epitelio normal (tinción de hematoxilina y eosina, 40×). D) La sustancia amorfa se tiñe selectivamente con rojo Congo (400×). Recuadro: detección de amiloide P con el empleo de métodos inmunohistoquímicos (400×).
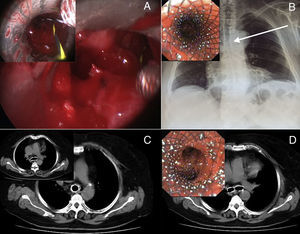
Tras la resección completa de la masa (A), la colocación de la prótesis en Y se aseguró mediante la introducción de una guía en cada bronquio principal (recuadro de A). Las observaciones realizadas en la radiografía de tórax (B, flecha blanca) y en la endoscopia (recuadro de B) confirmaron la expansión completa del dispositivo. Cinco meses después, la TC (C y D) y la broncoscopia (recuadro de la parte D) mostraron una permeabilidad normal del árbol traqueobronquial, sin recidiva del depósito de amiloide.
A continuación se investigó el tipo de amiloidosis AL (primaria) mediante la identificación de cadenas ligeras monoclonales utilizando electroforesis de inmunofijación (IFE) en suero y/u orina. Se obtuvo también una biopsia de médula ósea con aguja gruesa para identificar la discrasia de células plasmáticas subyacente y descartar un mieloma de células plasmáticas2. Los resultados de la IFE no confirmaron la presencia de una gammapatía monoclonal; y la biopsia de médula ósea no mostró un depósito de amiloide. En consecuencia, no estaba indicado un tratamiento más agresivo con el empleo de dosis altas de melfalán y autotrasplante de células madre3. Se aplicó fisioterapia, tratamiento de inhalación y medicación mucolítica para facilitar la expectoración y prevenir la formación de tapones en la prótesis de la bifurcación traqueal.
Cinco meses más tarde, la paciente evolucionaba bien; la TC (fig. 2C,D) y el examen broncoscópico (recuadro de la fig. 2D) mostraron una permeabilidad normal del árbol traqueobronquial, sin recidiva del depósito amiloide.
DiscusiónLa amiloidosis respiratoria puede manifestarse en forma de una enfermedad parenquimatosa difusa (el subgrupo de peor pronóstico), un nódulo en el parénquima (que es con frecuencia un hallazgo casual) o una amiloidosis (laringo)traqueobronquial, que puede mostrar una progresión y llevar a una obstrucción de las vías aéreas1. El caso presentado corresponde a este tercer subgrupo. La cirugía de reducción de la masa puede aliviar la obstrucción de vías aéreas causada por los depósitos de amiloide, pero no previene las recidivas. Después de la extirpación de una masa aislada, las recidivas son muy poco frecuentes. Se han descrito también otros tratamientos, como la neumectomía, la radioterapia o la fotorresección con láser4.
La forma de presentación inicial aguda de este caso es poco habitual. La amiloidosis se manifestó por una masa aislada, que sugería claramente una enfermedad maligna, causante de una oclusión casi completa de la parte distal de la tráquea y del bronquio principal izquierdo. La lesión de la vía aérea central no era susceptible de tratamiento con cirugía; la extirpación endobronquial era el único tratamiento que permitía restablecer la permeabilidad de la vía aérea. Sin embargo, estas lesiones recidivan con frecuencia en un plazo de 12meses tras la resección, y existe un riesgo elevado de perforación o estenosis traqueobronquial cicatrizal. Puede producirse una hemorragia durante la cirugía, y se han descrito casos mortales5. En consecuencia, realizamos una resección de la masa con el empleo de láser Nd-YAG; tras la recanalización completa de la vía aérea, implantamos una prótesis en Y, metálica con recubrimiento, autoexpansible. Aunque no se ha publicado ningún artículo que describa el uso de una prótesis tras una resección de amiloide, consideramos que su uso podía ser ventajoso para preservar la permeabilidad de la vía aérea y prevenir la recidiva de depósito de amiloide.
Optamos por una prótesis autoexpansible en vez de una de silicona, debido al mayor diámetro transversal de la vía aérea a causa de la pared más fina, y la mejor conformación en vías irregulares como consecuencia de la fuerza autoexpasiva. Por lo demás, esta prótesis imita una tráquea normal y tiene una mejor eliminación de las secreciones6.
El tamaño de la prótesis (longitud y diámetro) se estableció mediante el examen endoscópico previo y la TC de tórax tridimensional. Se prefirió el uso de una prótesis con recubrimiento para evitar el crecimiento de amiloide a través de la malla. Además, las prótesis con recubrimiento pueden ser retiradas de manera efectiva y segura, sin que se produzcan complicaciones importantes, en caso necesario7.
Los resultados de la IFE no confirmaron la presencia de una gammapatía monoclonal, y la biopsia de médula ósea no mostró depósito de amiloide. Así pues, en este caso no estaba indicado un tratamiento más agresivo con el empleo de dosis altas de melfalán y autotrasplante de células madre2. Se utilizó fisioterapia y medicación inhalada y mucolítica para prevenir la formación de un tapón en la prótesis8.
En conclusión, nuestra experiencia pone de manifiesto que la amiloidosis puede ser una forma de presentación poco habitual de la obstrucción traqueobronquial que remede un carcinoma broncógeno; la resección endoscópica con láser e implantación de una prótesis puede ser un tratamiento apropiado.