La serotonina es un potente vasoconstrictor y factor de proliferación vascular pulmonar cuya concentración se incrementa en pacientes con hipertensión arterial pulmonar (HAP). Sus funciones están mediadas en parte por la proteína transportadora de serotonina (SERT), cuyo gen puede presentar dos formas alélicas, una larga (L) y otra corta (S). La primera se ha asociado a mayor función.
ObjetivosConocer si la prevalencia de la forma alélica L del gen de SERT es mayor en pacientes con HAP que en población general. Ver si existe alguna diferencia clínica en los pacientes con HAP en función del alelo SERT.
MétodosSe incluyeron pacientes diagnosticados de HAP con cateterismo en base a los criterios establecidos. Se extrajo una muestra de sangre periférica y posteriormente el ADN de los leucocitos periféricos. Se amplificó la región promotora de SERT mediante reacción en cadena de polimerasa y se separaron los productos mediante electroforesis. Se compararon las muestras de los pacientes con 50 controles sanos y entre los tipos más frecuentes de HAP (idiopática, tromboembólica y asociada a conectivopatías). Se valoraron diversas variables clínicas en función de los diversos alelos del gen SERT.
ResultadosSe incluyó a 50 pacientes, y se obtuvo muestra adecuada en 49 (30mujeres). La edad media en el momento del diagnóstico fue 56±16 años. No se observaron diferencias en la distribución de alelos entre pacientes y controles (p=0,54). Tampoco existieron diferencias entre los tres tipos más frecuentes de HAP (p=0,3). La forma más frecuente fue LS (54% pacientes, 56% controles). Tanto la edad de diagnóstico como la respuesta al tratamiento no fueron diferentes en función de los alelos SERT. Hubo una tendencia a presentar mayores valores de la presión pulmonar media en las formas LL (49±5 vs. 42±9mmHg, p=0,07).
ConclusionesLa distribución de los alelos del gen SERT no parece ser diferente en los pacientes con HAP de cómo se presenta en la población normal. Diversos tipos de HAP tienen una distribución de alelos similar. Las formas LL no parecen conferir diferencias clínicas ni de respuesta al tratamiento.
Serotonin is a potent vasoconstrictor and pulmonary vascular growth factor whose concentration is increased in patients with pulmonary arterial hypertension (PAH). Its functions are mediated in part by the serotonin transporter protein (SERT) whose gene can have two allelic forms, both long (L) and short (S). The first was associated with greater function.
ObjectivesTo determine whether the prevalence of the L allelic form of SERT is higher in patients with PAH than in the general population. To observe whether there are any clinical differences in patients with PAH based on the SERT allele.
MethodsWe included patients diagnosed with PAH with catheterization based on the established criteria. Peripheral blood samples were taken and the DNA was extracted from the peripheral leukocytes. We amplified the promoter region of SERT by polymerase chain reaction and separated the products by electrophoresis. The patient samples were compared with samples from 50 healthy controls and among the most common types of PAH (idiopathic, thromboembolic and associated with connective tissue disorders). Several clinical variables were assessed according to the SERT gene alleles.
ResultsThe study included 50 patients, and adequate samples were obtained in 49 (30 women). Mean age at diagnosis was 56±16 years. No differences were seen in the distribution of alleles between patients and controls (P=.54). There were no differences among the three most common types of PAH (P=.3). The most frequent allelic form was LS (54% patients, 56% controls). There were no differences in either age of diagnosis or response to treatment according to the SERT alleles. There was a trend toward higher mean pulmonary pressure levels in the LL forms (49±5 vs 42±9mmHg, P=.07).
ConclusionsThe distribution of SERT gene alleles does not appear to be different in patients with PAH than in the normal population. Different types of PAH have a similar distribution of alleles. The LL forms do not appear to confer either clinical differences or differences in response to treatment.
La hipertensión arterial pulmonar (HAP) es una grave enfermedad en la que se produce un aumento progresivo de las resistencias vasculares pulmonares, manteniéndose normal la presión en el corazón izquierdo. Aunque no se conoce por completo la patogenia de la enfermedad, la investigación que ha tenido lugar en los últimos años ha permitido desvelar algunas de las vías celulares implicadas en el desarrollo de las lesiones características de la HAP. En el año 2000 se produjo uno de los hallazgos más importantes al desvelarse que la alteración genética responsable de las formas hereditarias se situaba en el gen que codifica BMPR2, uno de los receptores de las proteínas morfogenéticas del hueso1,2. Desde entonces se ha realizado una intensa búsqueda de posibles genes relacionados con la regulación vascular. La serotonina juega un papel crucial, y tiene además un importante efecto estimulante de la proliferación de células musculares lisas de la vasculatura pulmonar3. Hace ya algunos años se describió un incremento de la concentración plasmática de serotonina en 16 pacientes con HAP idiopática4. Para ejercer estas acciones puede actuar de dos formas: uniéndose a receptores específicos de la membrana celular o introduciéndose en el citoplasma gracias a la acción de la proteína transportadora de serotonina (SERT). Este último mecanismo de acción es el responsable de los efectos proliferativos5.
El gen SERT está localizado en el cromosoma 17 y consta de 14 exones que suman 31 kilobases. La parte promotora del gen puede tener dos variantes, una larga (L) y otra corta (S), situadas a una distancia de una kilobase de la zona de inicio transcripcional, que consiste en la inserción (formasL) o la deleción (formasS) de 44 pares de bases. La presencia del alelo L se asocia con una actividad transcripcional entre 2 y 3 veces superior al alelo S. En pacientes con enfermedad pulmonar obstructiva crónica el alelo LL se correlacionó con valores más elevados de presión arterial pulmonar6. Existe cierta disparidad de resultados en los escasos estudios realizados sobre la distribución de los genotipos SERT en pacientes con HAP en comparación con la población general, así como de su impacto en la forma de presentación y evolución de la enfermedad. Algún trabajo parece mostrar un incremento de las formas LL7. El objetivo de nuestro estudio fue conocer si los pacientes con HAP podrían tener mayor prevalencia de este genotipo LL y si ello guarda relación con la gravedad de la enfermedad.
Material y métodosLa población de estudio consistió en 50 pacientes consecutivos diagnosticados de HAP tanto idiopática como secundaria y 50 controles sanos (25 mujeres y otros tantos varones) seleccionados de forma aleatoria del Centro de Transfusión de Sangre de Galicia. El diagnóstico de HAP se basó en un cateterismo derecho con una presión arterial pulmonar media (PAPm) ≥25mmHg y una presión de enclavamiento inferior a 15mmHg sin tratamiento específico. En todos los casos se siguió el protocolo de manejo habitual acorde a las recomendaciones de la ERS/ESC8. Los pacientes se encontraban estables en el momento de la realización del cateterismo. Tanto los pacientes como los controles fueron informados detalladamente del estudio y dieron su consentimiento por escrito para participar en él. El comité ético local dio su aprobación al estudio.
Estudios de laboratorioSe realizó una extracción de sangre y se obtuvo el ADN de leucocitos periféricos mediante el kit FlexiGene DNA de Qiagen (Alemania). Para la amplificación de 50ng de ADN mediante reacción en cadena de la polimerasa (PCR) de la región promotora se utilizaron los siguientes primers:
5′GGCGTTGCCGCTCTGAATGC3′
5′GAGGGACTGAGCTGGACAACCAC3′
La amplificación se llevó a cabo en un medio con 1,5mM de MgCl2, con 0,2U de Taq polimerasa (Biotaq, Bioline, Reino Unido) y 35 ciclos de desnaturalización a 95°C durante 1min, anillamiento a 65°C durante 1min y una extensión a 72°C durante 1min. Los productos de la amplificación se separaron mediante electroforesis en un gel de agarosa al 2% teñido con bromuro de etidio. De los fragmentos obtenidos, el de 484 pares de bases (pb) corresponde al alelo S, mientras el fragmento de 528 pb corresponde al alelo L. Finalmente se realizó una electroforesis de los fragmentos amplificados (alelos S y L).
Correlación genotipo/clínicaEl objetivo primario fue conocer la prevalencia del genotipo LL en los pacientes con HAP en comparación con controles sanos. Por estudios previos parece que solo las formas LL tienen un incremento significativo de la acción de transporte de SERT9, por lo que comparamos esta forma genotípica con las otras dos (LS y SS), que parecen ser similares en este aspecto. Para conocer el impacto de la presencia de este polimorfismo en la presentación clínica comparamos la edad de diagnóstico, los valores de PAPm y la respuesta terapéutica en función del genotipo SERT. Para ello se valoraron los pacientes que alcanzaron al menos un año de seguimiento desde el inicio del tratamiento. Consideramos buena respuesta un incremento mayor de 50m en la distancia recorrida en el test de 6min de marcha o una mejoría de al menos una clase funcional a los 12meses del inicio del tratamiento. Dado el escaso número de fallecidos, no fue posible hacer curvas de supervivencia.
Análisis estadísticoTodos los valores están expresados como media±DS. Dado el tamaño de la muestra, las medias se compararon mediante test no paramétricos (test de Wilcoxon). La realización del cateterismo fue considerado el momento del diagnóstico. Las variables categóricas se analizaron mediante el test de Chi cuadrado, y se consideró significativo un valor igual o inferior a 0,05. Todos los análisis se realizaron con el programa estadístico SPSS versión 15.0 (SPSS, Inc., Chicago IL, EE. UU.).
ResultadosDe los 50 pacientes incluidos en el estudio, en 49 fue posible analizar correctamente el polimorfismo. De ellos, 14 correspondieron a HAP idiopática, 13 a HAP asociada a conectivopatías, 14 a enfermedad tromboembólica crónica, 4 casos estuvieron relacionados con cardiopatías congénitas, 2 estaban asociados a virus de la inmunodeficiencia humana, un caso a HAP con hipertensión portal y otro a enfermedad pulmonar obstructiva crónica (tabla 1). La edad en el momento del diagnóstico fue de 56±16 años (extremos, 25-78 años), siendo 30 mujeres y 19 varones.
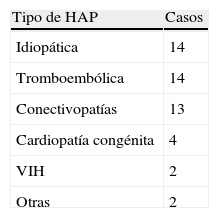
Tipos de hipertensión arterial pulmonar (HAP)
| Tipo de HAP | Casos |
| Idiopática | 14 |
| Tromboembólica | 14 |
| Conectivopatías | 13 |
| Cardiopatía congénita | 4 |
| VIH | 2 |
| Otras | 2 |
VIH: virus de la inmunodeficiencia humana.
Los tres tipos más frecuentes de HAP en nuestros pacientes fueron la idiopática, la tromboembólica y la asociada a conectivopatías. En el apartado otras se incluyeron una hipertensión porto-pulmonar y un caso asociado a enfermedad pulmonar obstructiva crónica.
La distribución de genotipos SERT no varió entre el grupo de controles y de pacientes (LL: 20% vs. 30%, p=0,54) (tabla 2). Tampoco se observaron diferencias entre los tres tipos predominantes de HAP (p=0,3) (tabla 3). El genotipo más frecuente fue el LS (54% de pacientes, 56% de controles), y aunque dentro del grupo de pacientes se observó una mayor frecuencia de genotipo LL en varones que en mujeres (25% vs. 14,8%), no alcanzó significación estadística (p=0,33).
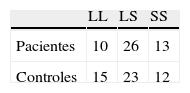
Distribución de los alelos SERT en pacientes y controles sanos
| LL | LS | SS | |
| Pacientes | 10 | 26 | 13 |
| Controles | 15 | 23 | 12 |
La distribución de los 3 alelos no mostró diferencias entre pacientes y controles (p=0,54). Al comparar el alelo LL vs. no LL tampoco existieron diferencias (p=0,27). En ambos grupos la forma LS fue la más frecuente.
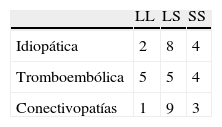
Distribución de los alelos SERT en los tres tipos más frecuentes de hipertensión arterial pulmonar (HAP)
| LL | LS | SS | |
| Idiopática | 2 | 8 | 4 |
| Tromboembólica | 5 | 5 | 4 |
| Conectivopatías | 1 | 9 | 3 |
Tampoco se observaron diferencias en la distribución de los alelos SERT entre las tres formas predominantes de HAP (p=0,3).
No hubo diferencias en la edad de diagnóstico (LL: 57±13 vs. 57±12 años, p=0,56). Se observó una tendencia a presentar mayores valores de PAPm en los pacientes con el genotipo LL, aunque sin llegar a la significación estadística (49±5 vs. 42±9mmHg, p=0,07). En 34 pacientes el periodo de seguimiento alcanzó al menos un año. En 18 casos hubo buena respuesta al tratamiento. La distribución de formas LL o no LL no varió en función de ser o no respondedores (p=0,8). Se produjeron únicamente 3 fallecimientos durante el periodo de seguimiento, todos ellos en pacientes con genotipos no LL.
DiscusiónEn nuestra serie de pacientes la distribución de alelos del gen SERT fue similar a la encontrada en controles sanos. Tampoco se observaron diferencias entre los tres tipos más frecuentes de HAP ni entre sexos. La presencia de LL tampoco se asoció a un comportamiento distinto de la enfermedad en general a pesar de una cierta tendencia a tener un valor más elevado de la PAPm, parámetro que en la mayor parte de los trabajos no se correlaciona con la supervivencia10,11. La presencia de un tipo u otro de genotipos SERT tampoco influyó en la respuesta terapéutica a medio plazo.
Existen numerosos trabajos que parecen demostrar un papel muy importante de la serotonina en la patogenia de la HAP12. Hace ya algunos años se describió la «hipótesis de serotonina de la HAP», ya que el mecanismo de acción de algunos fármacos inhibidores del apetito —como el aminorex y la desfenfluramina— ligados a la aparición de esta enfermedad consistía en inhibición de la recaptación neuronal de serotonina y, por tanto, mayor secreción y estimulación de sus receptores13. La serotonina estimula la proliferación de células musculares lisas y fibroblastos de los vasos pulmonares y, si se cultivan con ella, estas células extraídas de pacientes con HAP proliferan con mucha mayor intensidad que las de controles sanos14. La vía de la serotonina es compleja y está influida por su síntesis, sus receptores y la proteína transportadora SERT15. Hace ya algunos años se descubrió la existencia de una variante en la región promotora del gen SERT, con un alelo largo que incrementaba la transcripción respecto a otro más corto. Un estudio inicial mostró mayor prevalencia del genotipo LL en pacientes con HAP7. Sin embargo, otros trabajos con mayor número de pacientes no encontraron diferencias con la población general. Un estudio franco-estadounidense que incluyó a 166 pacientes con HAP hereditaria y 83 con HAP idiopática no observó diferencias en la distribución de los tres genotipos SERT en comparación con 125 controles sanos. La forma LS, al igual que en nuestros pacientes, fue la más frecuente El único hallazgo relevante fue la aparición de la enfermedad en una edad inferior en los casos de HAP hereditaria si eran portadores del genotipo LL16. En los que presentaban HAP idiopática la edad de inicio fue similar, algo que también sucedió en nuestra serie. Los resultados no variaron al analizar la presencia de mutaciones en el receptor tipo 2 de las proteínas morfogenéticas del hueso (BMPR2). En nuestro estudio solo 3 pacientes de los 9 en los que estudiamos este gen eran portadores de alguna mutación, por lo que no pudimos hacer comparaciones. No hubo diferencias de supervivencia en función de genotipo SERT. En nuestra serie solo pudimos analizar la respuesta al tratamiento en 34 pacientes (70%), ya que en los demás el seguimiento era inferior a un año, sin que se encontrasen diferencias entre genotipos. Dado que solo se produjeron 3 fallecimientos, no fue posible hacer un análisis de supervivencia en función del genotipo SERT. Otro estudio realizado por Machado et al.17 sobre una amplia base de pacientes que incluyó formas familiares, idiopáticas y asociadas tampoco encontró diferencias en la distribución de los genotipos SERT. En este caso, la edad de inicio de la enfermedad en las formas familiares no mostró diferencias con las no familiares, en contraposición al anterior estudio. Al igual que en nuestro caso, una comparación por sexos tampoco presentó distinta distribución de los genotipos SERT. Es posible que en algunos tipos específicos de HAP la proteína SERT pueda tener un papel más relevante. Un trabajo ya comentado anteriormente y realizado en Francia y Reino Unido, en el que se incluyeron 103 pacientes diagnosticados de enfermedad pulmonar obstructiva crónica grave (FEV1 medio 37% del valor teórico), no encontró diferencias con los controles en la distribución de los genotipos SERT, aunque, como hallazgo más importante, la enfermedad fue más grave en los que portaban la forma LL que en las LS o SS (PAPm 34±3, 23±1 y 22±1mmHg, respectivamente, p<0,01)6. Ello se corresponde en parte con nuestros resultados, aunque en este caso sin alcanzar significación estadística. En este estudio la expresión de ARN mensajero para serotonina en las células musculares de las arterias pulmonares fue más del doble en los pacientes con formas LL que en los que tenían cualquier otra forma y, a su vez, si se sometían a hipoxia, un potente estimulante de la serotonina, las formas LL tenían 5 veces más expresión que las formas SS normóxicas. Todos estos datos hablan a favor del papel importante que la serotonina y sus vías de actuación pueden tener en la génesis de las lesiones que subyacen en la HAP.
La contribución del genotipo LL de SERT como favorecedor/agravante de HAP es difícil de cuantificar. Es muy probable que diversos factores genéticos estén implicados en el desarrollo de la enfermedad, y ello unido muy probablemente a factores ambientales. No es fácil diseñar estudios sobre posibles genes candidatos que tengan en cuenta el gran número de variables exógenas que podrían influir en la aparición y la evolución de la HAP. Ello, sumado a la baja prevalencia de esta enfermedad que dificulta incluir un número elevado de pacientes, puede dar lugar a sesgos significativos con resultados difíciles de interpretar. Por todas estas razones, creemos de gran importancia seguir realizando estudios genéticos para poder llegar a establecer perfiles de riesgo y abrir nuevas vías terapéuticas. Con los datos disponibles no parece que este polimorfismo en el gen SERT tenga un papel relevante en la aparición de HAP. Quizá las formas LL pudieran ser un factor agravante más que favorecedor de la enfermedad en algún tipo de pacientes, sobre todo si se asocian a hipoxia, algo que debería ser explorado.
Una de las limitaciones más importantes de nuestro estudio es el pequeño número de pacientes. Como ya hemos comentado, la HAP es una enfermedad con una baja prevalencia, estimada en torno a 15 casos por millón de habitantes18, lo que hace difícil reunir una muestra muy amplia. Es posible que los resultados fueran otros si el número de pacientes fuera mayor, pero la coincidencia de nuestros hallazgos con los obtenidos en las últimas publicaciones confiere un mayor crédito. En comparación con las otras series más grandes, donde se analizaron muestras de diferentes países con dificultad para obtener datos en un número importante de casos, nosotros dispusimos de toda la información clínica.
En conclusión, a pesar de las evidencias que otorgan al gen SERT y, sobre todo, a su forma LL un papel destacado en las acciones de la serotonina como posible candidato a incrementar la susceptibilidad para desarrollar HAP, no hemos podido demostrar un mayor número pacientes portadores de este alelo en comparación con la población general ni una asociación clara con la gravedad de la enfermedad.
FinanciaciónEste trabajo ha sido realizado gracias a una beca de investigación de Actelion.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.