La medición de la capacidad de difusión del monóxido de carbono postoperatorio (ppoDLCO) es esencial para la operabilidad del paciente y la estratificación del riesgo de aquellos subsidiarios de una resección pulmonar mayor por cáncer. Los estudios que fijan los límites de riesgo quirúrgico se basan en series de cirugía abierta. El objetivo de nuestro trabajo es analizar la morbimortalidad en relación con la ppoDLCO y comparar su comportamiento en cirugía abierta y cirugía torácica videoasistida (VATS).
MétodosComparación de la mortalidad a 90 días y la morbilidad en pacientes intervenidos por cirugía abierta frente a VATS en relación con el descenso de la ppoDLCO. Emparejamiento por puntaje de propensión (variables: edad, ASA, vasculopatía arterial, IMC, sexo, estadio, ppoDLCO y ppoFEV1) para realizar grupos comparables entre cirugía abierta y VATS.
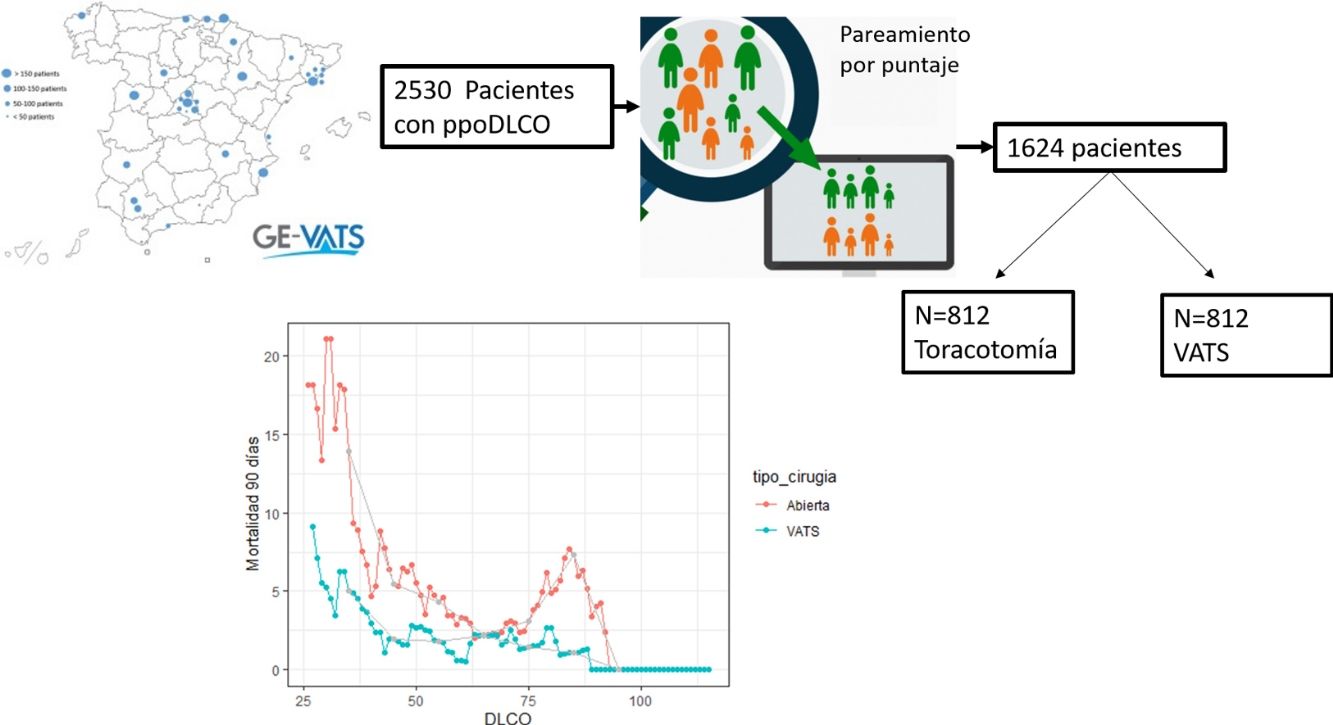
ResultadosDe 2.530 pacientes con cáncer de pulmón y medición de ppoDLCO, se obtiene tras el emparejamiento por puntaje una muestra de 1.624 (812 por grupo). El riesgo relativo de mortalidad de la toracotomía para una ppoDLCO<60 es de 2,66 (p<0,02) respecto a la VATS. Tanto para la morbilidad total como para la cardíaca y respiratoria, el riesgo de la toracotomía es superior a la de VATS para casi todos los valores de ppoDLCO.
ConclusionesLa resección mayor por VATS muestra una morbimortalidad inferior para una misma ppoDLCO. El aumento continuo del riesgo de mortalidad empieza a darse en valores de ppoDLCO superiores en toracotomía (∼60) que en VATS (∼45).
Measuring predicted post-operative diffusion capacity of the lung for carbon monoxide (ppoDLCO) is essential to determine patient operability and to stratify the risk of patients who are candidates for major lung cancer surgery. Studies that established surgical risk variables were based on open surgery series. The aim of our study was to analyze morbidity and mortality as a function of ppoDLCO and to compare its behavior in open and video-assisted thoracic surgery (VATS).
MethodsWe compared 90-day mortality and morbidity in patients undergoing open surgery versus VATS as a function of decline in ppoDLCO. Propensity score matching (using age, ASA, arterial vascular disease, BMI, sexo, stage, ppoDLCO, and ppoFEV1) was applied to create comparable open surgery and VATS groups.
ResultsOf 2,530 patients with lung cancer and ppoDLCO values, a sample of 1,624 (812 per group) was obtained after score matching. The relative risk of mortality associated with thoracotomy in patients with ppoDLCO<60 is 2.66 (P<.02) compared to VATS. The risk of thoracotomy in terms of overall and cardiac and respiratory morbidity is higher than that of VATS for almost all ppoDLCO values.
ConclusionsMajor resection by VATS shows lower morbidity and mortality in patients with the same ppoDLCO. A steady rise in the risk of mortality begins to occur at higher ppoDLCO values in thoracotomy (∼60) than in VATS (∼45).
Las pruebas de función respiratoria continúan siendo la base en el estudio preoperatorio para resección pulmonar. Dentro de ellas, la medición de la capacidad de difusión del monóxido de carbono (DLCO) y la estimación de la capacidad de difusión del monóxido de carbono postoperatoria (ppoDLCO) se consideran esenciales para estratificar el riesgo en pacientes con y sin EPOC1,2. Asimismo, para la estratificación del riesgo en las guías para el estudio preoperatorio se recomienda su uso3,4. Sin embargo, la mayoría de los trabajos para el estudio preoperatorio están realizados en pacientes intervenidos por toracotomía y son pocos los realizados en pacientes con cirugía mínimamente invasiva4–6. En modelos predictivos como el EUROLUNG, donde se incluyen las cirugías torácicas videoasistidas (VATS), este abordaje ha presentado menor tasa de complicaciones que la cirugía abierta7. En esa línea algunos estudios demuestran que pacientes con DLCO bajas pueden ser intervenidos por cirugía mínimamente invasiva de forma segura8.
A partir de una base de datos nacional del Grupo Español de Cirugía Torácica Video-asistida (GEVATS)9, hemos analizado si el abordaje toracoscópico sigue una curva de morbimortalidad en relación con la ppoDLCO diferente a la cirugía abierta.
Material y métodosSe han analizado los datos de la base de datos GEVATS, promovida por la Sociedad Española de Cirugía Torácica, en la cual se han seleccionado pacientes con resecciones pulmonares anatómicas desde el 20-12-2016 hasta el 20-03-20188. Esta base de datos incluye prospectivamente pacientes de 33 centros de cirugía torácica, siendo el estudio aprobado en los comités de ética de todos los centros participantes.
La ppoDLCO se ha calculado de forma automática y teniendo en cuenta el número de segmentos resecados en cirugías previas, utilizando el método anatómico mediante la ecuación ppoDLCO=DLCO×(19–segmentos resecados en cirugías previas–segmentos funcionantes resecados/19–segmentos no funcionantes–segmentos resecados en cirugías previas).
Se han definido como variables resultado la mortalidad hospitalaria y la mortalidad a los 90 días. Dentro de las complicaciones cardíacas se han definido como tales la arritmia auricular, la insuficiencia cardíaca, el infarto agudo de miocardio, el accidente cerebrovascular y la trombosis venosa profunda. Se consideraron complicaciones respiratorias la ventilación mecánica prolongada, la reintubación, la fuga aérea prolongada>5 días, la atelectasia, el neumotórax y/o el derrame pleural, la neumonía, el síndrome de distrés respiratorio del adulto, la fístula broncopleural, el empiema, el quilotórax y el tromboembolismo pulmonar. Se ha creado una variable que comprende todas las complicaciones respiratorias y otra en la que se han excluido la fuga aérea, la fístula broncopleural y el quilotórax. Se ha realizado esta subdivisión con el objetivo de disminuir el peso de la fuga aérea, la fístula broncopleural y el quilotórax del resto de las complicaciones respiratorias más graves, por considerarlas más relacionadas con la técnica quirúrgica que con la ppoDLCO del paciente.
Las variables preoperatorias continuas fueron descritas con la media y la desviación estándar, y las categóricas con la frecuencia y el porcentaje. Las comparaciones entre las variables preoperatorias continuas se llevaron a cabo mediante la prueba de los rangos con signo de Wilcoxon, ya que en ningún caso presentaron normalidad las 2 categorías comparadas. Las comparaciones entre variables categóricas se realizaron mediante la prueba exacta de Fisher. Se ha utilizado una p<0,05 como punto de corte de la significación estadística.
Para comparar las diferencias entre los tipos de operación abierta y VATS, se realizó un emparejamiento por puntaje de propensión para cada variable de morbimortalidad analizada. Para ello, se empleó el método Optimal de la librería MatchIt de R10, que realiza enlaces minimizando la distancia absoluta promedio en todos los pares coincidentes. Las distancias entre las muestras de los 2 grupos se calcularon mediante el método logit. Se descartaron los pacientes no emparejados y aquellos emparejados con una distancia superior a 0,05. Las variables con las que se realizó el emparejamiento por puntaje de propensión fueron seleccionadas en función de su importancia clínica y significación estadística: edad, ASA, vasculopatía arterial, IMC, sexo, volumen espiratorio forzado en el primer segundo postoperatorio (ppoFEV1), ppoDLCO y estadio TNM.
Para calcular la proporción de los eventos de las variables de morbimortalidad en función de ppoDLCO, se realizó un suavizado mediante una media móvil central con un rango de±5 valores de ppoDLCO.
ResultadosDe los 3.533 casos recogidos en la base de datos, 3.085 han sido incluidos con diagnóstico de cáncer de pulmón, de los cuales 2.530 (82%) tienen el registro del dato de DLCO. Estos últimos representan la muestra que hemos analizado. En primer lugar, se han descrito las variables basales de los pacientes y su distribución entre el grupo de cirugía abierta y cirugía VATS.
Las características de los pacientes a estudio se presentan en la tabla 1.
Características basales de los paciente a estudio
| Variable | Total (n=2.530) | Abierta (n=1.060) | VATS (n=1.470) | p |
|---|---|---|---|---|
| Edad, media (DE) | 65,07 (9,9) | 64,71 (10,3) | 65,33 (9,6) | 0,306 |
| Sexo, n (%) | <0,001 | |||
| Femenino | 767 (30,3) | 272 (25,7) | 495 (33,7) | |
| Masculino | 1.763 (69,7) | 788 (74,3) | 975 (66,3) | |
| IMC, media (DE) | 26,957 (4,6) | 26,965 (4,5) | 26,952 (4,6) | 0,825 |
| Tabaquismo, n (%) | 0,208 | |||
| Fumador | 709 (28,5) | 295 (28,4) | 414 (28,5) | |
| Exfumador (<1 año) | 326 (13,1) | 136 (13,1) | 190 (13,1) | |
| Exfumador (>1 año) | 1.078 (43,3) | 468 (45,0) | 610 (42,0) | |
| Nunca ha fumado | 377 (15,1) | 140 (13,5) | 237 (16,3) | |
| HTA, n (%) | 0,180 | |||
| Sí | 1.111 (43,9) | 449 (42,4) | 662 (45,1) | |
| No | 1.417 (56,1) | 611 (57,6) | 806 (54,1) | |
| Insuficiencia cardíaca, n (%) | 0,666 | |||
| Sí | 60 (2,4) | 26 (2,4) | 34 (2,3) | |
| No | 2.469 (97,6) | 1.033 (97,5) | 1.436 (97,7) | |
| Cardiopatía isquémica, n (%) | 0,666 | |||
| Sí | 218 (8,6) | 88 (8,3) | 130 (8,8) | |
| No | 2.312 (91,4) | 972 (91,7) | 1.340 (91,2) | |
| Arritmia, n (%) | 0,296 | |||
| Sí | 200 (7,9) | 91 (8,6) | 109 (7,4) | |
| No | 2.329 (92,1) | 968 (91,4) | 1.361 (92,6) | |
| AIT, n (%) | 0,776 | |||
| Sí | 120 (4,7) | 52 (4,9) | 68 (4,6) | |
| No | 2.409 (95,3) | 1.007 (95,1) | 1.402 (95,4) | |
| Vasculopatía arterial, n (%) | 0,888 | |||
| Sí | 225 (8,9) | 93 (8,8) | 132 (9,0) | |
| No | 2.304 (91,1) | 966 (91,2) | 1.338 (91,0) | |
| Diabetes, n (%) | 0,084 | |||
| Tipo 1 | 44 (1,7) | 25 (2,4) | 19 (1,3) | |
| Tipo 2 | 414 (16,4) | 181 (17,1) | 233 (15,8) | |
| No | 2.071 (81,9) | 853 (80,5) | 1.218 (82,9) | |
| Niveles de creatinina>2, n (%) | 0,334 | |||
| Sí | 72 (2,8) | 26 (2,5) | 46 (3,1) | |
| No | 2.458 (97,2) | 1.034 (97,5) | 1.424 (96,9) | |
| FEV1(%), media (DE) | 89,431 (20,2) | 85,852 (18,9) | 92,016 (20,7) | <0,001 |
| CVF (%), media (DE) | 97,135 (19,1) | 94,321 (18,1) | 99,174 (19,5) | <0,001 |
| DLCO (%), media (DE) | 83,356 (20,9) | 81,912 (20,7) | 84,397 (21,0) | <0,001 |
| Estadio TNM, n (%) | <0,001 | |||
| 0-II | 1.803 (82,4) | 691 (75,0) | 1.112 (87,7) | |
| III-IV | 386 (17,6) | 230 (25,0) | 156 (12,3) | |
| ASA, n (%) | 0,021 | |||
| I | 54 (2,1) | 19 (1,8) | 35 (2,4) | |
| II | 1.069 (42,4) | 414 (39,2) | 655 (44,6) | |
| III | 1.338 (53,0) | 593 (56,2) | 745 (50,8) | |
| IV | 62 (2,5) | 30 (2,8) | 32 (2,2) | |
| Tiempo de cirugía (minutos), media (DE) | 183,17 (69,4) | 196,99 (76,8) | 173,25 (61,8) | <0,001 |
AIT: accidente isquémico transitorio; ASA: American Society of Anesthesiologists; CVF: capacidad vital forzada; DE: desviación estándar; DLCO: capacidad de difusión pulmonar; FEV1: volumen espiratorio forzado en el primer segundo; HTA: hipertensión arterial; IMC: índice de masa corporal; VATS: cirugía torácica videoasistida.
Como se observa en las características de los pacientes analizados, tanto la edad media como el IMC son similares en ambos grupos. Las comorbilidades más frecuentemente observadas son la HTA (44,5%) y la DM (18,5%), con una distribución similar en ambos grupos. Las demás comorbilidades se observan en menos del 10% de los pacientes y con una distribución similar.
En cambio, sí se han observado diferencias en la estadificación, donde un 68% del grupo VATS pertenece al estadio i, por un 44% en el grupo de toracotomías. Asimismo, el porcentaje de estadios iii alcanza el 23,5% en el grupo de toracotomías, no llegando al 11% en el grupo VATS.
Destaca que las complicaciones cardíacas se observan en un 6%, siendo la mayoría de las mismas arritmias auriculares (70,6% de todas las complicaciones cardíacas; 4,5% de los pacientes de la muestra a estudio). Tanto en la arritmia auricular como en la insuficiencia cardíaca se observan diferencias significativas, con mayor tasa en el grupo de cirugía abierta.
En cuanto a las complicaciones respiratorias, se observan en un 23%, siendo la fuga aérea (13%), la neumonía (4,5%) y la atelectasia (3,6%) las más frecuentes. En todas las complicaciones respiratorias excepto en la fuga aérea, el neumotórax y/o el derrame y el quilotórax se han observado diferencias significativas, con una mayor tasa de complicaciones en el grupo de toracotomías.
Para intentar crear grupos comparables se ha realizado un emparejamiento por puntaje de propensión de los pacientes del grupo de las toracotomías y VATS. Se han obtenido 2 grupos comparables para las variables consideradas clínicamente relevantes (edad, vasculopatía arterial e IMC) y las variables que en nuestra muestra se distribuían asimétricamente con diferencias significativas entre el grupo de toracotomías y de VATS (ASA, sexo, estadio TNM). Tras el emparejamiento por puntaje de propensión se obtiene una muestra de 812 pacientes por grupo (n total=1.624). En la tabla 2 se muestran las características de las variables de la muestra obtenida tras realizar el emparejamiento por puntaje y se comparan las diferencias estandarizadas y los valores de p- de la nueva muestra con los valores obtenidos con la muestra anterior al emparejamiento.
Características de las variables tras el emparejamiento por puntaje
| Variable | Muestra posterior al emparejamiento por puntaje | Muestra anterior al emparejamiento por puntaje | ||||
|---|---|---|---|---|---|---|
| Abierta (n=812) | VATS (n=812) | p | Diferencia estandarizada | p- | Diferencia estandarizada | |
| Edad, media (DE) | 65,43 (10,3) | 65,60 (9,0) | 0,589 | −0,016 | 0,307 | −0,072 |
| ASA, n (%) | 0,021 | |||||
| I | 14 (1,7) | 13 (1,6) | 0,010 | −0,045 | ||
| II | 332 (40,9) | 318 (39,2) | 0,885 | 0,035 | −0,100 | |
| III | 445 (54,8) | 461 (56,8) | −0,040 | 0,098 | ||
| IV | 21 (2,6) | 20 (2,5) | 0,008 | 0,034 | ||
| Vasculopatía arterial, n (%) | −0,017 | 0,888 | −0,013 | |||
| Sí | 79 (9,7) | 83 (10,2) | 0,804 | |||
| No | 733 (90,3) | 729 (89,8) | ||||
| IMC, media (DE) | 26,89 (4,5) | 26,83 (4,6) | 0,616 | 0,014 | 0,825 | −0,019 |
| Sexo, n (%) | 0,006 | <0,001 | 0,185 | |||
| Femenino | 208 (25,6) | 210 (25,9) | 0,955 | |||
| Masculino | 604 (74,4) | 602 (74,1) | ||||
| Estadio TNM, n (%) | 0,082 | 0,086 | <0,001 | 0,295 | ||
| 0-II | 651 (80,2) | 679 (83,6) | ||||
| III-IV | 161 (19,8) | 133 (16,4) | ||||
| ppoFEV1, media (DE) | 69,75 (16,9) | 69,70 (16,0) | 0,954 | 0,004 | <0,001 | −0,288 |
| ppoDLCO, media (DE) | 66,04 (17,6) | 66,18 (18,0) | 0,952 | −0,008 | <0,001 | −0,148 |
ASA: American Society of Anesthesiologists; DE: desviación estándar; IMC: índice de masa corporal; ppoDLCO: capacidad de difusión de monóxido de carbono postoperatorio; ppoFEV1: volumen espiratorio forzado en el primer segundo postoperatorio; VATS: cirugía torácica videoasistida.
La diferencia estandarizada se calcula dividiendo la diferencia de los promedios de los 2 grupos por la desviación estándar en la población total. Para ello, las variables categóricas (ASA) y binarias (sexo, estadio TNM) se tratan como variables dummies.
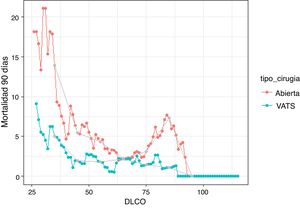
Se ha realizado un estudio comparativo de la mortalidad a los 90 días en relación con la ppoDLCO entre la VATS y la toracotomía (fig. 1). Ambas curvas muestran un aumento en la proporción de mortalidad a 90 días a medida que el valor de ppoDLCO decrece a valores de riesgo. La curva de mortalidad de los pacientes de toracotomía comienza a crecer en valores de DLCO situados en torno a 60, mientras que la curva de pacientes operados por VATS lo hace en torno a 45. La diferencia de ambas se hace mayor a medida que se llega a valores de ppoDLCO de 30. El riesgo relativo (RR) se sitúa en 2.778 (p=0,24) y 2,83 (p=0.26) en los rangos [30-40] y [40-50] de ppoDLCO, si bien no existen diferencias significativas. En el resto de los rangos el RR se sitúa en valores más bajos, exceptuando los valores de ppoDLCO situados en torno a 80 en el grupo de toracotomía, que muestran una subida en la proporción de eventos de mortalidad a 90 días.
La gráfica muestra las proporciones de pacientes fallecidos tras 90 días de la operación obtenidas con una media móvil central con un rango de±5 valores. Solo se muestran las proporciones de valores que se han calculado con al menos 10 pacientes. Los puntos grises muestran los resultados de la media móvil en los valores 35, 45, 55, 65, 75, 85 y 95. Los resultados que muestran los puntos grises se obtienen sin superponer la población en diferentes puntos.
En la tabla 3 se expone la comparación entre la mortalidad a los 90 días en ambas técnicas, agrupando a pacientes con valores de ppoDLCO menores que distintos puntos de corte.
Mortalidad a los 90 días a distintos puntos de corte de la ppoDLCO
| ppoDLCO | Cantidad de eventos (%) | p | RR | Tamaño muestral | ||
|---|---|---|---|---|---|---|
| Abierta | VATS | Abierta | VATS | |||
| <30 | 1 (12,5) | 0 (0) | 1 | Inf. | 8 | 5 |
| <35 | 4 (21,1) | 1 (5,3) | 0,33977 | 4 | 19 | 19 |
| <40 | 6 (13,6) | 2 (4,4) | 0,1572 | 3,068 | 44 | 45 |
| <45 | 7 (8,4) | 3 (3,4) | 0,2037 | 2,446 | 83 | 87 |
| <50 | 11 (8,1) | 4 (2,7) | 0,06063* | 3,015 | 135 | 148 |
| <55 | 14 (6,7) | 7 (2,9) | 0,07381* | 2,278 | 209 | 238 |
| <60 | 19 (5,9) | 7 (2,2) | 0,02602** | 2,655 | 320 | 313 |
| <65 | 21 (5) | 8 (1,9) | 0,02182** | 2,594 | 420 | 415 |
| <70 | 23 (4,6) | 11 (2,2) | 0,03713** | 2,104 | 497 | 500 |
| <75 | 26 (4,4) | 11 (1,9) | 0,0183** | 2,327 | 588 | 579 |
| <80 | 28 (4,3) | 13 (2,0) | 0,02587** | 2,088 | 658 | 638 |
| <85 | 32 (4,5) | 14 (2,0) | 0,01039** | 2,225 | 710 | 691 |
| <90 | 34 (4,6) | 14 (1,9) | 0,00485** | 2,392 | 740 | 729 |
| <95 | 34 (4,5) | 14 (1,9) | 0,00482** | 2,413 | 760 | 755 |
ppoDLCO: capacidad de difusión de monóxido de carbono postoperatorio; RR: riesgo relativo; VATS: cirugía torácica videoasistida.
La tabla muestra los resultados de la comparación de las distribuciones de la mortalidad a 90 días entre los 2 grupos para pacientes con valores de ppoDLCO menores que distintos puntos de corte. Las métricas de comparación son la prueba exacta de Fisher y el riesgo relativo. Las filas con asteriscos muestran diferencias entre los grupos con tendencia a la significación
Se puede observar que existen diferencias significativas en el riesgo de mortalidad a 90 días entre pacientes operados con VATS o con toracotomía. Los grupos de pacientes con ppoDLCO menores de 30, 35, 40, 45, 50 y 55 no muestran diferencias entre toracotomía y VATS debido al pequeño tamaño de la muestra. Si se atiende al RR, los valores más altos se alcanzan en los pacientes agrupados en los ppoDLCO más pequeños. Exceptuando el caso de los pacientes con ppoDLCO<30, los cortes donde el riesgo de mortalidad se triplica son los menores de 35 (3), de 40 (3.068) y de 50 (3.015).
Con el mismo procedimiento se han analizado la morbilidad total (morbilidad respiratoria+cardíaca), la morbilidad cardíaca, la morbilidad respiratoria total y la morbilidad respiratoria que excluye la fuga aérea, la fístula broncopleural y el quilotórax.
Además, se han hecho comparaciones entre pacientes tratados con toracotomía y VATS para los valores de ppoDLCO situados entre [30-40], [40-50], [50-60], [60-70], [70-80], [80-90] y [90-100]. Los resultados significativos de estas comparaciones se muestran en la figura 2.
Las gráficas muestran las proporciones de distintas morbilidades obtenidas con una media móvil central con un rango de±5 valores. Los puntos de las gráficas pertenecen a los valores 35, 45, 55, 65, 75, 85 y 95. Las barras representan el tamaño muestral de los rangos [30-40], [40-50], [50-60], [60-70], [70-80], [80-90] y [90-100], con la cantidad exacta mostrada justo debajo. Las estrellas resaltan aquellos intervalos donde se observan diferencias significativas entre los grupos de pacientes de toracotomía y VATS.
En los parámetros de morbilidad total, morbilidad cardíaca y morbilidad respiratoria una vez eliminados la fuga aérea, la fístula broncopleural y el quilotórax, es evidente que las curvas se disocian mostrando un mayor riesgo en la cirugía abierta.
DiscusiónExiste cierto consenso en que la ppoDLCO es una de las mediciones más importantes en el estudio preoperatorio del paciente subsidiario de resección pulmonar mayor11. Es por ello que dicha medición se incluye de forma rutinaria en la mayoría de las guías internacionales2,3. Así, la toma de decisión sobre si un paciente con cáncer de pulmón resecable es candidato a la cirugía o no, se basa en gran parte en este valor. Valores por debajo del 30% son considerados como alto riesgo y obligan a una prueba de consumo de oxígeno para poder conocer el riesgo real y para que en el caso de que el paciente presentara complicaciones en el postoperatorio, conocer cuál es su reserva funcional para superar la cirugía y la complicación2. En la guía de práctica clínica de la ACCP se considera que pacientes con valores en el consumo de oxígeno inferiores a 10ml/kg/min son de alto riesgo, a los que se debe ofrecer una cirugía alternativa (cirugía de resección menor o cirugía mínimamente invasiva) u ofrecer una opción no quirúrgica2.
Por otro lado, la mayoría de los estudios previos para determinar el punto de corte de la ppoDLCO se han realizado sobre series de pacientes que no han sido intervenidos por VATS12,13. Estudios más recientes han demostrado que en la VATS la morbimortalidad en relación con la ppoDLCO es menor que en los pacientes con toracotomía5,7,14. Si bien en algunos trabajos mantienen que la ppoDLCO es un predictor válido tanto para toracotomía como para VATS15, en este mismo trabajo se observa un número significativo mayor de complicaciones respiratorias en el grupo de toracotomías. Así, creemos que no cabe duda de que la ppoDLCO es un predictor válido para los diferentes accesos quirúrgicos, pero sí parece que el incremento de riesgo en relación con la ppoDLCO difiere según la técnica empleada.
Burt et al. publicaron8 las curvas de mortalidad y las complicaciones en relación con la ppoDLCO, donde se demuestra que la VATS tiene una morbimortalidad menor ante una misma ppoDLCO. A diferencia de lo que ocurre en nuestro trabajo, en este no se separan la morbilidad cardíaca y la respiratoria, pero las curvas obtenidas tienen un gran parecido. Mientras la mortalidad aumenta linealmente en la VATS según disminuye la ppoDLCO, en la toracotomía lo hace de manera exponencial.
Cao et al. han publicado recientemente16 la morbilidad respiratoria en relación con la ppoDLCO en pacientes con cirugía asistida por robot, donde se pueden observar curvas similares a las de la VATS que presentamos, si bien en este estudio no se compara con otro tipo de cirugía.
Dentro de las fortalezas de nuestro estudio hemos de recalcar que es multicéntrico a nivel nacional con un registro prospectivo. Además, hemos podido realizar un emparejamiento por puntaje de propensión para intentar minimizar los sesgos de selección entre ambos grupos comparados. Es de asumir que un porcentaje mayor de casos complejos pertenecen al grupo de cirugía abierta, por lo que la comparación directa de complicaciones postoperatorias entre ambas técnicas no es aceptable por su importante sesgo de selección. En nuestro trabajo, se han creado varios modelos con diferentes grados de restricción, mostrando en el artículo el modelo más restrictivo. Por ello, en algunos grupos no se observa una diferencia significativa, consecuencia de la disminución del tamaño muestral, pero hemos considerado que el RR y las curvas de los gráficos expresan de manera adecuada la tendencia.
Es cierto que existen tendencias en los datos que no son fáciles de explicar. La más destacada es la subida de la proporción de eventos de mortalidad a 90 días que se observa en los valores de DLCO situados en torno a 80 en el grupo de toracotomía. Aún no se ha encontrado una explicación definitiva a este incremento, pero se descartan problemas asociados al método estadístico, debido a que este ha aparecido en todos los métodos de reducción de sesgo testeados y se sustenta, asimismo, en un tamaño muestral considerable (rango de ppoDLCO [70-80] nVATS=138 y nABIERTA=161; rango de ppoDLCO [80-90] nVATS=91 y nABIERTA=82).
Hemos de considerar también como factor limitador el número bajo de pacientes con ppoDLCO<40. Esto se debe a que la serie es quirúrgica y muchos pacientes con severa disminución de la ppoDLCO pueden haber sido descartados para la cirugía de resección puesto que se consideran de alto riesgo6,17,.
Por otro lado, se han podido evaluar solo los pacientes cuya medición de ppoDLCO ha sido posible (n=2.530). Esto significa que el 18% de los pacientes de cáncer de pulmón incluidos en el registro no tienen el dato de la DLCO, bien porque se ha realizado solo la medición de la ppoFEV1, bien porque se ha realizado directamente la prueba del consumo de oxígeno.
También debemos asumir que no se trata de un ensayo clínico aleatorizado, por lo que aunque el emparejamiento por puntaje tiene como objetivo crear 2 grupos comparables, pueden persistir variables que no se distribuyan de manera homogénea.
Otras limitaciones que debemos asumir son las distintas variables no estudiadas que indirectamente pueden interferir en la morbimortalidad. Por ejemplo, variables como la estadificación ganglionar intraoperatoria o el manejo de la fisioterapia respiratoria no son homogéneas en todos los centros participantes.
ConclusionesLa lobectomía VATS muestra una morbimortalidad inferior a la toracotomía para una misma ppoDLCO. En los valores de ppoDLCO bajos el riesgo de mortalidad a 90 días puede llegar a triplicarse. Además, el aumento continuo del riesgo de mortalidad empieza a darse en valores de ppoDLCO superiores en la toracotomía (∼60) que en la VATS (∼45).
Por lo tanto, es importante ajustar el estudio funcional en la valoración del riesgo posquirúrgico cuando el procedimiento a realizar es subsidiario de realizarse por VATS. Para ello, las guías de práctica clínica futuras del estudio funcional de riesgo quirúrgico deberían ser adaptadas a la cirugía mínimamente invasiva.
FinanciaciónTodos los gastos relacionados con la puesta en marcha y el mantenimiento de la base de datos GEVATS fueron cubiertos por Ethicon, Johnson & Johnson. Los autores tuvieron libertad de investigación y control total del diseño del estudio, los métodos utilizados, los parámetros de resultado y los resultados, el análisis de datos y la producción del informe escrito.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
A todos los participantes del proyecto GEVATS: Raul Embun, Iñigo Royo-Crespo, José Luis Recuero Díaz, Sergio Bolufer, Sergi Call, Miguel Congregado, David Gómez-de Antonio, Marcelo F. Jimenez, Nicolas Moreno-Mata, Borja Aguinagalde, Sergio Amor-Alonso, Miguel Jesús Arrarás, Ana Isabel Blanco Orozco, Marc Boada, Alberto Cabañero Sánchez, Isabel Cal Vázquez, Ángel Cilleruelo Ramos, Silvana Crowley Carrasco, Elena Fernández-Martín, Santiago García-Barajas, Maria Dolores García-Jiménez, Jose María García-Prim, Jose Alberto Garcia-Salcedo, Juan José Gelbenzu-Zazpe, Carlos Fernando Giraldo-Ospina, María Teresa Gómez Hernández, Jorge Hernández, Jennifer D. Illana Wolf, Alberto Jauregui Abularach, Unai Jiménez, Iker López Sanz, Néstor J. Martínez-Hernández, Elisabeth Martínez-Téllez, Lucía Milla Collado, Roberto Mongil Poce, Francisco Javier Moradiellos-Díez, Ramón Moreno-Balsalobre, Sergio B. Moreno Merino, Carme Obiols, Florencio Quero-Valenzuela, María Elena Ramírez-Gil, Ricard Ramos-Izquierdo, Eduardo Rivo, Alberto Rodríguez-Fuster, Rafael Rojo-Marcos, David Sanchez-Lorente, Laura Sanchez Moreno, Carlos Simón, Juan Carlos Trujillo-Reyes, Florentino Hernando Trancho, Cipriano López, Juan José Fibla, Julio Sesma.
Agradecemos a Johnson & Johnson su colaboración en el desarrollo del Grupo VATS español. Agradecemos también a todos los responsables de los servicios de documentación clínica de cada hospital por participar activamente en la auditoría de nuestro estudio.








![Las gráficas muestran las proporciones de distintas morbilidades obtenidas con una media móvil central con un rango de±5 valores. Los puntos de las gráficas pertenecen a los valores 35, 45, 55, 65, 75, 85 y 95. Las barras representan el tamaño muestral de los rangos [30-40], [40-50], [50-60], [60-70], [70-80], [80-90] y [90-100], con la cantidad exacta mostrada justo debajo. Las estrellas resaltan aquellos intervalos donde se observan diferencias significativas entre los grupos de pacientes de toracotomía y VATS. Las gráficas muestran las proporciones de distintas morbilidades obtenidas con una media móvil central con un rango de±5 valores. Los puntos de las gráficas pertenecen a los valores 35, 45, 55, 65, 75, 85 y 95. Las barras representan el tamaño muestral de los rangos [30-40], [40-50], [50-60], [60-70], [70-80], [80-90] y [90-100], con la cantidad exacta mostrada justo debajo. Las estrellas resaltan aquellos intervalos donde se observan diferencias significativas entre los grupos de pacientes de toracotomía y VATS.](https://static.elsevier.es/multimedia/03002896/0000005700000012/v2_202112040821/S0300289621000557/v2_202112040821/es/main.assets/thumbnail/gr2.jpeg?xkr=ue/ImdikoIMrsJoerZ+w98FxLWLw1xoW2PaQDYY7RZU=)









