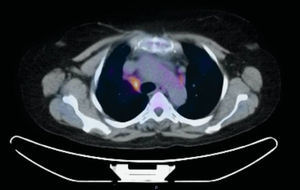
Presentamos el caso de una mujer de 58 años con antecedentes de trombosis venosa profunda subclavio-yugular, en enero de 2014, con tromboembolismo pulmonar secundario e hipertensión pulmonar no estudiada por falta de consentimiento por parte de la paciente, insuficiencia tricuspídea moderada y asma bronquial intermitente. Natural de Marruecos, con último viaje en septiembre de 2013. Vive en ambiente urbano y convive con 2 perros, con adecuado seguimiento veterinario. Ausencia de otros datos epidemiológicos, de antecedentes familiares, de alergias medicamentosas conocidas y de hábitos tóxicos o exposiciones ocupacionales de interés. Acude al servicio de neumología, en febrero de 2015, derivada por su médico de cabecera, debido a un cuadro de 6-8 semanas de evolución, consistente en sensación distérmica con fiebre no termometrada, disnea de medianos esfuerzos, tos con escasa expectoración blanquecina y espesa, hiporexia y astenia. En el examen físico destacó una ligera taquipnea, boca séptica con pérdida de varias piezas dentales, sin aftas, tonos cardiacos rítmicos y sin soplos, y murmullo vesicular globalmente disminuido con crepitantes finos bibasales. Sin otros datos de interés. Las pruebas de laboratorio mostraron un aumento leve de la proteína C-reactiva y una discreta leucocitosis. Sin hallazgos patológicos en muestras de esputo seriadas (baciloscopias y cultivos). La radiografía de tórax mostró una cardiomegalia global y un infiltrado intersticio-alveolar basal derecho. Se realizó tomografía axial computarizada (TAC) de tórax, evidenciándose adenopatías hiliares bilaterales y mediastínicas de tamaño significativo, estas últimas a nivel paratraqueal bajo y subcarinal junto con un infiltrado de características alveolares a nivel del lóbulo inferior derecho. Dados los hallazgos de la TAC, se solicitó la realización de una tomografía por emisión de positrones (PET) y se confirmó el aumento de metabolismo a nivel paratraqueal derecho bajo (standardized uptake value [SUV] de 4,7, fig. 1), hiliar bilateral (SUV de 2,2) y sobre zona de infiltrado alveolar basal derecho (SUV de 2,3), compatible con proceso infeccioso/inflamatorio. Se realizó broncoscopia flexible, sin evidenciarse alteraciones endobronquiales, con resultados microbiológicos y citológicos dentro de la normalidad. Posteriormente se llevó a cabo exploración mediante ecobroncoscopia (EBUS) lineal con adenopatía a nivel 4R de 12mm de eje corto, que se punciona con aguja citológica de 22 G en 3 ocasiones con citopatólogo «in situ», que objetivó la presencia de estructuras ramificadas en parte del material valorado. Se remitieron las muestras obtenidas para su análisis citológico y microbiológico, aislándose en todas las muestras remitidas a microbiología Actinomyces graevenitzii (A. graevenitzii), resistente a ciprofloxacino. Tras tratamiento antibiótico dirigido con amoxicilina-clavulánico y clindamicina se constata mejoría del cuadro clínico.
La actinomicosis es una enfermedad granulomatosa crónica, lentamente progresiva, causada por bacterias filamentosas grampositivas anaerobias o microaerofílicas de la familia Actinomycetaceae (género Actinomyces). Concretamente, A. graevenitzii fue descrita por primera vez en 1997 por Ramos et al.1. Al igual que otros actinomicetos, A. graevenitzii forma parte de la flora orofaríngea y fue aislada inicialmente en las superficies de los implantes dentales. Sin embargo, poco se sabe acerca de las características clínicas y patogenia de esta bacteria. La afectación pulmonar alcanza el 15% de los casos de actinomicosis y se piensa que es causada principalmente por la inhalación o aspiración de contenido gastrointestinal u orofaríngeo. La infección puede involucrar a parénquima pulmonar, vía aérea, pleura, mediastino y pared torácica, provocando complicaciones clínicas tales como la obstrucción bronquial, empiema pleural, fístulas, destrucción costal y síndrome de vena cava superior2. Los factores de riesgo más importantes para el desarrollo de la actinomicosis pulmonar incluyen mala higiene orofaríngea (como en el caso de nuestra paciente), enfermedad dental preexistente y alcoholismo. Además, afecciones pulmonares como la enfermedad pulmonar obstructiva crónica, bronquiectasias, enfermedad micobacteriana crónica y aspergiloma, se consideran otros factores de riesgo por la formación de un ambiente anaerobio en el tejido pulmonar dañado que favorece el crecimiento de esta bacteria3. Los pacientes inmunodeprimidos o los ingresados en unidades de cuidados intensivos son igualmente vulnerables a la infección por patógenos oportunistas, cuyo diagnóstico puede ser facilitado con técnicas de ecoendoscopia. Dado sus características clínicas y radiológicas inespecíficas, se debe establecer el diagnóstico diferencial con otras entidades tales como el cáncer de pulmón, tuberculosis4, neumonía, enfermedades granulomatosas y abscesos pulmonares. Se han publicado pocos casos en los que se describan infecciones por A. graevenitzii y este es el primero conocido cuyo diagnóstico es establecido por punción de adenopatía guiada por ecobroncoscopia lineal5.