La cirugía del sistema nervioso simpático torácico (SNST) ha experimentado un gran auge en los últimos años, generando gran expectación entre la población general y la comunidad científica. Esto se ha debido a los excelentes resultados que ha obtenido la simpatectomía torácica por videotoracoscopia en el tratamiento de la hiperhidrosis esencial y en otros trastornos del SNST.
Esta técnica de cirugía mínimamente invasiva ha demostrado ser efectiva y con baja morbilidad, aceptada como una de las mejores opciones terapéuticas para el tratamiento de la hiperhidrosis palmar y axilar bilateral, viéndose incrementado de manera considerable el número de pacientes que consultan con intención de operarse.
Aunque la sudoración compensadora, intensa en ocasiones, aparece con gran frecuencia tras la cirugía, éste y otros efectos secundarios de la técnica son bien tolerados por los pacientes.
La evidencia actual respecto a la cirugía del SNST y del tratamiento de la hiperhidrosis esencial se basa en estudios observacionales, haciendo difícil comparar series y extraer conclusiones. Se ha discutido mucho para unificar la técnica, definir los niveles de sección más favorables y elegir el tipo de denervación con menos efectos secundarios. Este hecho crea la necesidad de elaborar esta normativa que clarifique y unifique criterios para el manejo de los pacientes con trastornos del SNST.
Thoracic sympathetic nervous system (TSNS) surgery has increased in importance in the last few years, generating great expectations among the general population and the scientific community. This has been due to the excellent results obtained by videothoracoscopy-assisted thoracic sympathectomy in the treatment of essential hyperhidrosis and other TSNS disorders.
This minimally invasive surgical technique has been shown to be effective, and with a low morbidity it is accepted as one of the best therapeutic options for the treatment of palmar and bilateral axillary hyperhidrosis and the number of patients consulting with the intention of having the operation has increased considerably.
Although compensatory sweating, which is occasionally intense, often occurs after the surgery, this and other secondary effects of the technique are well tolerated by patients.
The current evidence on TSNS and the treatment of essential hyperhidrosis is based on observational studies, making it difficult to compare series and draw conclusions. There has been much discussion on standardising the technique, defining the most favourable levels for clipping, and choosing the type of denervation with least secondary effects. This has led to the need to draw up these guidelines which should clarify and standardise the criteria for managing patients with disorders of TSNS.
La cirugía del sistema nervioso simpático torácico (SNST) no es un procedimiento nuevo. Se practicó desde principios del siglo xx para mejorar la circulación de las extremidades superiores, observándose un efecto en ciertas funciones como la sudoración, y se adoptó como procedimiento electivo para problemas de hiperhidrosis desde los años veinte. Posteriormente su popularidad decayó de forma significativa, ya que los pacientes se sometían a un procedimiento de cirugía mayor para mitigar un problema considerado menor.
A finales de los años ochenta, con el desarrollo de las técnicas de la cirugía mínimamente invasiva, se inició, de nuevo, su aplicación. Su popularidad ha sido tal, que la técnica se ha extendido por todo el mundo y, en la actualidad, se cuenta con grupos, principalmente suecos y japoneses, con una gran experiencia.
La mayor parte de la evidencia actual respecto a la cirugía del SNST, y concretamente, en el tratamiento de la hiperhidrosis primaria localizada, procede de estudios observacionales. En dichos trabajos existe una falta de uniformidad tanto en las definiciones como en las medidas y los métodos de exposición de los resultados. Ello hace difícil comparar las distintas series y extraer conclusiones generalizables.
La ausencia de una normativa sobre cirugía del SNST para el tratamiento de la hiperhidrosis primaria localizada y otras entidades clínicas, invita a elaborar una con el objetivo de mejorar, facilitar y unificar el manejo de los pacientes con estas patologías. Las recomendaciones se han establecido según el sistema GRADE (“The Grades of Recommendation, Assessment, Development and Evaluation”)1 (tabla 1). En aquellos aspectos en que la evidencia científica es insuficiente, se han incluido las recomendaciones acordadas por consenso de los autores.
Clasificación de las recomendaciones y calidad de evidencia científica según el sistema GRADE
| Grado de recomendación | Calidad de evidencia | Implicaciones |
| 1. Recomendación consistente.a Calidad de evidencia alta. | ECA bien realizados o excepcionalmente EO bien realizados. | Aplicarse en la mayoría de pacientes en la mayoría de circunstancias. |
| 2. Recomendación consistente.a Calidad de evidencia moderada. | ECA con limitaciones o EO bien realizados con efectos importantes. | Aplicarse en la mayoría de pacientes en la mayoría de circunstancias. |
| 3. Recomendación consistente.a Calidad de evidencia baja. | Evidencia para al menos un resultado importante de EO o ECR con defectos mayores importantes o evidencia muy indirecta. | Puede cambiar cuando se disponga de evidencia. |
| 4. Recomendación consistente.a Calidad de evidencia muy baja. | Evidencia para al menos un resultado importante de observaciones clínicas no sistemáticas o evidencia muy indirecta. | Puede cambiar cuando se disponga de evidencia mayor. |
| 5. Recomendación débil.b Calidad de evidencia alta. | ECA bien realizados o excepcionalmente EO bien realizados. | Puede diferir dependiendo de las circunstancias o de los pacientes. |
| 6. Recomendación débil.b Calidad de evidencia moderada. | ECA con limitaciones o EO bien realizados con efectos importantes. | Otras alternativas pueden ser mejores para algunos pacientes en ciertas circunstancias. |
| 7. Recomendación débil.c Calidad de evidencia baja. | Evidencia para al menos un resultado importante de EO o ECR con defectos mayores importantes o evidencia indirecta. | Otras alternativas pueden ser igualmente razonables. |
| 8. Recomendación débil.d Calidad de evidencia muy baja. | Evidencia para al menos un resultado importante de observaciones clínicas no sistemáticas o evidencia muy indirecta. | Otras alternativas pueden ser igualmente razonables. |
ECA: estudios controlados aleatorizados; ECR: Estudios controlados randomizados; EO: estudios observacionales.
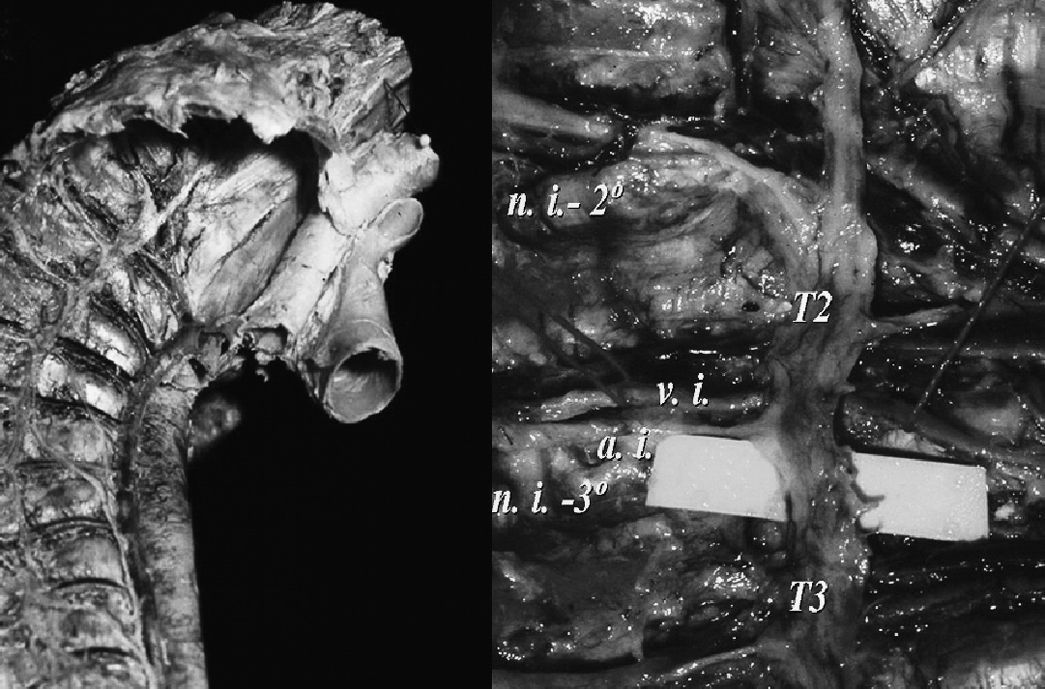
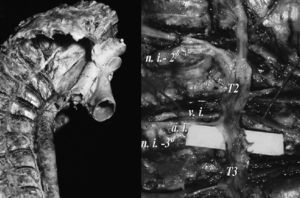
El sistema nervioso autónomo simpático se compone de tres neuronas: el cuerpo neuronal de la primera, llamada preganglionar o conectora, está situado en el asta intermediolateral de la médula espinal toracolumbar. Su axón alcanza el ganglio de la cadena, vía raíz anterior medular y ramo comunicante blanco. El cuerpo neuronal de la segunda neurona, localizada en el ganglio simpático (fig. 1), presenta un axón amielínico, que abandona la cadena a través del ramo comunicante gris hasta el nervio radicular correspondiente. Esta segunda neurona es conocida como postganglionar o fibra efectora. La neurona postganglionar acompaña a las fibras cerebroespinales en su trayecto hacia la piel.
List y Peet2 en 1938, tras los estudios realizados en pacientes simpatectomizados a distintos niveles de la cadena simpática, describieron los dermatomas simpáticos, relacionando las fibras preganglionares con regiones corporales determinadas, similares a los dermatomas sensoriales. La amplificación neuronal existente entre una fibra preganglionar y varias fibras postganglionares, hacen que estos dermatomas simpáticos se solapen y sean de difícil sistematización.
En la porción torácica del sistema simpático, está bien documentada la existencia de una serie de ganglios, cuyo número suele corresponderse, de forma aproximada, con el de los nervios espinales torácicos. El primer ganglio torácico suele estar fusionado con el ganglio cervical inferior, formando el ganglio estrellado o cervicomediastínico. Excepto los tres últimos ganglios torácicos, los demás descansan en las cabezas costales y se encuentran posteriores a la pleura parietal.
Sin embargo, con respecto a la posición anatómica de los ganglios del SNST, múltiples estudios describen su localización más frecuente para ser identificados en el campo quirúrgico. Los ganglios torácicos T2-T3 se localizan, en la mayoría de los casos, al nivel de los espacios intercostales y no sobre el arco costal3.
Ramsaroop, en 2001, identificó, en un exhaustivo estudio anatómico, múltiples conexiones entre la cadena simpática y los nervios intercostales y sugirió que la denominación de nervio de Kuntz se limitara a los ramos intratorácicos a nivel del primer espacio intercostal, siendo las demás conexiones existentes denominadas “conexiones simpáticas adicionales” o “ramos comunicantes adicionales”4.
Hiperhidrosis primaria localizadaDefinición, clínica y diagnósticoLa hiperhidrosis se define como una excesiva producción de sudor ecrino a uno o varios niveles del organismo. Suele ser causa de graves trastornos de índole social y ocupacional. Se acepta que la sudoración normal de la piel podría oscilar entre 8 y 15 mcg/cm2/min, incluyendo la superficie de ambas manos5. Es una afección, de origen desconocido, que se inicia en la infancia, se manifiesta en la adolescencia y, sin tratamiento específico, persiste durante toda la vida.
Algo más frecuente en mujeres, tiene una evidente predisposición familiar y su incidencia es más alta en ciertas poblaciones (asiáticos y sefardíes), llegando a representar el 1% de la población6. Afecta de forma bilateral, simétrica y a veces se relaciona o exacerba con situaciones de carácter emocional o estacional.
Aunque existen formas generalizadas, la hiperhidrosis localizada es el modo de presentación más frecuente, siendo la hiperhidrosis palmar y axilar las más habituales, seguidas de la hiperhidrosis plantar. Lo habitual es que se combinen dos o más localizaciones afectadas, sin que por ello deba calificarse como hiperhidrosis generalizada. A pesar de su notable incidencia, sólo un pequeño porcentaje de estos pacientes consultan, ya que la mayoría desconoce su posibilidad de tratamiento7.
El diagnóstico de la hiperhidrosis localizada primaria es clínico, apoyado en una correcta historia clínica. Aquellos datos relacionados con la historia familiar, el patrón de distribución, la frecuencia de los síntomas, etc, ayudan a distinguir una hiperhidrosis localizada de una generalizada. En este sentido, el Grupo de Trabajo Multidisciplinar en Hiperhidrosis de Estados Unidos ha propuesto unos criterios para el diagnóstico de la hiperhidrosis localizada (tabla 2)8.
Criterios diagnósticos de la hiperhidrosis localizada primaria
| – Hipersudoración local y visible durante por lo menos un período de seis meses de duración sin una causa secundaria conocida. |
| – Al menos dos de las siguientes características: |
| • Bilateral y simétrica. |
| • Frecuencia de un episodio semanal como mínimo. |
| • Interferencia con las actividades diarias habituales. |
| • Edad de aparición por debajo de los 25 años. |
| • Historia familiar. |
| • Cese de la hipersudoración durante el sueño. |
Aunque la ansiedad se ha descrito como un componente habitual en la historia clínica de estos enfermos, parece tratarse más de un comportamiento reactivo al trastorno que la propia hiperhidrosis supone en el quehacer diario de estos pacientes9.
Se han propuesto diferentes exámenes para evaluar esta afección. Las pruebas de laboratorio no son necesarias en el diagnóstico de la hiperhidrosis primaria, aunque pueden ayudar a descartar otras enfermedades que producen hiperhidrosis secundaria (síndromes infecciosos, hipertiroidismo, cardiopatía, feocromocitoma, tumor carcinoide, etc). En cuanto a la medición de la hiperhidrosis, se han propuesto diferentes métodos. La evaporimetría, que mide la cantidad de sudor evaporado por estos pacientes, ha sido propuesta por Krogstad10 como método de cuantificación de la sudoración cutánea. La gravimetría permite calcular la tasa de producción de sudor por minuto. Éstos y otros test (test del almidón iodado, test de la ninhidrina) han sido recomendados en el diagnóstico de la hiperhidrosis en el ámbito de la Dermatología, sobre todo en el estudio de la efectividad del tratamiento con toxina botulínica11.
Clasificación y diagnóstico diferencialLa hiperhidrosis se puede clasificar según el área de afectación en dos tipos:
- –
Localizada o focal: de predominio en zonas específicas, existiendo diferentes formas:
- •
Hiperhidrosis primaria idiopática con afectación en palmas, plantas, axilas, región inguinal o craneofacial.
- •
Síndrome de Frey o sudoración gustativa.
- •
Neurológicas, como ocurre en determinadas neuropatías y enfermedades que afectan a la médula espinal.
- •
- –
Sistémica o generalizada: variante con afectación de la totalidad de la piel. Se observa en una amplia gama de enfermedades: embarazo, obesidad, menopausia, ansiedad, hipertiroidismo, feocromocitoma, tumor carcinoide, así como en diferentes trastornos dermatológicos como el vitíligo, la paquidermoperiostosis, la epidermólisis bullosa, etc. Una lesión estructural del SNST puede causar anomalías de la sudoración. Los tumores de la corteza cerebral, los ictus, o las infecciones pueden producir una hiperhidrosis contralateral. Las enfermedades de la médula espinal (siringomielia, lesión medular, tabes) también pueden causar diaforesis12.
En función de su origen, la hiperhidrosis se puede clasificar en5-12:
- –
Hiperhidrosis primaria o esencial: con predominio en palmas, plantas, axila, pliegue mamario y región craneofacial.
- –
Hiperhidrosis secundaria: (tabla 3).
Tabla 3.Hiperhidrosis secundaria
– Enfermedades de la piel: hongos, bacterias, dermatitis de contacto… – Fiebre – Endocrinológicas: hipertiroidismo, feocromocitoma, hiperpituitarismo, síndrome carcinoide, acromegalia, obesidad, diabetes, menopausia, embarazo. – Infecciones sistémicas: tuberculosis, endocarditis. – Cardiovasculares: shock, insuficiencia cardíaca, insuficiencia respiratoria. – Fármacos: fluoxetina, venlafaxina, alcohol, abstinencia de opiáceos, anticolinesterásicos, pilocarpina, alprazolam, lorazepam, mercurio, arsénico, archilamida, antisecretores/inhibidores de la bomba de protones. – Neurológicas: • Enfermedad de Parkinson. • Afectación de la médula espinal: ○ Lesión medular, siringomielia o tabes. • Accidente cerebrovascular. – Oncológicas • Síndromes mieloproloferativos. • Enfermedad de Hodgkin. – Trastornos del sistema nervioso central: • Tumores cerebrales, accidentes cerebrales vasculares. • Hiperhidrosis familiar primaria: trastorno neurológico caracterizado por excesiva sudoración, usualmente focal con asociación familiar. – Psicógeno. – Enfermedades de la piel: vitíligo, epidermólisis ampollosa, paquidermoperiostosis, queratólisis punctata, urticaria de esfuerzo, síndrome de Raynaud, perniosis, paniculitis, acrocianosis, lupus eritematosos (formas localizadas), eritema de Igne. – Ingesta crónica de mercurio.
Muchos son los trabajos recientes que han revisado los tratamientos no quirúrgicos de la hiperhidrosis primaria localizada. Haider y Solish han analizado la evidencia de los tratamientos médicos de la hiperhidrosis localizada en nueve estudios donde se ha usado el cloruro de aluminio, la iontoforesis y la toxina botulínica7.
Tratamiento tópicoLas sales de aluminio en forma de cloruro o clorhidrato son las más usadas. Los “antitranspirantes” que se encuentran en el mercado contienen concentraciones bajas que oscilan entre el 15 y 19%. El mecanismo de acción de estos productos se basa en la oclusión mecánica de los conductos secretores de las glándulas ecrinas durante un tiempo más o menos prolongado, ocasionando, a largo plazo, una atrofia de las células secretoras13.
En aquellos pacientes en los que los “antitranspirantes” comerciales no son efectivos, se recomienda prescribir preparados con concentraciones más altas de aluminio, como el cloruro de aluminio al 20% en etanol (Drysol©) o el tetracloruro de aluminio al 6,25% (Xerac©). La evidencia demuestra que las sales de aluminio a alta concentración son el tratamiento tópico de primera elección en el manejo de la hiperhidrosis primaria localizada14.
IontoforesisLa iontoforesis consiste en la aplicación de sustancias ionizantes, a través de la piel, mediante una corriente alterna. Se puede emplear una corriente continua de 20-50V y un amperaje máximo de 15-30mA. La corriente alterna consigue similares resultados aplicando corrientes más bajas de 8-12mA y voltaje fijo de 16V. En aquellos individuos en los que la iontoforesis no es efectiva, algunos autores recomiendan añadir anticolinérgicos al tratamiento15.
Toxina botulínicaEl uso de toxina botulínica A (BTX-A) es un tratamiento eficaz para la hiperhidrosis axilar, con una efectividad del 90% a las 4 semanas de iniciar el tratamiento8. Los resultados no son tan buenos en pacientes con hiperhidrosis palmar y es poco útil en la hiperhidrosis plantar y craneofacial.
La BTX-A se administra de forma intradérmica. En la región axilar se recomienda utilizar 50 U en cada una, diluidas en suero salino al 0,9% y en la región palmar 100 U en cada mano. Se hacen múltiples inyecciones con una distribución uniforme, separadas 1-2cm. Es preciso realizar el test de Minor (yodo-almidón) para identificar la zona a tratar. Tras la aplicación de BTX-A se repite el test para demostrar el grado de respuesta7.
La reducción de la sudoración se comienza a notar entre el 2° y 4° día después del tratamiento y deberá ser evidente a partir de la 2ª semana. Debe repetirse la administración de BTX-A cada 4-17 meses.
Tratamiento sistémicoLos tratamientos por vía oral con anticolinérgicos se han utilizado, con unos resultados discutibles, en el caso de hiperhidrosis graves. Éstos son mejores en pacientes en los que aparece sudoración compensadora (SC) tras el tratamiento quirúrgico. La oxibutinina (Ditropan©) en dosis de 5-15mg/día y la tolterodina (Ditrusitol©) 4mg/día son los más utilizados.
La asociación de agentes anticolinérgicos con sedantes o tranquilizantes ha sido muy usada, pero mal aceptada por parte de los pacientes, ya que les puede producir visión borrosa, sequedad de boca, adormecimiento y retención urinaria. Estos síntomas obligan a la suspensión del tratamiento en muchas ocasiones7.
Tratamiento quirúrgicoIndicaciónLa simpatectomía torácica está principalmente indicada en los casos de hiperhidrosis craneofacial, palmar y axilar con mala respuesta al tratamiento médico16,17. Otros desórdenes en los que puede ser utilizada son el rubor facial, síndrome de Raynaud y trastornos principalmente de origen vascular en los miembros superiores18. La esplanicectomía se usa, de forma casi exclusiva, en algunos pacientes con dolor abdominal resistente al tratamiento médico19,20.
Una vez sentada la indicación de cirugía, es obligado informar al paciente del carácter prácticamente definitivo de la intervención y los posibles efectos adversos que puedan aparecer.
TécnicaPosiciónLa posición del paciente depende del tipo de interrupción de la cadena simpática y de si el abordaje es unilateral o bilateral. Cuando la técnica empleada para la simpaticolisis es la resección de la cadena o del ganglio, la posición en decúbito lateral facilita la intervención, ya que permite el empleo de instrumental diverso y una exposición más cómoda de la cavidad pleural. El resto de técnicas de interrupción de la cadena se pueden realizar cómodamente desde la posición de semi-Fowler, descrita más adelante.
Rara vez el abordaje es unilateral; en este caso es más aconsejable utilizar el decúbito lateral ya que permite identificar mejor las dos primeras costillas. La posición en decúbito prono, menos empleada, permite igualmente el acceso a ambos hemitórax sin modificar la colocación del paciente en la mesa operatoria.
No existen estudios que demuestren la superioridad de una posición frente a otra. La práctica cotidiana y la mayoría de las publicaciones de series de casos sostienen que la posición más habitual es la de semi-Fowler, que ayuda a separar el pulmón del vértice de la caja torácica. El paciente se coloca semisentado, con los brazos separados 90° y con una ligera rotación al lado contrario al que se va a intervenir. Esta posición permite el acceso a los dos hemitórax sin modificar la situación del paciente en la mesa de quirófano21.
AnestesiaSe han utilizado diferentes técnicas para la ventilación intraoperatoria de estos pacientes. La intubación orotraqueal con tubo de doble luz es la más empleada, pero se han descrito tanto la ventilación con mascarilla laríngea como la cirugía con sedación y ventilación espontánea, con resultados satisfactorios22. Si se elige la ventilación bipulmonar con un tubo orotraqueal, la cámara de neumotórax se puede conseguir con pequeñas pausas de apnea que permitirán acceder a la cadena o mediante el empleo de CO2. Este se usa a presión de hasta 10cm de H2O con un flujo de 0,5-2 L/min, suficiente para colapsar el vértice pulmonar y separarlo del “sulcus” superior21.
Puertas de entradaHabitualmente se realizan dos puertas de entrada. Una para el sistema óptico y de iluminación, y la otra para introducir el instrumental con el que se realiza la técnica quirúrgica. Si se dispone de un toracoscopio con canal de trabajo, sólo es necesario utilizar una puerta de entrada21.
Tipos de interrupciónDiferentes son las opciones de interrupción de la cadena, y ninguna ha demostrado ser superior a las restantes. La sección de la cadena, que se realiza sobre la costilla, la resección de ganglios, la ramicotomía y la ablación mediante termocoagulación, son técnicas definitivas. La interrupción de la cadena del SNST mediantes grapas (“clipping”), bien sobre la costilla o por encima y por debajo del ganglio, es una técnica potencialmente reversible.
Las técnicas definitivas son las más utilizadas para pacientes con hiperhidrosis palmo-plantar, donde la probabilidad de requerir la reversibilidad es baja. Son candidatos a la técnica reversible aquellos pacientes en los que el beneficio terapéutico sea más dudoso y mayor el riesgo de SC. En este grupo se incluyen aquellos pacientes con hiperhidrosis craneofacial, axilar o rubor facial21.
Nivel de secciónUno de los puntos más delicados a la hora de realizar una simpaticolisis es elegir el nivel más adecuado de la cadena simpática en el que actuar, entendiéndose que, cuando se recomienda, por ejemplo, T3, significa la sección sobre la 3a costilla.
La dificultad para determinar el nivel idóneo sobre el que actuar, viene dada fundamentalmente por dos factores:
- 1.
Los resultados, tanto en efectividad como en efectos adversos aportados por los diferentes autores que han intentado encontrar el nivel ideal en el que actuar, no han sido coincidentes, haciendo imposible hasta ahora concretar pautas aceptadas por todos como ideales.
- 2.
Los estudios neuro-anatómicos permiten conocer bien la distribución típica del sistema simpático, pero también revelan la frecuente existencia de variaciones anatómicas.
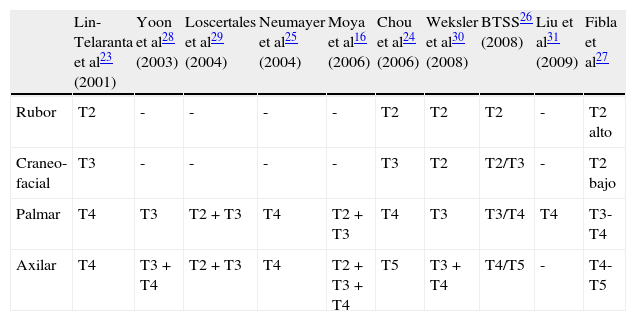
De esta forma, es necesario utilizar una clasificación clínica que sirva para después poder recomendar unos niveles de actuación. En este sentido, resulta práctico seguir la publicada por Lin-Telaranta23 y empleada por diferentes autores24,25 en la que clasifica la disfunción simpática en tres categorías. La primera categoría para los pacientes diagnosticados de rubor facial, la segunda para pacientes que sufren hiperhidrosis cráneo-facial con o sin rubor facial, y la tercera para los casos de hiperhidrosis palmar y axilar. Una clasificación más detallada, es la utilizada por la Sociedad Brasileña de Cirugía Torácica26 en la que las categorías anteriores son subdivididas en función de la intensidad de los síntomas.
Tomando como base la clasificación de Lin-Teleranta, se pueden analizar los resultados de diferentes autores (tabla 4)16,23-31 encontrando suficientes diferencias entre ellos para no indicar categóricamente los niveles precisos en los que hay que actuar, pero a la vez, encontrando suficiente nivel de evidencia para recomendar niveles específicos de sección:
- –
Pacientes con rubor y/o sudoración facial: sección nivel T2 y/o T3.
- –
Pacientes con hiperhidrosis palmar: sección nivel T3 y/o T4.
- –
Pacientes con hiperhidrosis axilar: sección nivel T4 o T4-T5.
Niveles actuación utilizados por diferentes autores
| Lin-Telaranta et al23 (2001) | Yoon et al28 (2003) | Loscertales et al29 (2004) | Neumayer et al25 (2004) | Moya et al16 (2006) | Chou et al24 (2006) | Weksler et al30 (2008) | BTSS26 (2008) | Liu et al31 (2009) | Fibla et al27 | |
| Rubor | T2 | - | - | - | - | T2 | T2 | T2 | - | T2 alto |
| Craneo-facial | T3 | - | - | - | - | T3 | T2 | T2/T3 | - | T2 bajo |
| Palmar | T4 | T3 | T2+T3 | T4 | T2+T3 | T4 | T3 | T3/T4 | T4 | T3-T4 |
| Axilar | T4 | T3+T4 | T2+T3 | T4 | T2+T3+T4 | T5 | T3+T4 | T4/T5 | - | T4-T5 |
La existencia de vías accesorias en el SNST fue documentada en 1927 por Kuntz32 tras descubrir la existencia de una conexión nerviosa que desde el 2° nervio intercostal alcanzaba el plexo braquial sin pasar por el 2° ganglio simpático. Así se acuñó el epónimo “nervio de Kuntz” que genéricamente se ha utilizado para referirse al conjunto de fibras simpáticas alternativas del SNST, si bien de acuerdo con Ramsaroop4, debe reservarse exclusivamente para las ramas localizadas en el primer espacio intercostal. Su prevalencia ha sido cifrada en alrededor de un 10% de las exploraciones quirúrgicas.
Del mismo modo, Kim33 encuentra a la altura de la 3ª cabeza costal vías accesorias laterales y mediales a la cadena simpática en un 12,5 y 9% respectivamente.
La existencia del nervio de Kuntz, así como la de vías accesorias, ha sido clásicamente descrita como una causa de fallo terapéutico en la hiperhidrosis palmar34. Hay, por tanto, evidencias que hacen recomendable intentar la identificación e interrupción del nervio de Kuntz, así como extender lateralmente la coagulación sobre el borde costal superior e inferior.
InstrumentaciónSi bien las primeras simpaticotomías videotoracoscópicas se realizaron de forma sistemática con diatermia, desde el año 1996, cuando se inició la aplicación clínica del bisturí armónico o ultrasónico, se planteó su aplicación en el ámbito de la cirugía del SNST. Su ventaja frente al cauterio es que no genera calor en la zona de aplicación, lo que reduce la probabilidad de lesión del ganglio estrellado y otras estructuras vecinas. Sin embargo, en la actualidad, no existe evidencia científica de que el bisturí ultrasónico sea el instrumento de elección35.
Drenajes y cuidados postoperatoriosTras la finalización del procedimiento, se recomienda colocar un drenaje fino a través de la puerta de 5mm, con el fin de evacuar el neumotórax generado para la intervención, siendo conectado a un sistema de sellado hidráulico. El correcto tratamiento de las náuseas, vómitos y el dolor postoperatorio, ha hecho que se pueda realizar este procedimiento en programas de cirugía sin ingreso36,37.
ResultadosLa eficacia y resultado intraoperatorio de la técnica se suelen objetivar valorando el incremento de la onda del pulso con un pulsioxímetro y/o viendo la elevación de la temperatura gracias a un sensor de temperatura colocado en la eminencia tenar, ambos en la extremidad superior del lado intervenido. También se puede medir el flujo sanguíneo con un doppler láser38.
La recurrencia de la hiperhidrosis aparece en el 1-27% en los tres años siguientes a la cirugía. El 76% de las recurrencias se produce en los 6 primeros meses y suele ser moderada. Se ha relacionado con la experiencia del cirujano, las variaciones anatómicas, la interrupción incompleta de la cadena simpática o la posible regeneración nerviosa39. No se deben considerar un fallo de la técnica los períodos transitorios de hiperhidrosis palmar que pueden aparecer entre el 1° y 7° día tras la operación y que luego desaparecen definitivamente.
La mejoría clínica se sitúa siempre por encima del 90%, pero el grado de satisfacción depende de la intensidad de la SC, que es grave en el 1-30% de los pacientes, según las series40,41. Esta mejoría y el grado de la satisfacción son mayores en la hiperhidrosis palmar que en la axilar.
ComplicacionesSe debe distinguir entre complicaciones, en torno al 10%, y efectos no deseados o secundarios.
Complicaciones intraoperatoriasLa variabilidad anatómica de la cadena del SNST, la presencia de abundante tejido adiposo o la existencia de múltiples adherencias pueden, en ocasiones, dificultar o incluso impedir la técnica quirúrgica. La producción de lesiones arteriales o venosas y la aparición de alteraciones del ritmo como la bradicardia, son casi anecdóticas.
Complicaciones postoperatoriasLa complicación postoperatoria más frecuente es la aparición de un neumotórax que suele ser de pequeño tamaño y que requiere drenaje pleural en un 30% de los casos. En un escaso número de pacientes se produce un derrame pleural, hemotórax y quilotórax39. El dolor es, por lo general, moderado y se resuelve con analgésicos convencionales en un período máximo de 2 a 4 semanas. El síndrome de Horner sólo aparece de forma definitiva en menos del 0,5% de casos. Otras complicaciones poco frecuentes son el enfisema subcutáneo, la infección de herida operatoria, la presencia de atelectasias segmentarias pulmonares y la lesión transitoria del plexo braquial41.
Efectos secundarios o no deseadosLa Sudoración compensadora se define como la sudoración intensa en otras áreas anatómicas después de la simpatectomía: región dorsal, abdomen, región inguinal y muslos. Esta situación puede cambiar con el tiempo y suele ser difícil de evaluar. Según las series revisadas por Dumont, la forma leve oscila entre el 15 y 90% y la forma severa entre el 1 y 30%41. Según algunos autores, cuanto más alta se realiza la simpatectomía (T2) y cuanto más extensa la resección (T2–T5), mayores son las probabilidades de que se produzca una SC grave39,41.
Otros efectos no deseados suceden con menor frecuencia. Entre ellos se hallan la sudoración gustatoria (1-32%) y la sequedad de manos (42%), que suelen ser bien aceptadas por los pacientes, de la misma forma que el efecto rebote, limitado en el tiempo. Los cambios producidos por la simpatectomía torácica sobre la vía aérea de pequeño calibre y la frecuencia cardiaca son poco significativos desde un punto de vista clínico39,42.
ReversibilidadSi algo se desprende de la extensa bibliografía publicada al respecto, es que los resultados y efectos secundarios, incluida la SC, son similares sea cual sea la técnica quirúrgica empleada (simpatectomía, simpaticotomía, ramicotomía o “clipping”). No obstante, los procedimientos que seccionan el nervio tienen en común el hecho de ser irreversibles41.
Las opciones de tratamiento de la SC en estos casos son muy limitadas. Varios autores han intentado la reconstrucción de la cadena simpática colocando injertos de distintos nervios con resultados muy diferentes43,44.
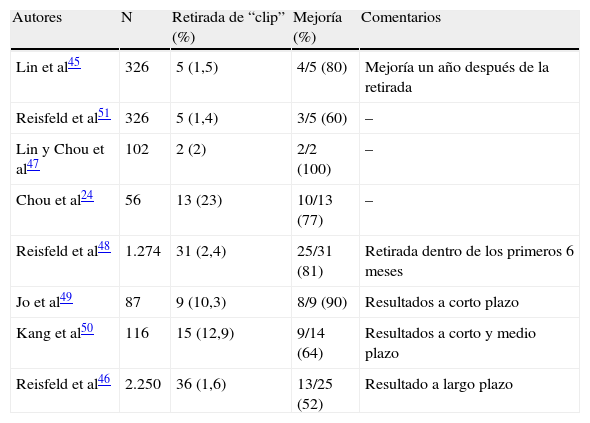
El grapado o “clipping” de la cadena simpática surgió como el único procedimiento que, hasta el momento, podría ser capaz de revertir los efectos del bloqueo del SNST. La experiencia publicada en lo que concierne a la retirada del “clip” es variada. En la tabla 524,45-51 se exponen las principales series de la literatura. Los autores han conseguido resultados diferentes, que están entre el 52 y el 100% de mejoría.
Resultados de la retirada del clip en la literatura
| Autores | N | Retirada de “clip” (%) | Mejoría (%) | Comentarios |
| Lin et al45 | 326 | 5 (1,5) | 4/5 (80) | Mejoría un año después de la retirada |
| Reisfeld et al51 | 326 | 5 (1,4) | 3/5 (60) | – |
| Lin y Chou et al47 | 102 | 2 (2) | 2/2 (100) | – |
| Chou et al24 | 56 | 13 (23) | 10/13 (77) | – |
| Reisfeld et al48 | 1.274 | 31 (2,4) | 25/31 (81) | Retirada dentro de los primeros 6 meses |
| Jo et al49 | 87 | 9 (10,3) | 8/9 (90) | Resultados a corto plazo |
| Kang et al50 | 116 | 15 (12,9) | 9/14 (64) | Resultados a corto y medio plazo |
| Reisfeld et al46 | 2.250 | 36 (1,6) | 13/25 (52) | Resultado a largo plazo |
Los resultados a largo plazo son prometedores, si bien, la evidencia demuestra que el efecto de la retirada del “clip” requiere más estudios para su completo conocimiento. Sin embargo, el mero hecho de que la reversibilidad sea una opción real, con resultados aceptables a largo plazo, hace que el “clipping” posea un atractivo extra sobre el resto de técnicas27.
Otras indicaciones de la cirugía del sistema nervioso simpático torácicoTrastornos vasomotoresLas alteraciones vasculares susceptibles de mejorar con una intervención sobre el SNST se describen a continuación:
Rubor facialEl rubor facial o “blushing” se define como la sensación de calor y enrojecimiento de la cara, orejas, cuello y, en ocasiones, de la parte superior del tórax debido a un aumento transitorio del flujo de sangre en dichas localizaciones. Su incidencia no está clara, pero son conocidas sus variaciones geográficas, siendo frecuente en los países escandinavos y raro en Asia52.
Ante una persona afecta de rubor facial, el primer paso es excluir una patología subyacente causante del mismo, como el síndrome carcinoide. La primera opción terapéutica es el tratamiento médico con agentes beta-bloqueantes, ansiolíticos, inhibidores de la recaptación de serotonina y otros fármacos antidepresivos. Aunque los resultados con este tipo de tratamiento son poco esperanzadores, deben de intentarse antes que la cirugía.
En esta patología, no está indicado el uso intradérmico de toxina botulínica tipo A, hasta que estudios bien diseñados demuestren su eficacia. Una vez intentada la solución con el tratamiento médico, si éste no es efectivo, se puede realizar la simpatectomía videotoracoscópica con la interrupción de T253.
Síndrome de RaynaudLa indicación quirúrgica es fundamentalmente en la forma primaria y cuando existe sintomatología grave y de larga duración, refractaria a tratamiento farmacológico. El empleo actual de algunos fármacos (prostaglandinas, vasodilatores, anticoagulantes) y de medidas generales contra el frío (guantes) debe ser considerado en primer lugar antes de sentar la indicación quirúrgica. La presencia de ulceraciones en los dedos, asociada a sintomatología dolorosa, que impide y limita la actividad cotidiana, refuerza la indicación de cirugía. Los resultados, con la interrupción de la cadena simpática al mismo nivel que la sudoración palmar son aceptables, pero no tan satisfactorios como los de la hiperhidrosis primaria18.
Arteriopatía obstructiva periférica y enfermedad de BuergerLa simpatectomía a nivel T2-T3 está indicada en el caso de enfermedad en estadio avanzado que no responde al tratamiento médico, o cuando está contraindicada, o no es posible la revascularización quirúrgica directa54. La presencia de úlceras o gangrena representa la indicación ideal y universalmente aceptada, aunque la intervención puede ser propuesta en estadios más precoces si tienen intensa sintomatología dolorosa, incluso en reposo. Se han publicado porcentajes de éxito terapéuticos muy variables55.
Síndromes coronariosAntes del empleo de los fármacos actuales, la única forma de provocar un bloqueo del sistema nervioso simpático del corazón era la ablación a una determinada altura de la cadena simpática. Aunque no hay un consenso sobre el nivel de sección, T3-T4 o T4-T5, parece aceptado que debe siempre incluir el 4° ganglio simpático dorsal. Durante los años treinta a los cincuenta del pasado siglo se utilizó la simpatectomía torácica a cielo abierto para el tratamiento de la angina pectoris y la taquiarritmia. Con el desarrollo de nuevos fármacos más específicos, esta indicación casi desapareció, quedando sólo reservada para casos de arritmias refractarias o a pacientes anginosos que no responden a la terapia convencional y no pueden someterse a terapia de revascularización56.
Distrofia simpático reflejaLa distrofía simpático refleja, llamada también síndrome regional doloroso complejo, es una afección que presenta una amplia gama de síntomas. Es de afectación multisistémica y suele comprometer a una o más extremidades, pudiendo afectar a cualquier parte del cuerpo.
En estos pacientes se debe intentar siempre la aplicación de diferentes técnicas de bloqueo simpático ya que, si se produce una remisión de los síntomas, además de confirmar este síndrome, ayuda a identificar los pacientes que se pueden beneficiar de una simpatectomía definitiva57. El nivel y longitud de la extirpación de la cadena simpática varía dependiendo de la zona afecta. En general, para las lesiones en las extremidades superiores se aconseja de T2 a T4 o T5, aunque no hay ningún consenso ni estudios aleatorizados que demuestren esto, por lo que el grado de evidencia científica es muy bajo.
Tratamiento del dolor abdominal. EsplanicectomíaEl tratamiento del dolor abdominal en pacientes con carcinoma pancreático o pancreatitis crónica es otra de las indicaciones para la exéresis de un segmento de la cadena simpática, en este caso el nervio esplácnico. En 1943, Mallet-Guy58 mostró que la denervación simpática del páncreas produce una interrupción del estímulo doloroso en este tipo de pacientes. La indicación de una esplanicectomía se plantea cuando fracasa el tratamiento médico y si el conducto pancreático no está dilatado o es pequeño.
Se recomienda acceder a la cadena simpática por videotoracoscopia bilateral secuencial, colocando al paciente en decúbito lateral, primero de un lado y luego del otro, ya que la posición de semi-Fowler no es buena para acceder a este segmento tan caudal del SNST. A través de tres puertas de entrada, una de 10mm para la cámara y dos de 5mm para el instrumental quirúrgico, se localiza la cadena simpática dorsal y se sigue en sentido caudal para identificar los nervios esplácnicos mayor y menor. Hasta la fecha, la técnica indicada es su extirpación.
En cuanto al porcentaje de éxito, se han publicado datos muy dispares que oscilan entre el 94% de Moodley19 (con un seguimiento de sólo 12 meses) y el 31% de Howard20.
Nota: No se hará constar el grado de recomendación en las circunstancias que impliquen práctica habitual o recomendable por no ser evaluables otras alternativas desde el punto de vista ético.
- –
Las pruebas de laboratorio no son necesarias en el diagnóstico de la hiperhidrosis primaria, aunque se recomiendan para descartar otras enfermedades que producen hiperhidrosis secundaria. R4 (Recomendación consistente. Calidad de evidencia muy baja).
- –
Las sales de aluminio a alta concentración son el tratamiento tópico de primera elección recomendado en el tratamiento de la hiperhidrosis primaria localizada. R2 (Recomendación consistente. Calidad de evidencia moderada).
- –
El uso de toxina botulínica A es muy eficaz en el control de la hiperhidrosis axilar (90%). Los resultados no son tan buenos en pacientes con hiperhidrosis palmar y es poco útil en la hiperhidrosis plantar y craneofacial. R2 (Recomendación consistente. Calidad de evidencia moderada).
- –
El tratamiento de la hiperhidrosis palmar, cuando fracasa el tratamiento médico, debe ser la interrupción de la cadena simpática por vía toracoscópica resultando una técnica segura y eficaz. R1 (Recomendación consistente. Calidad de evidencia alta).
- –
En el tratamiento de la hiperhidrosis axilar y/o cráneo-facial debe considerarse como una opción terapéutica la simpaticolisis toracoscópica. R3 (Recomendación consistente. Calidad de evidencia baja).
- –
Es obligado informar detalladamente al paciente de los resultados y posibles efectos secundarios de la simpaticolisis ya que esto puede condicionar la decisión del paciente. R2 (Recomendación consistente. Calidad de evidencia moderada).
Técnica quirúrgica
- –
Se recomienda sobre los niveles específicos de sección. R2 (Recomendación consistente. Calidad de evidencia moderada):
- •
Pacientes con rubor y/o sudoración facial: sección a nivel T2 y/o T3.
- •
Pacientes con hiperhidrosis palmar: sección a nivel T3 y/o T4.
- •
Pacientes con hiperhidrosis axilar: sección a nivel T4 o T4-T5.
- •
- –
Se recomienda la identificación e interrupción del nervio de Kuntz, así como extender lateralmente la coagulación sobre el segmento costal correspondiente. R2 (Recomendación consistente. Calidad de evidencia moderada).
- –
En la hiperhidrosis esencial primaria, el acceso ha de ser bilateral, en posición de semi-Fowler y con una o dos puertas de entrada. R2 (Recomendación consistente. Calidad de evidencia moderada).
- –
El procedimiento se puede realizar sin drenaje pleural o con su retirada precoz. R2 (Recomendación consistente. Calidad de evidencia moderada).
- –
La simpaticolisis torácica puede ser incluida en programas de cirugía sin ingreso, dado el escaso índice de morbilidad asociada. R2 (Recomendación consistente. Calidad de evidencia moderada).
- –
El tratamiento quirúrgico del rubor facial mediante la interrupción de la cadena simpática dorsal a nivel de T2 por videotoracoscopia se debe considerar cuando fracasa el tratamiento médico. R2 (Recomendación consistente. Calidad de evidencia moderada).
- –
La realización de una simpatectomía en situaciones como el síndrome de Raynaud, la enfermedad de Buerger, el síndrome coronario y el dolor abdominal intratable se debe condicionar a un estudio individualizado del paciente y a la valoración conjunta con otros especialistas médicos implicados en el tratamiento de éstas. R4 (Recomendación consistente. Calidad de evidencia muy baja).