La quinta fase de la Guía Española para el Manejo del Asma (GEMA) que incluye las versiones 5.0 y 5.1, ha efectuado una profunda revisión de su contenido. El presente texto tiene como objetivo contextualizar los principales cambios. Estos se podrían resumir en: DIAGNÓSTICO: nuevo punto de corte de óxido nítrico en aire exhalado (FENO) y clasificación de gravedad basada en el tratamiento necesario para mantener el control; ASMA INTERMITENTE: concepto más restrictivo y tratamiento ampliado a combinación de glucocorticoide/adrenérgico a demanda; ASMA LEVE: tratamiento con glucocorticoide/adrenérgico a demanda como alternativa si baja adhesión terapéutica a esteroide fijo clásico; ASMA GRAVE: reajuste de los fenotipos, incorporación de la triple terapia en un solo inhalador y criterios para la selección del fármaco biológico en asma grave no controlada; OTROS: puntualizaciones concretas en asma infantil, incorporación de determinados aspectos organizativos (flujos entre niveles asistenciales, unidades de asma y telemedicina), nuevas secciones de COVID-19 y de poliposis nasal.
In this fifth phase of development, the contents of the Spanish Asthma Management Guidelines (GEMA), which include versions 5.0 and 5.1, have undergone a thorough review. The aim here is to set the main changes in context. These could be summarized as follows: DIAGNOSIS: new FENO cut-off and severity classification based on treatment needed to maintain control; INTERMITTENT ASTHMA: a more restrictive concept and treatment extended to include a glucocorticoid/adrenergic combination as needed; MILD ASTHMA: glucocorticoid/adrenergic therapy as needed as an alternative in case of low therapeutic adherence to conventional fixed-dose steroids; SEVERE ASTHMA: readjustment of phenotypes, incorporation of triple therapy in a single inhaler, and criteria for selection of a biologic in severe uncontrolled asthma; OTHERS: specific scoring in childhood asthma, incorporation of certain organizational aspects (care circuits, asthma units, telemedicine), new sections on COVID-19 and nasal polyposis.
La Guía Española para el Manejo del Asma (GEMA), es hoy la guía de práctica clínica (GPC) de referencia internacional en español sobre la enfermedad asmática. En sus últimas ediciones de la quinta fase, versiones 5.0 y 5.1, han intervenido 108 expertos en asma o en aspectos relacionados con el mismo, que fueron seleccionados por las 21 sociedades científicas, asociaciones o fundaciones que la sustentan, españolas, portuguesa o latinoamericanas. Desde sus inicios, hace más de 20 años, la guía ha pretendido erigirse en un documento útil para el profesional sanitario que debe atender al paciente asmático, trasladando la mejor evidencia científica en recomendaciones prácticas, redactadas de forma escueta y sencilla.
Cada cinco años se renueva prácticamente en su totalidad, tanto en la forma (nueva redacción y presentación), como en el fondo (cambios conceptuales o de enfoque), para posteriormente ir efectuando breves actualizaciones anuales, en particular de las recientes novedades bibliográficas. En dicha línea, la pasada edición, la versión 5.0, presentó importantes cambios que se resumieron en una publicación en esta revista1. Por tanto, el presente texto complementa al anterior y tiene un doble objetivo, por un lado, recopila las novedades de esta nueva GEMA 5.1 y por otro, contextualiza los principales cambios de esta 5 ª fase recién estrenada. Cambios que, en ocasiones, no están exentos de cierta polémica (de ahí el título de este artículo), en su gran mayoría porque sus recomendaciones, muchas veces, no siguen exactamente las propuestas en otras GPC, en particular las de la guía internacional de referencia, la Global Initiative for Asthma (GINA)2. Sorprende que ambas guías basadas en pruebas o evidencia científica propongan recomendaciones diferentes. El hecho guarda relación con la interpretación que sus autores efectúan de la evidencia disponible, lo cual pone de manifiesto una cierta limitación de la actual medicina científica, por la que diferentes interpretaciones de una misma evidencia conllevan recomendaciones dispares.
Hemos estructurado estos cambios conceptuales y novedades en los siguientes cinco grandes bloques:
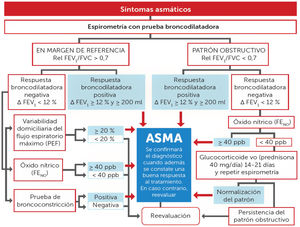
DiagnósticoÓxido nítrico exhalado (FENO). La figura 1 muestra el clásico algoritmo de GEMA elaborado para confirmar de forma objetiva el diagnóstico de asma. Este descansa en el uso de la espirometría con prueba broncodilatadora al demostrar en un paciente con síntomas de la enfermedad una obstrucción reversible significativa de los flujos espiratorios. No obstante, en muchas ocasiones, la exploración no resulta diagnóstica (la mayoría de la población asmática es de tipo leve, en los que la función pulmonar no es patológica), por lo que, en dicho contexto, GEMA recomienda utilizar otras técnicas complementarias que pueden incrementar la tasa de diagnósticos. Aunque todas ellas, incluida la espirometría con prueba broncodilatadora, pueden proporcionar falsos positivos, en un contexto clínico de alta sospecha de asma, pueden ayudar al clínico a asumir razonablemente el diagnóstico de la enfermedad. Entre estas destaca la medición del FENO, que proporciona de forma sencilla, no invasiva e inmediata, una medida indirecta de la inflamación bronquial del fenotipo T2, en parte relacionada con la inflamación eosinofílica3. El punto de corte para establecer el diagnóstico es arbitrario, cuanto mayor, más exigente pero más seguro y lo contrario, si es menor. Ha ido evolucionando con los años, inicialmente se estableció en 25 ppb, se incrementó luego a 50, para bajarlo en esta nueva GEMA a 40; siendo este último el que la mayoría de los consensos y GPC asumen actualmente como más razonable4,5.
Clasificación del nivel de gravedad. La gravedad del asma es una propiedad intrínseca de la enfermedad, que refleja la intensidad de las anomalías fisiopatológicas y su respuesta al tratamiento. La GEMA establece, en el asma del adulto, cuatro niveles: intermitente, persistente leve, persistente moderada y persistente grave. Establecer el nivel de gravedad es un paso imprescindible en la práctica clínica, pues naturaleza, pronóstico y necesidades terapéuticas distan mucho entre los diferentes niveles. Desde un punto de vista pragmático, por ejemplo, asma intermitente y asma grave son tan dispares que casi podrían ser dos entidades diferentes. La forma de establecer la gravedad también ha ido evolucionando con el paso del tiempo. La nueva GEMA, así como otras GPC recomiendan no efectuarlo al inicio de la terapia, sino cuando el paciente ya está recibiendo un tratamiento de mantenimiento adecuado y se ha evaluado y ajustado tras un período de tiempo razonable. Además, no es estática, puede variar a lo largo del tiempo.
En definitiva, el nivel de gravedad guarda relación con la cantidad de medicación que un paciente necesita para mantener el control y prevenir exacerbaciones6, tal y como muestra la tabla 1. Por ejemplo, si un individuo requiere el tratamiento de mantenimiento recomendado en el escalón 3 para mantener el control, padecerá un asma persistente moderada.
Clasificación de la gravedad del asma controlada tras ajustar el tratamiento de mantenimiento para mantener el control
| Gravedad | Intermitente | Persistente | ||
|---|---|---|---|---|
| Leve | Moderada | Grave | ||
| Necesidades mínimas de tratamiento para mantener el control | Escalón 1 | Escalón 2 | Escalón 3 o Escalón 4 | Escalón 5 o Escalón 6 |
Concepto. El primer nivel de gravedad de la enfermedad, el asma intermitente, supone todavía hoy un tema de debate no cerrado. Este nivel albergaría aquellas formas de asma con baja frecuencia de aparición de síntomas, por las que solo esporádicamente estos pacientes pueden presentar síntomas de la patología. Para algunos autores y algunas GPC, como por ejemplo GINA2, no existiría, incorporando estas formas ocasionales de asma como parte del asma persistente leve. A fin y al cabo el punto de corte de la frecuencia de síntomas para establecer la posible diferencia entre asma intermitente y leve es arbitraria. Además, el tratamiento clásico de dicho escalón basado exclusivamente en la administración a demanda de un agonista β2 adrenérgico de acción corta inhalado (SABA) podría favorecer el abuso de dicha terapia en detrimento del apropiado tratamiento antiinflamatorio con glucocorticoide inhalado (GCI) cuando aumenta la necesidad de uso del SABA. Sin embargo, negar su existencia obligaría a establecer un tratamiento de mantenimiento persistente en pacientes con síntomas de asma muy ocasionales, como por ejemplo sucede en personas con asma alérgica a pólenes, que pueden estar totalmente asintomáticos entre estaciones; o en niños con síntomas muy esporádicos en los que no se quiere iniciar una terapia prolongada con GCI.
Por dichos argumentos, la mayoría de los miembros del Comité Ejecutivo de GEMA, tras intenso debate, decidieron mantener este nivel, pero endureciendo sus criterios. En estas nuevas versiones de GEMA, se entiende como asma intermitente cuando los síntomas de la enfermedad o la necesidad de medicación de alivio se presentan con una frecuencia de ≤ 2 veces al mes, sin exacerbaciones y la función pulmonar dentro de los valores de referencia, cuando en pasadas ediciones era de ≤ 2 a la semana, tal y como se observa en la tabla 2.
Clasificación del control del asma en adultos
| Bien controlada (todos los siguientes) | Parcialmente controlada (cualquier medida en cualquier semana) | Mal controlada | |
|---|---|---|---|
| Síntomas diurnos | Ninguno o ≤ 2 días al mes | > 2 días al mes | Si ≥ 3 características de asma parcialmente controlada |
| Limitación de actividades | Ninguna | Cualquiera | |
| Síntomas nocturnos/despertares | Ninguno | Cualquiera | |
| Necesidad medicación de alivio (rescate) (agonista β2 adrenérgico de acción corta) | Ninguna o ≤ 2 días al mes | > 2 días al mes | |
| Función pulmonarFEV1PEF | ≥ 80% del valor teórico o z-score (-1,64)≥ 80% del mejor valor personal | < 80% del valor teórico z-score (-1,64)< 80% del mejor valor personal | |
| Exacerbaciones | Ninguna | ≥ 1/año | ≥ 1 en cualquier semana |
FEV1: volumen espiratorio forzado en el primer segundo; PEF: pico del flujo espiratorio o flujo espiratorio máximo.
Tratamiento. El cambio conceptual de la definición de asma intermitente se acompañó también de un cambio de su tratamiento, en esta quinta fase de GEMA. Como antes se comentó, dicho nivel se ha venido tratando tradicionalmente con SABA a demanda administrado según la necesidad percibida por el propio paciente ante la presencia de síntomas de asma. Sin embargo, esta estrategia, de forma inadvertida, podría promover el sobreuso de SABA, infrautilizando los GCI7. Diversos estudios mostraron que existe un abuso de SABA y que este se asocia a una mayor morbimortalidad de la enfermedad8,9. Por otro lado, algunos trabajos observaron la eficacia y seguridad en dicho nivel de la administración a demanda de la combinación en un solo inhalador de un GCI (budesónida o beclometasona) a dosis bajas y formoterol o salbutamol10,11.
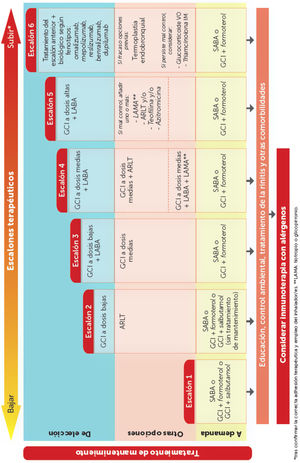
De esta forma, las nuevas versiones de GEMA proponen tratar a estos pacientes con asma intermitente con una de las tres siguientes opciones de fármacos administrados a demanda (fig. 2): SABA, combinación GCI (dosis bajas)/formoterol o combinación GCI (dosis bajas)/salbutamol, en función de las características clínicas del paciente, que permitirían seleccionar un tratamiento individualizado en cada caso. No obstante, los enfermos deberían ser evaluados con técnicas complementarias (espirometría, FENO) para descartar formas más graves de la enfermedad que cursen con pocos síntomas y que, en consecuencia, necesitarán de tratamientos de mantenimiento más enérgicos.
Asma leveSin duda, uno de los puntos más polémicos en la actualidad es cuál es la mejor opción terapéutica para el tratamiento de dicho grupo de pacientes. Cuestión no menor, pues la mayoría de la población asmática se encuadra en este nivel de gravedad y, por tanto, por las importantes consecuencias económicas que ello supone, tanto para el que lo debe sufragar (frecuentemente los sistemas de salud pública), como para el fabricante/vendedor (industria farmacéutica). Recientemente, un grupo internacional de expertos, en su mayoría los líderes de la actual GINA, ante la constatación de que el control del asma de la mayoría de los pacientes seguía siendo deficiente a pesar de disponer de cada vez más efectivos y seguros tratamientos, promovieron un cambio de paradigma terapéutico7.
Con la intención de demostrar la eficacia de una nueva estrategia terapéutica, la administración a demanda de la combinación de budesónida/formoterol frente al tratamiento clásico de GCI (dosis bajas) fijo y diario, en la terapia de mantenimiento del asma leve, se promovieron dos ensayos clínicos, los denominados estudios SYGMA. En los que se compararon la eficacia de ambas estrategias sobre diferentes variables: prevención de exacerbaciones (principal), control, función pulmonar y calidad de vida12,13. Ambas estrategias presentaron una capacidad similar en la prevención de exacerbaciones, pero en general, los pacientes que fueron tratados con budesónida/formoterol a demanda presentaron significativos peores niveles de control, función pulmonar y calidad de vida. Con la hipótesis de que los pacientes con asma leve, particularmente los jóvenes, cursan con una baja adhesión terapéutica a GCI fijo y, por tanto, la administración a demanda de budesónida/formoterol pudiera proporcionar una mayor eficacia terapéutica, se efectuaron posteriormente dos estudios en «vida real», novelSTART14 y PRACTICAL15, con similares variables y supuestos que sus predecesores. No obstante, se han cuestionado ambos por adolecer de diseños subóptimos (inclusión de casos con asma moderada infratratados) y por presentar tasas de adhesión terapéutica sorprendentemente elevadas (76%) para tratarse de escenarios de vida real y con resultados dispares de ambos estudios.
Si bien GINA2 acepta esta evidencia como prueba suficiente para promover la indicación de la combinación budesónida/formoterol como primera opción en el tratamiento del asma leve, al mismo nivel que GCI fijo, la valoración de las autoridades sanitarias europeas fue negativa. Consideran que dicha evidencia muestra justo lo contrario, la inferioridad de la nueva opción, y por el momento, esta combinación no cuenta con la aprobación (legal en ficha técnica) para ser administrada a demanda en asma leve o intermitente. Entre ambas posturas, equidistante, se encuentra la opinión de GEMA (fig. 2), que sigue considerando como tratamiento de elección en el asma persistente leve (escalón 2) la administración diaria y prolongada de un GCI a dosis bajas (recomendación 3.4). Pero, como alternativa, podría considerarse el uso a demanda de budesónida/formoterol, beclometasona/formoterol, o beclometasona/salbutamol en pacientes con baja adhesión terapéutica en los que fracasó una intervención educativa correctora específica (recomendación 3.5). No obstante, como ya se ha comentado, esta estrategia no está aprobada en sus fichas técnicas y se desconoce su coste-efectividad.
El tema no está cerrado, persisten muchas incógnitas por responder acerca de esta posible nueva estrategia: ¿existe un perfil de paciente idóneo?, por el contrario, ¿otro no idóneo?, ¿está suficientemente tratada la inflamación bronquial subyacente?, ¿cómo será la evolución clínica de estos pacientes a medio y largo plazo? Se requiere más evidencia, entre otros estudios, sigue pendiente efectuar uno bien diseñado en condiciones de verdadera vida real para establecer definitivamente su efectividad.
Asma graveLa aparición de nuevos tratamientos específicos para determinadas variantes de asma grave ha incrementado notablemente el estado del conocimiento. Ello ha condicionado el lógico crecimiento de dicho apartado en la guía.
Fenotipos. Con la visión práctica que caracteriza a la GEMA en estas nuevas ediciones se ha restringido la necesidad de establecer el fenotipo a solo el asma grave. Básicamente, porque realizarlo en los niveles de menor gravedad probablemente incrementa innecesariamente la complejidad (relevante en el ámbito de la atención primaria), máxime cuando son formas clínicas que responden excelentemente al tratamiento habitual.
Establecer el fenotipo de asma en los pacientes con asma grave no controlada (AGNC) constituye parte de la acción diagnóstica a realizar en dichos enfermos, pues puede conllevar un tratamiento diferencial y tener implicaciones pronósticas. A tal fin, se utilizan las siguientes características clínicas (edad, inicio de los síntomas, presencia de síntomas alérgicos, afectación de la vía respiratoria superior, existencia de enfermedad respiratoria exacerbada por aspirina [EREA]), funcionales (espirometría, FENO), y analíticas (eosinófilos en sangre y esputo, inmunoglobulina E [IgE] total, neutrófilos en esputo inducido)16–18. Esta información identifica dos tipos de patrón inflamatorio: T2 alto y T2 bajo, lo cual permite clasificar al AGNC en tres fenotipos, T2-alérgico, T2-eosinofílico y no T2 (tabla 3), aunque es frecuente observar cierto grado de solapamiento entre ambos fenotipos T2. Se ha prescindido del antiguo fenotipo de «asma grave asociada a obesidad», pues probablemente la obesidad (significativamente más frecuente en asma grave) más que un fenotipo específico, sea una comorbilidad.
Fenotipos de asma grave
| Fenotipos | Características clínicas | Biomarcadores | Tratamiento |
|---|---|---|---|
| Alérgica (T2) | Síntomas alérgicos + Sensibilización a alérgeno (Prick test y/o IgE específica) | IgE específicaCitocinas Th2PeriostinaEosinófilos y neutrófilos en esputo | GlucocorticoidesOmalizumabAnti IL-5/IL-5R (mepoluzimab, reslizumab, benralizumab)Dupilumab |
| Eosinofílica (T2) | Rinosinusitis crónica/poliposis nasalEREACorticodependiente o insensible a glucocorticoides | Eosinófilos en sangre y esputo IL-5Cisteinil-leucotrienos | ARLTAnti IL-5/IL-5R (mepoluzimab, reslizumab, benralizumab)Dupilumab |
| No T2 | Menor FEV1Mayor atrapamientoAntecedente de tabaquismo | Neutrófilos o paucigranulocítica en esputoActivación TH17IL-8 | Azitromicina |
EREA: enfermedad respiratoria exacerbada por ácido acetilsalicílico; FEV1: volumen espiratorio forzado en el primer segundo; IgE: inmunoglobulina E; IL: interleucina.
Tratamiento con triple terapia en un solo inhalador. Probablemente la novedad más destacada de la GEMA 5.1 sea la incorporación al arsenal terapéutico del tratamiento del asma la combinación en un solo inhalador de un GCI, un agonista β2 adrenérgico de acción larga (LABA) y un antimuscarínico de acción larga (LAMA) (fig. 2). Si bien en el pasado ya figuraba tiotropio, como único LAMA aceptado para el tratamiento del asma grave, añadido a una combinación de GCI/LABA, este se administraba en otro inhalador (Respimat®). Diversos ensayos clínicos recientes han demostrado que la triple combinación en un solo inhalador, en el que el LAMA era glicopirronio (en cartucho presurizado o en polvo seco monodosis), mejoraba la función pulmonar y reducía las exacerbaciones en pacientes insuficientemente controlados con un GCI/LABA, particularmente en los que cursaban con obstrucción del flujo aéreo (relación FEV1/FVC postbroncodilatador ≤ 70%)19–21.
Selección del fármaco biológico en el tratamiento del asma grave no controlada. Una de las novedades destacadas de esta quinta generación GEMA fue la incorporación de fármacos biológicos recientemente comercializados para el tratamiento del AGNC. En la actualidad, aprobados por la EMA y recogidos en la guía, se dispone de los siguientes biológicos utilizados en el tratamiento del AGNC T2: con acción anti IgE (omalizumab), anti interleucina 5/interleucina 5Rα (IL5/IL-5Rα) (mepolizumab, reslizumab y benralizumab) y anti IL4/IL13 (dupilumab).
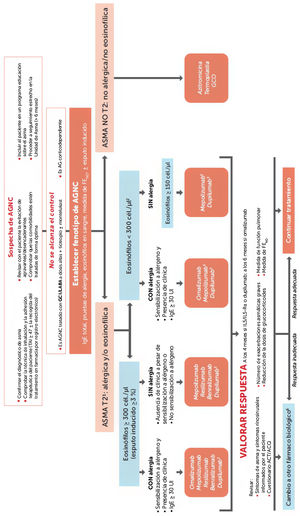
Especialmente novedosa, en comparación con otras GPC, es la propuesta de selección del biológico como recoge el algoritmo de la figura 3, basado en gran medida en el consenso previo Sociedad Española de Neumología y Cirugía Torácica (SEPAR) sobre asma grave22. Tras establecer el fenotipo del asma del paciente tal y como antes se describió, pero principalmente según el resultado de la IgE total, pruebas cutáneas de alergia, eosinófilos en sangre (o esputo inducido) y FENO, se clasifica el asma como T2 o noT2. En el caso de asma T2 el recuento en sangre de eosinófilos (mayor o menor a 300 μL), ubica al paciente en uno de dos grandes grupos: asma T2 eosinofílica o asma T2 no eosinofílica. A continuación, en cada uno de ellos, si es eosinofilia alérgica o no, según el resultado de las pruebas cutáneas de alergia, IgE total e historia clínica sugestiva de alergia, se asignará el paciente a uno de los cuatro grupos que muestra el algoritmo. En función de este, se propone una primera opción terapéutica, que se podrá cambiar si concurriesen otras circunstancias (intolerancias, alergias, vía de administración, etc.), o fracaso de la respuesta terapéutica (total o parcial), por algunos de los otros disponibles en cada grupo.
Tratamiento del asma grave no controlada según fenotipo inflamatorio. ACQ: Cuestionario de Control del Asma; ACT: Test de Control del Asma; AG: asma grave; AGNC: asma grave no controlada; GCI: glucocorticoides inhalados; GCO: glucocorticoides orales; LABA: broncodilatadores de larga duración; TAI: Test de Adhesión a Inhaladores.
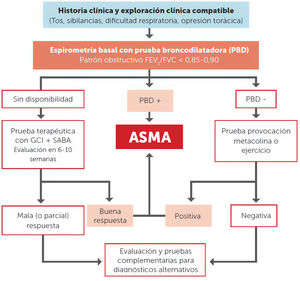
La limitación de la extensión del presente texto imposibilita incluir y describir con detalle todos los cambios de esta nueva GEMA, pero entre estos, en este cajón de sastre que supone este quinto apartado, se podrían destacar la inclusión de algunos consensos multidisciplinares locales elaborados para la mejora del flujo de pacientes entre niveles asistenciales y con los servicios de urgencias23,24. Así como la descripción de las Unidades de Asma acreditadas por SEPAR o por Sociedad Española de Alergología e Inmunología Clínica (SEAIC)25, y del papel de la telemedicina en el seguimiento de los pacientes asmáticos. La inclusión de nuevas secciones como, por ejemplo, sobre rinosinusitis y poliposis nasal (6.5) en el capítulo 6 de rinitis asociada a asma y en la GEMA 5.1, sobre la aspergilosis broncopulmonar alérgica (8.8) en el capítulo 8 de circunstancias especiales. En cuanto a la recomendación de emplear intervenciones educativas reducidas o mínimas si no se puede aplicar un programa de educación formal o clásico en asma, se propone en este contexto utilizar un sencillo plan de acción por escrito reducido26,27. Hay que destacar también los múltiples cambios efectuados en diferentes secciones que abordan el asma infantil, entre estos, la propuesta de algoritmo diagnóstico (fig. 4), el papel de la FENO en su seguimiento, algunas puntualizaciones en el tratamiento general y en la prescripción de mepolizumab en la sección de asma grave.
Y dada la pandemia actual por la infección del betacoronavirus SARS-CoV-2 y las múltiples publicaciones que evalúan su impacto sobre el asma o viceversa, el asma sobre la infección, la guía no podía dejar de incluir una sección para exponerlas. En resumen, se podría afirmar (provisionalmente) que con la evidencia actual disponible padecer asma no grave, no se asociaría a una mayor probabilidad para desarrollar, cursar con mayor gravedad o fallecer por la COVID-1928. Sin embargo, en el asma grave la información es ambivalente, algunas series constatan una mayor frecuencia y morbimortalidad29, otras no30. Por otro lado, estudios recientes efectuados sobre amplias muestras de casos parecen sugerir que el tratamiento con GCI podría ofrecer cierta capacidad protectora contra la infección31. Se ha incluido además una práctica tabla de las posibles interacciones farmacológicas entre los fármacos empleados para tratar la infección y el asma32.
Finalmente, queremos destacar la posición ponderada que en determinados aspectos controvertidos GEMA ocupa y en la que nos sentimos cómodos. Más allá de los debates, en los que todos participamos, la guía se debe basar en la evidencia y esta debe ser evaluada con la mayor imparcialidad posible, sin dejarse influenciar por creencias, otras GPC y presiones externas. A fin de cuentas, lo que pretende GEMA es elaborar un texto sencillo, pero riguroso, que resulte fácil de aplicar por el profesional sanitario en la asistencia de sus pacientes con asma.
Conflicto de interesesLos redactores de la guía declaran haber recibido en los dos últimos años honorarios por su participación en reuniones, congresos o trabajos de investigación organizados por las siguientes industrias farmacéuticas: ALK, AstraZeneca, Bial, Boehringer-Ingelheim, Chiesi, Esteve, GlaxoSmithKline, Leti, Menarini, MSD, Mundipharma, Novartis, Orion, Pfizer, Sanofi, Teva y Zambón.