Las normativas internacionales y españolas recomiendan el tratamiento intensivo de la tuberculosis (TB) con cuatro fármacos. El objetivo es determinar si en España se sigue esta recomendación y los factores asociados a utilizar tres fármacos (pauta estándar sin etambutol).
MetodologíaEstudio multicéntrico descriptivo, retrospectivo, en el que se analizaron los datos de los pacientes diagnosticados de TB en prácticamente todas las Comunidades Autónomas españolas entre 2007 y 2012. El estudio de factores asociados a prescribir tres fármacos se basó en regresión logística, calculándose las odds ratio (OR) y sus correspondientes intervalos de confianza del 95% (IC).
ResultadosSe incluyeron 3.189 pacientes, de los que 1.413 (44,3%) fueron tratados con tres fármacos. Este porcentaje fue del 41,2% en los pacientes con baciloscopia positiva, del 36,1% en los que tenían al menos resistencia a un fármaco, del 31,4% en los que tenían infección por VIH y del 24,8% en los inmigrantes. Los factores asociados al uso de tres fármacos fueron: ser mujer (OR=1,18; IC: 1,00-1,39); ser autóctono (OR=3,09; IC: 2,58-3,70); estar jubilado (OR=1,42; IC: 1,14-1,77); vivir sin techo (OR=3,10; IC: 1,52-6,43), vivir solo (OR=1,62; IC: 1,11-2,36) o en familia (OR=1,97; IC: 1,48-2,65); ser atendido por especialistas de zona (OR=1,37; IC: 1,10;1,70); no estar infectado por el VIH (OR=1,63; IC: 1,09-2,48) y tener baciloscopia negativa con cultivo positivo (OR=1,59; IC: 1,25-2,02).
ConclusionesExiste una proporción importante de tratamiento intensivo con tres fármacos. Se deben seguir las recomendaciones del tratamiento de la TB, tanto en la práctica clínica habitual como por parte del Plan para la Prevención y Control de la TB en España.
International and Spanish guidelines recommend a 4-drug regimen in the intensive treatment of tuberculosis (TB). The aim of our study was to determine if these recommendations are followed in Spain, and the factors associated with the use of 3 drugs (standard regimen without ethambutol).
MethodologyObservational, multicenter, retrospective analysis of data from patients diagnosed with TB in practically all Spanish Autonomous Communities between 2007 and 2102. Factors associated with the use of 3 drugs were analyzed using logistic regression, and odds ratios (OR) and corresponding 95% confidence intervals (CI) were calculated.
ResultsA total of 3,189 patients were included, 1,413 (44.3%) of whom received 3 drugs. The percentage of 3-drug users among patients with positive sputum smear was 41.2%; among patients with resistance to at least 1 drug, 36.1%; among HIV-infected patients, 31.4%; and among immigrants, 24.8%. Factors associated with the use of 3 drugs were: female sex (OR=1.18; CI: 1.00-1.39); native Spanish (OR=3.09; CI: 2.58-3.70); retired (OR=1.42; CI: 1.14-1.77); homeless (OR=3.10; CI: 1.52-6.43); living alone (OR=1.62; CI: 1.11-2.36); living in a family (OR=1.97; CI: 1.48-2.65); seen by specialists in the region (OR=1.37; CI: 1.10;1.70); no HIV infection (OR=1.63; CI: 1.09-2.48); and negative sputum smear with positive culture (OR=1.59; CI: 1.25-2.02).
ConclusionsA large proportion of TB patients receive intensive treatment with 3 drugs. TB treatment recommendations should be followed, both in routine clinical practice and by the National Plan for Prevention and Control of Tuberculosis in Spain.
Las normativas internacionales1-3 y españolas4-7 del tratamiento de la tuberculosis (TB) recomiendan el tratamiento habitual o estándar en el periodo intensivo o inicial con 4 fármacos (isoniacida, rifampicina, piracinamida y etambutol). No obstante, es motivo de discusión, dependiendo del nivel de resistencias a los fármacos antituberculosos en la zona geográfica en la que se desarrolle la enfermedad o del tipo de TB (localización, datos microbiológicos) que presente el paciente, el que se pueda suprimir el cuarto fármaco (etambutol) en el tratamiento intensivo de la enfermedad.
El motivo principal de añadir etambutol en la fase intensiva es instaurar un tratamiento con suficiente número de fármacos eficaces, intentando cubrir la posibilidad de que existan resistencias a los fármacos de primera línea y evitar el desarrollo de nuevas resistencias, por lo que el dato más importante para su indicación es la cifra de resistencias que existen en un determinado país o área geográfica, aunque en el momento actual en el que existe una globalización importante, con un traslado constante de personas de unos países a otros, es difícil conocer si una determinada persona va o no va a tener resistencias. Aparte de los flujos de personas entre países, la transmisión de la TB tiene unos mecanismos muy variables, por lo que personas que tienen altos niveles de resistencias pueden transmitir la enfermedad a grupos que tradicionalmente las tienen reducidas, lo que puede ocurrir también en sentido contrario. Por ello las guías nacionales e internacionales recomiendan la utilización sistemática de cuatro fármacos en el tratamiento intensivo de la TB pulmonar por lo menos hasta conocer los resultados del antibiograma y, por lo tanto, de las resistencias a fármacos.
Un estudio reciente nacional y multicéntrico sobre resistencias llevado a cabo en España8 muestra cifras de resistencia a isoniacida del 6,7% y de TB multirresistente (MDR, acrónimo del término anglosajón multidrug resistant, resistencia al menos a hidracidas y rifampicina) del 1,9%; además, un análisis preliminar de los datos disponibles acerca del uso de 3 o 4 fármacos en el tratamiento intensivo de la TB indicaba que un alto porcentaje de los casos en España se trataban con tres fármacos9, a pesar de las indicaciones de las distintas guías mencionadas. Esta situación es la que sugirió la necesidad de llevar a cabo el presente estudio.
El objetivo de nuestro estudio es determinar si en España se sigue la normativa del tratamiento intensivo de la TB con cuatro fármacos, así como identificar factores asociados a prescribir solamente tres fármacos (pauta estándar sin etambutol) en dicha fase intensiva.
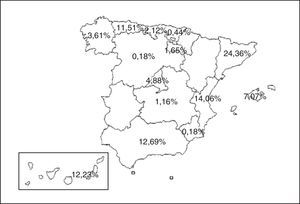
Material y métodosSujetosSe analizaron los datos de los pacientes diagnosticados de TB pertenecientes a prácticamente todas las Comunidades Autónomas españolas (fig. 1) e incluidos en la base de datos del Programa Integrado de Investigación en Tuberculosis (PIITB) de la Sociedad Española de Neumología y Cirugía Torácica (SEPAR) entre los años 2007 y 2012, ambos inclusive. Los criterios de inclusión fueron: a)baciloscopia positiva, o negativa con cultivo positivo de Mycobacterium tuberculosis, o en caso de TB extrapulmonares, demostración de granulomas caseificantes en la histología; b)pacientes con sospecha clínica, radiológica, epidemiológica y/o de laboratorio en los que su médico considere adecuado iniciar tratamiento antituberculoso, y c)consentimiento informado.
DiseñoEstudio multicéntrico descriptivo, retrospectivo. La información obtenida de cada paciente se almacenó en un cuaderno de recogida de datos electrónico (CRD) disponible en una aplicación informática a la que se accede a través de una web mediante una clave y un identificador personalizados para cada uno de los investigadores colaboradores en el estudio. El control de la cumplimentación de las encuestas y la base de datos se llevó a cabo mediante comunicación telefónica y correo electrónico.
Variables de estudioTodas las variables habían sido recogidas en el CRD de forma prospectiva y se describen a continuación. Datos sociodemográficos (edad; sexo; país de origen; situación laboral; profesión; convivencia; fecha y lugar de asistencia; antecedentes de uso de tabaco, alcohol y otras drogas). Patologías asociadas (VIH; otras inmunodepresiones). Anamnesis (antecedentes de TB; fecha de inicio de los síntomas). Métodos diagnósticos (fecha de solicitud de pruebas diagnósticas; localización de la TB; enfermedades asociadas; baciloscopia; cultivo; radiología; sensibilidad a fármacos). Tratamiento (pauta; fecha de inicio del tratamiento; fecha prevista de finalización; evolución clínica; adherencia al tratamiento; tratamiento directamente observado; comprensión de la enfermedad y del tratamiento). Conclusión final de la terapia (curación, tratamiento completado, fracaso, traslado, abandono, muerte por TB, muerte por otra causa, fecha de defunción, prolongación de tratamiento, perdido).
Análisis de datosSe analizó la distribución de frecuencias de las variables de interés, y a nivel bivariante se llevó a cabo la comparación de proporciones entre grupos mediante la prueba de χ2. Los factores asociados a dar 3 o 4 fármacos en el tratamiento inicial se analizaron mediante el método de selección stepwise, incluyendo los factores significativos a nivel bivariante con una p<0,05. Se calcularon las odds ratio (OR) y sus correspondientes intervalos de confianza del 95% (IC), y se consideró significativa una p<0,05. Para realizar los análisis se utilizó el software estadístico IBM SPSS Statistics 19.
ResultadosUn total de 3.189 pacientes fueron incluidos en este estudio. Destaca un predominio de varones (1.940; 60,8%), y que 1.122 (35,2%) eran inmigrantes. La localización fue pulmonar en 2.476 (77,6%) casos. Tenían baciloscopia positiva 1.669 (52,3%), baciloscopia negativa con cultivo positivo 907 (28,4%) y baciloscopia y cultivo negativos 524 (16,4%). No tenían resistencias a ningún fármaco 2.981 (93,5%) y presentaban resistencia a al menos un fármaco 208 (6,5%). Un total de 1.776 (55,7%) fueron tratados con cuatro fármacos y 1.413 (44,3%) con tres (tabla 1).
Características diferenciales del uso de 3 vs 4 fármacos en la fase inicial del tratamiento de la tuberculosis
| Total | 4F | 3F | |||
|---|---|---|---|---|---|
| n=3.189 | n=1.776 | % | n=1.413 | % | |
| Sexo | |||||
| Hombre | 1.940 | 1.094 | 56,4 | 846 | 43,6 |
| Mujer | 1.128 | 605 | 53,6 | 523 | 46,4 |
| País de origen | |||||
| Otros | 1.122 | 844 | 75,2 | 278 | 24,8 |
| España | 2.067 | 932 | 45,1 | 1.135 | 54,9 |
| Situación laboral | |||||
| Activo | 1.601 | 953 | 59,5 | 648 | 40,5 |
| En paro | 647 | 369 | 57 | 278 | 43 |
| Jubilado | 524 | 205 | 39,1 | 319 | 60,9 |
| Incapacidad laboral | 40 | 22 | 55 | 18 | 45 |
| Tipo de convivencia | |||||
| Grupo | 372 | 293 | 78,8 | 79 | 21,2 |
| Familia | 2.269 | 1.177 | 51,9 | 1.092 | 48,1 |
| Solo | 276 | 158 | 57,2 | 118 | 42,8 |
| Sin techo | 42 | 19 | 45,2 | 23 | 54,8 |
| Confinado | 38 | 21 | 55,3 | 17 | 44,7 |
| Lugar de asistencia | |||||
| Urgencias | 1.569 | 924 | 58,9 | 645 | 41,1 |
| Especialista zona | 539 | 249 | 46,2 | 290 | 53,8 |
| Médico de atención primaria | 616 | 324 | 52,6 | 292 | 47,4 |
| VIH | |||||
| Sí | 137 | 94 | 68,6 | 43 | 31,4 |
| No | 2.465 | 1.416 | 57,4 | 1.049 | 42,6 |
| Microbiología | |||||
| Cultivo(−) | 524 | 320 | 61,1 | 204 | 38,9 |
| BK(+) | 1.669 | 982 | 58,8 | 687 | 41,2 |
| BK(−)/cultivo(+) | 907 | 421 | 46,4 | 486 | 53,6 |
| Resistencia a fármacos | |||||
| Sí | 208 | 133 | 63,9 | 75 | 36,1 |
| No | 2.981 | 1.643 | 55,1 | 1.338 | 44,9 |
| Comprensión de la enfermedad y del tratamiento | |||||
| Difícil | 192 | 115 | 59,9 | 77 | 40,1 |
| Fácil | 2.579 | 1.407 | 54,6 | 1.172 | 45,4 |
| Año de diagnóstico | |||||
| 2009 | 528 | 366 | 69,3 | 162 | 30,7 |
| 2007 | 717 | 373 | 52 | 344 | 48 |
| 2008 | 501 | 301 | 60,1 | 200 | 39,9 |
| 2010 | 443 | 236 | 53,3 | 207 | 46,7 |
| 2011 | 563 | 307 | 54,5 | 256 | 45,5 |
| 2012 | 437 | 193 | 44,2 | 244 | 55,8 |
4F: cuatro fármacos: 3F: tres fármacos; BK: baciloscopia.
En ocasiones los datos no suman el total de casos por existir variables que no se han cumplimentado al 100% (missings).
Los resultados del análisis estadístico de las características de los casos tratados con 3 vs 4 fármacos y los factores asociados al uso de solamente tres fármacos se muestran en las tablas 1 y 2, respectivamente, destacando que se trató con cuatro fármacos a 982 pacientes de los que tenían baciloscopia positiva, (58,8%), a 844 de los inmigrantes (75,2%), a 94 de los que tenían infección por VIH (68,6%), a 293 de los que vivían en grupo (77,8%), y a 133 de los que tenían resistencias a al menos un fármaco (63,9%). Fueron tratados con tres fármacos 687 (41,2%) pacientes de los que tenían baciloscopia positiva, 278 (24,8%) de los pacientes inmigrantes, 43 (31,4%) de los que tenían infección por VIH y 75 (36,1%) pacientes que tenían al menos resistencia a un fármaco.
Factores asociados al uso de solamente 3 fármacos en una cohorte de 3.189 pacientes con tuberculosis. Análisis univariante
| Análisis univariante | ||
|---|---|---|
| OR (IC 95%) | p | |
| Sexo | ||
| Hombre | Ref. | Ref. |
| Mujer | 1,12 [0,96-1,30] | 0,139 |
| País de origen | ||
| Otros | Ref. | Ref. |
| España | 3,69 [3,15-4,34] | <0,001 |
| Situación laboral | ||
| Activo | Ref. | Ref. |
| En paro | 1,11 [0,92-1,33] | 0,278 |
| Jubilado | 2,29 [1,87-2,80] | <0,001 |
| Incapacidad laboral | 1,21 [0,63-2,27] | 0,566 |
| Tipo de convivencia | ||
| Grupo | Ref. | Ref. |
| Familia | 3,43 [2,66-4,49] | <0,001 |
| Solo | 2,76 [1,96-3,91] | <0,001 |
| Sin techo | 4,46 [2,31-8,72] | <0,001 |
| Confinado | 3,00 [1,49-5,97] | 0,002 |
| Lugar de asistencia | ||
| Urgencias | Ref. | Ref. |
| Especialista zona | 1,67 [1,37-2,03] | <0,001 |
| Médico de primaria | 1,29 [1,07-1,56] | 0,008 |
| VIH | ||
| Sí | Ref. | Ref. |
| No | 1,62 [1,12-2,36] | 0,009 |
| Microbiología | ||
| Cultivo(−) | Ref. | Ref. |
| BK(+) | 1,10 [0,90-1,34] | 0,365 |
| BK(−)/cultivo(+) | 1,81 [1,45-2,25] | <0,001 |
| Resistencia a fármacos | ||
| Sí | Ref. | Ref. |
| No | 1,44 [1,08-1,94] | 0,013 |
| Año de diagnóstico | ||
| 2009 | Ref. | Ref. |
| 2007 | 2,08 [1,65-2,64] | <0,001 |
| 2008 | 1,50 [1,16-1,94] | 0,002 |
| 2010 | 1,98 [1,52-2,58] | <0,001 |
| 2011 | 1,88 [1,47-2,42] | <0,001 |
| 2012 | 2,85 [2,19-3,72] | <0,001 |
BK: baciloscopia.
Ref. es el dato de la variable que se ha utilizado como referencia para el análisis.
El análisis multivariante confirmó la asociación del uso de tres fármacos principalmente con ser mujer; ser autóctono; estar jubilado; vivir sin techo, solo o en familia (tomando como referencia el vivir en grupo); haber sido tratado por especialistas de zona (en referencia a haber sido atendido en Urgencias); no tener infección por VIH, y tener baciloscopia negativa y cultivo positivo (tabla 3).
Factores asociados al uso de solamente 3 fármacos en una cohorte de 3.189 pacientes con tuberculosis. Análisis multivariante
| Análisis multivariante | ||
|---|---|---|
| OR (IC 95%) | p | |
| Sexo | ||
| Hombre | Ref. | Ref. |
| Mujer | 1,18 [1,00-1,39] | 0,039 |
| País de origen | ||
| Otros | Ref. | Ref. |
| España | 3,09 [2,58-3,70] | <0,001 |
| Situación laboral | ||
| Activo | Ref. | Ref. |
| En paro | 1,18 [0,96-1,45] | 0,103 |
| Jubilado | 1,42 [1,14-1,77] | 0,001 |
| Incapacidad laboral | 0,80 [0,40-1,58] | 0,531 |
| Tipo de convivencia | ||
| Grupo | Ref. | Ref. |
| Familia | 1,97 [1,48-2,65] | <0,001 |
| Solo | 1,62 [1,11-2,36] | 0,011 |
| Sin techo | 3,10 [1,52-6,43] | 0,001 |
| Confinado | 2,03 [0,95-4,27] | 0,062 |
| Lugar de asistencia | ||
| Urgencias | Ref. | Ref. |
| Especialista zona | 1,37 [1,10-1,70] | <0,001 |
| Médico de primaria | 1,21 [0,98-1,48] | 0,062 |
| VIH | ||
| Sí | Ref. | Ref. |
| No | 1,63 [1,09-2,48] | 0,017 |
| Microbiología | ||
| Cultivo(−) | Ref. | Ref. |
| BK(+) | 1,00 [0,80-1,25] | 0,964 |
| BK(−)/cultivo(+) | 1,59 [1,25-2,02] | <0,001 |
| Resistencia a fármacos | ||
| Sí | Ref. | Ref. |
| No | 1,30 [0,94-1,79] | 0,105 |
| Año de diagnóstico | ||
| 2009 | Ref. | Ref. |
| 2007 | 2,49 [1,92-3,23] | <0,001 |
| 2008 | 1,70 [1,29-2,25] | <0,001 |
| 2010 | 2,23 [1,69-2,97] | <0,001 |
| 2011 | 2,01 [1,54-2,63] | <0,001 |
| 2012 | 2,98 [2,25-3,96] | <0,001 |
BK: baciloscopia.
Ref. es el dato de la variable que se ha utilizado como referencia para el análisis.
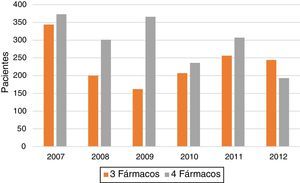
En la evolución del tratamiento (3 vs. 4 fármacos) a lo largo de los años (fig. 2 y tabla 1) destaca un aumento de la proporción de casos tratados con cuatro fármacos en los años 2008 y 2009, con un descenso posterior, llegando incluso en 2012 a haber un porcentaje mayor de pacientes tratados con tres que con cuatro fármacos.
En relación con la evolución clínica de los casos o conclusión final del tratamiento, no se detectaron diferencias significativas entre los que fueron tratados con 3 o 4 fármacos. Constaban como tratamiento satisfactorio (curados o con tratamiento completado) el 79,9% de los pacientes que fueron tratados con tres fármacos y el 76,2% de los que fueron tratados con cuatro. En cuanto a la evolución de pacientes que tuvieron al menos una resistencia tratados con tres fármacos, hubo una proporción de tratamiento satisfactorio del 73%, vs el 81% en los pacientes con resistencias tratados con 4 fármacos, con diferencia no significativa (p=0,18).
Por otro lado, recibieron tratamiento prolongado más pacientes en el grupo de pacientes con resistencias que en los que tenían gérmenes sensibles (13 vs 3,1%; p<0,001).
DiscusiónEn el estudio realizado en pacientes con TB de prácticamente todas las Comunidades Autónomas de España existe una proporción importante de pacientes, algunos de ellos en riesgo de presentar resistencias, que no son tratados de acuerdo a las normativas nacionales e internacionales con relación al tratamiento intensivo de la enfermedad con cuatro fármacos.
Han sido tratados con cuatro fármacos el 58% de los pacientes con baciloscopia positiva, por lo que en el resto de los pacientes bacilíferos existe la posibilidad de encontrarnos en una situación comprometida en el caso de tener resistencias que se conocerían varias semanas después, pues se tendría que cambiar el tratamiento o incluso se podían haber provocado y/o transmitido nuevas resistencias con la posibilidad de crear casos de TB MDR y XDR (TB extremadamente resistente, definida como TB MDR asociada a resistencia a las quinolonas y al menos a un inyectable de segunda línea). Es posible que el uso generalizado de nuevas técnicas de diagnóstico molecular de resistencias, tales como el Xpert MTB/RIF assay o GeneXpert®10, que permite comprobar resistencia a rifampicina y por lo tanto sospecha de TB MDR desde el momento inicial del diagnóstico y tratamiento, o GenoType MTBDRplus11 para la detección rápida de resistencia a rifampicina e hidracidas, pueda minimizar, aunque solo en parte, el riesgo señalado.
En relación con los pacientes con baciloscopia negativa, se han tratado más (53,6%) con tres que con cuatro fármacos. Ello puede tener una explicación práctica, pues en el momento en que el microbiólogo comunica un resultado positivo en el cultivo, el clínico que inicia el tratamiento conoce que el microbiólogo, generalmente, va a proporcionar el antibiograma en un periodo corto de tiempo, por lo que en el caso que el paciente presente resistencias, el riesgo de provocar nuevas resistencias por tratamiento inadecuado sería menor al no haber tiempo para el desarrollo de las mismas.
En población inmigrante destaca en nuestro estudio que solamente el 75,2% de pacientes son tratados con cuatro fármacos, lo que indica que una cuarta parte son tratados con tres. Desde el punto de vista clínico, no parece una práctica aceptable, puesto que es sabido que las tasas de resistencias en pacientes inmigrantes son superiores a las de los nativos (resistencia a isoniacida del 11,9% en inmigrantes en comparación con el 4,1% en autóctonos, según un estudio reciente en España8), y que el porcentaje de pacientes extranjeros en el global de pacientes con TB en España es del 29,7% según un estudio previo12 y del 35% en nuestro estudio actual, por lo que el inicio de tratamiento con tres fármacos en pacientes extranjeros es una práctica inadecuada de alto riesgo.
El tratamiento de los pacientes autóctonos con tres fármacos más frecuentemente (54,9%) que con cuatro, puede indicar la confianza de los médicos que indican el tratamiento en los datos que referencian cifras bajas de resistencias en nuestro país. No obstante, datos recientes publicados por nuestro grupo8 indican que en autóctonos también hay un porcentaje de resistencias mayor de lo esperado (4,1% de resistencia a isoniacida) que aconsejan tratar a los pacientes inicialmente con cuatro fármacos.
Hay que destacar que en 75 pacientes con la presencia de resistencia a fármacos de primera línea (36,1% de los que la tenían) se inició tratamiento con tres fármacos, lo cual puede ser un problema importante con el tratamiento por los motivos comentados (necesidad de tener que replantear un retratamiento a la vista de los resultados del antibiograma con resistencias). Esto es un dato más para insistir en la necesidad de indicar tratamiento inicial con cuatro fármacos, puesto que en cualquier paciente podemos encontrar resistencias que hagan difícil el tratamiento y que, además, prolonguen en el tiempo el periodo de transmisión de la enfermedad, por ser casos en los que la terapia suele ser efectiva con mayor retraso. El porcentaje similar de tratamiento satisfactorio en pacientes tratados con 3 o 4 fármacos, tanto en pacientes con formas sensibles como con formas resistentes, puede tener justificación en que los médicos que tratan a los pacientes con TB en España y que han participado en nuestro estudio son profesionales especializados en dicha enfermedad y con amplia experiencia en su manejo, por lo que se puede pensar que en el caso de aparición de dichas resistencias los médicos habrán indicado una nueva pauta terapéutica de acuerdo con las resistencias aparecidas, lo que habrá llevado a conseguir una buena evolución final de los pacientes. De ahí que el tratamiento se haya prolongado en más casos con resistencias (13%) que en casos con gérmenes sensibles (3,1%).
La evolución del uso de una pauta u otra a lo largo de los años de estudio muestra un incremento del tratamiento con cuatro fármacos en los años 2008 y 2009 que puede ser debido a la influencia de la publicación de las normativas españolas en dicho periodo de tiempo. Sin embargo, la proporción ha ido disminuyendo posteriormente, hasta que en el año 2012 hay más pacientes tratados con tres que con cuatro fármacos, lo cual es indicador del abandono del seguimiento de la normativa a medida que transcurre el tiempo. Este dato resulta preocupante si se tiene en cuenta el incremento en los últimos años (en base a los dos últimos estudios nacionales multicéntricos llevados a cabo8,13), tanto de las cifras de resistencia inicial a isoniacida como de las de MDR. Además, debemos tener en cuenta que no existen estudios específicos en cada una de las Comunidades Autónomas de nuestro país que permitan aplicar la terapia de 3 vs 4 fármacos en base a las cifras de resistencias y MDR halladas en cada una de ellas. La introducción de Xpert MTB/RIF y otras técnicas de amplificación de ácidos nucleicos, ya citadas, podría cambiar la morbilidad y la mortalidad por TB por la mejora en el diagnóstico, en la detección precoz de resistencias y en el tratamiento temprano de nuevos casos, con el impacto que además conlleva sobre la dinámica de transmisión a largo plazo11.
A escala internacional, existen muy pocas publicaciones que evalúen el seguimiento de las recomendaciones del tratamiento en la fase intensiva de la TB. En Malasia observaron que solo el 49,4% de los pacientes completaron la fase intensiva de la enfermedad de dos meses, a pesar de las recomendaciones de la Organización Mundial de la Salud (OMS)14. En Francia, en un estudio realizado mediante un cuestionario enviado a médicos de este país, se describe que un número significativo de ellos (12,2%) usan de forma sistemática una pauta de tres fármacos en el tratamiento inicial en vez de la recomendación de cuatro, sin conocerse en este estudio la proporción de pacientes tratados con tres fármacos, dado que cada médico trataba a un número diferente de pacientes; los autores concluyen que se han de hacer esfuerzos para conseguir el cumplimiento de las guías de tratamiento15. En la India, el Revised National Tuberculosis Control Programme utiliza una pauta inicial que contiene rifampicina administrada de forma intermitente 3 veces a la semana, incluyendo pacientes infectados por VIH, mientras que la OMS recomienda tratamiento administrado diariamente al menos en la fase intensiva de la enfermedad, y el resultado en estos pacientes demostró una alta mortalidad16.
El estudio tiene como limitaciones el que no se ha podido demostrar que el uso de tres fármacos genere casos de resistencias, puesto que no se ha realizado estudio de transmisión de la enfermedad, ni a nivel clínico-epidemiológico ni a nivel molecular. Tampoco hemos podido demostrar una diferencia en la clasificación o evolución final de los pacientes tratados con 3 o 4 fármacos, posiblemente porque el nivel de resistencias en España es pequeño y porque el tratamiento ha sido hecho por médicos con práctica clínica habitual en el tratamiento de la TB que, ante el hallazgo de resistencias iniciales, hayan optado por cambiar a una pauta efectiva. Como fortalezas, destacar que el estudio refleja la práctica habitual de un grupo numeroso de médicos especialistas en esta enfermedad, representantes de prácticamente todas las Comunidades Autónomas españolas.
ConclusionesA pesar de las normativas actuales sobre el tratamiento de la TB, existe una proporción importante de pacientes tratados en la fase intensiva con tres fármacos (44,3%). Supone un riesgo probable que un porcentaje importante de inmigrantes o no autóctonos, de pacientes con baciloscopia positiva y de pacientes con resistencias iniciales hayan sido tratados inicialmente con tres fármacos, ya que se pueden generar resistencias. Es preocupante que el último año del estudio haya habido más pacientes tratados con tres que con cuatro fármacos.
Por estos motivos es recomendable que se insista en difundir las normativas y en articular sistemas de control por parte del Plan para la Prevención y Control de la Tuberculosis en España, para que se sigan las recomendaciones de las guías internacionales y nacionales del tratamiento de la TB, con la prescripción de cuatro fármacos en la fase intensiva de la enfermedad, salvo que se pueda disponer de pruebas rápidas de resistencia en pocas horas.
AutoríaJMGG, TR, JAC: concepción del estudio. JMGG, TR, JAC: redacción del manuscrito. MC: análisis estadístico. JMGG, TR, JC, MC: análisis de resultados. JMGG, TR, MC, JAC, TPP, JRM: lectura crítica, revisión y aprobación final del manuscrito. Grupo de Trabajo PIITB: recogida de datos y aprobación final del manuscrito.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
R. Agüero (Hospital Marqués de Valdecilla, Santander); J.L. Alcázar (Instituto Nacional de Silicosis, Oviedo); N. Altet (Unidad de Prevención y Control de la Tuberculosis, Barcelona); L. Altube (Hospital Galdakao, Galdakao); F. Álvarez Navascués (Hospital San Agustín, Avilés, Asturias); L. Anibarro (Unidad de Tuberculosis de Pontevedra, Vigo); M. Barrón (Hospital San Millán-San Pedro, Logroño); P. Bermúdez (Hospital Universitario Carlos Haya, Málaga), R. Blanquer (Hospital Dr. Peset, Valencia); L. Borderías (Hospital San Jorge, Huesca); A. Bustamante (Hospital Sierrallana, Torrelavega); J.L. Calpe (Hospital La Marina Baixa, Villajoyosa); J.A. Caminero (Complejo Hospitalario Dr. Negrín, Las Palmas de Gran Canaria); F. Cañas (Hospital Insular de Gran Canaria, Las Palmas de Gran Canaria); F. Casas (Hospital Clínico San Cecilio, Granada), X. Casas (Hospital de Sant Boi, Sant Boi de Llobregat), E. Cases (Hospital Universitario La Fe, Valencia); R. Castrodeza (Hospital El Bierzo Ponferrada-León, Ponferrada); J.J. Cebrián (Hospital Costa del Sol, Marbella); J. E. Ciruelos (Hospital de Cruces, Guetxo); A.E. Delgado (Hospital Santa Ana, Motril), M.L. de Souza (Unidad de Prevención y Control de la Tuberculosis, Barcelona); D. Díaz (Complejo Hospitalario Juan Canalejo, La Coruña); B. Fernández (Hospital de Navarra, Pamplona); A. Fernández (Hospital Río Carrión, Palencia); J. Gallardo (Hospital Universitario de Guadalajara, Guadalajara); M. Gallego (Corporación Sanitaria Parc Taulí, Sabadell); M.M. García Clemente (Hospital Central de Asturias, Oviedo), C. García (Hospital General Isla Fuerteventura, Puerto del Rosario); F.J. García (Hospital Universitario de la Princesa, Madrid); F.J. Garros (Hospital Santa Marina, Bilbao), J.A. Gullón (Hospital San Agustín, Avilés, Asturias); C. Hidalgo (Hospital Universitario Virgen de las Nieves, Granada), M. Iglesias (Hospital Marqués de Valdecilla, Santander); G. Jiménez (Hospital de Jaén), M.A. Jiménez (Unidad de Prevención y Control de la Tuberculosis, Barcelona); J.M. Kindelan (Hospital Universitario Reina Sofía, Córdoba); J. Laparra (Hospital Donostia-San Sebastián, San Sebastián); R. Lera (Hospital Dr. Peset, Valencia), T. Lloret (Hospital General Universitario de Valencia, Valencia); M. Marín (Hospital General de Castellón, Castellón); J.T. Martínez (Hospital Mutua de Terrassa, Terrassa); E. Martínez (Hospital de Sagunto, Sagunto); A. Martínez (Hospital de La Marina Baixa, Villajoyosa); J.F. Medina (Hospital Universitario Virgen del Rocío, Sevilla); C. Melero (Hospital 12 de Octubre, Madrid); C. Milà (Unidad de Prevención y Control de la Tuberculosis, Barcelona); I. Mir (Hospital Son Llàtzer, Palma de Mallorca); C. Morales (Hospital Universitario Virgen de las Nieves, Granada), M.A. Morales (Hospital Cruz Roja Inglesa, Ceuta); V. Moreno (Hospital CarlosIII, Madrid); A. Muñoz (Hospital Universitario Carlos Haya, Málaga), L. Muñoz (Hospital Reina Sofía, Córdoba); C. Muñoz (Hospital Clínico Universitario de Valencia, Valencia); J.A. Muñoz (Hospital Universitario Central, Oviedo); I. Parra (Hospital Universitario Virgen de la Arrixaca, El Palmar); A. Penas (Complejo Hospitalario Xeral-Calde, Lugo); J.A. Pérez (Hospital Arnau de Vilanova, Valencia); P. Rivas (Hospital Virgen Blanca, León); J. Rodríguez (Hospital Universitario Virgen de las Nieves, Granada), J. Ruiz-Manzano (Hospital Universitario Germans Trías i Pujol, Badalona); J. Sala (Hospital Universitario JoanXXIII, Tarragona); M. Sánchez (Unidad de Tuberculosis Distrito Poniente, Almería); P. Sánchez (Hospital del Mar, Barcelona); F. Sanz (Hospital General Universitario de Valencia, Valencia); M. Somoza (Consorcio Sanitario de Tarrasa, Barcelona), E. Trujillo (Complejo Hospitalario de Ávila, Ávila); E. Valencia (Hospital CarlosIII, Madrid); A. Vargas (Hospital Universitario Puerto Real, Cádiz); I. Vidal (Complejo Hospitalario Juan Canalejo, La Coruña); R. Vidal (Hospital Vall d’Hebron, Barcelona); M.A. Villanueva (Hospital San Agustín, Avilés, Asturias); A. Villar (Hospital Vall d’Hebron, Barcelona); M. Vizcaya (Complejo Hospitalario Universitario de Albacete, Albacete); M. Zabaleta (Hospital de Laredo, Laredo); G. Zubillaga (Hospital Donostia-San Sebastián, San Sebastián).