Puntos clave:
- •
Muchos pacientes con EPOC avanzada pueden beneficiarse de los cuidados paliativos (CP).
- •
Los CP están infrautilizados en la EPOC y deben valorarse en pacientes que persistan sintomáticos a pesar de un tratamiento óptimo de su enfermedad.
Los CP son las atenciones que se brindan para mejorar la calidad de vida de los pacientes con una enfermedad grave o potencialmente mortal. La meta de los CP es prevenir o tratar los síntomas de una enfermedad, los efectos secundarios del tratamiento y los problemas psicológicos, sociales y espirituales relacionados con una enfermedad o su tratamiento1,2.
Los CP no se limitan a pacientes oncológicos con enfermedad terminal. Muchos pacientes con una insuficiencia orgánica avanzada, como la EPOC, pueden beneficiarse de ellos. Los CP por sí mismos no aceleran la muerte y mejoran la calidad de vida3.
Síntomas de los pacientes con EPOC avanzadaLos pacientes con EPOC muy grave (BODE > 6) tienen a menudo tantos o más síntomas físicos y emocionales, además de mayor limitación funcional y peor calidad de vida, que los pacientes con neoplasias avanzadas4–6.
Entre los síntomas asociados a la EPOC avanzada el más prevalente es la disnea (presente en el 97% de los pacientes), la somnolencia, la falta de energía (68%) y el dolor (43%). La presencia de depresión se puede detectar en casi el 50% de los pacientes, mientras que la prevalencia de ansiedad alcanza el 25%. Muchas veces los síntomas coexisten.
Dada la larga evolución de la enfermedad, los síntomas pueden pasar desapercibidos si no se interroga de forma dirigida. Los pacientes acaban incorporando los síntomas y las limitaciones derivadas de estos a su estilo de vida7–9.
P10. ¿Cómo tratar la EPOC al final de la vida?
Puntos clave:
- •
Los CP son complementarios y no sustituyen al tratamiento convencional de la EPOC.
- •
Los CP deben basarse en las necesidades de los pacientes y no en la esperanza de vida.
- •
La comunicación con el paciente y los familiares o cuidadores es fundamental y constituye una herramienta terapéutica esencial que da acceso al principio de autonomía, al consentimiento informado, a la confianza mutua y a la seguridad e información que el paciente necesita para recibir ayuda y ayudarse a sí mismo.
- •
Se debe atender de forma especial al tratamiento farmacológico de la disnea y de la ansiedad y/o depresión.
Los pacientes con EPOC avanzada tienen una carga de síntomas similar o mayor que la de los pacientes oncológicos, con menores posibilidades de recibir CP, a pesar de que estos han demostrado mejorar los síntomas y la calidad de vida de estos pacientes sin disminuir, e incluso aumentando, la supervivencia. Una de las características de la EPOC es su incertidumbre pronóstica, por lo que la decisión de iniciar CP para el control de síntomas refractarios a la terapia convencional no debe basarse en la esperanza de vida, sino que se deben incorporar según las necesidades del paciente mediante la valoración periódica de los síntomas y la incorporación progresiva de las medidas de paliación sin abandonar el tratamiento reglado de la enfermedad (fig. 1). Los CP son complementarios al resto de tratamientos establecidos, entre los que se incluye la ventilación mecánica no invasiva. La intensidad y la relación entre los tratamientos clásicos y los CP deben modularse durante el curso de la enfermedad.
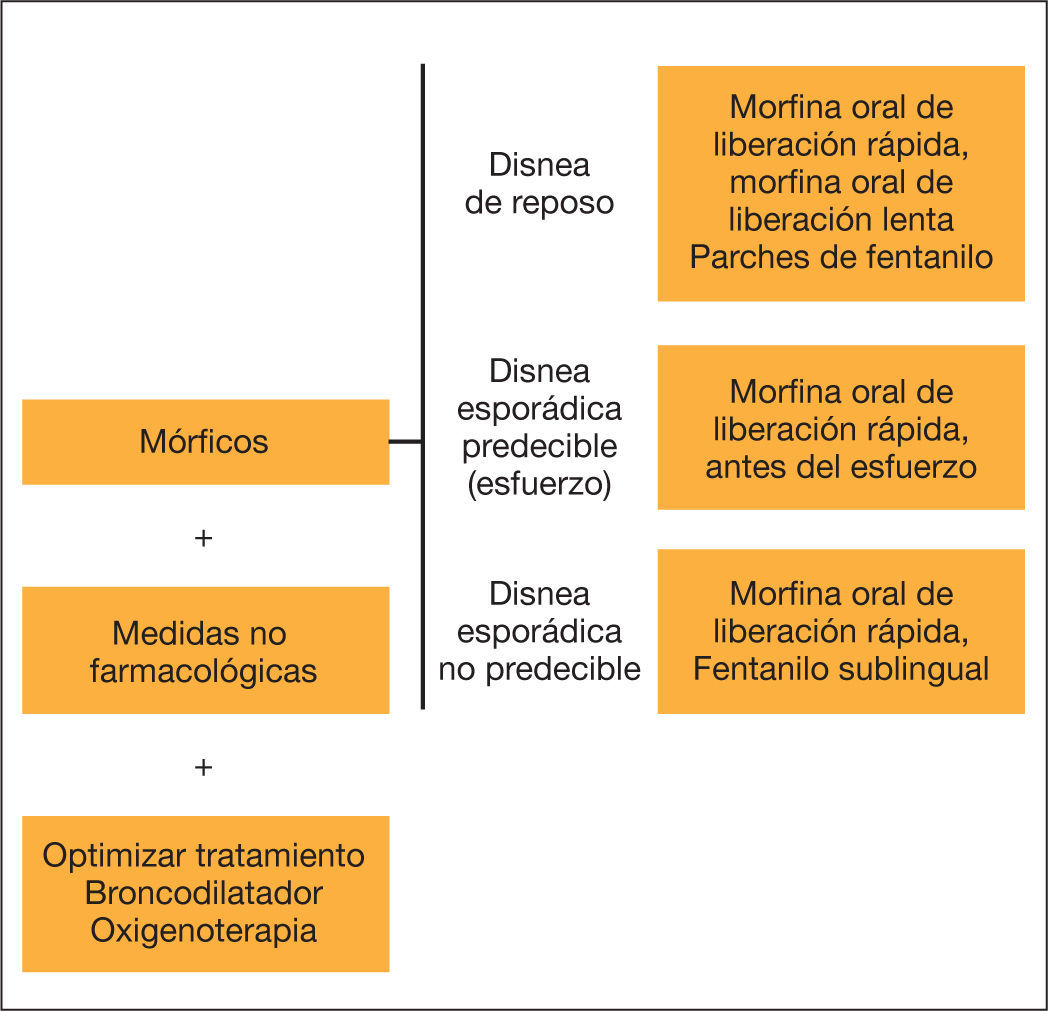
La comunicación con el paciente y sus familiares es fundamental; debe contemplar sus deseos y respetar sus creencias, e incluir sus preferencias en caso de descompensación grave. Esta comunicación debe realizarse preferentemente con el paciente estable, a través de varias entrevistas, y las preferencias del paciente deben reflejarse en la historia clínica y revaluarse durante la evolución de la enfermedad. En caso de crisis con riesgo vital sin toma previa de decisiones, puede ser útil pactar con el paciente y su familia el límite de las intervenciones. Junto a la optimización del tratamiento broncodilatador y la aplicación de medidas no farmacológicas, como la rehabilitación, el uso juicioso de mórficos a dosis bajas (tabla 1) ha demostrado mejorar la disnea refractaria con unos efectos secundarios prevenibles y tratables, sin aumentar la mortalidad incluso en pacientes con EPOC avanzada e insuficiencia respiratoria. Por el contrario, las benzodiacepinas no parecen ser de utilidad excepto en casos seleccionados.
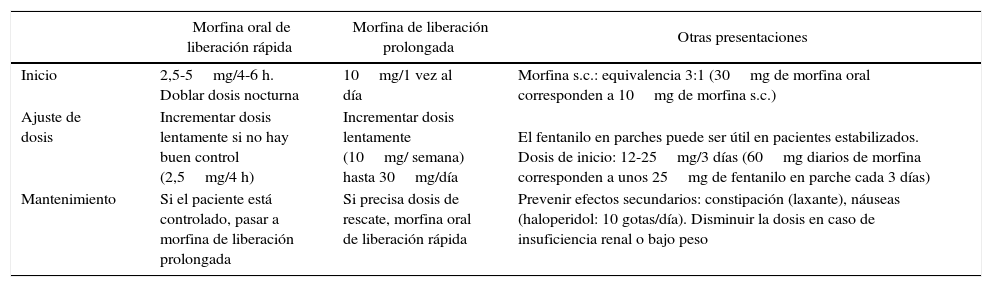
Dosis recomendadas de mórfico al inicio del tratamiento, ajuste y mantenimiento.
| Morfina oral de liberación rápida | Morfina de liberación prolongada | Otras presentaciones | |
|---|---|---|---|
| Inicio | 2,5-5mg/4-6 h. Doblar dosis nocturna | 10mg/1 vez al día | Morfina s.c.: equivalencia 3:1 (30mg de morfina oral corresponden a 10mg de morfina s.c.) |
| Ajuste de dosis | Incrementar dosis lentamente si no hay buen control (2,5mg/4 h) | Incrementar dosis lentamente (10mg/ semana) hasta 30mg/día | El fentanilo en parches puede ser útil en pacientes estabilizados. Dosis de inicio: 12-25mg/3 días (60mg diarios de morfina corresponden a unos 25mg de fentanilo en parche cada 3 días) |
| Mantenimiento | Si el paciente está controlado, pasar a morfina de liberación prolongada | Si precisa dosis de rescate, morfina oral de liberación rápida | Prevenir efectos secundarios: constipación (laxante), náuseas (haloperidol: 10 gotas/día). Disminuir la dosis en caso de insuficiencia renal o bajo peso |
s.c.: subcutánea.
Los CP buscan mejorar la calidad de vida de los pacientes y sus familias cuando se enfrentan a los problemas asociados a enfermedades amenazantes para la vida a través de la prevención y el alivio del sufrimiento mediante su identificación temprana unida a una evaluación y tratamiento impecable del dolor y otros problemas: físicos, psicológicos o espirituales10. Los CP deben incorporarse progresivamente a lo largo de la enfermedad, sin esperar a que el riesgo de fallecimiento del paciente se considere elevado a corto plazo11. Es fundamental no confundir los CP con la sedación paliativa —que es solo una parte de los CP— en la que se busca la disminución deliberada del nivel de consciencia del paciente mediante la administración de los fármacos apropiados con el objetivo de evitar un sufrimiento intenso e innecesario causado por uno o más síntomas refractarios a los tratamientos habituales. Los profesionales sanitarios que atienden a estos pacientes deberán estar familiarizados con los CP y, si no lo están o la atención es compleja, deberán contactar con un equipo de soporte de CP.
En algunos estudios se ha demostrado que los pacientes con EPOC avanzada tienen una carga de síntomas similar o mayor a la de los pacientes con cáncer de pulmón no operable, con más síntomas físicos, sociales y emocionales, y mayor prevalencia de depresión11,12. Los CP disminuyen los síntomas, mejoran la calidad de vida e incluso en algunos ensayos se ha demostrado un aumento de la supervivencia. En un estudio realizado en pacientes con cáncer de pulmón no operable, el inicio temprano de los CP se asoció a una esperable mejoría de la calidad de vida, pero también a un aumento de la supervivencia13,14. En otro estudio, realizado en pacientes con enfermedades respiratorias avanzadas (de los cuales un 54% tenían EPOC), se obtuvieron resultados similares15. Desafortunadamente, los pacientes con EPOC tienen menos posibilidades de recibir atención paliativa que los pacientes oncológicos11,13,14,16.
A pesar del mayor conocimiento de los factores pronósticos en la EPOC, la supervivencia de un paciente individual sigue siendo incierta. Algunos pacientes con EPOC grave permanecen estables durante meses, mientras que otros pierden rápidamente funcionalidad y fallecen. Además, la EPOC se caracteriza por presentar exacerbaciones que pueden ocurrir de forma impredecible y que en las fases avanzadas de la enfermedad se asocian a un marcado incremento de la mortalidad. Aunque se sabe que cada exacerbación aumenta el riesgo de fallecimiento y que es muy probable que el fallecimiento se produzca en los días o semanas posteriores a una exacerbación, se desconoce si la actual exacerbación será la última de un paciente concreto. Esto puede llevar a lo que algunos autores han denominado “parálisis pronóstica”, en la que el médico pospone el inicio de los CP por no poder predecir la supervivencia, aun cuando el paciente presente síntomas que podrían beneficiarse de estos.
En la EPOC hay muchos factores reconocidos de peor pronóstico, tanto en variables individuales como agrupadas en los llamados índices multicomponente. Sin embargo, ninguno de ellos ofrece una suficiente fiabilidad pronóstica a nivel individual a corto plazo. Una de las aproximaciones clásicas propuestas para valorar la necesidad de CP es la denominada pregunta sorpresa: ¿Me sorprendería que mi paciente falleciera en los próximos 12 meses? En caso de que la repuesta sea negativa, el paciente se consideraría candidato a CP. Aunque esta pregunta tiene la ventaja de obligar a plantearse la necesidad de CP, muchos autores consideran que su uso exclusivo no es útil en los pacientes con EPOC y puede retrasar innecesariamente el inicio de los CP17. Por otra parte, el margen de error con esta pregunta en la EPOC es excesivamente alto. En consecuencia, la decisión de iniciar los CP no debe basarse en la esperanza de vida, sino que estos se deben incorporar progresivamente según las necesidades del paciente —mediante la valoración periódica de los síntomas y la incorporación progresiva de las medidas paliativas— sin abandonar el tratamiento reglado de la enfermedad (fig. 1).
La planificación de los cuidados avanzados es siempre la estrategia preferible. Esta planificación debe basarse en un proceso de comunicación con el paciente en fase estable para ayudarle en la toma de decisiones contemplando sus opiniones, preferencias, valores y creencias para facilitar al equipo médico la toma de decisiones, incluyendo las que se refieren al final de vida. Las intervenciones en estos pacientes deben ser de carácter educativo y preventivo. En ellas se deben incluir aspectos dirigidos a mantener la salud del cuidador18, así como la del paciente: movilización, higiene, nutrición, medicación, orientación en actividades de la vida diaria y autoestima. Los cuidados deberán extenderse durante la fase de duelo y en el proceso de adaptación a la pérdida.
Es importante que el paciente y sus familiares entiendan que discutir sobre el pronóstico o realizar un plan terapéutico no significa dejar de cuidar al paciente ni suspender tratamientos que le sean útiles. Tampoco se puede obligar al paciente a recibir información no solicitada. Durante las entrevistas, el profesional debe plantearse si el paciente quiere más información, qué es lo que quiere saber y si está preparado para recibir la información. La comunicación no se alcanza en una única entrevista, sino en múltiples y a través de un proceso de maduración. Lamentablemente, este tipo de comunicación sigue siendo escasa entre los profesionales sanitarios y los pacientes con EPOC avanzada19.
No es infrecuente que los pacientes ingresen en el hospital en situación de riesgo vital y sin unas directrices claras previas de sus deseos respecto a la utilización de medidas como la reanimación cardiopulmonar, la intubación o el ingreso en la unidad de cuidados intensivos. En estos pacientes es razonable que el equipo encargado de su atención establezca con el paciente y sus familiares el denominado “techo terapéutico” (es decir, los límites del tratamiento) con una información realista. Por ejemplo: ¿Si tuviese una parada cardiorrespiratoria, querría que le realizáramos medidas de reanimación cardiopulmonar? En nuestra experiencia, aunque en ocasiones son remisos a plantearse claramente el pronóstico, los pacientes sí quieren participar en este tipo de decisiones. Estas directivas deben quedar claramente reflejadas en la historia clínica y pueden variar durante el ingreso y en función de la evolución del paciente20. Cuando el paciente solicita información sobre un pronóstico vital que para el médico resulta incierto, algunos autores proponen ofrecerla de forma clara y basándose en la mejor evidencia disponible (p. ej., “En un paciente con una enfermedad como la suya los estudios dicen que la posibilidad de que fallezca durante el próximo año es de aproximadamente del 50%”).
Entre los síntomas asociados a la EPOC avanzada, el más prevalente es la disnea (presente en el 97% de los pacientes), junto a la fatiga (68%) y el dolor (43%). La presencia de depresión se puede detectar en casi el 50-90% de los pacientes, mientras que la prevalencia de ansiedad alcanza el 25%13,14. En muchas ocasiones, los síntomas coexisten y pueden pasar desapercibidos si no se interroga a los pacientes de forma dirigida21.
Aunque la desaparición completa de la disnea en las últimas fases de la EPOC puede ser un objetivo no realista, existen medidas farmacológicas y no farmacológicas que permiten mejorar su control, como la rehabilitación pulmonar o las técnicas de relajación22. Entre las terapias farmacológicas, aparte de los tratamientos clásicos como los broncodilatadores, los fármacos mejor estudiados son los opiáceos. En un metaanálisis reciente realizado por la Cochrane, se demostró un efecto favorable de los opiáceos orales o parenterales en la mejoría de la disnea, incluyendo a los pacientes con EPOC, mientras que los opiáceos nebulizados no mostraron efectividad23. Estos datos se han corroborado en otros estudios24. La recomendación es iniciar los mórficos a dosis bajas y aumentar lentamente las dosis hasta la mejoría de la disnea, anticipándose a los efectos secundarios (constipación, náuseas, etc.). La administración de opiáceos a dosis bajas (< 30mg/día de morfina oral) no aumenta el riesgo de ingreso hospitalario ni el de fallecimiento, incluso en pacientes con oxigenoterapia domiciliaria25. Por el contrario, no hay evidencias de mejoría clara con el uso de benzodiacepinas para la disnea, por lo que debe considerarse un tratamiento de tercera línea. Para las crisis de disnea aguda en pacientes ambulatorios, algunos autores recomiendan el uso de fentanilo sublingual (12,5-25mg) por su rápido inicio de acción. No obstante, la evidencia es escasa y sus efectos secundarios, menos estudiados24.