Los acontecimientos adversos respiratorios (AAR) constituyen causas importantes de morbimortalidad postoperatoria. En el presente estudio se investigó la incidencia y los factores determinantes de los AAR postoperatorios.
MétodosEste estudio prospectivo observacional se llevó a cabo en una unidad de cuidados postanestésicos (UCPA). Se estudió a un total de 340 pacientes adultos ingresados de forma consecutiva, y se evaluaron los AAR después de intervenciones de cirugía programada. Se registraron las características demográficas de la población, los parámetros perioperatorios, la frecuencia de AAR y la duración de la estancia postoperatoria en la UCPA y en el hospital. Los datos se analizaron mediante estadística descriptiva, con la prueba de U de Mann-Whitney y con la prueba de χ2 o la prueba exacta de Fisher. Se realizaron análisis multivariantes con una regresión binaria logística, y se calculó la odds ratio (OR) y su intervalo de confianza (IC) del 95%.
ResultadosSe produjeron AAR postoperatorios en 67 pacientes (19,7%). Los AAR fueron más frecuentes después de intervenciones quirúrgicas de riesgo alto (42% frente a 24%; p=0,003), en los pacientes a los que se practicaron operaciones de cirugía mayor (37% frente a 25%, p=0,041), en los que fueron intervenidos bajo anestesia general (85% frente a 67%, p=0,004) y en los pacientes a los que se administraron relajantes musculares intraoperatorios (79% frente a 55%; p<0,001) y neostigmina (69% frente a 49%, p=0,002). Los pacientes con AAR postoperatorios experimentaron con mayor frecuencia una emergencia hipoactiva (13% frente a 5%, p=0,015) y un bloqueo neuromuscular residual (46% frente a 11%, p<0,001). En los análisis multivariantes, el bloqueo neuromuscular residual fue un factor de riesgo independiente para la aparición de los AAR en la UCPA (OR 6,4; IC 3,0-13,4; p<0,001).
ConclusionesLos AAR constituyen una complicación postoperatoria importante y frecuente. El bloqueo neuromuscular residual fue un factor de riesgo independiente para la aparición de AAR en la UCPA.
Adverse respiratory events (ARE) are a leading causes of postoperative morbidity and mortality. This study investigated the incidence and determinants of postoperative ARE.
MethodsThis observational prospective study was conducted in a post anesthesia care unit (PACU). A total of 340 adult subjects were admitted consecutively, and AREs were measured after elective surgery. Population demographics, perioperative parameters, ARE occurrence, and length of stay in the postoperative PACU and in hospital were recorded. Data were analyzed descriptively using the Mann-Whitney U-test and the Chi-square or Fisher's exact test. Multivariate analyses were carried outusing logistic binary regression, and the odds ratio (OR) and 95% confidence interval (CI) were calculated.
ResultsPostoperative AREs occurred in 67 subjects (19.7%). AREs were more frequent after high-risk procedures (42% vs 24%; P=.003), in patients undergoing major surgery (37% vs 25%; P=.041), those receiving general anesthesia (85% vs 67%; P=.004), and in patients administered intraoperative muscle relaxants (79% vs 55%; P<.001) and neostigmine (69% vs 49%; P=.002). Hypoactive emergence (13% vs 5%; P=.015) and residual neuromuscular blockade (46% versus 11%; P<.001) were more frequent in subjects with postoperative ARE. On multivariate analyses, residual neuromuscular blockade was an independent risk factor for ARE in the PACU (OR 6.4; CI 3.0-13.4; P<.001).
ConclusionsARE is an important and common postoperative complication. Residual neuromuscular blockade was an independent risk factor for ARE in the PACU.
Los acontecimientos adversos respiratorios (AAR) continúan siendo una de las causas más importantes de morbimortalidad postoperatoria1. La incidencia descrita de complicaciones respiratorias postoperatorias oscila entre el 5 y el 80%, según cuál sea la población de pacientes y qué criterios diagnósticos se utilicen para definir una complicación2. Los episodios respiratorios aparecidos inmediatamente después de la intervención quirúrgica son frecuentes, y en estudios prospectivos se ha observado una incidencia de AAR del 1,3-6,9% después del ingreso en una unidad de cuidados postanestésicos (UCPA)3,4.
Los problemas respiratorios se observan con frecuencia en la UCPA5. La inmensa mayoría son debidos a obstrucción de las vías aéreas, hipoventilación o hipoxemia; y esta última es la vía final frecuente que conduce a una morbimortalidad grave, sea cual sea su etiología. La hipoxemia puede ser producida por una hipoventilación o por un compromiso del intercambio de oxígeno alveolar, que hacen aumentar el gradiente de oxígeno alveoloarterial. Los pacientes con comorbilidades significativas, en especial las de disfunción neuromuscular, pulmonar o cardiaca, son los que presentan un mayor riesgo de compromiso respiratorio, pero cualquier paciente puede desarrollar una hipoxemia postoperatoria. La hipoxemia postoperatoria se produce en el 30-50% de las intervenciones de cirugía abdominal y hasta el 8-10% de los pacientes requieren reintubación y ventilación mecánica6.
Durante el periodo postoperatorio inmediato, las causas más frecuentes de hipoventilación son la obstrucción de las vías aéreas, los anestésicos, los analgésicos (por ejemplo, los opiáceos), los sedantes, el bloqueo neuromuscular residual (BNMR) y el mal control del dolor de la incisión que dificulta la respiración4,5,7–11. Puede producirse un deterioro postoperatorio del intercambio de oxígeno de forma secundaria a un cortocircuito intrapulmonar, edema pulmonar y embolia pulmonar12. Los trastornos médicos preoperatorios, como la apnea obstructiva del sueño, predisponen también al paciente a la obstrucción de las vías aéreas en la UCPA13.
La causa más frecuente de obstrucción de las vías aéreas en la UCPA es la laxitud faríngea causada por una debilidad muscular de la faringe11. Otras causas son el espasmo laríngeo, el edema de las vías aéreas, el hematoma o la presencia de cuerpo extraño.
La pérdida del tono motor de la faringe da lugar a una laxitud muscular y es producida por el bloqueo neuromuscular residual, los efectos residuales de los anestésicos o los opiáceos10,14,15.
El diafragma se recupera con mayor rapidez que la musculatura de la faringe de los efectos de los fármacos relajantes musculares. La parálisis residual de los músculos faríngeos hace que la base de la lengua y los tejidos orofaríngeos posteriores se desplacen unos hacia otros, y ello produce una obstrucción de la entrada supraglótica16,17.
El objetivo de este estudio fue medir la incidencia y los factores determinantes de los AAR postoperatorios en la UCPA.
MétodosDiseño, contexto y participantesEste estudio prospectivo observacional se llevó a cabo en el Centro Hospitalar São João (Oporto, Portugal), que es un hospital de nivel terciario, de 1.124 camas, y se realizó en la UCPA de 13 camas a lo largo de un periodo de 3 semanas (entre el 9 de mayo y el 27 de mayo de 2011) durante el cual los pacientes fueron ingresados, monitorizados y tratados. El estudio fue aprobado por el Comité Ético del Centro Hospitalar São João. Se obtuvo el consentimiento informado durante la consulta preanestésica. Se registró la incidencia de AAR durante la hospitalización en la UCPA en pacientes adultos consecutivos de habla portuguesa, ingresados en la UCPA y para los que se había programado una intervención quirúrgica. Los pacientes a los que se practican intervenciones de cirugía neurológica, torácica o pulmonar no ingresan en la UCPA tras la operación; estos pacientes son hospitalizados en las unidades de cuidados intensivos e intermedios.
Los criterios de inclusión fueron la capacidad de dar un consentimiento informado por escrito y la ventilación espontánea al ingreso.
Los pacientes en los que se aplicó una ventilación pulmonar programada y necesitaron un ingreso durante una noche en la unidad de cuidados intensivos (UCI) no fueron ingresados en la UCPA y se les excluyó del estudio. Otros criterios de exclusión fueron el rechazo del paciente, la incapacidad de dar un consentimiento informado, una puntuación <25 en la escala Mini-Mental State Examination (MMSE), la presencia de una enfermedad neuromuscular conocida, la cirugía de urgencia o de extrema urgencia, la neurocirugía y las intervenciones que requerían hipotermia terapéutica.
Datos de las intervenciones y de los participantesAntes de la operación se llevó a cabo una entrevista breve para la obtención del consentimiento, para la aplicación de la escala MMSE18 y para registrar los antecedentes patológicos del paciente. Durante la entrevista, los pacientes respondieron al cuestionario STOP-BANG19. Este cuestionario fue validado para una población quirúrgica por F. Chung et al.19 y es un modelo de puntuación que incluye 8 preguntas fáciles de plantear, a las que se designa con el acrónimo de STOP-BANG (por las siglas inglesas de ronquidos, cansancio durante el día, apnea observada, presión arterial elevada, índice de masa corporal, edad, circunferencia del cuello y sexo). Este cuestionario se puntúa mediante respuestas de Sí/No (puntuación: 1/0), y los valores de la puntuación van de 0 a 8. Una puntuación de ≥3 tiene una alta sensibilidad para detectar la apnea obstructiva del sueño. Se recogieron también los datos relativos al índice de masa corporal (IMC), la edad, la circunferencia del cuello y el sexo (BANG). Se clasificó a los pacientes como de riesgo alto de apnea obstructiva del sueño (HR-OSA) si la puntuación STOP-BANG era de 3 o superior.
Se rellenó un formulario estandarizado para la obtención de datos en cada paciente y se registró en él la edad, el peso, la altura, el IMC y el estado físico de la American Society of Anesthesiologists (ASA-PS). Se calculó el Revised Cardiac Risk Index (RCRI) según lo descrito por Lee et al.20 y que incluye la cirugía de riesgo alto (es decir, intraperitoneal, intratorácica o vascular suprainguinal) y los factores de riesgo clínicos (cardiopatía isquémica previa, enfermedad cardiaca compensada, insuficiencia cardiaca, enfermedad cerebrovascular, diabetes mellitus e insuficiencia renal).
La intervención quirúrgica se clasificó como mayor (cavidades corporales o vasos sanguíneos principales expuestos a la temperatura ambiente), media (cavidades corporales expuestas en menor grado) o menor (cirugía superficial). La cirugía mayor se definió como la que requería 2 días o más de hospitalización.
Manejo anestésicoEl anestesiólogo responsable no conocía la participación del paciente en el estudio y no fue informado de la realización de la investigación. La anestesia fue administrada y supervisada según el criterio del anestesiólogo, pero siguió las normas mínimas de aplicación en el departamento. Se administraron fármacos bloqueantes neuromusculares (FBNM) para la intubación traqueal y de forma adicional si eran necesarios. La monitorización neuromuscular se realizó a criterio del anestesiólogo y no hay ninguna política escrita respecto a su uso.
Generalmente, los pacientes fueron extubados en el área quirúrgica y trasladados luego a la UCPA. Los criterios para la extubación fueron la elevación sostenida de la cabeza o la sujeción con la mano durante más de 5s, la capacidad de cumplir órdenes sencillas, un patrón ventilatorio estable con una saturación arterial de oxígeno aceptable (SpO2 >95%) y una respuesta contráctil a la estimulación en tandas de cuatro (TOF) superior a 0,80. A todos los pacientes se les administró oxígeno al 100% mediante mascarilla tras la extubación traqueal. El anestesiólogo determinó si debía administrarse o no oxígeno durante el traslado e ingreso en la UCPA.
A su llegada a la UCPA, se administró oxígeno a todos los pacientes mediante cánula nasal o mascarilla. El BNMR se definió como un TOF <0,9 y se cuantificó al ingreso en la UCPA con el empleo de una aceleromiografía del músculo aductor del pulgar (TOF-Watch®).
Otros parámetros intraoperatorios registrados fueron el tipo de anestesia, la intervención quirúrgica, la duración de la anestesia, la duración de la operación, los líquidos intraoperatorios, el uso de FBNM y el uso de suxametonio.
Datos postoperatorios y acontecimientos adversos respiratoriosCada AAR postoperatorio se registró en el formulario de recogida de datos aplicando los siguientes criterios, según lo descrito por Murphy et al.21:
- 1.
Obstrucción de vías aéreas altas que requiere intervención (empuje mandibular, vía aérea oral o nasal).
- 2.
Hipoxia leve-moderada (SpO2=93-90%) mientras se administra oxígeno a 3l/min a través de una cánula nasal, y que no mejora después de una intervención activa (aumento del flujo de O2>3l/min, administración de O2 con mascarilla de alto flujo, indicaciones verbales de respirar profundamente o estimulación táctil).
- 3.
Hipoxia intensa (SpO2<90%) durante la administración de 3l/min de O2 mediante cánula nasal que no mejora tras una intervención activa (aumento del flujo de O2 a >3 l/min, administración de O2 con mascarilla de alto flujo, indicaciones verbales de respirar profundamente o estimulación táctil).
- 4.
Signos de dificultad respiratoria o fallo ventilatorio inminente (frecuencia respiratoria >20respiraciones/min, uso de músculos accesorios o tirón traqueal).
- 5.
Incapacidad de respirar profundamente cuando se lo indica el personal de enfermería de la UCPA.
- 6.
Síntomas de debilidad de la musculatura de las vías respiratorias o las vías aéreas altas (dificultad de respiración, deglución o habla) indicados por el paciente.
- 7.
Reintubación durante la permanencia en la UCPA.
- 8.
Evidencia o sospecha clínica de aspiración pulmonar después de la extubación traqueal (observación de contenido gástrico en la orofaringe e hipoxemia).
Los pacientes fueron objeto de una observación continuada por parte del personal de enfermería de la UCPA que contactaba de inmediato con un investigador del estudio si se observaba un AAR. La incapacidad de respirar profundamente, los síntomas de dificultad respiratoria y la debilidad de vías aéreas altas se evaluaron a intervalos de 10min. Un investigador del estudio examinó al paciente para confirmar que cumplía al menos un criterio de AAR.
Un equipo de médicos adecuadamente formados evaluó la emergencia de la anestesia de los pacientes. Los pacientes fueron evaluados 10min después del ingreso en la UCPA. El delirium de emergencia y la emergencia hipoactiva, así como su gravedad, se diagnosticaron según la escala Richmond Agitation and Sedation Scale (RASS)22,23. El delirium de emergencia se definió por una RASS≥+1 y la emergencia hipoactiva por una RASS≤–2.
Se realizó un examen de detección del delirium en el momento del alta de la UCPA con el empleo de la escala de evaluación de enfermería Nursing Delirium Screening Scale (Nu-DESC)24, y en los pacientes con una puntuación de 2 puntos o más después de al menos una evaluación se consideró que había un resultado positivo para delirium. El equipo de investigadores evaluó el delirium cuando cada paciente fue declarado formalmente apto para el alta para pasar a una sala general. Se registró también la duración de la estancia en la UCPA y la de la hospitalización.
Análisis estadísticoSe utilizó un análisis descriptivo de las variables para resumir los datos. Se realizaron análisis univariantes con el empleo de la prueba de U de Mann-Whitney para comparar las variables continuas y la prueba de χ2 o la prueba exacta de Fisher para comparar las proporciones.
Se utilizaron regresiones múltiples binarias logísticas con la inclusión forzada en el modelo de todas las variables, con objeto de identificar los factores predictivos independientes para los AAR. En este modelo se incluyeron todas las covariables con un valor de p<0,05 en el análisis univariante. Los datos se analizaron con el programa SPSS para Windows versión 19.0 (SPSS, Chicago, IL, EE.UU.).
ResultadosDe un total de 357 pacientes ingresados de forma consecutiva en la UCPA durante el periodo de estudio y que dieron su consentimiento, se evaluó a un total de 340 participantes.
Diecisiete pacientes fueron excluidos: 7 fueron ingresados en una unidad de cuidados intensivos quirúrgicos, 3 no pudieron dar el consentimiento informado o tenían una puntuación de la MMSE<25, 3 no fueron operados, uno tenía menos de 18años de edad, uno no hablaba portugués, uno rechazó la participación y en uno se realizó una operación de neurocirugía.
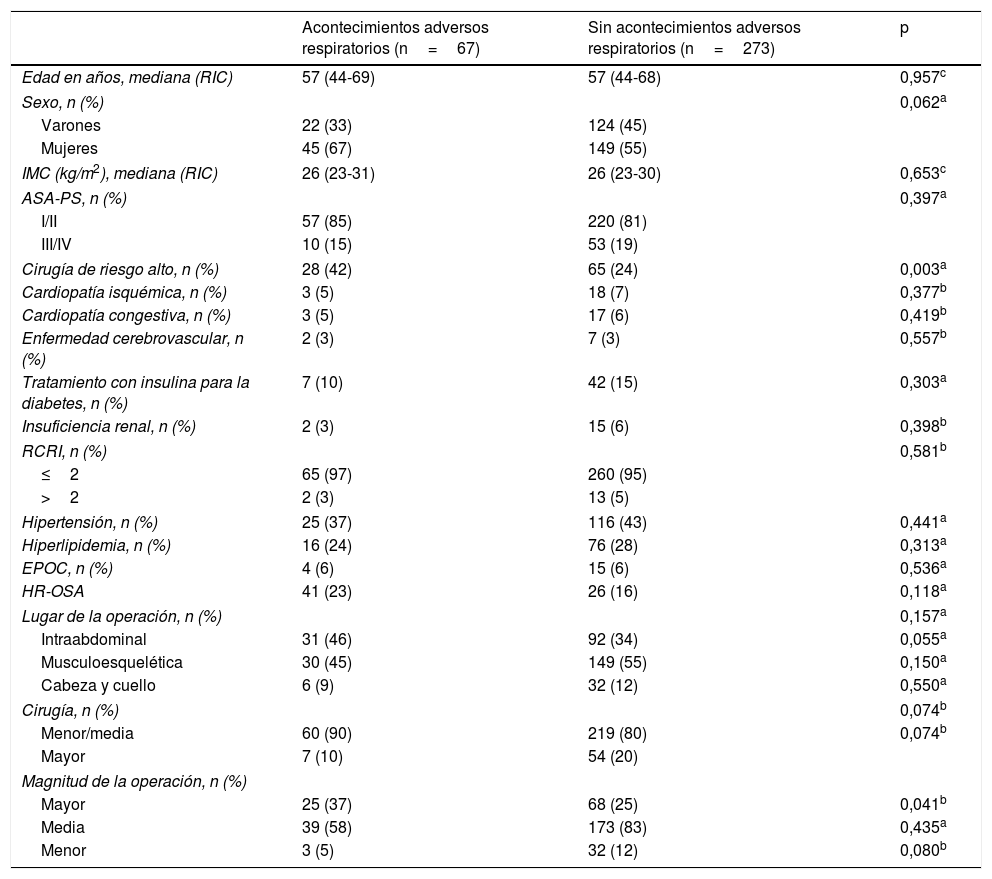
La mediana de edad de los pacientes fue de 57años, y la mediana de IMC fue de 26kg/m2. Las características demográficas de la población, los datos operatorios, el manejo anestésico y los datos de la UCPA se resumen en las tablas 1–3.
Características del paciente y acontecimientos adversos respiratorios en la unidad de cuidados postanestésicos
| Acontecimientos adversos respiratorios (n=67) | Sin acontecimientos adversos respiratorios (n=273) | p | |
|---|---|---|---|
| Edad en años, mediana (RIC) | 57 (44-69) | 57 (44-68) | 0,957c |
| Sexo, n (%) | 0,062a | ||
| Varones | 22 (33) | 124 (45) | |
| Mujeres | 45 (67) | 149 (55) | |
| IMC (kg/m2), mediana (RIC) | 26 (23-31) | 26 (23-30) | 0,653c |
| ASA-PS, n (%) | 0,397a | ||
| I/II | 57 (85) | 220 (81) | |
| III/IV | 10 (15) | 53 (19) | |
| Cirugía de riesgo alto, n (%) | 28 (42) | 65 (24) | 0,003a |
| Cardiopatía isquémica, n (%) | 3 (5) | 18 (7) | 0,377b |
| Cardiopatía congestiva, n (%) | 3 (5) | 17 (6) | 0,419b |
| Enfermedad cerebrovascular, n (%) | 2 (3) | 7 (3) | 0,557b |
| Tratamiento con insulina para la diabetes, n (%) | 7 (10) | 42 (15) | 0,303a |
| Insuficiencia renal, n (%) | 2 (3) | 15 (6) | 0,398b |
| RCRI, n (%) | 0,581b | ||
| ≤2 | 65 (97) | 260 (95) | |
| >2 | 2 (3) | 13 (5) | |
| Hipertensión, n (%) | 25 (37) | 116 (43) | 0,441a |
| Hiperlipidemia, n (%) | 16 (24) | 76 (28) | 0,313a |
| EPOC, n (%) | 4 (6) | 15 (6) | 0,536a |
| HR-OSA | 41 (23) | 26 (16) | 0,118a |
| Lugar de la operación, n (%) | 0,157a | ||
| Intraabdominal | 31 (46) | 92 (34) | 0,055a |
| Musculoesquelética | 30 (45) | 149 (55) | 0,150a |
| Cabeza y cuello | 6 (9) | 32 (12) | 0,550a |
| Cirugía, n (%) | 0,074b | ||
| Menor/media | 60 (90) | 219 (80) | 0,074b |
| Mayor | 7 (10) | 54 (20) | |
| Magnitud de la operación, n (%) | |||
| Mayor | 25 (37) | 68 (25) | 0,041b |
| Media | 39 (58) | 173 (83) | 0,435a |
| Menor | 3 (5) | 32 (12) | 0,080b |
ASA-PS: estado físico de la American Society of Anesthesiologists; EPOC: enfermedad pulmonar obstructiva crónica; HR-OSA: riesgo alto de apnea obstructiva del sueño; IMC: índice de masa corporal; RCRI: Revised Cardiac Risk Index; RIC: rango intercuartiles.
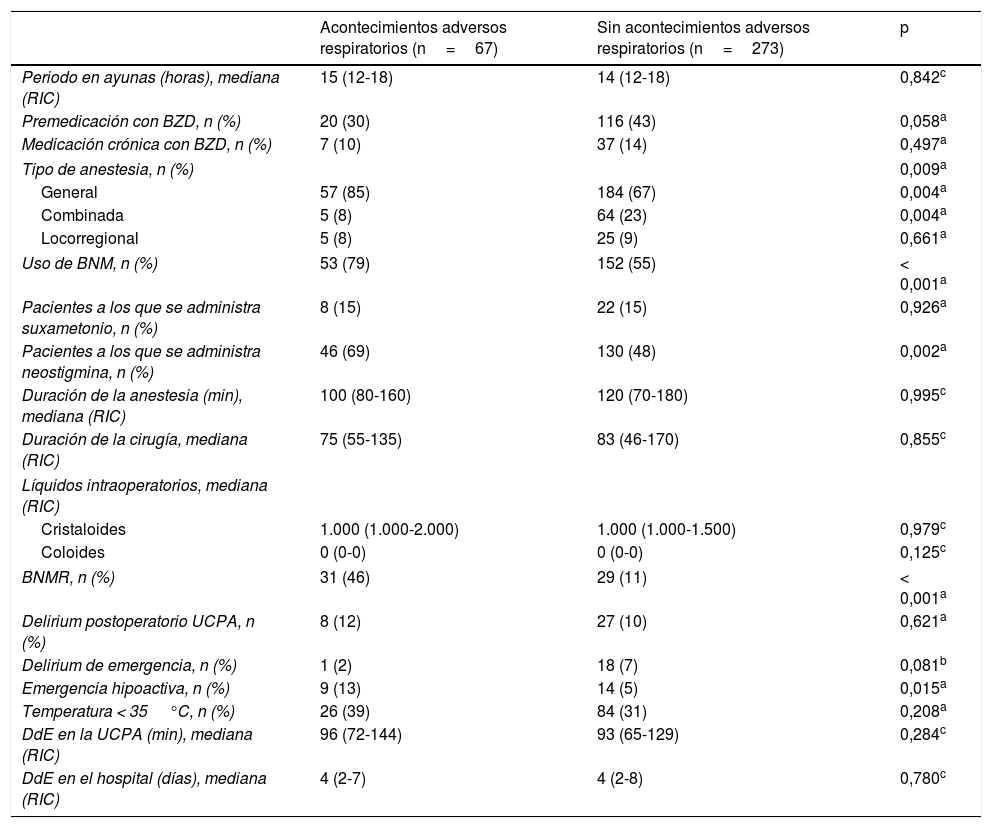
Características perioperatorias y acontecimientos adversos respiratorios postoperatorios en la unidad de cuidados postanestésicos
| Acontecimientos adversos respiratorios (n=67) | Sin acontecimientos adversos respiratorios (n=273) | p | |
|---|---|---|---|
| Periodo en ayunas (horas), mediana (RIC) | 15 (12-18) | 14 (12-18) | 0,842c |
| Premedicación con BZD, n (%) | 20 (30) | 116 (43) | 0,058a |
| Medicación crónica con BZD, n (%) | 7 (10) | 37 (14) | 0,497a |
| Tipo de anestesia, n (%) | 0,009a | ||
| General | 57 (85) | 184 (67) | 0,004a |
| Combinada | 5 (8) | 64 (23) | 0,004a |
| Locorregional | 5 (8) | 25 (9) | 0,661a |
| Uso de BNM, n (%) | 53 (79) | 152 (55) | < 0,001a |
| Pacientes a los que se administra suxametonio, n (%) | 8 (15) | 22 (15) | 0,926a |
| Pacientes a los que se administra neostigmina, n (%) | 46 (69) | 130 (48) | 0,002a |
| Duración de la anestesia (min), mediana (RIC) | 100 (80-160) | 120 (70-180) | 0,995c |
| Duración de la cirugía, mediana (RIC) | 75 (55-135) | 83 (46-170) | 0,855c |
| Líquidos intraoperatorios, mediana (RIC) | |||
| Cristaloides | 1.000 (1.000-2.000) | 1.000 (1.000-1.500) | 0,979c |
| Coloides | 0 (0-0) | 0 (0-0) | 0,125c |
| BNMR, n (%) | 31 (46) | 29 (11) | < 0,001a |
| Delirium postoperatorio UCPA, n (%) | 8 (12) | 27 (10) | 0,621a |
| Delirium de emergencia, n (%) | 1 (2) | 18 (7) | 0,081b |
| Emergencia hipoactiva, n (%) | 9 (13) | 14 (5) | 0,015a |
| Temperatura < 35°C, n (%) | 26 (39) | 84 (31) | 0,208a |
| DdE en la UCPA (min), mediana (RIC) | 96 (72-144) | 93 (65-129) | 0,284c |
| DdE en el hospital (días), mediana (RIC) | 4 (2-7) | 4 (2-8) | 0,780c |
BNM: fármacos bloqueantes neuromusculares; BNMR: bloqueo neuromuscular residual; BZD: benzodiazepinas; DdE: duración de la estancia; RIC: rango intercuartiles; UCPA: unidad de cuidados postanestésicos.
Un total de 67 pacientes (19,7%) presentaron un AAR (tabla 4). Los AAR observados con mayor frecuencia fueron los siguientes: incapacidad de respirar profundamente (15,9%), hipoxemia leve-moderada (5,9%) y debilidad de vías aéreas altas (3,2%). Otros AAR registrados fueron los de obstrucción de vías aéreas altas (2,7%), signos de dificultad respiratoria o fallo ventilatorio inminente (2,1%) y la hipoxemia grave (1,5%). No hubo ningún paciente que necesitara reintubación, y ninguno mostró evidencia clínica o sospecha de aspiración pulmonar durante la hospitalización en la UCPA. Se observaron múltiples AAR en 21 pacientes (6,2%).
Incidencia de episodios respiratorios agudos en la unidad de cuidados postanestésicos(n=340)
| Variable | (n = 67) (19,7%) |
|---|---|
| Obstrucción de vías aéreas altas | 9 (2,7%) |
| Hipoxia leve-moderada | 20 (5,9%) |
| Hipoxia intensa | 5 (1,5%) |
| Dificultad respiratoria | 7 (2,1%) |
| Incapacidad de respirar profundamente | 54 (15,9%) |
| Debilidad de vías aéreas altas | 11 (3,2%) |
Los AAR se produjeron con mayor frecuencia en los pacientes a los que se practicaron intervenciones quirúrgicas de riesgo alto (42% frente a 24%, p=0,003) y de cirugía mayor (37% frente a 25%, p=0,041).
Los AAR fueron más frecuentes en los pacientes en los que se utilizó anestesia general (85% frente a 67%, p=0,004) y menos frecuentes en los pacientes operados bajo anestesia combinada (8% frente a 23%, p=0,004).
En los pacientes en los que se utilizó anestesia locorregional, la incapacidad de respirar profundamente se diagnosticó en 5 casos.
Se utilizaron relajantes neuromusculares en el 66% de los pacientes; los AAR se dieron con mayor frecuencia en estos pacientes (79% frente a 55%, p<0,001). Los AAR fueron también más frecuentes en los pacientes que recibieron neostigmina (69% frente a 48%, p=0,002).
Ni la duración de la anestesia ni la duración de la operación influyeron en la incidencia de AAR.
Los AAR fueron más frecuentes en los pacientes en los que hubo un BNMR (46% frente a 11%, p<0,001) y en los pacientes a los que se diagnosticó una emergencia hipoactiva (13% frente a 5%, p=0,015).
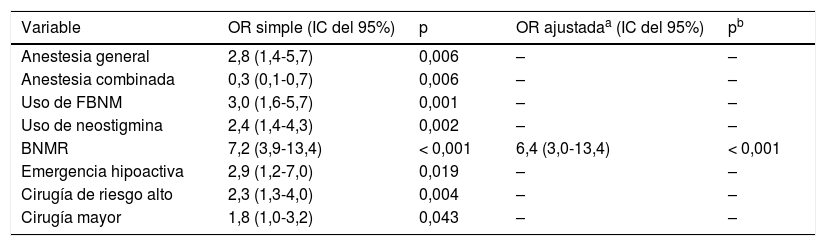
En los análisis multivariantes (tabla 5), después de introducir un ajuste respecto a los factores predictivos univariantes (anestesia general, anestesia combinada, uso de relajante neuromuscular y de neostigmina, emergencia hipoactiva y cirugía mayor y de riesgo alto) se identificó el BNMR como factor predictivo independiente para los AAR.
Análisis de regresión multivariante para los factores predictivos de los episodios respiratorios agudos
| Variable | OR simple (IC del 95%) | p | OR ajustadaa (IC del 95%) | pb |
|---|---|---|---|---|
| Anestesia general | 2,8 (1,4-5,7) | 0,006 | – | – |
| Anestesia combinada | 0,3 (0,1-0,7) | 0,006 | – | – |
| Uso de FBNM | 3,0 (1,6-5,7) | 0,001 | – | – |
| Uso de neostigmina | 2,4 (1,4-4,3) | 0,002 | – | – |
| BNMR | 7,2 (3,9-13,4) | < 0,001 | 6,4 (3,0-13,4) | < 0,001 |
| Emergencia hipoactiva | 2,9 (1,2-7,0) | 0,019 | – | – |
| Cirugía de riesgo alto | 2,3 (1,3-4,0) | 0,004 | – | – |
| Cirugía mayor | 1,8 (1,0-3,2) | 0,043 | – | – |
BNMR: bloqueo neuromuscular residual; FBNM: fármacos bloqueantes neuromusculares; IC: intervalo de confianza; OR: odds ratio.
El 20% de los pacientes sufrieron al menos un AAR durante la estancia en la UCPA.
La incidencia registrada de acontecimientos adversos respiratorios en la UCPA muestra amplias oscilaciones, y en los estudios observacionales se describe una incidencia del 1,3-34%4,25,26 según cuál sea la definición de AAR utilizada, la duración de la observación y la población de pacientes incluidos. En un estudio de Murphy et al.26 la incidencia de la hipoxia leve fue del 22%, lo cual es similar a la incidencia observada en este estudio, pero el mismo autor describió una incidencia muy inferior en otro estudio.
Los pacientes que presentaron AAR en la UCPA fueron con más frecuencia pacientes a los que se habían practicado intervenciones quirúrgicas de riesgo alto. La cirugía de riesgo alto se definió según el RCRI20. Esta puntuación fue diseñada inicialmente para predecir los episodios cardíacos mayores, pero puede predecir también otras complicaciones postoperatorias27.
Los AAR fueron también más frecuentes después de la cirugía mayor; estos pacientes pueden haber recibido un manejo anestésico diferente, una monitorización más estricta y probablemente una intervención quirúrgica de mayor duración. En estos pacientes era mucho más probable un mal estado preoperatorio, lo cual puede haber influido también en la incidencia de AAR.
Las operaciones de cirugía mayor abdominal, cirugía mayor vascular y cirugía torácica se clasificaron también como cirugía mayor en un estudio de Warner28, que señaló que la hipoxemia postoperatoria y la insuficiencia respiratoria aguda se produjeron principalmente después de la cirugía abdominal o torácica.
La incidencia global del BNMR en la población en estudio fue del 18%. Los pacientes con AAR presentaron una incidencia de BNMR superior a la de los pacientes sin AAR.
Tiene interés señalar que el porcentaje de pacientes a los que se administró neostigmina fue superior en aquellos a los que se diagnosticó un AAR. La mayor parte de los anestesiólogos administraron de manera sistemática una reversión del relajante muscular; sin embargo, algunos pueden haber usado criterios subjetivos.
Muchos centros europeos han indicado que no utilizan fármacos de reversión29-31; sin embargo, teniendo en cuenta la evidencia actualmente existente, no se recomienda esta práctica en el manejo habitual de los pacientes32. En el hospital en el que se realizó este estudio, los fármacos para la reversión se administran habitualmente a todos los pacientes como medida estándar. Esto puede explicar la incidencia superior de AAR en los pacientes a los que se administró neostigmina.
La posibilidad de un alta tardía de la UCPA debida a AAR es difícil de evaluar y depende de factores individuales de cada centro, como la dotación de personal, el tamaño de la UCPA y la disponibilidad de camas. Un estudio reciente ha sugerido que los AAR retrasaron el alta de la sala de reanimación, pero no se detectaron diferencias entre los 2 grupos en el presente estudio33. En este estudio, los pacientes tuvieron una mediana de estancia en la UCPA corta; las unidades quirúrgicas de nivel intermedio pueden explicar en parte la ausencia de diferencias en la duración de la estancia en la UCPA entre los pacientes con y sin AAR.
Los AAR fueron más frecuentes después de la anestesia general, lo cual era algo esperado y que se ha documentado en estudios anteriores4; sin embargo, el efecto protector observado frente a la aparición de AAR con la anestesia combinada en nuestro estudio fue sorprendente. Es posible que la anestesia combinada pueda hacer que la administración de FBNM sea menos frecuente y que la analgesia sin el empleo de opiáceos sea más eficiente.
No hubo ninguna relación entre la duración de la intervención quirúrgica y los AAR; sin embargo, la duración de la anestesia y la de la operación pueden estar relacionadas con las complicaciones pulmonares postoperatorias tras el alta de la UCPA, según lo descrito por Canet34; estos episodios pueden no haberse detectado, ya que el periodo de observación en el presente estudio fue el de la hospitalización en la UCPA.
Los pacientes con AAR fueron menos activos en la UCPA. La emergencia hipoactiva se definió por una puntuación de la RASS≤–2, que puede haber correspondido a un paciente más sedado tras el ingreso en la UCPA35.
En comparación con la incidencia descrita por Radtke et al.35, esta población tuvo una incidencia elevada de emergencia inadecuada (12%), principalmente por una emergencia hipoactiva, que se produjo en el 6,8% de los pacientes.
La cirugía abdominal es un factor de riesgo descrito que se asocia a la emergencia hipoactiva36, y puede haber influido en la asociación observada entre la cirugía de riesgo alto y la incidencia de BNMR. La cirugía abdominal puede estar relacionada con la asociación entre la cirugía de riesgo alto y la incidencia del BNMR, así como con la mayor frecuencia de delirium hipoactivo en los pacientes con BNMR. Otra posibilidad es que la relación entre los AAR y la emergencia hipoactiva pueda reflejar el nivel de sedación del paciente, que aumenta la probabilidad de hipoxemia y atelectasias en un paciente no ventilado.
El AAR más frecuente durante la hospitalización en la UCPA fue la incapacidad de respirar profundamente, que se registró en el 16% (54 de 340) de los pacientes y en el 81% (54 de 67) de los pacientes con AAR. Esta elevada incidencia puede deberse al BNMR y al estado hipoactivo. La hipoxemia leve-moderada fue el segundo AAR más frecuente y se produjo en el 6% (20 de 340) de los pacientes y en el 29,9% (20 de 67) de los pacientes con AAR. Otros estudios han descrito una asociación entre el BNMR y la hipoxemia postoperatoria; sin embargo, el presente estudio no se diseñó para establecer el mecanismo que subyace en la hipoxemia inducida por el bloqueo neuromuscular. Aunque el deterioro de la respuesta ventilatoria a la hipoxia y de la fuerza de los músculos respiratorios son causas importantes de la hipoxemia postoperatoria, tal como señalaron Murphy et al.21, estas etiologías no pueden evaluarse en el examen clínico ordinario. La obstrucción de las vías aéreas altas, que es otra causa frecuente de AAR descrita con anterioridad, se produjo con una incidencia del 3% (9 de 340) en la población en estudio, y representó el 13% del total de los AAR; los opiáceos y los anestésicos inhalados deben considerarse factores relevantes, pero el BNMR puede desempeñar también un papel importante.
Nuestro estudio tiene varias limitaciones que es preciso reconocer. En primer lugar, la muestra es pequeña y corresponde a un solo centro, lo cual hace difícil la generalización de esos resultados más allá de nuestro centro de estudio. En segundo lugar, fue un estudio prospectivo observacional. No hubo ninguna práctica anestésica de intervención antes, durante ni después de la intervención quirúrgica, y todos los tratamientos quedaron bajo el criterio del clínico responsable cada día de la UCPA.
Además, la definición de los AAR tiene varios criterios subjetivos que pueden influir en el diagnóstico. Por último, no se realizó una monitorización del estado de BNM intraoperatorio, y ello puede haber influido en la función respiratoria postoperatoria. Esto limita la posibilidad de interpretar la influencia de la administración de neostigmina y la duración del bloqueo neuromuscular. Aunque anteriormente se ha demostrado que la monitorización aceleromiográfica intraoperatoria reduce el riesgo de AAR en la UCPA26, este beneficio es menos manifiesto cuando se administran de manera sistemática fármacos para la reversión37.
En conclusión, los AAR se produjeron de manera frecuente en la UCPA. Los AAR fueron más frecuentes después de intervenciones quirúrgicas de riesgo alto y de cirugía mayor. El BNMR postoperatorio, la emergencia hipoactiva postoperatoria y la administración de neostigmina y de relajantes musculares intraoperatoriamente fueron factores determinantes de la aparición de AAR. La presencia de un BNMR constituyó un factor de riesgo independiente para los AAR postoperatorios en la UCPA.
AutoríaFernando Abelha y Alice Santos: concepción y diseño.
Fernando Abelha: análisis e interpretación
Alice Santos y Daniela Xará: redacción de la propuesta de manuscrito en cuanto a contenido intelectual importante.
Conflicto de interesesLos autores no tienen conflictos de intereses.