Determinar el impacto de la implementación de una guía de práctica clínica (GPC) en el proceso asistencial de la neumonía adquirida en la comunidad (NAC) en un servicio de urgencias (SU), analizando los indicadores de manejo (decisión de alta o ingreso, adecuación y precocidad de la antibioterapia, solicitud de estudios complementarios) y de resultados (tiempo de estabilización clínica, tiempo de estancia hospitalaria, reconsultas en el SU y mortalidad).
MétodosEstudio prospectivo, observacional, descriptivo y comparativo realizado desde el 1 enero de 2008 al 1 agosto de 2009 en 2fases, antes y después de la implantación de la GPC «Manejo de la NAC en los SU» SEMES-SEPAR 2008. Se incluyó a 200pacientes adultos atendidos en el SU con el diagnóstico de NAC tanto en el grupo preintervención como en el postintervención.
ResultadosEl uso de la GPC consiguió aumentar la administración precoz adecuada del antibiótico (p<0,001) y disminuir el tiempo de tratamiento antibiótico total (p<0,001) e intravenoso (p=0,042), así como reducir el tiempo hasta la estabilización clínica (p=0,027), la estancia hospitalaria (1,14 días, p=0,01) y la mortalidad intrahospitalaria (p=0,004) y global a los 30días (p=0,044). El uso del Pneumonia Severity Index (PSI) y los biomarcadores ayudaron a mejorar la adecuación de la decisión: alta o ingreso (p<0,001).
ConclusionesLa implementación de la GPC SEMES-SEPAR 2008 con el uso del PSI y los biomarcadores mejoró de forma significativa todo el proceso asistencial de la NAC, siendo beneficiosa para los enfermos y para el sistema al lograr disminuir la mortalidad y el resto de indicadores de resultados y de manejo.
To determine the impact of implementing clinical practice guidelines (CPGs) in the treatment of community-acquired pneumonia (CAP) in the emergency department (ED) by analyzing case management decisions (admission or discharge, appropriateness and timeliness of antibiotic therapy, complementary tests) and the consequent results (clinical stabilization time, length of hospital stay, re-admission to ED and mortality).
MethodsA prospective, observational, descriptive, comparative study carried out from 1st January 2008 to 1st August 2009 in two phases: before and after the implementation of the «Management of CAP in ED» SEMES-SEPAR (Spanish Society of Emergency Medicine - Spanish Society of Pneumology and Thoracic Surgery) clinical practice guidelines from 2008. Two hundred adult patients treated in the ED with a diagnosis of CAP were included in the study, both in the pre-intervention and post-intervention groups.
ResultsThe application of the guidelines increased the administration of early and appropriate antibiotic therapy (P<.001) and shortened both the total antibiotic therapy (P<.001) and the intravenous antibiotic therapy (P=.042) times. Time to clinical stabilization (P=.027), length of hospital stay (1.14 days, P=.01), intra-hospital mortality (P=.004) and total 30-day mortality (P=.044) were all reduced. Assessment with the Pneumonia Severity Index (PSI) and biomarkers aided in appropriate decision-making concerning admission/discharge (P<.001).
ConclusionsThe implementation of the SEMES-SEPAR 2008 guidelines, along with the use of PSI and biomarkers, significantly improved the entire treatment process of CAP. This benefitted both patients and the system by reducing mortality and improving the results of other patient management factors.
La neumonía adquirida en la comunidad (NAC) representa la principal causa de muerte por enfermedad infecciosa en los países occidentales (del 10 al 14%, según la edad y los factores de riesgo asociados) y es el origen de gran parte de las sepsis (S), sepsis grave (SG) y shock sépticos (SS) que se atienden en los servicios de urgencias (SU)1. En España su incidencia está en torno a los 2-5casos/1.000 habitantes/año y puede aumentar a 15-35casos/1.000 habitantes/año en épocas de epidemia viral, en los mayores de 65años y en enfermos crónicos o con hábitos tóxicos2. Es conocida la gran variabilidad existente, entre distintos centros y entre los clínicos de un mismo centro, en el abordaje y manejo de todos los aspectos diagnóstico-terapéuticos de los pacientes con NAC3-5. Este hecho constituye una de las razones que explican la existencia de tasas de ingreso muy diferentes, que oscilan del 22 al 61% según los centros, los distintos especialistas y la época del año. También la solicitud de estudios complementarios, la elección de la pauta antimicrobiana, la intensidad de cuidados o el empleo de recursos son muy diferentes entre distintos centros, lo que viene determinado muchas veces por las características, los recursos, la ubicación y la experiencia de los médicos que trabajan en los SU6. Pero esta variabilidad implica que el pronóstico y la evolución de los enfermos con NAC también sean diferentes7. Se estima que el 75% de todas las NAC son atendidas en los SU, lo que nos revela el importante papel del médico de urgencias (MU) en el manejo inicial de estos procesos que podrá marcar su evolución y su morbimortalidad1,2,6. Entre las decisiones más importantes que debe tomar el MU, determinar la necesidad de ingreso del paciente con NAC (el cuándo), su ubicación adecuada (el dónde) y los cuidados que precisan los pacientes (el cómo) va a condicionar tanto el pronóstico del paciente (morbimortalidad) como la solicitud de pruebas de laboratorio y de estudios microbiológicos, la elección de la pauta antimicrobiana inicial, la intensidad de la observación clínica y el uso de recursos sociosanitarios8. De todo ello dependerán los costes finales, que se incrementan de 8 a 25 veces en el paciente ingresado respecto al tratado en el domicilio9. Junto a la decisión de destino del paciente, la administración precoz de la pauta antimicrobiana adecuada y de las medidas de soporte hemodinámico y respiratorio necesarias constituyen los factores más determinantes en la evolución y la mortalidad de los pacientes con NAC10. Por ello, en los últimos años muchos son los autores que reclaman la necesidad de un protocolo o de una guía de práctica clínica (GPC), «Código NAC o Neumonía Cero»10, que consiga, como en el caso del síndrome coronario agudo o en el del ictus11, que el paciente con NAC en el SU, sobre todo si presenta SG o SS, sea siempre priorizado y tratado inmediatamente por objetivos, lo que puede contribuir a la disminución de la variabilidad clínica y de la mortalidad10,12. Muchos estudios han demostrado la utilidad y la eficacia de las GPC en relación con la NAC13-16: la mayoría han sido realizados por especialistas en neumología y solo analizan a los pacientes que ingresan en el hospital, aunque recientemente se han publicado otros que incluyen a los pacientes dados de alta (que constituyen el 35-50% de los pacientes con NAC atendidos en los SU)17,18. A pesar de que la eficacia y la eficiencia de las GPC es reconocida, su seguimiento y adherencia por los clínicos son escasos en general, y hasta el 35-65% confiesan no utilizarlas4,19-20.
La implantación de una GPC en un SU consensuada con el resto de especialistas y adaptada al centro es, probablemente, la principal herramienta para disminuir la variabilidad clínica y mejorar el manejo del proceso15-18. En nuestro hospital, durante el año 2008 pudimos comprobar que existía una gran variabilidad clínica y una adherencia muy escasa (menos del 40%) a la GPC de referencia21. Ese año se publicó el documento «Manejo de la NAC en los SU»1,22, elaborado por TIR-SEPAR (Área de Tuberculosis e Infecciones Respiratorias de la Sociedad Española de Neumología y Cirugía Torácica) e INFURG-SEMES (grupo de estudio Infecciones en Urgencias de la Sociedad Española de Medicina de Urgencias y Emergencias) con el objetivo de servir de instrumento para disminuir la variabilidad clínica y mejorar el manejo integral de la NAC desde los SU1. El objetivo de nuestro estudio fue determinar el impacto de la implementación de la GPC SEMES-SEPAR 2008 desde nuestro SU en el proceso asistencial de la NAC, comparando los indicadores de manejo (decisión de alta o ingreso, adecuación y precocidad de la antibioterapia, solicitud de estudios complementarios) y de resultados (tiempo de estancia hospitalaria y estabilización clínica, reconsultas en el SU y mortalidad) antes y después de la intervención.
Pacientes y métodosSitio del estudioEl estudio se realiza en el Complejo Hospitalario de Toledo. Se trata de un centro de tercer nivel de 800 camas perteneciente al Servicio de Salud de Castilla-La Mancha (SESCAM) con un área de referencia de 435.000 personas. El SU dispone de un área de medicina interna atendida por MU de plantilla propia y residentes de distintas especialidades médicas. Durante los años 2008 y 2009 se valoraron de media 416 y 430urgencias/día y la incidencia de la NAC en pacientes ≥18 años supuso el 0,92 y el 0,98% de todos los enfermos vistos en el SU (3,21 y 3,56casos/1.000 habitantes/año, respectivamente). Los pacientes con NAC pueden ser dados de alta desde el SU (incluyendo a los que permanecen en observación hasta 24h), ingresar en la unidad de cuidados intensivos (UCI) o ingresar en la unidad de corta estancia (UCE), en planta de neumología, de medicina interna o geriatría y, en menor medida (<3%), en otros servicios con especialistas de guardia propios las 24h (nefrología y hematología). El MU determina la decisión de ingreso y el servicio de destino inicial, salvo en el caso de la UCI, donde realiza consulta al intensivista de guardia.
Diseño del estudioEstudio observacional, a simple ciego y con seguimiento prospectivo de los pacientes en 2fases: antes y después de una intervención consistente en la implantación de la GPC «Manejo de la NAC en los SU» (SEMES-SEPAR 2008)1,22 junto con sesiones formativas sobre la misma a todos los MU y residentes del centro, tal y como se describe más adelante.
Periodos del estudio y población estudiadaDos colaboradores, independientes y sin conocimiento por el resto de MU durante todo el estudio, valoraron la elegibilidad inicial de los sujetos que acudieron al SU desde el 1 de enero de 2008 hasta el 1 de agosto de 2009, hasta incluir de forma consecutiva 200pacientes de la fase preintervención (1 enero de 2008 hasta el 30 de septiembre de 2008) y otros tantos de la fase postintervención (4 de octubre de 2008 hasta 1 agosto de 2009). Para ser incluidos, los pacientes debían cumplir los siguientes criterios: ser adultos (≥18 años) y diagnosticados de NAC en el SU por sus médicos responsables. Se excluyeron los pacientes inmunodeprimidos (aquellos con infección por el virus de la inmunodeficiencia humana, pacientes con trasplante de víscera sólida, esplenectomía, tratados con 10mg o más de prednisona al día o equivalentes, durante más de 30días, o tratados con otros agentes inmunodepresores) y los pacientes hospitalizados en los 14días previos. Los 2colaboradores se encargaron también, de forma ciega para el resto de los MU, de valorar la elegibilidad definitiva, retirando a los sujetos en que el médico responsable no mantuviera a los 30días el diagnóstico final de NAC (códigos 481, 482, 483, 485, 486 y 507 de la clasificación internacional de enfermedades 9.a revisión modificación clínica [CIE-9-MC]) y a los que tuvieron un diagnóstico final de tuberculosis, así como los casos diagnosticados de etiología viral, gripe, micosis o absceso de pulmón (correspondiente en la CIE-9-MC a los códigos 480, 487, 484 y 513). Tampoco se incluyó en el estudio a los pacientes que fueron diagnosticados de un segundo episodio de NAC durante el periodo del mismo. El estudio cumplía las normas éticas de nuestro hospital y fue aprobado por el Comité Ético de Investigación Clínica de nuestro centro. El seguimiento de todos los pacientes se realizó a través de la historia clínica informatizada del SU, hospitalaria y de atención primaria.
Intervención del estudio. Implementación y valoración de la adherencia a la guía de práctica clínicaEntre el 1 y el 3 de octubre de 2008 se entregó la GCP «Manejo de la NAC en los SU» (SEMES-SEPAR 2008)1,22, tanto completa como en díptico, y se impartieron sesiones formativas sobre ella a todos los MU y residentes del centro, solicitándoseles que en lo sucesivo aplicaran sistemáticamente las recomendaciones. Los 2colaboradores independientes y desconocidos para el resto de los MU se encargaron de aplicar los criterios de valoración de los pacientes. Para evaluar y analizar la actuación de los MU en cada caso se definió como «manejo adecuado» cuando existía coincidencia con las medidas y tratamientos efectuados por ellos con las citadas recomendaciones SEMES-SEPAR 20081,22 y «manejo inadecuado» cuando no coincidía. Esta valoración se realizó independientemente para la solicitud de estudios complementarios en el SU (de laboratorio, microbiológicos y biomarcadores), la valoración pronóstica y decisión de destino del paciente según el Pneumonia Severity Index (PSI) y para la elección y administración del tratamiento en el SU. Cuando existió discrepancia entre los 2evaluadores se excluyó el caso. Se definió NAC ante la existencia de una clínica aguda compatible (tos, disnea, fiebre, dolor torácico pleurítico, alteración del nivel de consciencia, etc.) y su demostración radiológica (presencia de infiltrado/s pulmonar/es no conocidos). Se definió como NAC grave (NACG) y su necesidad de valoración por la UCI cuando los pacientes cumplían un criterio mayor o 3menores según la normativa de la American Thoracic Society-Infectious Diseases Society of America (ATS/IDSA) de 20076.
Para valorar la gravedad y el pronóstico de los pacientes con NAC y la decisión de ingreso se utilizó el PSI, cuyas clases de riesgo se crearon de acuerdo con las propuestas de los autores originales23 aunque se incluyeron distintos criterios adicionales (también explicados y transmitidos en las sesiones formativas) de acuerdo con las recomendaciones de los miembros de las Sociedades Científicas SEMES y SEPAR en 2008; de esta forma se consideró que debían ingresar en planta todos los pacientes pertenecientes a las clases de riesgo iv-v (PSI) y los pertenecientes a las clases de riesgo i-iii en presencia de uno o más de los factores de riesgo o criterios adicionales recogidos en la tabla 1.
Criterios adicionales y factores de riesgo que condicionan el ingreso de los pacientes
| PaO2<60mmHg o saturación de O2 por pulsioximetría <90% |
| Evidencia de una comorbilidad descompensada |
| Derrame pleural (encapsulado, de ≥2cm en la radiografía de tórax en posición de decúbito lateral) |
| Afectación radiológica multilobular o bilateral |
| Criterios de sepsis grave o shock séptico |
| Gran probabilidad o sospecha de bacteriemia por la situación clínica y/o biomarcadores como PCR>90mg/ml y/o procalcitonina >1ng/ml |
| Situaciones o factores que impiden el correcto tratamiento domiciliario como intolerancia oral, problemas sociales (paciente dependiente sin cuidador disponible, alteraciones psiquiátricas, etilismo, etc.) |
| Falta de respuesta al tratamiento antibiótico previo (después de 72h de haber iniciado un tratamiento antibiótico adecuado ante la existencia de un empeoramiento clínico o radiológico) |
Los pacientes se repartieron en el grupo preintervención (Gpre) y postintervención (Gpos). Se recogieron todas las variables sociodemográficas, clínicas, exploratorias, analíticas y radiológicas incluidas en el PSI23, en los criterios de ingreso en la UCI del año 2007 ATS/IDSA6 y en los criterios de definición de S, SG y SS según la conferencia de expertos de sepsis de 200124. Se calculó el valor y el grado del PSI, del índice de Charlson25 original y ponderado por la edad y la existencia de S, SG y SS y NACG. A estas variables se añadieron: la toma de tratamiento antimicrobiano previo (durante las 72h antes de su consulta en el SU), el perfil del MU responsable (residente, facultativo del SU, otro especialista), la existencia de diabetes o de enfermedad pulmonar obstructiva crónica (EPOC), el número de comorbilidades (incluyendo las recogidas en el PSI más diabetes y EPOC), la solicitud de analítica indicada según la GPC (incluyendo según protocolo en cada caso hemograma, coagulación, bioquímica y gasometría), la solicitud de estudios microbiológicos adecuados según la GPC (hemocultivos, antigenuria en orina, cultivo de esputo), el registro y el valor de pulsioximetría (saturación de O2), la solicitud y valores de proteína C reactiva (PCR) y procalcitonina (PCT), la administración y precocidad (en las primeras 4h) del antibiótico, la elección de pauta antibiótica y posología adecuadas, el cambio de pauta antibiótica en los pacientes ingresados en las primeras 48h o en la pauta domiciliaria en las 72h tras el alta, la duración del tratamiento global e intravenoso, y la existencia de efectos secundarios y complicaciones. Finalmente, como variables de resultado se incluyeron: reconsulta en el SU y reingreso en los 30días, tiempos de estabilización clínica y de estancia hospitalaria, consecución de diagnóstico microbiológico, destino inicial del paciente (alta, observación, UCE, planta, UCI o muerte en el SU) y su adecuación, reevaluación a las 24-72h de los pacientes dados de alta, comprobación de la resolución clínica y radiológica a las 3-6semanas y la mortalidad en los dados de alta, en los ingresados en planta y en la UCI y la global a los 30días.
Tamaño muestralSe calculó que con 200pacientes por periodo se conseguiría una precisión no menor de ±10% en la estimación al 95% de confianza de la diferencia de porcentajes entre ambas fases. Además, el poder estadístico de un contraste bilateral al 5% de la diferencia entre proporciones sería al menos del 80% en caso de diferencias poblacionales a partir del 14%. Así mismo, con este tamaño muestral la probabilidad de que el intervalo de confianza al 95% de la diferencia de medias entre periodos no incluyera el valor cero sería igual o mayor que 0,8 para un tamaño del efecto de Cohen igual o superior a 0,2.
Análisis estadísticoSe utilizaron medias y sus desviaciones estándar (DE), rangos, medianas y porcentajes, según procediera, para describir las características demográficas, clínicas, evolutivas y de tratamiento de los pacientes de ambas fases. Además, para la estimación de los valores poblacionales se calcularon los límites de los intervalo de confianza al 95% (IC95%) de medias y porcentajes. La comparación de porcentajes entre fases (pre y postimplantación de la GPC) se realizó mediante la prueba chi-cuadrado o exacta de Fisher, según procediera, y la de variables de escala y ordinales, mediante la prueba t de Student y U de MannWhitney, según fueran aplicables. Además, al objeto de controlar en lo posible el sesgo de confusión, se ajustó un modelo de regresión logística no condicional, utilizando como variables dependientes la mortalidad intrahospitalaria y a los 30días y como independientes la fase (pre y postimplantación de la GPC) y las características clínicas, demográficas y de tratamiento que pudieran influir sobre la mortalidad y distribuirse heterogéneamente entre fases; de esta forma, se calcularon las odds ratio (OR) de asociación ajustadas entre mortalidad y fase y sus IC95%. Con la misma finalidad de control de la confusión y mediante el ajuste de un modelo de regresión lineal múltiple, se estudió si la eventual asociación entre duración del tratamiento y el grupo se mantenía tras controlar por el destino del paciente (alta, observación, UCE, planta o UCI). Finalmente, se calculó la proporción acumulativa de pacientes que permanecían ingresados a lo largo del tiempo mediante el método de Kaplan-Meier y se comparó entre fases con la prueba Log-Rank; este análisis se repitió estratificando por grupo según PSI y por destino del paciente. El mismo procedimiento se empleó para analizar el tiempo hasta la estabilización clínica. El análisis estadístico se realizó con el programa SPSS11 para Windows y se consideró como significativo un valor de p<0,05; todos los contrastes fueron bilaterales.
ResultadosSe incluyeron finalmente 200pacientes tanto en el grupo preintervención (Gpre) como en el postintervención (Gpos) tras excluir, respectivamente, 52 y 37 pacientes en los que no se confirmó el diagnóstico de NAC durante el seguimiento de acuerdo con los códigos definidos. Del mismo modo no se incluyó a 5 y a 3 pacientes en los que hubo discrepancias entre los colaboradores al valorar la actuación en el SU.
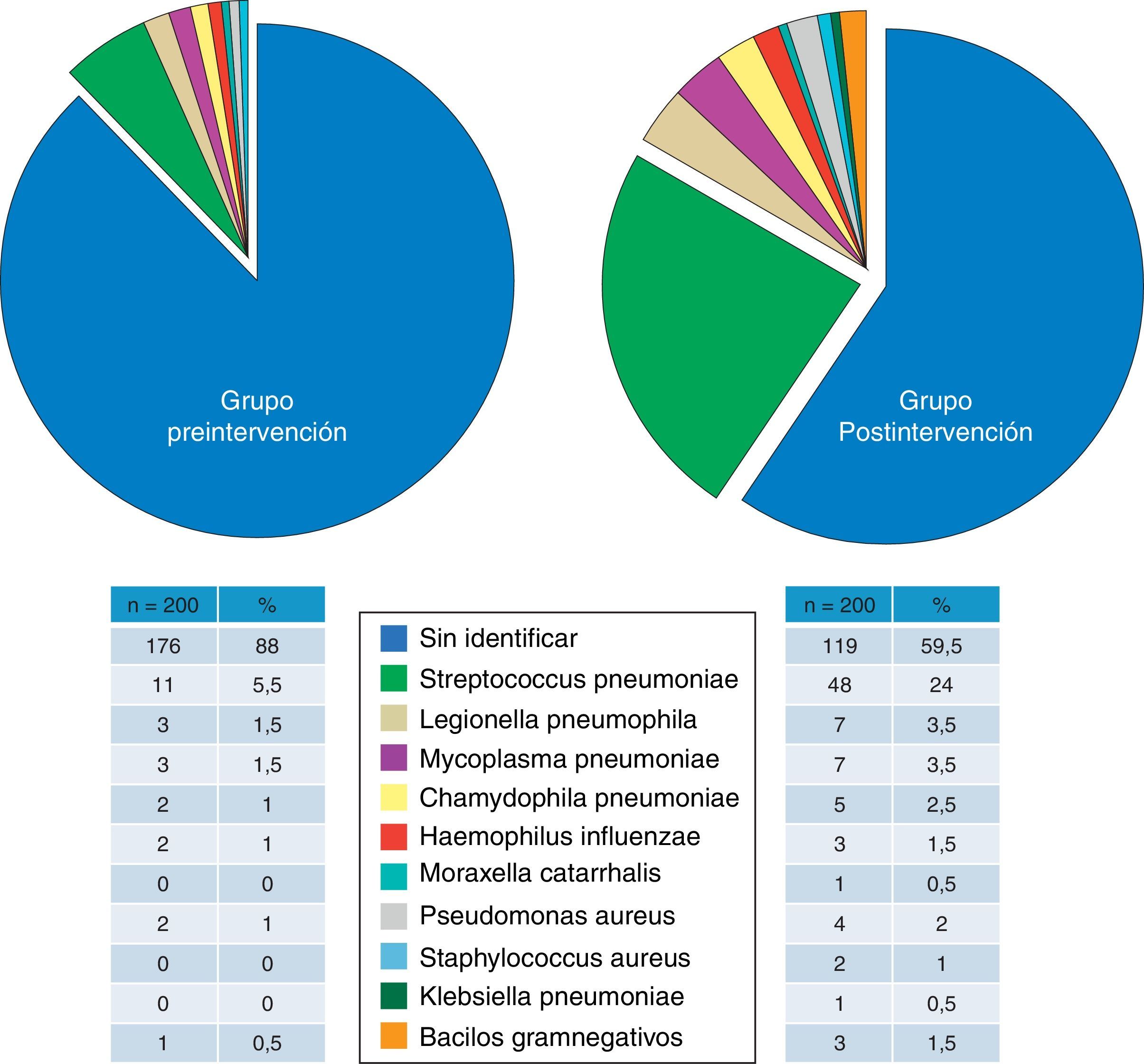
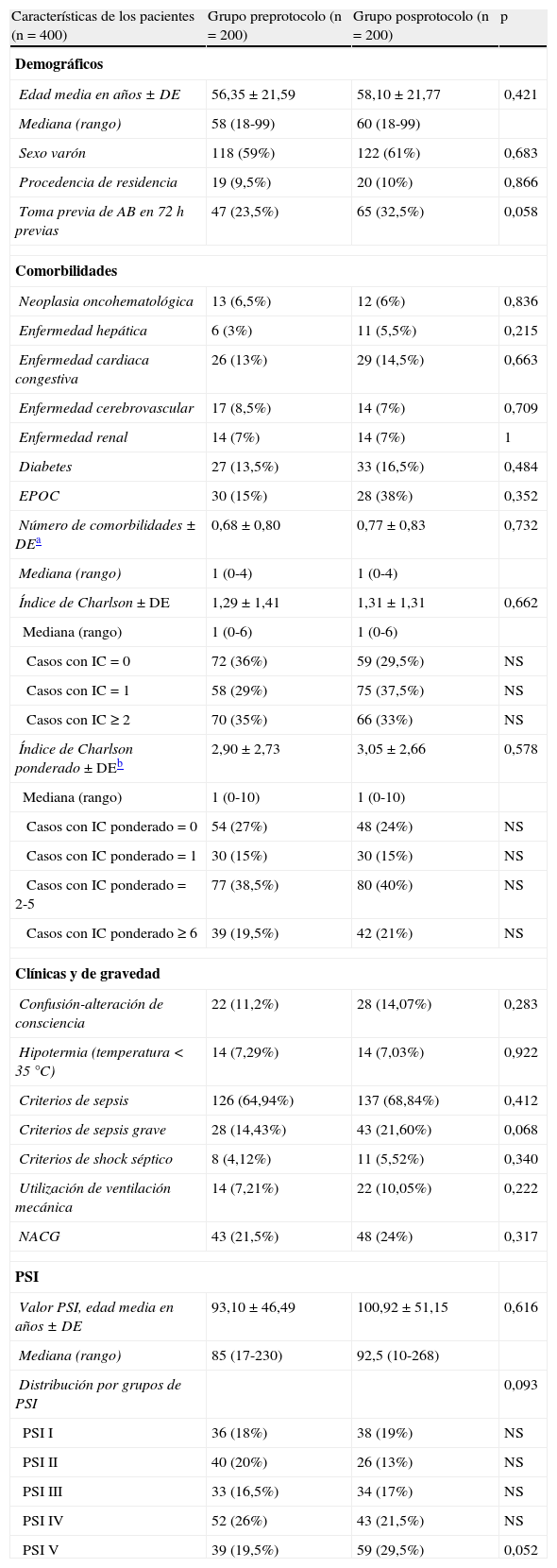
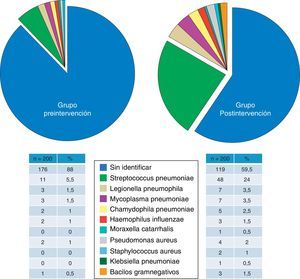
Comparabilidad de los gruposEn la tabla 2 se recogen las características sociodemográficas, clínicas y de gravedad, comorbilidades (y cálculo del índice de Charlson original y ponderado), y la distribución de los pacientes según la clasificación de PSI de todos los enfermos del estudio. Las diferencias entre grupos no alcanzaron el nivel nominal de significación en ninguna de las variables y, además, sus magnitudes no parecen relevantes salvo en el caso de la toma de antibióticos en las 72h previas y los criterios de SG (9 y 7,2% respectivamente más frecuentes en el grupo Gpos). Tampoco hubo diferencias, ni significativas ni importantes, entre el Gpre y el Gpos en la presentación radiológica (incidencia de NAC multilobar o bilateral y de derrame pleural) ni en los parámetros de laboratorio o gasométricos (tabla 3). Aunque la consecución del diagnóstico microbiológico final sí tuvo diferencias significativas (12% vs 40,5%, p<0,001), la distribución de los patógenos encontrados (fig. 1) fue proporcional, sin mostrar diferencias relevantes (p=0,22).
Características sociodemográficas y clínicas de los pacientes atendidos en el SU con NAC
| Características de los pacientes (n=400) | Grupo preprotocolo (n=200) | Grupo posprotocolo (n=200) | p |
| Demográficos | |||
| Edad media en años ± DE | 56,35 ± 21,59 | 58,10 ± 21,77 | 0,421 |
| Mediana (rango) | 58 (18-99) | 60 (18-99) | |
| Sexo varón | 118 (59%) | 122 (61%) | 0,683 |
| Procedencia de residencia | 19 (9,5%) | 20 (10%) | 0,866 |
| Toma previa de AB en 72h previas | 47 (23,5%) | 65 (32,5%) | 0,058 |
| Comorbilidades | |||
| Neoplasia oncohematológica | 13 (6,5%) | 12 (6%) | 0,836 |
| Enfermedad hepática | 6 (3%) | 11 (5,5%) | 0,215 |
| Enfermedad cardiaca congestiva | 26 (13%) | 29 (14,5%) | 0,663 |
| Enfermedad cerebrovascular | 17 (8,5%) | 14 (7%) | 0,709 |
| Enfermedad renal | 14 (7%) | 14 (7%) | 1 |
| Diabetes | 27 (13,5%) | 33 (16,5%) | 0,484 |
| EPOC | 30 (15%) | 28 (38%) | 0,352 |
| Número de comorbilidades ± DEa | 0,68 ± 0,80 | 0,77 ± 0,83 | 0,732 |
| Mediana (rango) | 1 (0-4) | 1 (0-4) | |
| Índice de Charlson ± DE | 1,29 ± 1,41 | 1,31 ± 1,31 | 0,662 |
| Mediana (rango) | 1 (0-6) | 1 (0-6) | |
| Casos con IC=0 | 72 (36%) | 59 (29,5%) | NS |
| Casos con IC=1 | 58 (29%) | 75 (37,5%) | NS |
| Casos con IC≥2 | 70 (35%) | 66 (33%) | NS |
| Índice de Charlson ponderado ± DEb | 2,90 ± 2,73 | 3,05 ± 2,66 | 0,578 |
| Mediana (rango) | 1 (0-10) | 1 (0-10) | |
| Casos con IC ponderado=0 | 54 (27%) | 48 (24%) | NS |
| Casos con IC ponderado=1 | 30 (15%) | 30 (15%) | NS |
| Casos con IC ponderado=2-5 | 77 (38,5%) | 80 (40%) | NS |
| Casos con IC ponderado≥6 | 39 (19,5%) | 42 (21%) | NS |
| Clínicas y de gravedad | |||
| Confusión-alteración de consciencia | 22 (11,2%) | 28 (14,07%) | 0,283 |
| Hipotermia (temperatura <35°C) | 14 (7,29%) | 14 (7,03%) | 0,922 |
| Criterios de sepsis | 126 (64,94%) | 137 (68,84%) | 0,412 |
| Criterios de sepsis grave | 28 (14,43%) | 43 (21,60%) | 0,068 |
| Criterios de shock séptico | 8 (4,12%) | 11 (5,52%) | 0,340 |
| Utilización de ventilación mecánica | 14 (7,21%) | 22 (10,05%) | 0,222 |
| NACG | 43 (21,5%) | 48 (24%) | 0,317 |
| PSI | |||
| Valor PSI, edad media en años ± DE | 93,10 ± 46,49 | 100,92 ± 51,15 | 0,616 |
| Mediana (rango) | 85 (17-230) | 92,5 (10-268) | |
| Distribución por grupos de PSI | 0,093 | ||
| PSI I | 36 (18%) | 38 (19%) | NS |
| PSI II | 40 (20%) | 26 (13%) | NS |
| PSI III | 33 (16,5%) | 34 (17%) | NS |
| PSI IV | 52 (26%) | 43 (21,5%) | NS |
| PSI V | 39 (19,5%) | 59 (29,5%) | 0,052 |
AB: antibiótico; DE: desviación estándar; EPOC: enfermedad pulmonar obstructiva crónica; IC: índice de Charlson; NAC: neumonía adquirida en la comunidad; NACG: neumonía adquirida en la comunidad grave; NS: no significativo o sin muestra suficiente; PSI: Pneumonia Severity Index; SU: servicio de urgencias.
Los porcentajes excluyen los datos perdidos, si los hubiere.
Características radiológicas, gasométricas y hallazgos de laboratorio en los pacientes atendidos en el SU con el diagnóstico de NAC
| Características de los pacientes (n=400) | Grupo preprotocolo (n=200) | Grupo posprotocolo (n=200) | p |
| Radiológicas y gasométricas | |||
| Infiltrado unilobar/multilobar/bilateral | 141/44/15 (70,5-22-7,5%) | 145/42/13 (72,5-21-6,5%) | 0,885 |
| Derrame pleural | 35 (17,5%) | 37 (18,5%) | 0,795 |
| pH arterial <7,35 | 23 (11,5%) | 25 (12,5%) | 0,651 |
| PO2/FiO2<250 | 25 (13,81%) | 34 (15,52%) | 0,395 |
| PO2<60mmHg | 75 (37,5%) | 82 (41%) | 0,322 |
| Hallazgos de laboratorio | |||
| Urea >64mg/dl o Cr >1,5mg/dl | 45 (23,43%) | 55 (27,63%) | 0,356 |
| Sodio <130mEq/l | 15 (7,81%) | 22 (11,05%) | 0,303 |
| Glucemia >250mg/dl | 22 (11,45%) | 26 (13,06%) | 0,628 |
| Hematocrito <30% | 20 (10,41%) | 16 (8,04%) | 0,485 |
| Leucocitosis >12.000/mm3o >10% cayados | 114 (59,37%) | 132 (66,33%) | 0,174 |
| Leucopenia <4.000/mm3 | 28 (14,58%) | 21 (10,55%) | 0,285 |
| Trombopenia <100.000/mm3 | 27 (14,06%) | 28 (14,07%) | 0,998 |
| Biomarcadores | |||
| Solicitados en el SU | 38 (19,28%) | 180 (90%) | < 0,001 |
| Niveles PCR (mg/l) ± DE (todos los pacientes) | 74,82 ± 18,72 | 58,90 ± 22,01 | < 0,001 |
| PCR (mg/l) ± DE en PSI I | 68 | 45,82 ± 24,58 | 0,383 |
| PCR (mg/l) ± DE en PSI II | 54,55 ± 31,34 | 51,02 ± 18,51 | 0,751 |
| PCR (mg/l) ± DE en PSI III | 69,92 ± 19,69 | 49,25 ± 16,06 | 0,004 |
| PCR (mg/l) ± DE en PSI IV | 78,69 ± 14,64 | 66,46 ± 18,28 | 0,069 |
| PCR (mg/l) ± DE en PSI V | 78,34 ± 15,06 | 70,04 ± 20,11 | 0,147 |
| Niveles PCT (ng/ml) ± DE (todos los pacientes) | 4,89 ± 11,31 | 2,51 ± 12,88 | <0,001 |
| PCT (ng/ml) ± DE en PSI I | 0,88 | 0,60 ± 0,32 | 0,416 |
| PCT (ng/ml) ± DE en PSI II | 3,31 ± 4,47 | 1,22 ± 1,47 | 0,079 |
| PCT (ng/ml) ± DE en PSI III | 3,63 ± 2,82 | 1,31 ± 1,47 | 0,011 |
| PCT (ng/ml) ± DE en PSI IV | 3,79 ± 4,00 | 1,56 ± 1,31 | 0,047 |
| PCT (ng/ml) ± DE en PSI V | 4,56 ± 3,65 | 5,16 ± 4,92 | 0,220 |
DE: desviación estándar; NAC: neumonía adquirida en la comunidad; PCR: proteína C reactiva; PCT: procalcitonina; PSI: Pneumonia Severity Index; SU: servicio de urgencias.
Los porcentajes excluyen los datos perdidos, si los hubiere.
No hubo diferencias significativas entre Gpre y Gpos en el perfil del médico responsable en el SU (residente/facultativo del SU/otros especialistas), p=0,339, con proporciones del 52,52-41,41-6.06% vs 54,5-42,5-3%, respectivamente.
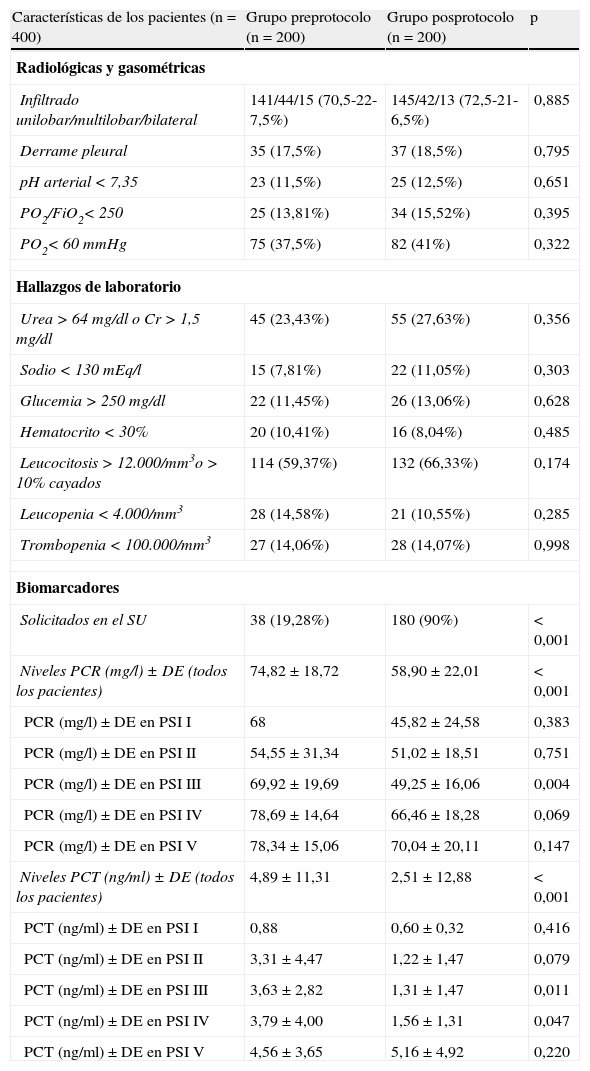
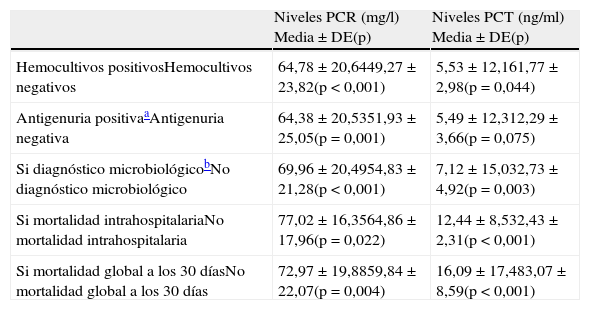
Como se recoge en la tabla 3, sí hubo diferencias significativas entre Gpre y Gpos en la solicitud de PCR y/o PCT en el SU (19,28% vs 90% respectivamente; p<0,001). Sin embargo (y quizá como consecuencia del mayor uso en Gpos), los niveles de PCR y de PCT fueron inferiores en el Gpos (74,82±18,72 vs 58,90±22,01mg/dl, para PCR, y 4,89±11,31 vs 2,51±12,88ng/ml, para PCT; p<0,001 en ambos casos). En la tabla 3 puede verse también cómo las diferencias de mayor magnitud en la concentración de ambos marcadores aparecen en los grupos intermedios (ii a iv) según el PSI. Al comparar las medias de PCR, de todos los pacientes del estudio, entre los subgrupos de pacientes según criterios de gravedad clínica se encontró diferencia significativa (p<0,05) al comparar los pacientes sin S con los que cumplían criterios de S (p=0,028), SG (p<0,001) y SS (p=0,024), así como entre los enfermos con S y SG (p=0,011), aunque no se encontraron al comparar los pacientes con SS con los que presentaron S y SG (p>0,05). De la misma manera, al valorar las medias de PCT se encontraron diferencias (p<0,05) entre los pacientes sin S con los que presentaban SG (p=0,042) y SS (p<0,001), entre los pacientes con S con los subgrupos de SG (p=0,017) y SS (p<0,001), y entre los pacientes con SG con los SS (p<0,001). Además, en el conjunto de pacientes se comprobó la existencia de relación (p<0,05) entre la solicitud de biomarcadores con la administración precoz (<4h) del antimicrobiano en el SU (82,6% vs 48,2%), con la elección de pauta antibiótica adecuada (66,5% vs 88,5%), con la decisión acertada de destino del paciente (89,3% vs 69,8%), con la solicitud de la analítica adecuada (92,2% vs 63,5%) y con la solicitud acertada de estudios microbiológicos (86,2% vs 61,2%). En la tabla 4 se muestran las asociaciones encontradas entre los niveles de biomarcadores y la consecución de diagnóstico microbiológico y la mortalidad intrahospitalaria y global a los 30días.
Relación entre niveles de biomarcadores con el diagnóstico microbiológico y la mortalidad
| Niveles PCR (mg/l) Media±DE(p) | Niveles PCT (ng/ml) Media±DE(p) | |
| Hemocultivos positivosHemocultivos negativos | 64,78 ± 20,6449,27 ± 23,82(p<0,001) | 5,53 ± 12,161,77 ± 2,98(p=0,044) |
| Antigenuria positivaaAntigenuria negativa | 64,38 ± 20,5351,93 ± 25,05(p=0,001) | 5,49 ± 12,312,29 ± 3,66(p=0,075) |
| Si diagnóstico microbiológicobNo diagnóstico microbiológico | 69,96 ± 20,4954,83 ± 21,28(p<0,001) | 7,12 ± 15,032,73 ± 4,92(p=0,003) |
| Si mortalidad intrahospitalariaNo mortalidad intrahospitalaria | 77,02 ± 16,3564,86 ± 17,96(p=0,022) | 12,44 ± 8,532,43 ± 2,31(p<0,001) |
| Si mortalidad global a los 30díasNo mortalidad global a los 30días | 72,97 ± 19,8859,84 ± 22,07(p=0,004) | 16,09 ± 17,483,07 ± 8,59(p<0,001) |
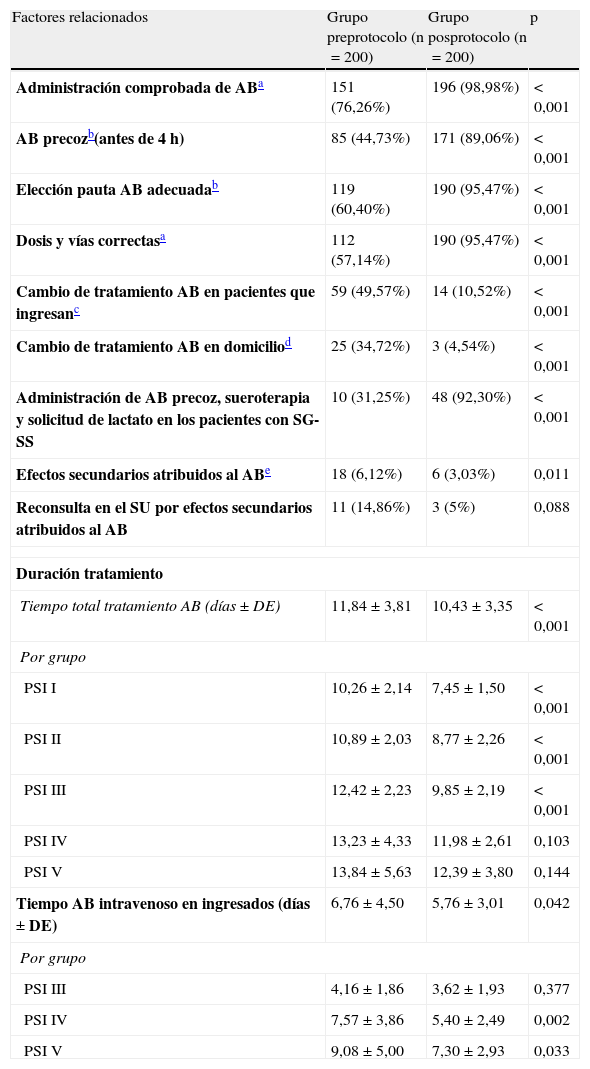
Existe una evidente diferencia entre el Gpre y el Gpos, en todos los casos con p<0,001, y diferencias entre el 22 y el 60% en las variables de actuación con el antibiótico en el SU que pueden cambiar e influir en el desarrollo, la evolución y el pronóstico de los pacientes con NAC (tabla 5). La administración del antibiótico en el SU, la administración precoz en las primeras 4h, la elección adecuada de la pauta y su posología, y la administración de antibiótico precoz y sueroterapia en los casos de SG y SS en el SU fueron mayores en el Gpos. Y por el contrario, los pacientes a los que se les cambió la pauta inicial de antibiótico tanto en planta o en UCI como en los dados de alta fue significativamente menor en el Gpos (número de casos y porcentajes en la tabla 5). La duración del tiempo de tratamiento antibiótico total en pacientes ingresados fue mayor en el Gpre, tanto globalmente (11,84±3,81 vs 10,43±3,35 días; p<0,001) como en cada uno de los grupos según el PSI (tabla 5). Lo mismo sucedió con la duración del tratamiento antibiótico intravenoso en el conjunto de pacientes (6,76±4,50días en el Gpre vs 5,76±3,01días en el Gpos; p=0,042) y en los subgrupos según el PSI (resultados en la tabla 5). Tras ajustar por destino del paciente (alta, observación, UCE, planta, UCI o fallecimiento) y grupo según el PSI, la media de la diferencia continuó siendo superior en el Gpre para el tiempo total de utilización de antibiótico (media=1,6; IC95%: 1,0 a 2,3 días) y para tiempo de uso intravenoso (media=1,4; IC95%: 0,6 a 2,2 días).
Factores relacionados y manejo de los antibióticos en los pacientes con NAC en el SU
| Factores relacionados | Grupo preprotocolo (n=200) | Grupo posprotocolo (n=200) | p |
| Administración comprobada de ABa | 151 (76,26%) | 196 (98,98%) | <0,001 |
| AB precozb(antes de 4h) | 85 (44,73%) | 171 (89,06%) | <0,001 |
| Elección pauta AB adecuadab | 119 (60,40%) | 190 (95,47%) | <0,001 |
| Dosis y vías correctasa | 112 (57,14%) | 190 (95,47%) | <0,001 |
| Cambio de tratamiento AB en pacientes que ingresanc | 59 (49,57%) | 14 (10,52%) | <0,001 |
| Cambio de tratamiento AB en domiciliod | 25 (34,72%) | 3 (4,54%) | <0,001 |
| Administración de AB precoz, sueroterapia y solicitud de lactato en los pacientes con SG-SS | 10 (31,25%) | 48 (92,30%) | <0,001 |
| Efectos secundarios atribuidos al ABe | 18 (6,12%) | 6 (3,03%) | 0,011 |
| Reconsulta en el SU por efectos secundarios atribuidos al AB | 11 (14,86%) | 3 (5%) | 0,088 |
| Duración tratamiento | |||
| Tiempo total tratamiento AB (días±DE) | 11,84±3,81 | 10,43±3,35 | <0,001 |
| Por grupo | |||
| PSI I | 10,26±2,14 | 7,45±1,50 | <0,001 |
| PSI II | 10,89±2,03 | 8,77±2,26 | <0,001 |
| PSI III | 12,42±2,23 | 9,85±2,19 | <0,001 |
| PSI IV | 13,23±4,33 | 11,98±2,61 | 0,103 |
| PSI V | 13,84±5,63 | 12,39±3,80 | 0,144 |
| Tiempo AB intravenoso en ingresados (días±DE) | 6,76±4,50 | 5,76±3,01 | 0,042 |
| Por grupo | |||
| PSI III | 4,16±1,86 | 3,62±1,93 | 0,377 |
| PSI IV | 7,57±3,86 | 5,40±2,49 | 0,002 |
| PSI V | 9,08±5,00 | 7,30±2,93 | 0,033 |
AB: antibiótico; IC: intervalo de confianza; OR: odds ratio; SG: sepsis grave; SS: shock séptico; SU: servicio de urgencias.
Los porcentajes excluyen los datos perdidos.
También se encuentran diferencias (p<0,05) entre los subgrupos según grados de PSI entre Gpre y Gpos.
También se encuentran diferencias (p<0,05) entre los subgrupos según grados de PSI y según grados de gravedad clínica (pacientes con sepsis, sepsis grave y shock séptico) entre Gpre y Gpos.
Incluye cualquier cambio de tipo de antimicrobiano y/o su posología en las primeras 48h del ingreso en la unidad de corta estancia, en la planta de hospitalización o en la unidad de cuidados intensivos. Esta diferencia es más relevante (p<0,05) en los grupos con PSI IV y V entre el Gpre y Gpos.
Incluye cualquier cambio de tipo de antimicrobiano y su posología en las primeras 72h por el médico de atención primaria, urgencias o en consultas externas en los pacientes dados de alta directamente o tras permanecer en observación. Esta diferencia es relevante (p<0,05) en los grupos con PSI I entre el Gpre y Gpos.
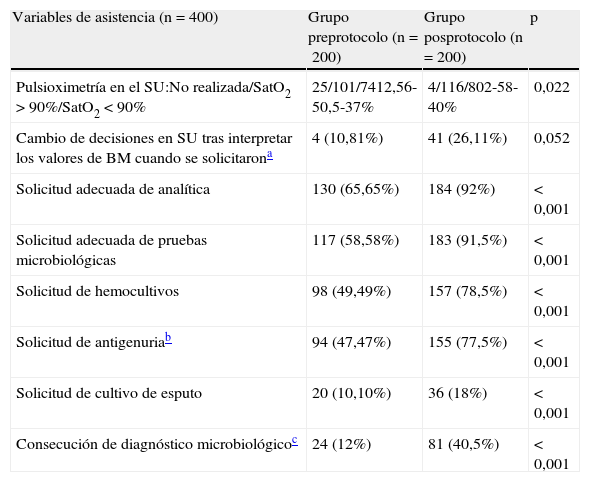
En cuanto a las decisiones de los MU en relación a actuaciones concretas en torno a la asistencia (tabla 6), hubo diferencias significativas y relevantes (con p<0,001 y diferencias superiores al 25% en todos los casos) a favor del Gpos en cuanto a la solicitud adecuada de analítica y de estudios microbiológicos (hemocultivos, antigenuria, cultivo de esputo). Así mismo, mientras que en el Gpre se alcanzó el diagnóstico microbiológico en el 12% de los casos, la cifra correspondiente en el Gpos fue del 45,5% (p<0,001). También hubo mayor número de cambios de decisiones (pautas o destino del paciente) tras interpretar los biomarcadores en el Gpos (10,81% vs 26,11%; p=0,052). Finalmente, es llamativo que en el 12,56% de los pacientes del Gpre no se reflejara la saturación de O2 frente al 2% en el GPos (p=0,022), siendo más evidente (p=0,010) al compararlo en el subgrupo de PSI I (27,8% vs 2,6%).
Factores relacionados con la adecuación de la atención de los pacientes con NAC en el SU
| Variables de asistencia (n=400) | Grupo preprotocolo (n=200) | Grupo posprotocolo (n=200) | p |
| Pulsioximetría en el SU:No realizada/SatO2 >90%/SatO2<90% | 25/101/7412,56-50,5-37% | 4/116/802-58-40% | 0,022 |
| Cambio de decisiones en SU tras interpretar los valores de BM cuando se solicitarona | 4 (10,81%) | 41 (26,11%) | 0,052 |
| Solicitud adecuada de analítica | 130 (65,65%) | 184 (92%) | <0,001 |
| Solicitud adecuada de pruebas microbiológicas | 117 (58,58%) | 183 (91,5%) | <0,001 |
| Solicitud de hemocultivos | 98 (49,49%) | 157 (78,5%) | <0,001 |
| Solicitud de antigenuriab | 94 (47,47%) | 155 (77,5%) | <0,001 |
| Solicitud de cultivo de esputo | 20 (10,10%) | 36 (18%) | <0,001 |
| Consecución de diagnóstico microbiológicoc | 24 (12%) | 81 (40,5%) | <0,001 |
BM: biomarcadores; NAC: neumonía adquirida en la comunidad; SU: servicio de urgencias.
Los porcentajes excluyen los datos perdidos.
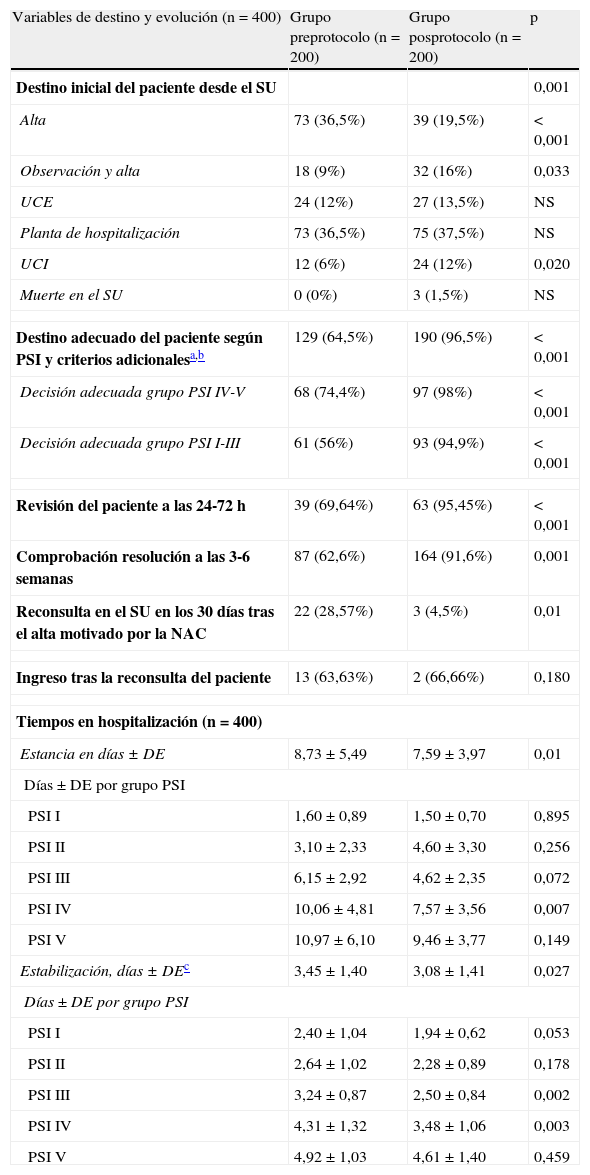
El alta directa desde el SU fue mayor en el Gpre, mientras que en el Gpos se decidió en más ocasiones dejar al paciente en observación y hubo mayor tasa de ingresos en la UCI desde el SU (valores en la tabla 7). El 35% de los pacientes del Gpre tuvo un destino inicial inapropiado (alta improcedente o ingreso inadecuado) por el 3,6% del Gpos (p<0,001) (tabla 7). También fue superior en el grupo Gpos la adecuación del destino del paciente desde el SU, juzgada según las recomendaciones del PSI y de los criterios adicionales señalados en la tabla 1 (64,5% vs 96,5%; p<0,001). De hecho, disminuyeron las «altas improcedentes» de los grupos PSI IV-V del 35,5% (Gpre) al 2% (Gpos) (p<0,001) y los ingresos o altas inadecuados de los grupos PSI I-III del 44 al 5,1% (p<0,001). Por otro lado, tanto la revisión del paciente a las 24-72h del alta como la comprobación de la resolución clínica y radiológica a las 3-6semanas fue significativamente mayor en el Gpos (p<0,01), mientras que el número de reconsultas en el SU tras el alta inicial fue menor en el Gpos (p=0,01).
Factores indicadores de evolución y destino de los pacientes diagnosticados de NAC en el SU
| Variables de destino y evolución (n=400) | Grupo preprotocolo (n=200) | Grupo posprotocolo (n=200) | p |
| Destino inicial del paciente desde el SU | 0,001 | ||
| Alta | 73 (36,5%) | 39 (19,5%) | <0,001 |
| Observación y alta | 18 (9%) | 32 (16%) | 0,033 |
| UCE | 24 (12%) | 27 (13,5%) | NS |
| Planta de hospitalización | 73 (36,5%) | 75 (37,5%) | NS |
| UCI | 12 (6%) | 24 (12%) | 0,020 |
| Muerte en el SU | 0 (0%) | 3 (1,5%) | NS |
| Destino adecuado del paciente según PSI y criterios adicionalesa,b | 129 (64,5%) | 190 (96,5%) | <0,001 |
| Decisión adecuada grupo PSI IV-V | 68 (74,4%) | 97 (98%) | <0,001 |
| Decisión adecuada grupo PSI I-III | 61 (56%) | 93 (94,9%) | <0,001 |
| Revisión del paciente a las 24-72h | 39 (69,64%) | 63 (95,45%) | <0,001 |
| Comprobación resolución a las 3-6 semanas | 87 (62,6%) | 164 (91,6%) | 0,001 |
| Reconsulta en el SU en los 30 días tras el alta motivado por la NAC | 22 (28,57%) | 3 (4,5%) | 0,01 |
| Ingreso tras la reconsulta del paciente | 13 (63,63%) | 2 (66,66%) | 0,180 |
| Tiempos en hospitalización (n=400) | |||
| Estancia en días±DE | 8,73±5,49 | 7,59±3,97 | 0,01 |
| Días±DE por grupo PSI | |||
| PSI I | 1,60±0,89 | 1,50±0,70 | 0,895 |
| PSI II | 3,10±2,33 | 4,60±3,30 | 0,256 |
| PSI III | 6,15±2,92 | 4,62±2,35 | 0,072 |
| PSI IV | 10,06±4,81 | 7,57±3,56 | 0,007 |
| PSI V | 10,97±6,10 | 9,46±3,77 | 0,149 |
| Estabilización, días±DEc | 3,45±1,40 | 3,08±1,41 | 0,027 |
| Días±DE por grupo PSI | |||
| PSI I | 2,40±1,04 | 1,94±0,62 | 0,053 |
| PSI II | 2,64±1,02 | 2,28±0,89 | 0,178 |
| PSI III | 3,24±0,87 | 2,50±0,84 | 0,002 |
| PSI IV | 4,31±1,32 | 3,48±1,06 | 0,003 |
| PSI V | 4,92±1,03 | 4,61±1,40 | 0,459 |
AB: antibiótico; IC: intervalo de confianza; NAC: neumonía adquirida en la comunidad; NS: no significativo o no procedente; OR: odds ratio; SG: sepsis grave; SS: shock séptico; SU: servicio de urgencias; UCE: unidad de corta estancia; UCI: unidad de cuidados intensivos.
Los porcentajes excluyen los datos perdidos.
Se tienen en cuenta además del PSI y los criterios adicionales reflejados en la tabla 1, la valoración o juicio clínico argumentado del médico de urgencias.
También se encuentran diferencias (p<0,05) entre todos los subgrupos según grados de PSI entre Gpre y Gpos.
Según criterios de Halm y Teirstein26: frecuencia cardiaca <100lpm, frecuencia respiratoria <24rpm, temperatura <37,2°C, presión arterial sistólica >90mmHg, saturación O2 >90%, buen nivel de consciencia y tolerancia a la vía oral.
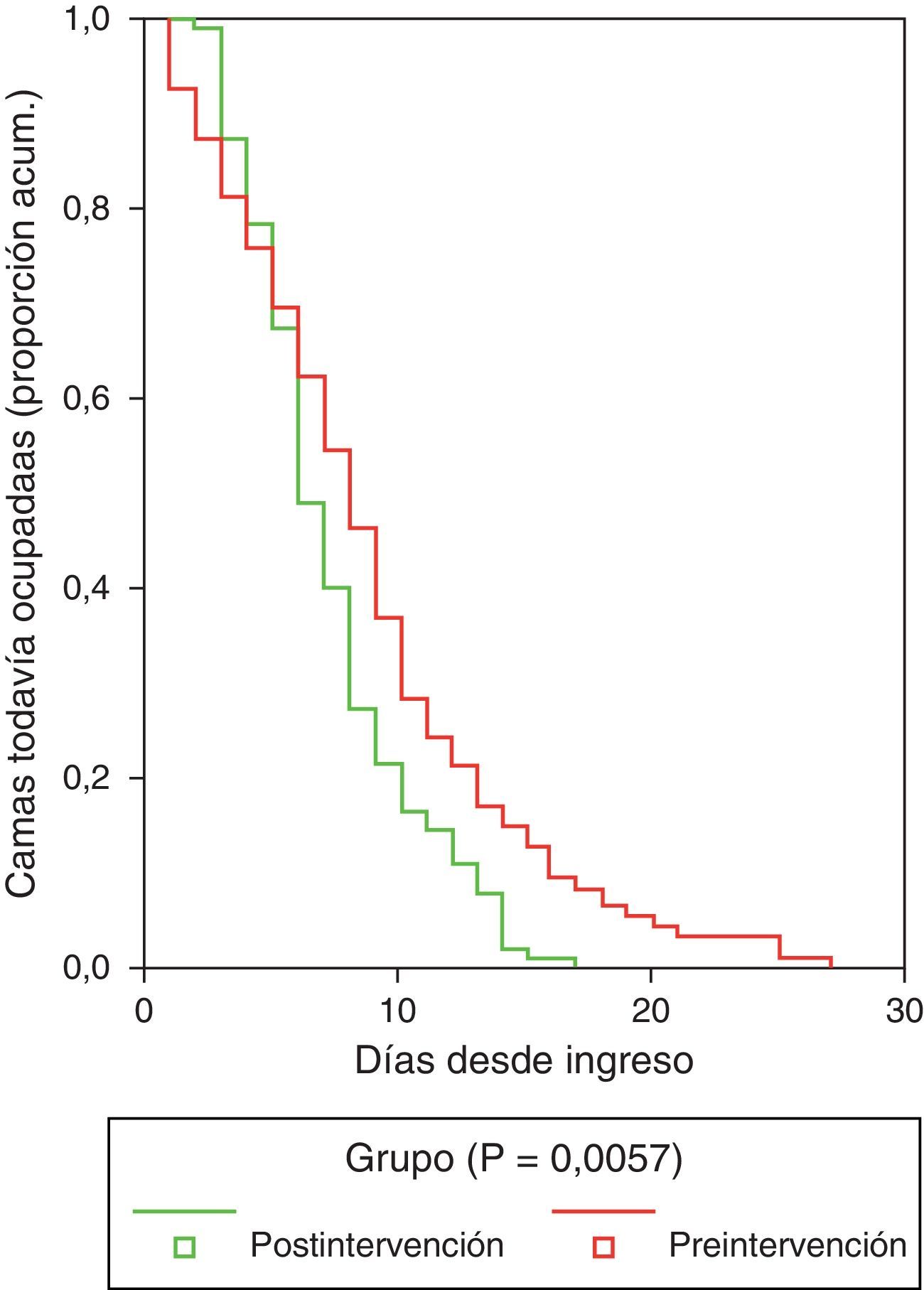
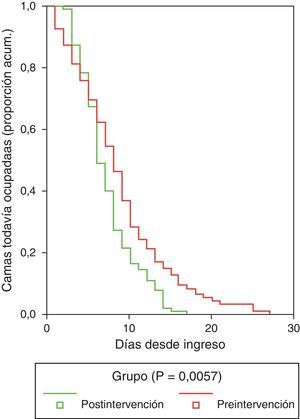
En relación con los tiempos de estancia hospitalaria y de consecución de la estabilización clínica según los criterios de Halm y Teirstein26, los resultados se señalan en la tabla 7. La mediana del tiempo hasta la consecución de la estabilización clínica entre los pacientes ingresados en la UCE y planta o en observación fue significativamente superior en el Gpre (4días; IC95%: 3,6 a 4,4días) que en el Gpos (3días; IC95%: 2,7 a 3,3días). Tras ajustar por grupo según el PSI o por lugar de destino (alta, observación, UCE, planta o UCI), este resultado se mantuvo. Se encontraron diferencias entre el Gpre y el Gpos, siendo globalmente mayor el tiempo de estancia hospitalaria en el Gpre (8,73±5,49 vs 7,59±3,97días, p=0,01). Tras ajustar por grupo de PSI y por destino del paciente (alta, observación, UCE, planta o UCI), la diferencia se mantuvo (p=0,011). De los datos encontrados derivados de la estancia hospitalaria cabe significar (fig. 2) que mientras en la primera fase el tiempo necesario para que consiguieran el alta el 50% de los pacientes ingresados en planta o UCE fue de 9días (IC95%: 8 a 10días), en el Gpos la cifra correspondiente fue de 7días (IC95%: 6 a 8días); así mismo, se necesitaron 8días (IC95%: 7-9) en el Gpre y 11días (IC95%: 9-13) en el Gpos para que fueran dados de alta el 75% de los pacientes. Tras controlar por grupo PSI y por lugar de ingreso, estas diferencias no se modificaron apreciablemente.
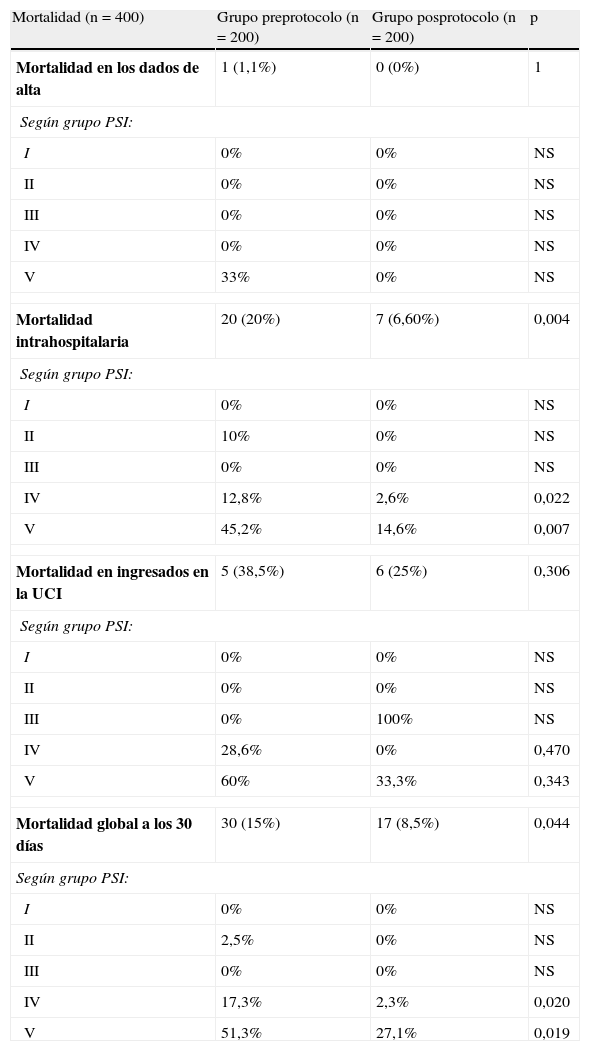
Los datos de mortalidad cruda se exponen en la tabla 8. No se encuentran diferencias significativas entre el Gpre y Gpos en relación con la mortalidad en los pacientes dados de alta (1,1% vs 0%, p=1) ni en los ingresados en la UCI, aunque esta fue mayor en los casos del Gpre frente al Gpos (38,5% vs 25%, p=0,306). Pero sí existieron en la mortalidad intrahospitalaria (20% vs 6,60%, p=0,004) y en la mortalidad global a los 30 días (15% vs 8,5%, p=0,044). Los resultados en función del grupo de PSI se reflejan en la tabla 8. Además se encontró que la elección de la pauta incorrecta de antibiótico en el SU frente a la correcta se relacionó tanto con la mortalidad intrahospitalaria (p=0,004) como con la mortalidad global a los 30 días (p=0,008). Por otro lado, la administración precoz del antibiótico en el SU se relacionó con una menor mortalidad global a los 30días (31,7% vs 15,3%, con p=0,068). Finalmente, al comparar entre el Gpre y Gpos la mortalidad intrahospitalaria controlada por las covariables relacionadas (edad, número de comorbilidades, índice de Charlson, grupo PSI y existencia de criterios de S, SG o SS) se mantuvo la diferencia significativa, con p=0,002 y OR: 0,191 (IC95%: 0,067-0,545). Y de la misma forma para la mortalidad global a los 30días ajustada por las covariables relacionadas (edad, número de comorbilidades, índice de Charlson, grupo PSI y existencia de criterios de S, SG o SS) también se encontró la persistencia de diferencias, con p=0,001 y OR: 0,270 (IC95%: 0,123-0,590).
Mortalidad de los pacientes con NAC tras ser vistos en el en el SU
| Mortalidad (n=400) | Grupo preprotocolo (n=200) | Grupo posprotocolo (n=200) | p |
| Mortalidad en los dados de alta | 1 (1,1%) | 0 (0%) | 1 |
| Según grupo PSI: | |||
| I | 0% | 0% | NS |
| II | 0% | 0% | NS |
| III | 0% | 0% | NS |
| IV | 0% | 0% | NS |
| V | 33% | 0% | NS |
| Mortalidad intrahospitalaria | 20 (20%) | 7 (6,60%) | 0,004 |
| Según grupo PSI: | |||
| I | 0% | 0% | NS |
| II | 10% | 0% | NS |
| III | 0% | 0% | NS |
| IV | 12,8% | 2,6% | 0,022 |
| V | 45,2% | 14,6% | 0,007 |
| Mortalidad en ingresados en la UCI | 5 (38,5%) | 6 (25%) | 0,306 |
| Según grupo PSI: | |||
| I | 0% | 0% | NS |
| II | 0% | 0% | NS |
| III | 0% | 100% | NS |
| IV | 28,6% | 0% | 0,470 |
| V | 60% | 33,3% | 0,343 |
| Mortalidad global a los 30días | 30 (15%) | 17 (8,5%) | 0,044 |
| Según grupo PSI: | |||
| I | 0% | 0% | NS |
| II | 2,5% | 0% | NS |
| III | 0% | 0% | NS |
| IV | 17,3% | 2,3% | 0,020 |
| V | 51,3% | 27,1% | 0,019 |
NAC: neumonía adquirida en la comunidad; NS: no significativo o no procedente por falta de muestra; PSI: Pneumonia Severity Index; SU: servicio de urgencias; UCI: unidad de cuidados intensivos.
La implementación de una GPC en un SU que incluya biomarcadores de inflamación e infección puede convertirse en una eficaz herramienta para, en primer lugar, disminuir la variabilidad de las decisiones más importantes que debe tomar el médico al atender a un paciente con NAC, como son la solicitud de estudios analíticos y microbiológicos, la administración del tratamiento adecuado precoz y la decisión de alta-ingreso (el cuándo) y el lugar apropiado (el dónde). Y, en segundo lugar, para mejorar la mortalidad global del proceso, disminuir la incidencia de altas improcedentes e ingresos inadecuados (y sus consecuencias) y reducir el tiempo necesario para conseguir la estabilización clínica y, por consiguiente, disminuir la estancia hospitalaria. Podemos decir que nuestra intervención resultó efectiva para el paciente y eficiente para el sistema al encontrar en todos los indicadores comentados un cambio positivo significativo entre el Gpre y el Gpos o, al menos, con cierta magnitud de sus efectos, reforzando lo publicado anteriormente17. En este sentido coincidimos con Capelastegui et al.13, que en un estudio pionero, tras implantar una GPC en su hospital, publicaron una reducción de los tiempos de tratamiento antibiótico (global 1,5días e intravenoso 1,3días), de la estancia hospitalaria (1,8días) y de la inadecuación de la pauta antibiótica elegida (del 28,6 al 11,8%). Además, también encontraron una reducción de la mortalidad intrahospitalaria (OR: 2,46; IC95%: 1,37-4,41) y de la global a los 30días (OR: 2,14; IC95%: 1,23-3,72). Son resultados muy similares a los nuestros, aunque hay que señalar 2 aspectos fundamentales diferenciales del estudio de Capelastegui et al.: contaron con un grupo control externo de otros centros y solo se incluyó a los pacientes ingresados. Blasi et al.14 demostraron en un estudio italiano sobre pacientes hospitalizados, con porcentajes y valores muy superponibles a los nuestros, que si bien el seguimiento de la GPC para la NAC de sus médicos era muy escaso (33%), como ocurría en nuestro SU, la eficacia de la misma fue evidente al reducir la mortalidad (OR: 0,77; IC95%: 0,51-0,98) y al aumentar la elección adecuada de la pauta antibiótica, hecho que se identificó como uno de los factores más relevantes relacionados con la reducción de la mortalidad (del 9,1 al 5,7%). En nuestro estudio también encontramos que la elección de la pauta incorrecta de antibiótico en el SU se relacionó tanto con la mortalidad intrahospitalaria (p=0,004) como con la global a los 30 días (p=0,008). Por otro lado, la administración precoz del antibiótico en el SU, aunque se relaciona con una menor mortalidad tanto intrahospitalaria como global a los 30 días (31,7% vs 15,3%), no lo hace con significación estadística pero tiene un efecto marcado. Dambrava et al.27, en un estudio de 780 pacientes hospitalizados con NAC comprobaron que existían diferencias entre la mortalidad según hubiera o no adherencia al antibiótico recomendado por la GPC utilizada en su centro (3% vs 10,6%); esta reducción es proporcionalmente comparable a la que nosotros hemos podido observar (8,5% vs 15%). Estos datos nos reafirman la importancia de administrar de forma precoz el antibiótico adecuado en el pronóstico de la NAC como nos indican las propias GPC1,2,6,12. Más allá de estas afirmaciones, Dean et al.16 llegaron a «cuantificar» el impacto de la implantación de una GPC para el manejo de la NAC, de forma que comunicaron que un incremento del 10% de uso de GPC entre los médicos se asoció con un descenso de la mortalidad (OR: 0,92; IC95%: 0,87-0,98, p=0,007), por lo que aunque solo una parte de los médicos se sumen al seguimiento de la GPC, el impacto beneficioso de la misma se conseguirá y el esfuerzo de la intervención estará compensado. Queda por dilucidar el efecto positivo de la aplicación de las GPC en la mortalidad a largo plazo, ya que hasta el momento se sabe que los pacientes ingresados por NAC tras 1-5 años presentan una mortalidad mayor de la esperada y frecuentes complicaciones cardiovasculares graves28, y que diversos marcadores biológicos relacionados con la inflamación y con la patología vascular están elevados en los pacientes con NAC con peor pronóstico a corto y a largo plazo29-33. Precisamente la inclusión de los biomarcadores (PCR y PCT) como elementos complementarios a las escalas pronósticas de gravedad (PSI y/o CURB-65)8,30, como predictores de bacteriemia34 y de mortalidad30-32 en la NAC e incluso para predecir etiología bacteriana35, cada día es más habitual en los SU. En nuestro estudio incluimos de forma arbitraria un valor de PCT>1ng/ml como criterio adicional de necesidad de ingreso (o al menos de seguimiento en observación), extracción de hemocultivos y administración precoz de antibiótico, debido a la probabilidad de bacteriemia y progresión a SG o SS que tendrían los pacientes según las recomendaciones de distintos autores29,34. Los resultados de nuestro estudio confirmaron que los valores elevados de los biomarcadores (y especialmente la PCT) se asociaron con el hallazgo de bacteriemia, con encontrar antigenuria positiva y/o diagnóstico microbiológico confirmado y con la mortalidad, siendo significativamente mayores (p<0,05) cuando la PCT es superior a 2ng/ml. Por ello, y de acuerdo con otros autores29,34, pensamos que estaría indicado en un enfermo con NAC y con PCT>0,5 ng/ml valorar la extracción de hemocultivos, la administración del antibiótico de forma precoz y tener este dato en consideración al realizar la valoración pronóstica con el PSI o CURB-65.
La decisión de ingresar o no al paciente determinará tanto la solicitud de estudios complementarios como el tipo de tratamiento y, por consiguiente, el pronóstico y la evolución del paciente, según esta haya sido o no acertada. Por ello es fundamental disminuir las altas improcedentes y los ingresos no justificados. Es conocido que la implantación rutinaria en un SU de una GPC que incorpore el PSI origina una disminución del porcentaje de ingresos no justificados, además de una mayor adecuación del lugar de tratamiento (ambulatorio u hospitalario) y de la adecuación y precocidad del tratamiento antibiótico18,36. La variabilidad del porcentaje de ingresos entre distintos centros y médicos es muy grande3,4 cuando no se sigue una GPC, e incluso cuando la adherencia es alta, ante la existencia de criterios o razones no contempladas en el PSI. Aujesky et al.20, en un estudio realizado en 12SU con alto seguimiento de una GPC con la escala PSI, encontraron que el 37,4% de los pacientes con PSI I-III fueron ingresados y el 3,2% de los casos con PSI IV-V fueron dados de alta. En este sentido, Labarere et al.37 también observaron que el 44,7% de los pacientes de bajo riesgo (PSI I-III) eran ingresados, y de estos el 20% no tenían justificación o algún criterio para haberlo hecho. En otro estudio reciente38, para valorar la adecuación de los ingresos hospitalarios por NAC, se comprobó una menor proporción de ingresos inadecuados (6,07%) en el grupo de bajo riesgo (PSI I-III) pero una gran proporción de altas improcedentes (según el PSI y criterios adicionales) que llegó al 32,89%. En nuestro estudio la elección de destino inicial inadecuado disminuyó significativamente en el Gpos (del 35,5 al 3,5%, p<0,001). Para los pacientes con PSI I-III observamos, como en el estudio de Hinojosa Mena-Bernal et al.38, que la inadecuación se debió en su mayoría a las altas improcedentes (al existir alguno de los criterios adicionales comentados en la tabla 1 que no se tuvieron en consideración) más que a ingresos inapropiados de pacientes con PSI I-III. Es decir, que se producía una infraestimación de la necesidad de ingreso desde el SU. Pensamos que la mejora de la adecuación de la decisión de alta o ingreso en nuestro estudio se debió a varios factores: el alta directa desde el SU fue mayor en el Gpre (36,5% vs 19,5%, p<0,001), en el Gpos se decidió en más ocasiones dejar al paciente en observación (9% vs 16%, p=0,033) y la existencia de PCT>1 ng/ml fue el criterio que cambió la decisión de alta a ingreso en el 26% de los pacientes con PSI I-III (al asumir una importante respuesta inflamatoria, probabilidad de bacteriemia elevada o existencia de criterios de S).
La implantación de la GPC también tiene implicaciones para el sistema. Además de evitar ingresos innecesarios y sus costes derivados9, se consigue una reducción de la estancia hospitalaria y del tiempo de tratamiento antibiótico13, como comprobamos también en nuestro estudio (1,14 y 1,41días, respectivamente). Otro dato aportado por nuestro trabajo es la reducción del tiempo de estabilización clínica (0,37días), que como hemos visto se relaciona con la administración precoz del antibiótico en el SU y con la liberación de camas hospitalarias más rápida, lo que para los nuevos pacientes con NAC que esperan para ingresar en nuestros SU frecuentemente saturados resultará también beneficioso39.
Aunque son varias las debilidades del estudio, creemos que este refleja fielmente el cambio de manejo y la mejora de la atención global al paciente con NAC en nuestro SU. Pero hay que señalar como limitaciones del mismo su carácter unicéntrico y no tener un grupo comparador externo, y que la muestra en determinadas comparaciones realizadas resultó escasa, sobre todo cuando se trataba de establecer comparaciones entre subgrupos según el PSI o de gravedad clínica (S-SG-SS). También hay que considerar que los MU en los 2grupos no fueron los mismos (existió un cambio estimado del 40% entre residentes y plantilla propia), por lo que podría producirse un sesgo según la experiencia y la adherencia a la GPC de unos y otros. Tampoco el periodo de recogida de casos fue un año natural para ambos grupos (lo que eliminaría una posible variación etiológica según la estacionalidad), aunque, como hemos visto, no hubo diferencias significativas en los diagnósticos encontrados. Y aunque la GPC tenía los mismos criterios para todos, la valoración de todos los puntos por 2colaboradores externos independientes (pese a que se excluyeron los casos en los que existían discrepancias) puede incluir siempre algún componente subjetivo. Por otro lado, el estudio no recoge el tiempo de evolución de la clínica de la NAC, lo que podía ser un factor que modificase algunos valores y la interpretación de los biomarcadores. A pesar de estas limitaciones, creemos que este estudio puede servir de referencia y ejemplo de cómo mejorar la atención para el conjunto de los pacientes que acuden al SU con NAC y, quizás, favorecer que quienes no lo hacen superen las barreras que llevan a los clínicos a no adherirse a las GPC40,41. Para futuras investigaciones queda la pregunta de si el efecto positivo tras la implantación de la GPC perdurará o serán necesarias nuevas intervenciones y reforzar la misma15.
En conclusión, la implementación de la GPC SEMES-SEPAR de 2008, que recomienda el uso del PSI y los biomarcadores, mejoró de forma significativa el proceso asistencial de la NAC en nuestro SU, siendo beneficiosa para los enfermos y para el sistema al lograr disminuir la mortalidad intrahospitalaria y global a los 30días consiguiendo una mayor adecuación de las decisiones de destino del paciente, de la solicitud de estudios indicados y de la administración del tratamiento antibiótico precoz y adecuado. Todo ello disminuyendo el tiempo necesario para la estabilización clínica del paciente y el de estancia hospitalaria.
Conflicto de interesesLos autores declaran que no existe ningún conflicto de intereses.
A Sancho Rodríguez Villar y a los Servicios de Admisión-Documentación y Microbiología del Complejo Hospitalario de Toledo por su ayuda en la recogida de datos y en la elaboración de este manuscrito. A todos los médicos que con su adhesión voluntaria a la GPC hicieron posible este estudio.