La aparición de la denominada triple terapia inhalada mediante la combinación de un agonista β2 de acción prolongada (LABA), un anticolinérgico de acción prolongada (LAMA) y un corticoide inhalado (ICS) en una combinación a dosis fijas (CDF) en un solo dispositivo de inhalación ha supuesto un cambio en el uso de este tratamiento. A pesar de que los ensayos clínicos nos aportan una idea de la eficacia y la seguridad de estas CDF, su aplicación a la clínica diaria puede presentar retos para el clínico sobre dos escenarios concretos. En pacientes que ya están recibiendo una triple terapia en dispositivos distintos el cambio a una CDF podría suponer beneficios en cuanto a disminución de errores críticos en el manejo de los inhaladores, mayor adherencia al tratamiento y menor coste, manteniendo la misma eficacia clínica. En pacientes que no están recibiendo una triple terapia en dispositivos distintos y que necesiten un cambio en el tratamiento, la CDF de triple terapia presenta beneficios mostrados en los ensayos clínicos. Aunque las diferencias metodológicas entre ensayos desaconsejan comparaciones directas, los resultados clínicos muestran una buena eficacia, pero también una considerable variabilidad y un número de resultados clínicos aún por explorar. En el futuro deberán desarrollarse ensayos que completen los datos de eficacia clínica, estudios en vida real que informen de su efectividad y trabajos encaminados a descubrir el perfil de paciente que presenta una mayor respuesta terapéutica a cada CDF, con el objeto de avanzar en el tratamiento personalizado.
The emergence of a fixed-dose combination (FDC) of a long-acting β2-agonists (LABAS), a long-acting anticholinergic agent (LAMA), and an inhaled corticosteroid (ICS) in a single inhalation device has changed the approach to inhaled therapy. Although clinical trials describe the efficacy and safety of these FDCs, their use in daily clinical practice can present challenges for the clinician in two specific scenarios. In patients who are already receiving triple therapy via different devices, switching to FDCs could confer benefits by reducing critical errors in the management of inhalers, improving therapeutic adherence, and lowering costs, while maintaining the same clinical efficacy. In patients who are not receiving triple therapy in different devices and who require a change in treatment, triple therapy FDC has shown benefits in clinical trials. Although methodological differences among the trials advise against direct comparison, clinical results show good efficacy, but also considerable variability, and a number of clinical outcomes have yet to be explored. In the future, trials must be developed to complete clinical efficacy data. Real-world efficacy trials are needed, and studies must be designed to determine the profile of patients who present a greater therapeutic response to each FDC in order to pave to way towards more personalized treatment.
La utilización de la denominada triple terapia inhalada mediante la combinación de un agonista ß2 de acción prolongada (LABA), un antimuscarínico de acción prolongada (LAMA) y un corticoide inhalado (ICS) está recomendada desde hace años como parte de la estrategia de escalonamiento en el tratamiento farmacológico de la enfermedad pulmonar obstructiva crónica (EPOC). Hasta el momento disponíamos de tres formas de establecer una triple terapia: empleando los tres fármacos por separado en tres dispositivos de inhalación, combinando una doble terapia de ICS/LABA +LAMA o bien con la combinación LABA/LAMA +ICS en dos dispositivos de inhalación. A pesar de que hasta el momento no existen estudios comparativos sobre cuál de las tres formas de administrarla era la más adecuada, se ha sugerido que para los pacientes con EPOC tendría más sentido usar LABA/LAMA +ICS, mientras que para el asma debería usarse LABA/ICS +LAMA1.
Sin embargo, la aparición de esta triple terapia en una combinación a dosis fijas (CDF) en un solo dispositivo de inhalación ha supuesto un cambio en el uso de esta triple combinación. Consecuentemente, el análisis de la eficacia y la seguridad, así como su coste-efectividad y su impacto en la vida real, son de interés, especialmente en la situación actual en la que existe una sobreprescripción de combinaciones que contienen ICS tanto en la atención médica comunitaria2 como en la hospitalaria3,4, independientemente del recuento de eosinófilos en sangre5. A pesar de que los ensayos clínicos nos aportan una idea de la eficacia y de la seguridad de estas CDF, su aplicación a la clínica diaria puede presentar retos para el clínico sobre los que sería conveniente hacer algunas reflexiones. Esta revisión tiene por objetivo evaluar la aplicación a la práctica clínica de la triple terapia en CDF teniendo en cuenta diversos escenarios clínicos.
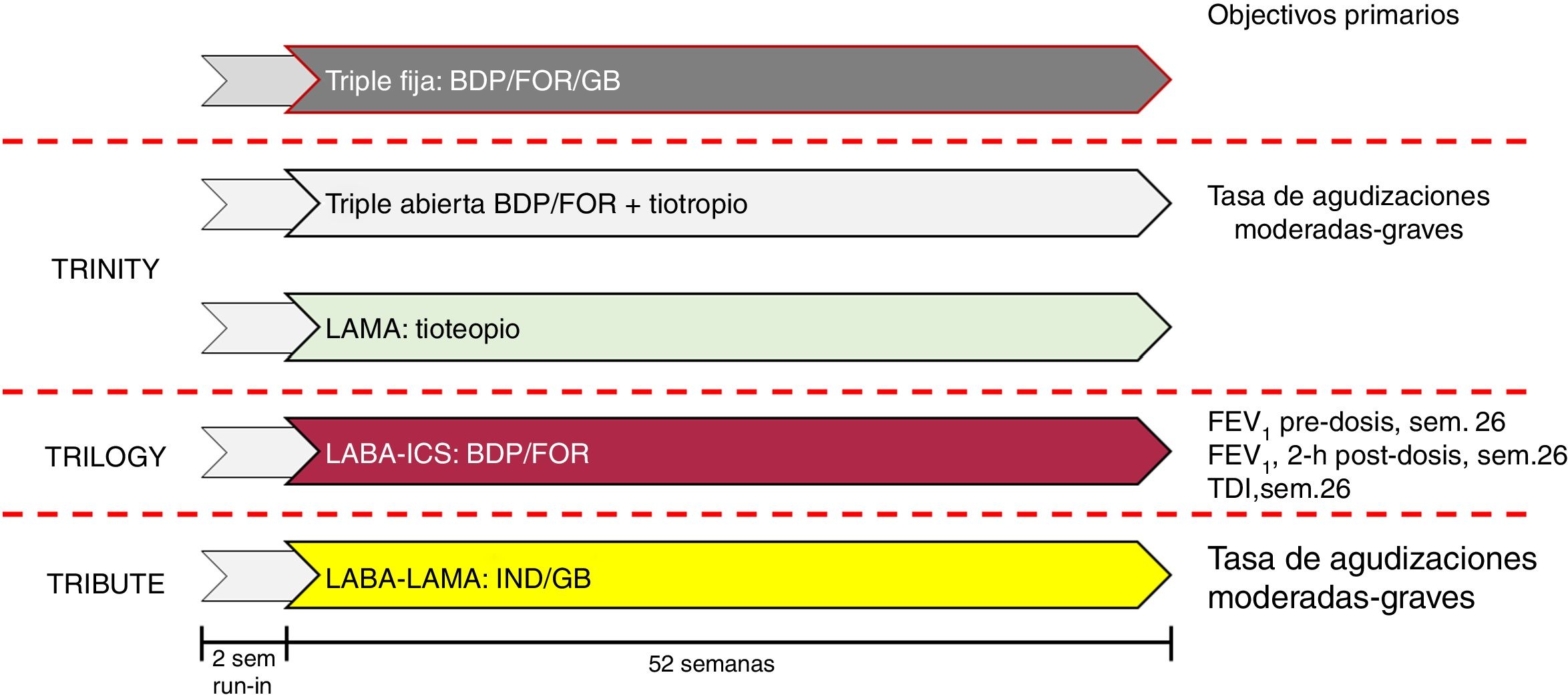
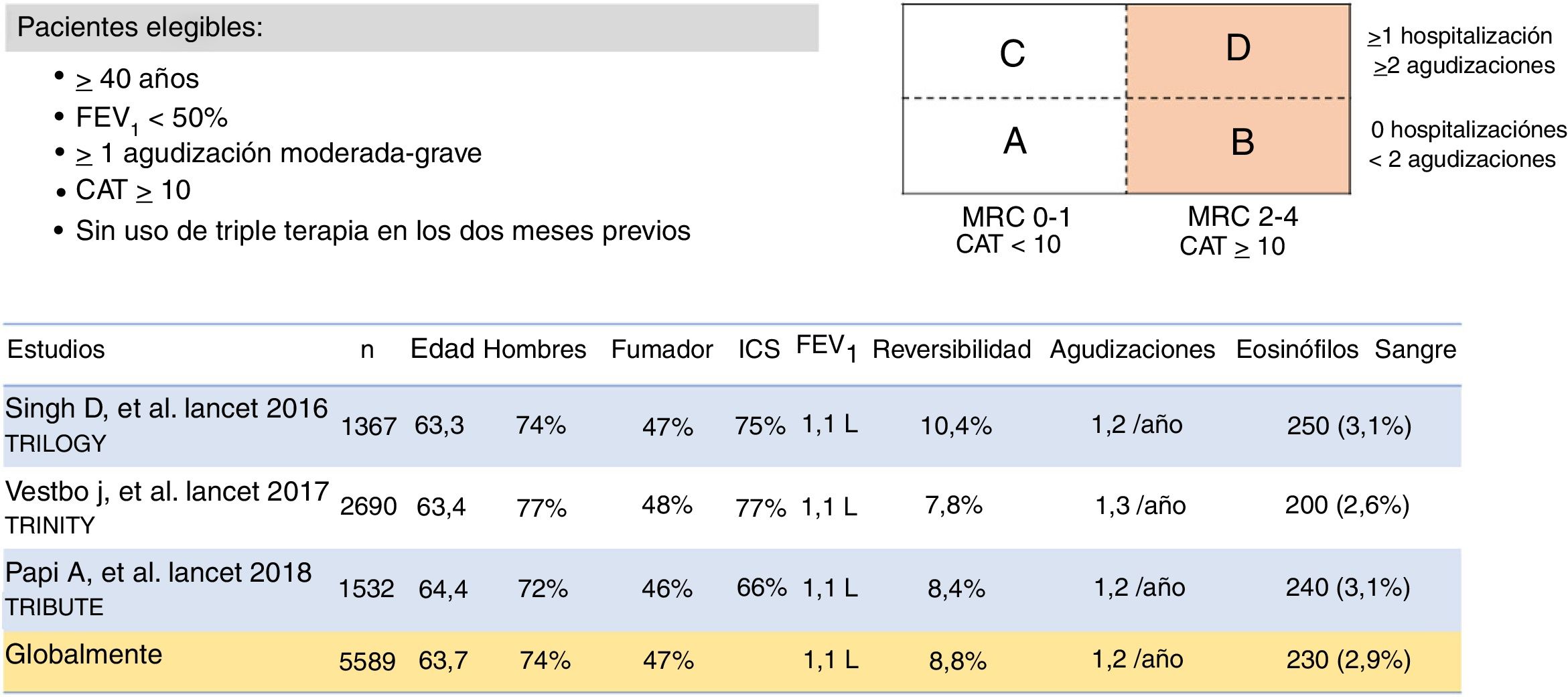
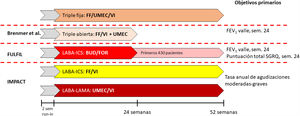
Desarrollo de las triples terapias en CDFHasta el momento hay cinco CDF de triple terapia, bien en desarrollo, bien ya comercializadas. La combinación de bromuro de glicopirronio (GB), fumarato de formoterol (FOR) y dipropionato de beclometasona (BDP) en cartucho presurizado (MDI)6 se ha estudiado en tres ensayos diferentes (fig. 1). Brevemente, TRILOGY aleatorizó a 1.367 pacientes para comparar la CDF de triple terapia con BDP/FOR. Aunque el ensayo duró 52semanas, los objetivos primarios se evaluaron a la semana26 y fueron el volumen espirado en el primer segundo (FEV1) previo a la dosis, el FEV1 de 2h después de la dosis y el cambio en el índice transicional de disnea (TDI)7. TRINITY aleatorizó 2.690 pacientes para comparar la CDF con tiotropio solo o con una triple combinación abierta de BDP/FOR +tiotropio. El objetivo primario fue la tasa anualizada de agudizaciones moderadas-graves frente a la monoterapia8. Finalmente, TRIBUTE aleatorizó a 2.690 pacientes para comparar la CDF contra indacaterol (IND)/GB con la dosis de 110/40 una vez al día. Su objetivo primario era la tasa anualizada de agudizaciones moderadas-graves9. Una peculiaridad de este desarrollo clínico es que el diseño, así como los criterios de inclusión y exclusión, fueron exactamente los mismos para los tres estudios (fig. 2).
Diseño de los trabajos de la combinación compuesta por BDP/FOR/GB.
BDP: dipropionato de beclometasona; FEV1: volumen espirado en el primer segundo; FOR: fumarato de formoterol; GB: bromuro de glicopirronio; ICS: corticoide inhalado; IND: indacaterol; LABA: agonista β2 de acción prolongada; LAMA: anticolinérgico de acción prolongada; TDI: índice transicional de disnea.
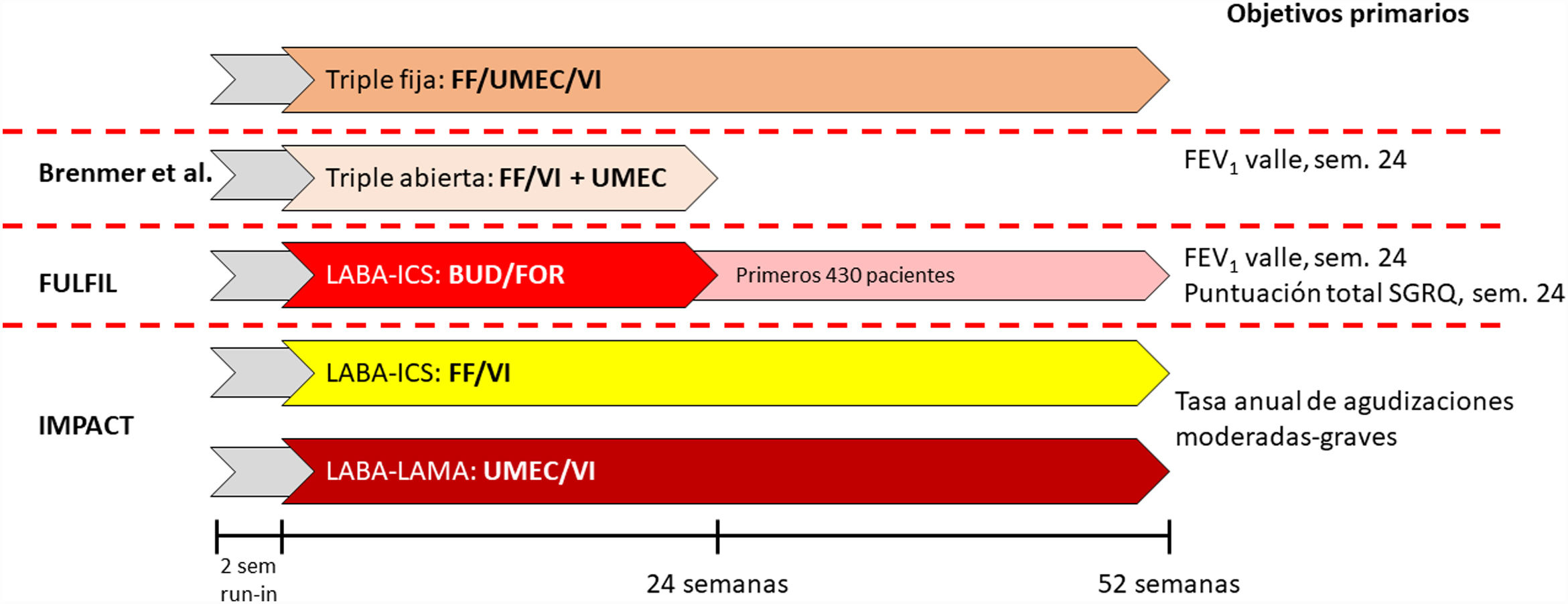
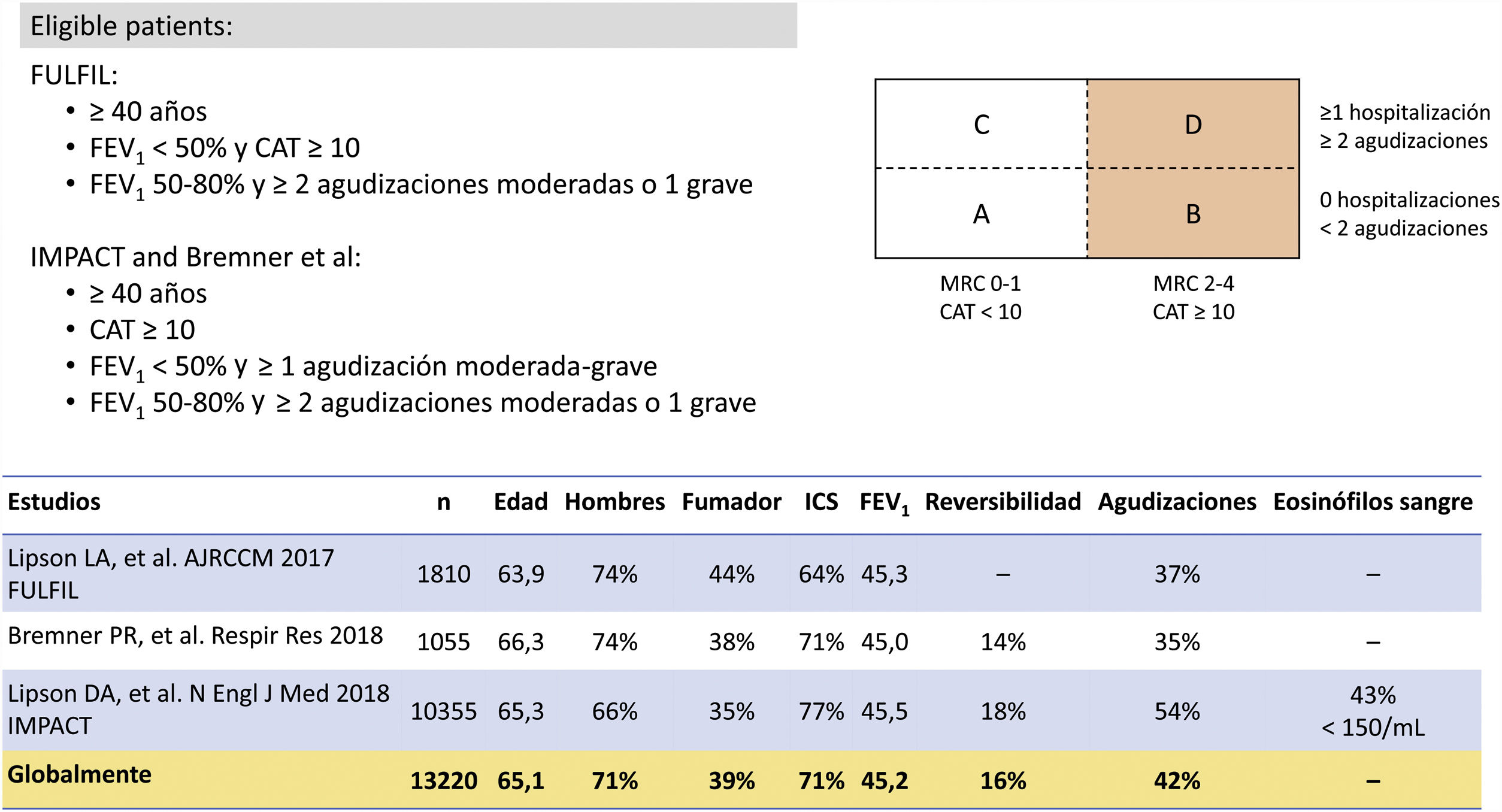
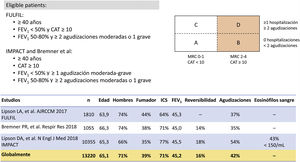
La combinación de bromuro de umeclidinio (UMEC), vilanterol trifenatato (VI) y furoato de fluticasona (FF)10 se ha evaluado mediante tres ensayos diferentes (fig. 3). Brevemente, FULFIL fue un ensayo clínico que aleatorizó a 1.810 pacientes para comparar la CDF con budesonida (BUD)/FOR. El objetivo primario fue el cambio desde el valor basal en el FEV1 valle y en la puntuación total del St. George's Respiratory Questionnaire (SGRQ) en la semana2411. En este estudio, un subconjunto de los primeros 430 pacientes en incluirse en el ensayo permaneció en el estudio hasta cumplir las 52semanas. El estudio de Bremner et al.12 aleatorizó a 1.055 pacientes con un diseño de no inferioridad para comparar la triple terapia en CDF en dispositivo Ellilpta con triple terapia abierta con FF/VI +UMEC en dos inhaladores Ellipta separados. El objetivo primario era el cambio desde el valor basal en el FEV1 valle a la semana24. Por último, el ensayo IMPACT aleatorizó a 10.355 pacientes para comparar la CDF con FF/VI y con UMEC/VIL, con la tasa anual de exacerbaciones moderadas o graves durante el tratamiento como objetivo primario13.
Diseño de los trabajos de la combinación compuesta por FF/UMEC/VI.
FEV1: volumen espirado en el primer segundo; FF: furoato de fluticasona; ICS: corticoide inhalado; LABA: agonista β2 de acción prolongada; LAMA: anticolinérgico de acción prolongada; SGRQ: St. George's Respiratory Questionnaire; UMEC: bromuro de umeclidinio; VI: vilanterol trifenatato.
La combinación de GB/FOR/BUD ha sido explorada en un ensayo en faseIII. El estudio KRONOS14 evaluó esta CDF en MDI en comparación con GB/FOR en MDI y con BUD/FOR en turbuhaler. Los objetivos primarios fueron el área bajo la curva de 0-4h en el FEV1 y el cambio desde basal en el FEV1 matutino pre-dosis contra GB/FOR y de no inferioridad contra BUD/FOR durante 24semanas. Los pacientes seleccionables tenían entre 40 y 80años, fumadores o exfumadores con un historial de tabaquismo de ≥10paquetes-año, diagnosticados de EPOC de leve a muy grave con un FEV1 entre 25 y 80%, con un CAT ≥10 a pesar de recibir dos o más terapias de mantenimiento inhaladas durante al menos 6semanas antes del cribado. Este estudio incluye pacientes con características diferentes y con un grado de afectación funcional más leve que las otras dos CDF comentadas hasta el momento.
Batefenterol/FF es una combinación de una molécula dual con actividad antimuscarínica y agonista β2 (MABA), por lo que puede hacer un efecto terapéutico de triple terapia con dos fármacos. Por el momento solo tenemos ensayos faseI en dispositivo Ellipta15. Finalmente, la combinación mometasona/IND/GB, de la que aún no hay publicaciones pero que está en desarrollo para el tratamiento del asma bronquial (https://clinicaltrials.gov/ct2/show/NCT03158311).
Tras varios meses desde la comercialización en España de dos de estas CDF, BDP/FOR/GB y FF/UMEC/VI, en la práctica clínica caben plantearse dos escenarios clínicos principales: el paciente que ya está en triple terapia en dispositivos por separado y el que no está aún recibiendo esta triple terapia.
Paciente que recibe triple terapia en dispositivos separadosEn este escenario clínico el paciente estará recibiendo tres fármacos inhalados en distintos dispositivos de inhalación posiblemente con distinta posología y proponemos unificarlo en un solo dispositivo con una única posología. Como cabe esperar, el manejo del nuevo dispositivo y los posibles cambios en el régimen de dosis diarias puede tener un papel importante para el paciente.
Para poder sustentar este cambio es necesario tener presente si se produce algún cambio en eficacia farmacológica y en el perfil de seguridad cuando se modifica una triple terapia abierta por una CDF. En este sentido, los datos para ambas CDF tienen algunos matices que necesitan un comentario. Para la combinación BDP/FOR/GB el estudio TRINITY encontró que el tratamiento con la CDF conseguía beneficios clínicos comparables con la terapia abierta8. Las únicas diferencias estadísticas encontradas fueron en calidad de vida medida por el SGRQ a las semanas26 y52, en la probabilidad de alcanzar 4puntos en el cuestionario SGRQ a la semana26, favoreciendo a la triple abierta, y en la tasa de exacerbaciones moderadas a graves en el subgrupo de pacientes con dos o más exacerbaciones en los 12 meses previos favoreciendo a la CDF (RR: 0,71; IC95%: 0,511-0,995; p=0,047)16. Posteriormente, un metaanálisis que compara triples terapias en CDF con triples terapias en abierto, encuentra que no existen diferencias en el riesgo de agudizaciones moderadas-graves, ni en hospitalizaciones, función pulmonar o calidad de vida17.
Por otro lado, en la combinación FF/UMEC/VI los autores concluyeron que la CDF no era inferior a la triple terapia separada en dos inhaladores (FF/VI +UMEC) en función pulmonar, síntomas ni agudizaciones o seguridad12.
Por tanto, con los datos globales de los ensayos podemos decir que el cambio de una triple terapia abierta a una CDF, en el tipo de paciente que se explora en estos ensayos, mantiene una eficacia clínica similar. En este contexto surge, por tanto, la duda sobre qué beneficios clínicos se obtienen al unificar una triple terapia abierta. Revisando la literatura se pueden identificar tres potenciales beneficios. En primer lugar, la disminución del número de inhaladores se ha asociado a una disminución en los errores en los manejos de los inhaladores18, lo que podría traducirse en una mayor efectividad. Este aspecto es especialmente relevante considerando que se trata de un tratamiento que engloba las tres familias de fármacos inhalados de que disponemos para el tratamiento de la EPOC. Consecuentemente, si se cometieran errores críticos que llevaran a una mala técnica se estarían dejando de recibir adecuadamente los tres fármacos. En segundo lugar, al disminuir el número de dispositivos es esperable una mayor adherencia al tratamiento19. No obstante, en este punto es importante recordar que la adherencia terapéutica es un concepto complejo en el que intervienen numerosos factores, entre los que el número de dispositivos representa uno solo de ellos20. En cualquier caso, es importante poner de manifiesto que la adherencia terapéutica debe ser un elemento central en la entrevista clínica y que, en cada contacto con el sistema sanitario, los profesionales que atienden a estos pacientes deben aprovechar la oportunidad para recalcar conceptos de educación sanitaria como es la adherencia terapéutica. En tercer lugar, otro potencial beneficio de cerrar una triple terapia es el precio. En las tablas 1 y 2 se resumen las diferencias en precio de las triples terapias abiertas frente a las cerradas. El análisis de los precios de las distintas combinaciones de fármacos inhalados deja algunos mensajes interesantes. Primero, que las dos triples terapias inhaladas en un solo dispositivo son más económicas que alguna terapia doble. Segundo, que casi todas las combinaciones abiertas tienen un coste superior a las cerradas, con diferencias que superan en muchos casos los 10€ al mes. Tercero, que no todas las combinaciones abiertas son más caras que las CDF (tablas 1 y 2), por lo que son necesarios estudios de coste-efectividad para evaluar el impacto presupuestario de este cambio a nivel de sistema sanitario, teniendo en cuenta el impacto en reducción de agudizaciones y, por tanto, de uso de recursos sanitarios.
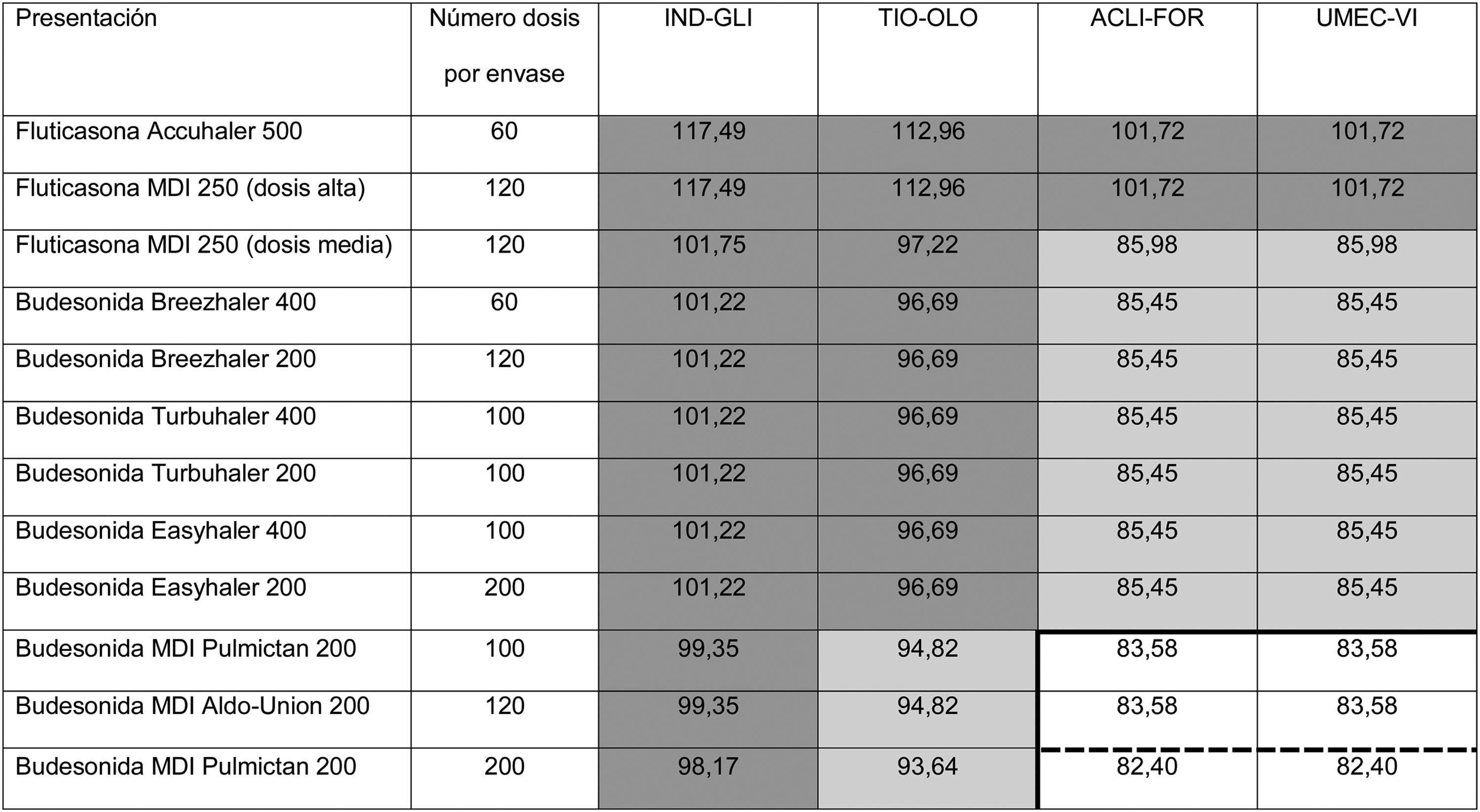
Distribución de precios de las triples terapias abiertas en comparación con las cerradas, según el nomenclátor de facturación del Ministerio de Sanidad, Consumo y Bienestar Social del Gobierno de España, a fecha mayo de 2019
Precios expresados en coste mensual en euros para España según precio de venta al público con el impuesto sobre el valor añadido incluido. Precio de FF/UMEC/VI 83,52€; BDP/FOR/GB 85,08€.
En gris oscuro, diferencias con el precio de la triple terapia cerrada de 10€ o más; en gris claro, menos de 10€; en blanco, triple terapia abierta más barata que la cerrada.
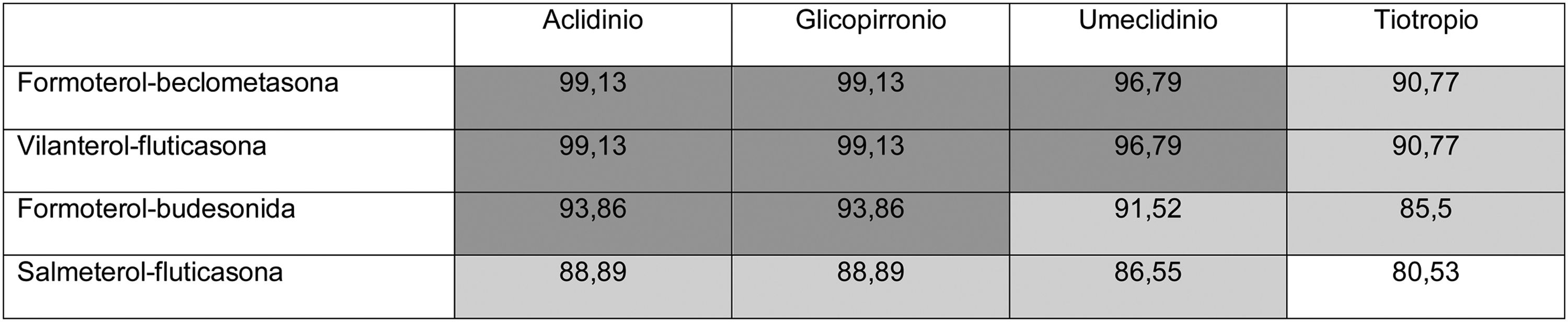
Distribución de precios de las triples terapias abiertas en comparación con BDP/FOR/GB, según el nomenclátor de facturación del Ministerio de Sanidad, Consumo y Bienestar Social del Gobierno de España, a fecha mayo de 2019
ACLI-FOR: aclidinio-formoterol; BDP/FOR/GB: combinación a dosis fijas de beclometasona, formoterol y glicopirronio; FF/UMEC/VI: combinación a dosis fijas de furoato de fluticasona, umeclidinio y vilanterol; IND-GLI: indacaterol-glicopirronio; MDI: inhalador de dosis medida; TIO-OLO: tiotropio-olodaterol; UMEC-VI: umeclidinio-vilanterol.
Precios expresados en coste mensual en euros para España según precio de venta al público con el impuesto sobre el valor añadido incluido. Precio de fluticasona referenciado para dosis altas de corticoide (1.000μg/día) o para dosis media (500μg/día) en administración cada 12h. Precio de budesonida referenciado solo para dosis medias (800μg/día) en administración cada 12h. BDP/FOR/GB 85,08€. Precio de FF/UMEC/VI 83,52€. En línea gruesa continua las combinaciones más económicas que BDP/FOR/GB, en línea discontinua las combinaciones más económicas que FF/UMEC/VI.
En resumen, los datos disponibles indican que la triple terapia en una CDF presenta una eficacia clínica superponible al actual esquema de tratamiento en dispositivos separados, con una posología cada 12 o 24h, un buen perfil de seguridad y un menor coste en la mayoría de las combinaciones abiertas. Además, de confirmarse con CDF de triple terapia los hallazgos para terapias dobles en adherencia y errores críticos, esto implicaría una mejor adherencia y una disminución de los errores en el manejo de inhaladores. Por tanto, en caso de que un paciente con EPOC necesite una triple terapia, como norma general tiene sentido considerar el cambio desde una abierta a una cerrada. En este cambio es necesario tener presente dos consejos: explicar el cambio al paciente para indicar que va a seguir tomando tres fármacos pero en un solo dispositivo de inhalación, de manera que no tenga la percepción de que le estamos reduciendo el tratamiento, y hacer una visita de evaluación a las pocas semanas para comprobar la eficacia y la tolerancia con el nuevo tratamiento, ya que está descrita la respuesta individualizada a componentes de la misma familia en los pacientes con EPOC21,22.
Paciente que NO está en triple terapiaOtro escenario es cuando el paciente no está recibiendo una triple terapia en abierto. Aunque no todos los pacientes incluidos en los ensayos de triple terapia en CDF realizaban un escalado de tratamiento (ver más adelante), esta es la filosofía con la que se diseñaron los ensayos clínicos y la indicación que viene recogida en la ficha técnica de las CDF comercializadas. Es importante tener presente que el desarrollo clínico se realizó en estos pacientes graves sintomáticos y con agudizaciones a pesar de recibir tratamiento con terapia doble o simple.
Lo primero que hay que tener presente es que muchos de los pacientes con terapia doble o simple están bien controlados y no necesitan cambio de medicación. En las distintas auditorías clínicas que se han realizado en nuestro país el porcentaje de pacientes evaluados en una visita de rutina en consultas externas de neumología y a los que no se les modificaba el tratamiento estuvo entre el 64,8%23 y el 77,5%4, según cada estudio. Sin embargo, el escenario que queremos abordar con el escalado a triple terapia es aquel paciente que, recibiendo tratamiento con terapia doble o simple, sigue estando limitado por la enfermedad, como se refleja en los criterios de elegibilidad de los estudios de triple terapia (figs. 2 y 4). La valoración de los ensayos clínicos que desarrollaron las dos CDF comercializadas en España, BDP/FOR/GB y FF/UMEC/VI, merecen algunas consideraciones tanto desde el punto de vista metodológico como de los resultados.
Desde el punto de vista metodológico, aunque el diseño es bastante parecido entre ambas CDF, existen algunas diferencias relevantes. En primer lugar, los criterios de elegibilidad fueron ligeramente distintos entre ambas (figs. 2 y 4). Como consecuencia, el perfil de pacientes y su gravedad según distintos parámetros clínicos y funcionales son diferentes. Aunque la puntuación del cuestionario COPD Assessment Test (CAT) fue muy similar entre todos los estudios, alrededor de 20puntos para todos los estudios que lo informaron, el FEV1 fue considerablemente menor (alrededor del 36%) para los estudios de BDP/FOR/GB, en comparación con los registrados por los estudios con FF/UMEC/VI (alrededor del 45%). Sin embargo, las tasas de exacerbaciones moderadas/graves durante el ensayo eran diferentes entre los estudios, independientemente del régimen de tratamiento, con un mayor número de eventos en el estudio IMPACT13 en comparación con el resto. En segundo lugar, una de las principales diferencias fue el diseño del periodo de pre-inclusión (run-in). Estos periodos de pre-inclusión son habituales en ensayos clínicos y tienen como principales objetivos la detección de participantes no seleccionables o no conformes, garantizar que los participantes se encuentran en una condición estable, proporcionar observaciones de referencia en las mismas circunstancias, homogeneizar el tratamiento antes de la aleatorización, asegurar la buena adherencia al tratamiento de los incluidos o identificar efectos adversos antes del inicio del estudio, entre otros24,25. En los ensayos de triple terapia en CDF cada estudio tuvo un período de pre-inclusión de 2semanas. Sin embargo, los pacientes en los estudios de BDP/FOR/GB recibieron un mismo tratamiento con terapias dobles o simples durante este período, mientas que los estudios de FF/UMEC/VI permitieron el uso de la terapia triple previamente prescrita, en concreto un 38% en IMPACT y un 28% en FULFIL12,13. Como consecuencia, en BDP/FOR/GB se producía un escalado en todos los casos tras un periodo de pre-inclusión con un tratamiento homogéneo, mientas que en el desarrollo de FF/UMEC/VI esto no se producía en todos los casos, produciéndose un cambio brusco en el tratamiento tras la asignación de los brazos de tratamiento26. Finalmente, algunos de estos estudios tenían un seguimiento a 6meses en lugar del año completo11,12. Como consecuencia de todo lo expuesto, las poblaciones descritas eras distintas, por lo que no se deben hacer comparaciones crudas directas. A falta de ensayos clínicos de comparación directa, actualmente existen algunos metaanálisis que puede resultar de utilidad27-29.
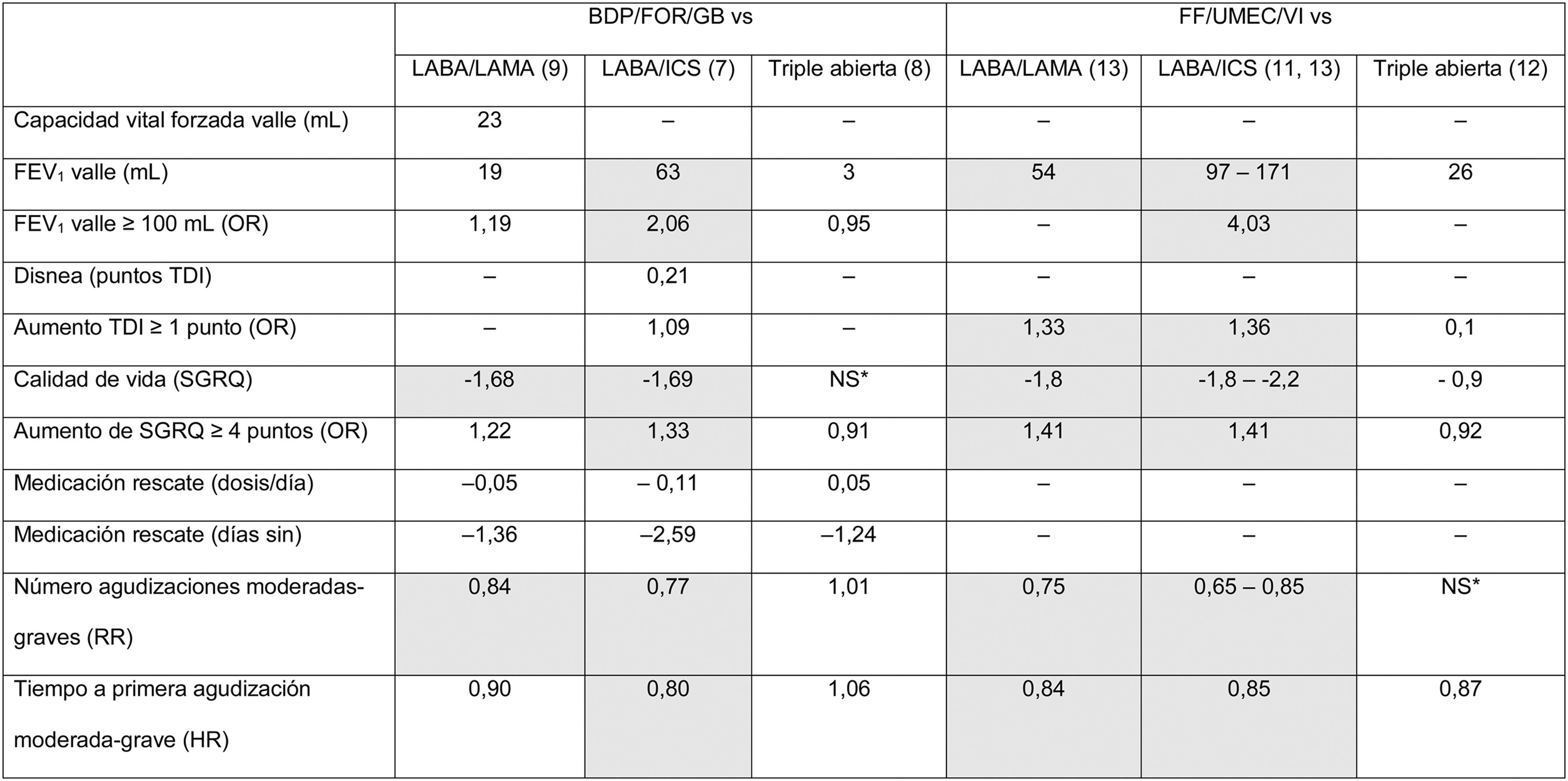
Desde el punto de vista de los resultados, los beneficios clínicos en términos de eficacia promedio pueden resumirse en la tabla 3, que muestra las diferencias promedio al final del ensayo clínico para cada uno de las variables sobre las que hay resultados. Un análisis tabulado más exhaustivo ha sido recientemente publicado30. Estos resultados se han analizado en diversos metaanálisis, confirmando la asociación del tratamiento de triple terapia con la eficacia clínica mostrada en la tabla 3 cuando se analizan los datos de manera agregada17,31. Del análisis y de la reflexión de estos estudios pueden sacarse algunas conclusiones. En primer lugar, aún existen numerosos resultados clínicos pendiente de explorarse. Resultados como el FEV1 matutino 5min post-dosis, el FEV1 pico, el área bajo la curva de 0 a 24h del FEV1, la capacidad pulmonar total, la capacidad residual funcional, el volumen residual o la capacidad inspiratoria no han sido suficientemente explorados o directamente no se han analizado en estos ensayos. De ellos llama especialmente la atención la evaluación de la disnea, de la que no hay datos en casi ninguno de los ensayos, o el uso de la medicación de rescate, no consistentemente reflejada en los estudios. En segundo lugar, existe una variabilidad considerable dentro de los resultados obtenidos, tanto entre CDF como dentro de la misma CDF. La variabilidad de los resultados es habitual cuando se resumen resultados de ensayos clínicos que muestran diferencias promedias entre brazos de tratamiento. Desde un punto de vista clínico, sin embargo, es necesario avanzar en la respuesta terapéutica de manera individualizada según el perfil clínico del paciente. Por tanto, en el futuro deberán desarrollarse estudios en vida real y trabajos encaminados a descubrir este perfil de paciente que presenta una mayor respuesta terapéutica a cada CDF.
Resultados de las estimaciones puntuales según se refieren en los ensayos clínicos originales con triple terapia en un solo dispositivo
BDP/FOR/GB: combinación a dosis fijas de beclometasona, formoterol y glicopirronio; FEV1: volumen espiratorio forzado en el primer segundo; FF/UMEC/VI: combinación a dosis fijas de furoato de fluticasona, umeclidinio y vilanterol; HR: hazard ratio; HRQL: calidad de vida relacionada con la salud; ICS: corticoide inhalado; LABA: agonistas ß2 de acción prolongada; LAMA: antimuscarínico de acción prolongada; NS: ningún estudio que informe de este dato encuentra diferencias significativas; OR: odds ratio; RR: risk ratio; SGRQ: cuestionario respiratorio de St. George; TDI: índice transicional de disnea.
Los datos muestran la diferencia promedio conseguida al final del seguimiento para cada variable entre el brazo de triple terapia en CDF frente a su comparador para cada variable. En el caso de existir más de un ensayo con estos resultados, se muestra el valor mayor y menor alcanzado en todos los ensayos que aporten este dato. En gris se marcan las diferencias estadísticamente significativas (p<0,05).
Desde el punto de vista de la seguridad, la proporción de efectos adversos fue similar entre los grupos de estudio, siendo el empeoramiento de la EPOC la manifestación adversa más común. Sobre las infecciones respiratorias, los ensayos describen un aumento numérico del número de pacientes con neumonía para los grupos de tratamiento con un ICS en el estudio IMPACT, que informaba de 317 (8%) casos en CDF de triple terapia, 292 (7%) para la combinación LABA/ICS y 97 (5%) para la combinación LABA/LAMA13. Además, el estudio FULFIL mostraba igualmente un aumento de estos eventos en la población por intención de tratar, con 19 (2%) eventos para la CDF de triple terapia y 7 (<1%) para la combinación LABA/ICS, cuyas diferencias desaparecieron en el estudio de extensión al año11. En la combinación BDP/FOR/GB el ensayo de TRINITY informó 28 (3%) casos de neumonía para la CDF de triple terapia vs 19 (2%) para tiotropio vs 12 (2%) para la triple terapia abierta8. El ensayo TRIBUTE9 detectó 28 (4%) neumonías para la CDF de triple terapia vs 27 (4%) para la CDF de LABA/LAMA. En el momento actual desconocemos los factores que pueden determinar estas diferencias. Es posible que aspectos como la dosis, las características farmacológicas de las moléculas o su administración en distintos dispositivos, así como factores asociados a una susceptibilidad individual, modulen el efecto inmunosupresor de los diferentes ICS en la vía aérea que finalmente influyan en el riesgo de neumonía asociados con ICS. En el futuro se deberán establecer estudios clínicos que permitan identificar al paciente en riesgo de desarrollar esta complicación con cada CDF.
ConclusionesEn resumen, el uso de la CDF de la triple terapia en España presenta algunos retos en su aplicación en la vida real. En los pacientes que ya tienen triple terapia en dispositivos por separado la evidencia científica indica que la eficacia clínica es similar al combinarlo en un solo dispositivo de inhalación. En estos casos es necesario hacer una evaluación a las pocas semanas del cambio para evaluar la respuesta terapéutica al cambio. En los pacientes en los que se escala tratamiento desde una doble terapia a una triple terapia tenemos datos que nos indican los beneficios promedios esperables durante el escalado. A pesar de las reflexiones aquí reflejadas, la comparación entre una doble y una triple terapia muestran mejorías en el contexto clínico de un paciente grave que persiste sintomático y con agudizaciones. Se trata, por tanto, de un paciente especialmente frágil que precisa el mejor tratamiento posible. Es posible que las características farmacológicas de cada CDF puedan influir en los resultados de eficacia o seguridad en los pacientes tratados, lo que debería ser abordado en el futuro. En conclusión, la disponibilidad de esta nueva forma de tratamiento aporta al clínico nuevas herramientas para poder hacer una medicina más simple, eficaz y coste-efectiva en pacientes sintomáticos y con agudizaciones frecuentes. Los trabajos futuros deberán completar los datos de eficacia clínica en otros resultados centrados en el paciente y abordar decididamente la respuesta individualizada a nivel de paciente con objeto de avanzar hacia la medicina personalizada.
Conflicto de interesesJLLC ha recibido honorarios en los últimos tres años por impartir conferencias, asesoría científica, participación en estudios clínicos o redacción de publicaciones para (en orden alfabético): AstraZeneca, Boehringer Ingelheim, Chiesi, CSL Behring, Esteve, Ferrer, Gebro, GlaxoSmithKline, Grifols, Menarini, Novartis, Rovi y Teva.
BAN declara haber recibido honorarios en los últimos tres años por impartir conferencias, asesoría científica, participación en estudios clínicos o fondos para investigación de (en orden alfabético): AstraZeneca, Boehringer Ingelheim, Chiesi, Gebro, GlaxoSmithKline, Laboratorios Ferrer, Laboratorios Menarini, Laboratorios Rovi, Novartis.
LCH ha recibido honorarios en los últimos tres años por impartir conferencias y participación en estudios clínicos para (en orden alfabético): AstraZeneca, Gebro, GlaxoSmithKline, Novartis, Rovi y Vertex.
LRR declara una colaboración con Laboratorios Ferrer.
El resto de los autores no declaran conflicto de intereses.
Este documento ha sido elaborado por los autores a partir de estudios clínicos y de su experiencia profesional, sin influencia de ninguna industria farmacéutica.