La enfermedad renal avanzada suele considerarse una contraindicación absoluta para el trasplante de pulmón, debido a la dificultad de manejo del paciente en el periodo postoperatorio, pero un trasplante combinado de pulmón-riñón podría ofrecer una oportunidad a algunos pacientes seleccionados con disfunción pulmonar y renal. En este trabajo se resume el éxito a largo plazo de un doble trasplante en un paciente varón de 38años con fibrosis quística que presentaba también insuficiencia respiratoria. Tras un periodo postoperatorio complicado, el paciente vive en la actualidad de manera completamente independiente 46meses después de la operación y disfruta de una excelente función pulmonar y renal.
Advanced kidney disease is usually considered an absolute contraindication for lung transplantation due to the difficult management of these patients in the post-operative period. Combined lung-kidney transplantation, however, could offer an opportunity for selected patients with renal and pulmonary dysfunction. This study summarizes the long-term success of a double transplantation in a 38-year-old male patient with cystic fibrosis who presented respiratory and kidney failure. After a complicated post-operative period, the patient currently lives completely independently 46months after the operation and he enjoys excellent pulmonary and renal function.
La International Society for Heart and Lung Transplantation considera que la disfunción grave de órganos principales constituye una contraindicación absoluta para el trasplante de pulmón1. No obstante, esta posibilidad debe contemplarse en algunos casos, puesto que los pacientes con insuficiencia renal presentan a veces otras disfunciones graves y podrían obtener un beneficio con un trasplante combinado de órganos sólidos. Así, el trasplante doble podría estar indicado en algunos pacientes seleccionados, como el del presente caso. Desde hace años se vienen realizando trasplantes combinados de corazón-pulmón y de hígado-pulmón con buenos resultados clínicos2-4, pero se han descrito muy pocos casos clínicos de trasplante combinado de pulmón-riñón (TCPR) en la literatura y, que nosotros sepamos, no hay ninguno que describa esta intervención en pacientes con enfermedad renal terminal en diálisis. Presentamos el primer caso de TCPR realizado con éxito en un paciente en diálisis en España.
Presentación de un casoEl receptor fue un paciente varón de 38 años con fibrosis quística (FQ) que presentaba insuficiencia respiratoria grave y una enfermedad renal terminal. La disfunción renal estaba relacionada con la exposición a largo plazo a aminoglucósidos. Tenía una dependencia de diálisis y había estado en hemodiálisis durante los 3 últimos años. En este paciente, con dependencia de oxígeno, se planteó un trasplante de pulmón en septiembre de 2008 a causa de la hipertensión pulmonar, la frecuencia de infecciones y los múltiples ingresos hospitalarios1.
Los análisis de sangre preoperatorios mostraron los siguientes resultados: hematocrito 29,1%, creatinina 10,1mg/dl, urea 160mg/dl, Na 140mEq/l y K 5,8mEq/l; los resultados de la gasometría arterial fueron los siguientes: pH=7,46, pO2=56mmHg y pCO2=42mmHg. La espirometría puso de manifiesto una enfermedad obstructiva, con una FVC de 2.690cc (50%) y un FEV1 de 1.480cc (30%). En el cultivo de esputo se detectó la presencia de Staphylococcus aureus resistente a la meticilina (SARM), Pseudomonas aeruginosa, Stenotrophomona maltophilia, Aspergillus fumigatus, Candida albicans y Candida tropicalis. La serología de CMV fue negativa. La ecocardiografía mostró una función sistólica normal, hipertensión pulmonar leve (media de PAP de 47mmHg), insuficiencia tricuspídea leve e insuficiencia aórtica mínima. La tomografía torácica puso de manifiesto la presencia de bronquiectasias bilaterales difusas y lesiones alveolares que afectaban principalmente a los lóbulos superiores.
La donante fue una mujer de 41años con antecedentes de hipertensión arterial crónica que sufrió una hemorragia cerebral. Su última gasometría arterial presentó los siguientes valores: PaO2=534mmHg con FiO2=100% y una presión teleespiratoria positiva (PEEP) de 5cmH2O. Los cultivos de aspirados endotraqueales y la serología de CMV dieron resultados negativos. La donante había permanecido 24h en la UCI y la cirugía de explantación se llevó a cabo sin complicaciones. Los pulmones se preservaron en Perfadex® (Vitrolife, Suecia).
Al receptor se le aplicó hemodiálisis inmediatamente antes de la cirugía y a continuación fue ingresado en la UCI con intubación y FiO2=100% y PEEP=10cmH2O. El hematocrito era de 30%, la creatinina de 3,6mg/dl, el Na de 146mEq/l y el K de 5,7mEq/l. Los valores de la gasometría fueron los siguientes: pH=7,35, pO2=295mmHg y pCO2=42mmHg. Se utilizó noradrenalina (0,48μg/kg/min) y óxido nítrico (60ppm) para establecer la hemodinámica durante las 48h siguientes. Se indujo una inmunosupresión con basiliximab y se mantuvo con tacrolimus (niveles en sangre 10ng/ml postoperatoriamente y 7ng/ml a los 6meses), micofenolato mofetilo (1.500mg/12h post-intervención y reducción gradual hasta el nivel de 4μg/ml en el mantenimiento) y prednisona. Los niveles de corticoides fueron de 30mg/día postoperatoriamente y se redujeron gradualmente hasta 15mg/día a los 6meses y 10mg/día después de un año.
Se practicó una toracoesternotomía transversa para un trasplante pulmonar doble secuencial, seguido de un trasplante renal en la fosa ilíaca derecha con la técnica habitual. El tiempo de isquemia fue de 2, de 4 y de 7h para el pulmón izquierdo, el pulmón derecho y el riñón, respectivamente.
El paciente fue extubado 34h después de la intervención. En los aspirados traqueales se detectó SARM, Pseudomonas aeruginosa, Pseudomonas mucoide, Candida albicans, y Candida tropicalis, pero las muestras fueron negativas para CMV. Se inició un tratamiento antibiótico intravenoso (linezolida, voriconazol, trimetoprim-sulfametoxazol y piperacilina/tazobactam) y un tratamiento inhalado (tobramicina y anfotericina en complejo lipídico).
El deterioro progresivo de la función respiratoria, con retención de CO2, motivó una nueva intubación en el día 10 del postoperatorio. Se sospechó un rechazo pulmonar agudo y se administraron corticosteroides durante 3días. El paciente presentó anuria durante el periodo postoperatorio inmediato y necesitó una hemodiálisis veno-venosa continua durante 25días. La ecografía Doppler renal mostró unos vasos sanguíneos permeables. La primera biopsia renal, con un nivel de tacrolimus en suero de 13ng/ml, mostró fibrosis intersticial leve, aterosclerosis leve, necrosis tubular aguda moderada, ausencia de patología glomerular y positividad para CD4 débil en los capilares peritubulares. La función renal se recuperó gradualmente, y el aclaramiento de creatinina fue de 42ml/min 2meses después de la intervención. En el día 50 del postoperatorio, el paciente presentó dolor abdominal asociado a leucocitosis. Se diagnosticó una colecistitis aguda y se le practicó una colecistectomía con lavado peritoneal, después de que una laparotomía de urgencia revelara la presencia de una vesícula biliar gangrenosa perforada, con coleperitonitis asociada.
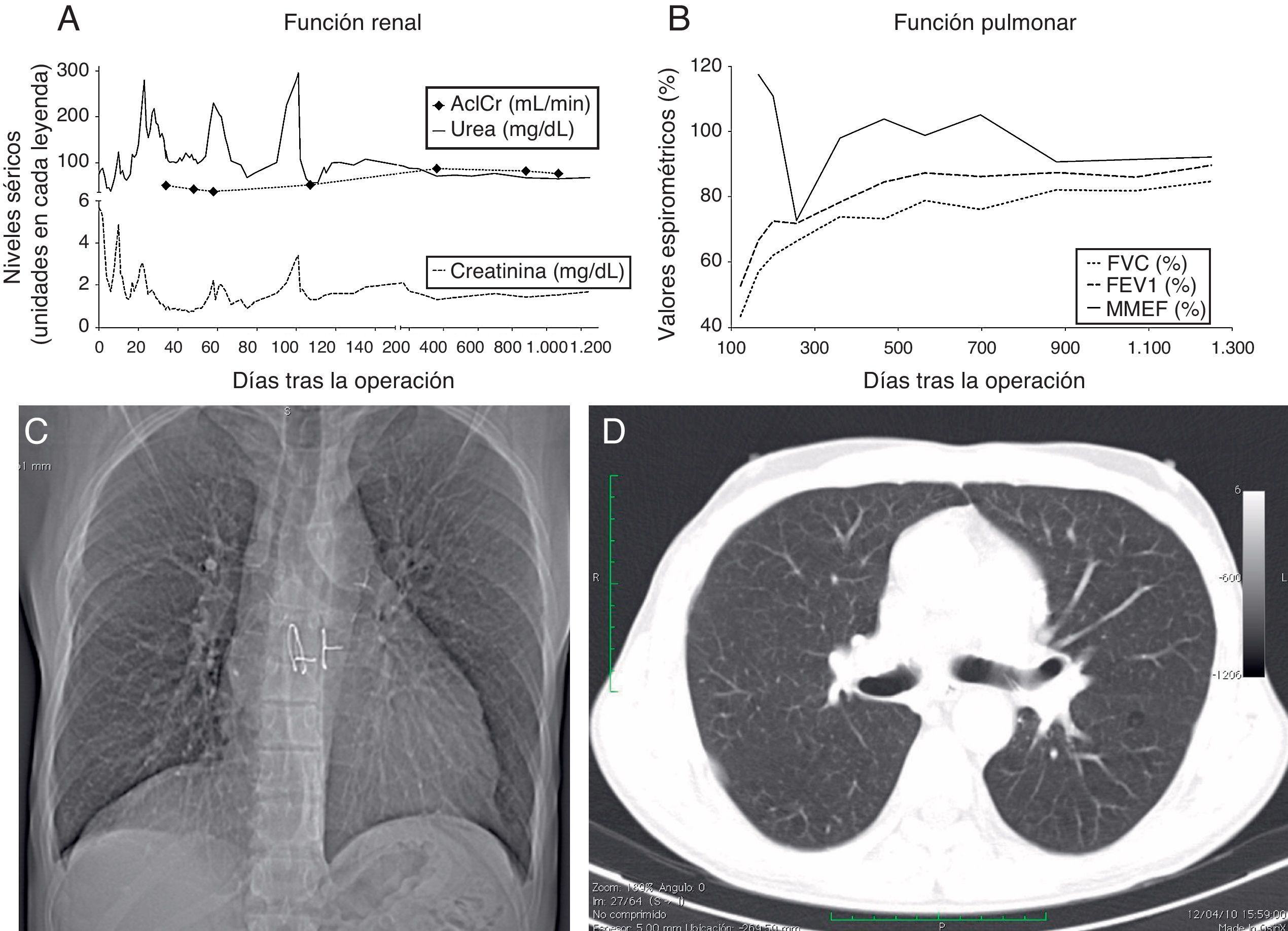
El paciente fue dado de alta 80 días después del trasplante, con una evolución favorable de la espirometría y la función renal (fig. 1A y B).
A los 42 meses del TCPR, el paciente estaba asintomático y llevaba una vida activa. La radiografía de tórax no mostró signos anormales (fig. 1C) y el FEV1 fue de 3.340cc (84,5%). El nivel de creatinina en suero fue de 1,3mg/dl, y el aclaramiento de creatinina, de 86ml/min.
DiscusiónSegún lo indicado en las guías clínicas para el trasplante de pulmón, la FQ es la tercera indicación más frecuente para la realización de trasplantes de pulmón, pero el carácter multisistémico del trastorno plantea dificultades adicionales en la selección de los candidatos1. Es frecuente que esos pacientes presenten una infección crónica por gérmenes resistentes a antibióticos que permanecen en las vías aéreas y los senos después del trasplante; en el contexto de una inmunosupresión, esto constituye un origen de posibles infecciones pulmonares5. Aunque la nefropatía es muy poco frecuente en la FQ, este trastorno muestra algunas anomalías de la función renal, y en el tratamiento de la FQ y las infecciones se utilizan diversos fármacos que pueden ser nefrotóxicos, como los aminoglucósidos6,7.
El primer caso de doble trasplante de pulmón-riñón se publicó en 1998 en un paciente con linfangioleiomiomatosis pulmonar y angiolipomas renales tras una nefrectomía unilateral. Ese paciente presentó un aclaramiento de creatinina aceptable, con lo que pudo evitarse un posible deterioro postoperatorio de la función renal2. Posteriormente no se han publicado casos similares, y aunque la base de datos de la International Society of Heart and Lung Transplantation incluye algunos casos de pacientes tratados con un trasplante combinado de un solo pulmón-riñón, no hay datos sobre su función renal preoperatoria ni sobre la supervivencia postoperatoria.
El trasplante simultáneo de órganos sólidos ha sido más frecuente en los últimos años, y en revisiones del trasplante combinado de hígado-riñón3 y del trasplante combinado de corazón-riñón8 se ha intentado analizar las indicaciones, consideraciones técnicas y resultados esperados. Rana et al.9 publicaron recientemente la descripción de un trasplante combinado simultáneo de corazón-pulmón-riñón con resultados satisfactorios, y resaltaron los resultados de un estudio previo, en el que el trasplante simultáneo de múltiples órganos procedentes del mismo donante mostró unas tasas de rechazo inferiores a las del trasplante de un solo órgano.
El TCPR es una intervención quirúrgicamente viable en la actualidad, pero el manejo postoperatorio del paciente puede resultar difícil, dado que el control estricto del volumen de líquidos que es necesario para evitar el edema pulmonar debe equilibrarse con la necesidad de una ingestión abundante de líquidos para la función renal. Además, el tratamiento inmunosupresor para el trasplante de pulmón debe optimizarse para reducir los efectos nefrotóxicos, en especial cuando se emplean fármacos anticalcineurina10. En nuestro caso, la dosis necesaria de fármacos anticalcineurina se redujo mediante el empleo de basiliximab para la inducción y de tacrolimus/micofenolato en vez de ciclosporina/azatioprina para el mantenimiento.
En conclusión, el TCPR podría estar indicado en pacientes candidatos a un trasplante de pulmón con una enfermedad renal terminal concomitante. Esta intervención es viable quirúrgicamente, pero el manejo perioperatorio del paciente es complejo. Para obtener buenos resultados, el TCPR solamente debe llevarse a cabo en centros especialmente preparados y con una selección adecuada de donantes y receptores.
Conflicto de interesesLos autores no tienen conflictos de intereses.