Los carcinoides tímicos son una entidad poco frecuente que puede asociarse a enfermedades endocrinológicas como el síndrome de Cushing o el síndrome de neoplasia endocrina múltiple tipo I (MEN1). Suponen el 4% de los tumores del mediastino anterior y se caracterizan por tener un comportamiento muy agresivo.
Presentamos el caso de un paciente diagnosticado de síndrome MEN1 a quien durante el seguimiento de su enfermedad se detectó una imagen torácica compatible con carcinoide tímico. Tras intervenirle quirúrgicamente mediante timectomía ampliada a grasa peritímica, se confirmó el diagnóstico clínico. A los 14 meses de seguimiento se halló en las pruebas de imagen una lesión sospechosa de recidiva local, motivo por el que fue reintervenido. El informe anatomopatológico de dicha intervención fue de fibrosis rádica.
Así mismo, presentamos una revisión del manejo diagnóstico y terapéutico actual en pacientes con síndrome MEN1 diagnosticados de carcinoide tímico.
Thymic carcinoids are a rare entity that may be associated with endocrine diseases like Cushing's syndrome or multiple endocrine neoplasia syndrome type I (MEN1). These tumors represent 4% of anterior mediastinal tumors and are characterized by their very aggressive behavior.
We present the case of a patient with a previous MEN 1 diagnosis in whom, during the follow up of his disease, a thoracic image compatible with thymic carcinoid was detected. After an extended thymectomy that included peri-thymic fat resection, the clinical diagnosis was confirmed. A follow up examination 14 months later revealed a suspicious lesion that suggested local recurrence, therefore the patient was reoperated on. The pathology report of this surgery indicated post-radiation fibrosis.
Likewise, we present a review of the current diagnostic and therapeutic management of patients with MEN1 syndrome who are diagnosed with thymic carcinoid.
Los carcinoides tímicos fueron descritos por primera vez por Rosai e Higa en 1972 como entidad independiente a los carcinomas tímicos1. Son tumores neuroendocrinos derivados de las células APUD del timo. Suponen el 4% de los tumores del mediastino anterior, teniendo predilección por hombres entre la cuarta y la sexta décadas de la vida2. Clínicamente pueden ser desde asintomáticos hasta dar clínica de dolor o por compresión, pudiendo ir asociados a síndromes como el de Cushing hasta en el 40% o a la neoplasia endocrina múltiple tipo 1 (MEN1) hasta el 25% de los casos, entre otros3-5. Se caracteriza por tener un comportamiento muy agresivo, presentando con frecuencia invasión local al diagnóstico. En cuanto a la invasión ganglionar y metastásica a distancia, puede observarse en el 50 y el 20% de los casos, respectivamente6.
Observación clínicaPresentamos el caso de un paciente varón de 43 años con antecedentes personales de síndrome MEN 1 con adenoma hipofisario gigante intervenido en 2 ocasiones y radioterapia adyuvante, hiperparatiroidismo primario que precisó paratiroidectomía total con autotransplante en antebrazo izquierdo con resultado anatomopatológico de hiperplasia y un área de adenoma, así como un gastrinoma en tratamiento con análogos de somatostatina. Secundario a este último, presentó un ulcus perforado a vía biliar que requirió gastrectomía Billroth II. En una gammagrafía con octreótido de seguimiento por su gastrinoma, en marzo de 2006, se objetivó de forma casual una captación patológica en mediastino anterior, motivo por el cual se remite a cirugía torácica para valorar tratamiento ante la sospecha de un segundo tumor primario.
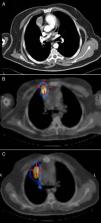
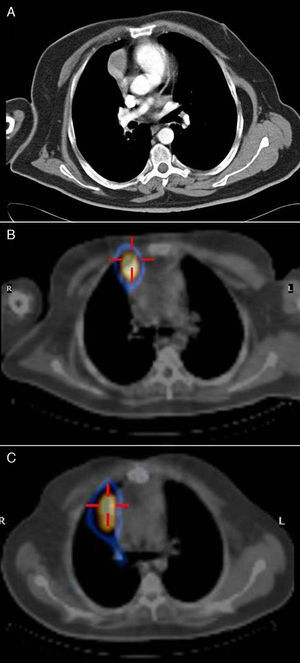
A la exploración física se presentaba asintomático. Los valores analíticos a destacar fueron: prolactina, 139ng/ml; testosterona total, 1,16ng/ml; testosterona libre, 3,41pg/ml; PTH, 2.112pg/ml; gastrina, >1.050pg/ml; calcio, 11,2mg/dl; fósforo, 2,82mg/dl. En la tomografía axial computarizada (TAC) se observaba una masa de 3cm de diámetro, sólida y con captación de contraste intravenoso, en el mediastino anterior en contacto con la pleura y el pericardio derecho junto a la aurícula homolateral, sin calcificación ni cavitación (fig. 1A). En la gammagrafía con octreótido que lo detectó se podían apreciar 2 lesiones nodulares con elevada densidad de receptores de somatostatina, una en hemitórax derecho y una segunda en la cola del páncreas. Se le realizó un SPECT-TC que confirmó la localización de ambas lesiones (fig. 1B).
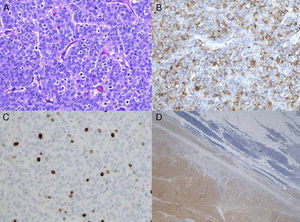
En agosto de 2006 se intervino, realizándosele una timectomía ampliada mediante esternotomía media. Se apreció un tumor tímico dependiente de lóbulo derecho de 5cm diámetro que no infiltraba estructuras mediastínicas. Se efectuó timectomía total ampliada a pleura mediastínica derecha. El estudio anatomopatológico diagnosticó un carcinoide tímico (fig. 2A-D), estadificándose en un grado II de la clasificación de Masaoka y pT1N0M0, estadio I. El postoperatorio transcurrió sin incidencias, dándose de alta al cuarto día postoperatorio. En octubre de 2006 inició radioterapia adyuvante mediastínica con dosis de 56Gy sin complicaciones.
Durante el seguimiento en consultas externas, se objetivó en el SPECT-TAC de octubre de 2007 un incremento de captación paramediastínica derecha (fig. 1C). La TAC confirmó la presencia de una consolidación de mediastino anterior con morfología seudonodular en contacto con la pleura y el pericardio derecho, próxima a la aurícula ipsilateral. En febrero de 2008 el paciente fue reintervenido mediante una toracotomía derecha sin visualizarse ni palparse ninguna nodulación, por lo que se resecó una parte de pericardio y área de fibrosis en la teórica localización sugerida por la captación de la gammagrafía. La anatomía patológica no evidenció neoplasia alguna, y el diagnóstico fue de fibrosis rádica. Actualmente el paciente se encuentra libre de enfermedad y sigue los controles oncológicos oportunos mediante la realización de TAC anual.
En enero de 2010, el hermano del paciente fue diagnosticado del mismo síndrome a partir de un hiperparatiroidismo. En el momento de realizarse la pertinente paratiroidectomía, le fue practicada una timectomía profiláctica.
DiscusiónEn todo paciente diagnosticado de un síndrome MEN 1 es importante descartar la presencia de un carcinoide tímico, debido a que hasta en el 25% de los casos pueden asociarse ambas entidades. Se han propuesto para el cribado y seguimiento de estos pacientes la realización de una radiografía de tórax anual y una TAC torácica cada 3 años7,8.
El diagnóstico de los carcinoides tímicos debe basarse en la TAC torácica, debiendo ampliarse a hemiadomen superior para descartar la existencia de una posible afectación secundaria. Típicamente se presentan como masas irregulares que pueden contener calcificaciones y se realzan de forma importante con el contraste intravenoso9,10. Durante su progresión pueden mostrar signos de invasión local, y la pleura, el pericardio y el parénquima pulmonar son las estructuras con más frecuencia comprometidas. La gammagrafía con octreótido es una prueba más específica, que además puede ayudar a detectar metástasis a distancia y servir como método de seguimiento en el caso de demostrarse positiva en el estudio preoperatorio11.
Otras pruebas con las que existe menos experiencia son la resonancia nuclear magnética (RNM), útil sobre todo para la valoración de invasión locorregional de estructuras mediastínicas, la tomografía computarizada por emisión de fotones individuales (SPECT) y la tomografía por emisión de positrones (PET)11. Aunque la experiencia con PET en los carcinoides tímicos es limitada, parece ya demostrada su utilidad para el caso de timomas invasivos y carcinomas tímicos, lo cual en teoría apoyaría su uso en la evaluación de un tumor tan agresivo como es el carcinoide tímico12. Se están estudiando nuevos trazadores que diagnostiquen con mayor exactitud tumores carcinoides, en especial carcinoides tímicos13.
El tratamiento de elección, cuando es posible, es la cirugía, y la técnica de elección es la exéresis en bloque del timo con las estructuras adyacentes que comprometa14. Puede asociarse con quimioterapia y/o radioterapia bien de forma neoadyuvante o adyuvante, aunque aún está por establecer cuál es el mejor esquema de tratamiento, dado que los estudios existentes están hechos a partir de series con pocos pacientes. En relación a la radioterapia, se han publicado trabajos que reflejan la utilidad de esta en la prevención de la recidiva6,14-16. Así mismo, es probable que la quimioterapia deba considerarse de forma sistemática debido a la alta tasa de metástasis a distancia, hasta un 20%3. Otra opción terapéutica es la hormonoterapia con octreótido, dada su buena actividad antiproliferativa en tumores neuroendocrinos incluso en caso de pacientes con metástasis a distancia17. Para ello, es recomendable determinar el estado de receptores de somatostatina mediante la gammagrafía con octreótido18. Se ha publicado algún caso con tratamiento multidisciplinario con quimiorradioterapia de inducción, cirugía y hormonoterapia adyuvante con éxito3.
En nuestro caso, al no tener un diagnóstico histológico preoperatorio de la lesión, se sometió al paciente directamente a la timectomía en bloque con pleura mediastínica. Como tratamiento adyuvante se optó por radioterapia y análogos de la somatostatina, encontrándose el paciente libre de enfermedad después de 52 meses de seguimiento.
En cuanto a los factores relacionados con una mayor recidiva, los referidos con más frecuencia son la resección incompleta y un estadio avanzado19. La supervivencia en la serie de Gal et al. varió en función de la resecabilidad, y para pacientes con resección completa es a los 5 años del 77% y a los 10 años del 30%; para los resecados parcialmente, la supervivencia a los 5 y 10 años es del 65 y del 19%, respectivamente; y para los no resecados, del 28 y del 0%, respectivamente19. Moran confirmó dichos resultados con una supervivencia a los 5 y 10 años del 28 y del 10%, respectivamente2. Otro de los factores pronósticos implicados ha sido el grado de diferenciación tumoral, de tal modo que para tumores de bajo grado, la mediana de supervivencia varía de 9 a 11 años; para los de grado intermedio oscila entre 5 y 7 años, mientras que para los de alto grado la mediana de supervivencia varía de 18 meses a 3 años2,19.
En relación a las medidas preventivas, se contempla la opción de realizar una timectomía profiláctica simultánea la paratiroidectomía total o subtotal20. De este modo se disminuye el riesgo de recidiva del hiperparatiroidismo como consecuencia de glándulas supernumerarias ectópicas, así como el riesgo de desarrollar un carcinoide tímico asociado a dicho cuadro.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.