El objetivo de este estudio es evaluar la reactividad traqueal tras la implantación de distintos stents metálicos autoexpandibles (SMAE).
Material y métodosSe utilizaron 40 conejos hembra de raza neozelandesa, que se dividieron en 4 grupos. En 3 grupos se implantaron SMAE: de acero (SA), de nitinol (NiTi) o stents liberadores de nitinol (SLF). El cuarto grupo fue el grupo de control (sin stent).
Los stents se implantaron por vía percutánea bajo control fluoroscópico. Los animales se evaluaron mediante tomografía axial computarizada (TAC) multicorte y las tráqueas se extirparon para su estudio anatomopatológico (EAP). Los datos de la TAC y el EAP se analizaron estadísticamente y se correlacionaron.
ResultadosEl grupo que recibió SLF presentaba la mayor longitud de estenosis (20,51±14,08mm frente a 5,84±12,43 y 6,57±6,54mm en los grupos NiTi y SA, día 30; p<0,05) y el mayor índice de formación de granulomas evidenciados mediante TAC (50% de los casos). El grupo al que se implantaron stents NiTi mostró el menor grado de estenosis (2,86±6,91% frente a 11,28±13,98 y 15,54±25,95% en los grupos SLF y SA; p<0,05).
En el estudio AP, el grupo SA presentó reactividad proliferativa intensa en comparación con los otros 2 grupos. En el grupo SLF se observó una respuesta destructiva en el 70% de animales, mientras que el stent NiTi fue el que menos reacción provocó.
La TAC resultó ser superior para detectar el engrosamiento (correlación positiva de un 68,9%; p < 0,001) que para la observación de granulomas (n.s.).
ConclusionesEl grupo SA desarrolló granulomas y estenosis significativas. El stent NiTi fue el que menos reacción indujo, mientras que el SLN provocó lesiones importantes que podrían estar relacionadas con la dosis de fármaco. Por consiguiente, este tipo de SLF no se recomienda para el tratamiento de la estenosis traqueobronquial.
The objective of this study was to assess tracheal reactivity after the deployment of different self-expandable metal stents (SEMS).
Material and methodsForty female New Zealand rabbits were divided into four groups. Three groups received three different SEMS: steel (ST), nitinol (NiTi), or nitinol drug-eluting stent (DES); the fourth group was the control group (no stent).
Stents were deployed percutaneously under fluoroscopic guidance. Animals were assessed by multi-slice, computed tomography (CT) scans, and tracheas were collected for anatomical pathology (AP) study. Data from CT and AP were statistically analyzed and correlated.
ResultsThe DES group had the longest stenosis (20.51±14.08mm vs. 5.84±12.43 and 6.57±6.54mm in NiTi and ST, respectively, day 30; P<.05), and higher granuloma formation on CT (50% of cases). The NiTi group showed the lowest grade of stenosis (2.86±6.91% vs. 11.28±13.98 and 15.54±25.95% in DES and ST, respectively; P<.05).
The AP study revealed that the ST group developed intense proliferative reactivity compared to the other groups. In the DES group, a destructive response was observed in 70% of the animals, while the NiTi was the least reactive stent.
CT was more effective in detecting wall thickening (positive correlation of 68.9%; P<.001) than granuloma (not significant).
ConclusionsThe ST group developed granulomas and significant stenosis. NiTi was the least reactive stent, while DES caused significant lesions that may be related to drug dosage. This type of DES stent is therefore not recommended for the treatment of tracheobronchial stenosis.
Aunque la exéresis quirúrgica es el principal procedimiento utilizado para el tratamiento de la estenosis traqueobronquial1, la colocación de stents traqueales constituye un tratamiento satisfactorio para la obstrucción de las vías aéreas superiores en pacientes no quirúrgicos, junto con otras técnicas mínimamente invasivas como la radiofrecuencia, la ablación con láser y la crioterapia2. Las prótesis de silicona son las más utilizadas, pero su implantación requiere el uso de un broncoscopio rígido y anestesia general. Por el contrario, los stents metálicos se pueden implantar mediante fluoroscopia o a través de un fibrobroncoscopio flexible o un tubo endotraqueal bajo una sedación ligera y proporcionan un alivio sintomático inmediato3. Otras ventajas de los stents metálicos respecto a los de silicona son que tienen mayor fuerza radial y mejor relación entre los diámetros interno y externo, que presentan menor incidencia de migración y menor riesgo de obstrucción por mucosidad y de colonización bacteriana4. No obstante, estas importantes ventajas se han visto empañadas por sus complicaciones a largo plazo (como la reestenosis debida a la formación de granulomas o al desarrollo de tumores) y las dificultades para su extracción5. Estos problemas dieron lugar a que, en 2005, la Administración de Alimentos y Medicamentos de Estados Unidos (Food and Drug Administration [FDA]) advirtiera del peligro del uso de stents metálicos en las lesiones benignas6.
A pesar de ello, desde 2005 se han publicado estudios que indican que los stents metálicos son seguros para el tratamiento de la estenosis traqueobronquial, tanto benigna como maligna6–9. La reestenosis, provocada por un sobrecrecimiento en el interior de la luz, se ha descrito principalmente con los stents de acero10. Los estudios realizados con stents de nitinol autoexpandibles cortados con láser han mostrado mejores resultados. Sin embargo, los stents de nitinol se emplean mayoritariamente en otros territorios, como en indicaciones cardiovasculares y de la vía biliar. En las indicaciones cardiovasculares se utilizan fármacos antiproliferativos para evitar la reestenosis11,12, pero hay poca experiencia de utilización en las vías aéreas.
Planteamos la hipótesis de que los stents liberadores de nitinol podían combinar las ventajas de los stents metálicos para el manejo de la estenosis traqueal, al tiempo que evitarían o atenuarían la posibilidad de reestenosis debida al sobrecrecimiento intraluminal a través de la propia malla y en los extremos del stent. En consecuencia, el propósito de este estudio fue evaluar las respuestas traqueales a 3 stents metálicos autoexpandibles (SMAE) distintos (stent liberador de nitinol [SLF], stent de nitinol [NiTi] y stent de acero inoxidable [SA] no recubierto) en un modelo animal.
MétodosAnimales y stentsEn este estudio se utilizaron 40 conejos neozelandeses hembra adultos (3,95±0,48kg). Los cuidados y el uso de los animales cumplieron la Directiva del Consejo de las Comunidades Europeas (86/609/EEC) y las leyes, recomendaciones y normativas de protección de animales de España; el estudio fue aprobado por el Comité Ético de la Universidad de Zaragoza. Los animales se distribuyeron aleatoriamente en 4 grupos: SA (n=10), stent de acero (Wallstent™, Boston Scientific, Natick, MA, EE.UU.); NiTi (n=10), stent de nitinol (Zilver®Flex™ Vascular Stent, Cook Medical, Bjaeverskov, Dinamarca); SLF (n= 0), stent de nitinol liberador de paclitaxel (Zilver®PTX® Drug Eluting Peripheral Stent, Cook Medical, Bjaeverskov, Dinamarca) y un grupo de control (n=10) al que no se aplicó ningún stent. Los 2 tipos de stents de nitinol están cortados con láser y comparten exactamente el mismo tipo de diseño, mientras que el stent de acero está constituido por una malla trenzada. Todos los stents eran autoexpandibles y medían 8×40mm, con una relación 1:1 respecto a la tráquea del modelo animal. Los stents se liberaron por vía percutánea bajo anestesia general y con orientación fluoroscópica. El seguimiento de los animales fue de 90días.
Técnica de implantación del stentAntes de la implantación, todos los conejos fueron examinados para comprobar su estado de salud y se mantuvieron en ayunas durante 8h. Se les administró medicación por vía intramuscular: 0,5mg/kg de medetomidina (Sedator®, Eurovet Animal Health, Holanda) y 25mg/kg de ketamina (Imalgene 1000®, Merial, Barcelona, España). La anestesia se mantuvo con isoflurano inhalado al 1-2% (Isovet, Braun, Barcelona, España). Durante el procedimiento se monitorizó a los animales (equipo de anestesia Samurai, La Bouvet, Madrid, España, y monitor Dash 3000, General Electric Company, Helsinki, Finlandia).
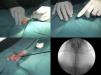
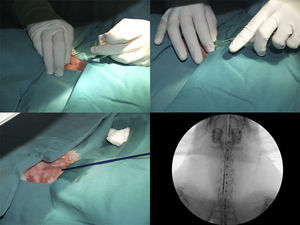
Se colocó al animal en decúbito supino y con el cuello en hiperextensión y se le administraron 50mg/kg de oxitetraciclina (Terramicina LA, Pfizer, Madrid, España). A continuación se introdujo en el esófago un catéter recto de 5F (Aurous®, Cook Medical, Bjaeverskov, Dinamarca) como referencia de medición. El acceso a la tráquea se llevó a cabo puncionando entre los 2 primeros anillos traqueales con una aguja 18G ensamblada a un catéter (Introcan®, Braun, Alemania); seguidamente se administraron 0,15ml de lidocaína (Braun, Barcelona, España) en la tráquea. Se hizo avanzar hacia el interior de la tráquea una guía hidrofílica de 0,035pulgadas (Radifocus® Guide Wire M Standard type, Terumo, Leuven, Bélgica) empapada en lidocaína y se extrajo el catéter. El sistema de liberación del stent se insertó directamente sobre la guía y se colocó en la posición definida (en la marca distal del stent, 1cm por encima de la carina traqueal), donde se liberó el stent bajo control fluoroscópico (C-arm system BV Endura, Philips, Eindhoven, Holanda). Una vez colocado el stent, se retiraron el sistema de liberación, la guía y el catéter, supervisándose al animal hasta su recuperación (fig. 1).
En el grupo de control todos los procedimientos se efectuaron del mismo modo, utilizando un sistema de liberación para stent que no contenía stent.
Seguimiento y estudio mediante tomografía axial computarizadaTras la colocación del stent, se supervisó a todos los animales para detectar posibles signos de obstrucción de las vías aéreas o de infección de la herida quirúrgica. Se evaluó el estado general de salud de los animales por medio de exámenes clínicos diarios.
En los casos en los que el animal murió antes de finalizar el estudio, se obtuvieron muestras y se procesaron inmediatamente de acuerdo con el protocolo. La única prueba que no fue posible realizar en caso de muerte fue la tomografía axial computarizada (TAC).
Los estudios traqueales con TAC se realizaron, bajo sedación, 30 y 90días después de la implantación del stent (Phillips Brilliance CT 16-slice, Holanda). Se utilizó un grosor de corte de 1mm, 0,5mm de separación entre cortes y un paso (pitch) de 0,69, y se obtuvieron reconstrucciones tridimensionales.
Los parámetros que se evaluaron mediante TAC fueron: la estenosis máxima de la luz traqueal en la proyección axial (%), la longitud de la estenosis en la proyección sagital (mm) y la detección de imágenes compatibles con granulomas (presentes o ausentes).
También se calculó una puntuación del grado de estenosis, según se describe en la tabla 1, con el fin de evaluar mejor la tráquea en su totalidad. Para simplificar la interpretación de la TAC se definieron 5 segmentos traqueales (P: tejido inmediatamente craneal respecto al extremo proximal del stent; 0: extremo proximal del stent; 2: segmento central del stent; 4: extremo distal del stent, y D: tejido inmediatamente caudal respecto al extremo distal del stent).
Puntuaciones de los estudios con tomografía axial computarizada (TAC) y anatomopatológico (AP)
| Estudio | Parámetro | Puntuación | La puntuación total es la suma de los valores de los 5 segmentos (P, 0, 2, 4, D) |
|---|---|---|---|
| TAC | Porcentaje de estenosis | 0: 0%1: 1-20%2: 21-40%3: 41-60%4: 61-80%5: >80% | Valor mínimo=0Valor máximo=25 |
| AP | Engrosamiento del epitelio | 0: Normal <50μm1: Leve: 50-100μm2: Moderado: 100-150μm3: Severo: >150μm | Valor mínimo=0Valor máximo=15 |
| AP | Engrosamiento subepitelial | 0: Normal ≤400μm1: Leve: 400-600μm2: Moderado: 600-800μm3: Severo:>800μm | Valor mínimo=0Valor máximo=15 |
| AP | Formación de granulomas | 0: Ausente1: Un granuloma2: Más de un granuloma | Valor mínimo=0Valor máximo=10 |
P, 0, 2, 4 D: segmentos traqueales evaluados (P, tejido inmediatamente craneal respecto al extremo proximal del stent; 0, extremo proximal del stent; 2, parte central del stent; 4, extremo distal del stent; D, tejido inmediatamente caudal respecto al extremo distal del stent).
Dos radiólogos experimentados revisaron de forma enmascarada los estudios con TAC y asignaron las puntuaciones de manera independiente en cada uno de los casos. En caso de discrepancia, se consultó a un tercer observador.
Estudio anatomopatológicoLos animales fueron sacrificados el día 90 con una inyección intravenosa de pentobarbital sódico (Dolethal®, Vétoquinol, Francia), momento en que se obtuvieron las muestras de tráquea para los estudios anatomopatológicos (AP).
La tráquea entera se fijó en formaldehído al 10%. La parte que contenía el stent metálico se incrustó en metil metacrilato; se efectuaron cortes con un micrótomo con banda de sierra y recubrimiento de diamante (EXAKT 310 CS/CP, Norderstedt, Alemania) y se pulieron para obtener cortes de 8μm de grosor (EXAKT 400CS Norderstedt, Alemania). Los segmentos inmediatamente craneal y caudal respecto al stent, y la totalidad de la tráquea en el caso de los animales del grupo de control, se incrustaron en parafina y se realizaron cortes de 3-5μm de grosor (Leica Reichert-Jung BIOCUT 2030 Microtome, Wetzlar, Alemania). Las muestras se tiñeron con hematoxilina-eosina y se examinaron con un microscopio óptico (Nikon Eclipse 80i, Nikon Instruments Europe).
En el estudio histológico se utilizaron los mismos 5 segmentos traqueales (P, 0, 2, 4 y D) definidos para el estudio mediante TAC. Los parámetros histológicos estudiados fueron: grosor epitelial y subepitelial, modificación del epitelio respiratorio, metaplasia escamosa, formación de granulomas, inflamación y vascularización. Algunos de ellos se puntuaron según la tabla 1.
Análisis estadísticoTodo el procesamiento de datos y análisis estadísticos se realizaron con el programa SPSS Statistics 17.0 para Windows. Se estableció un error α de 0,05. Las variables cualitativas se expresaron mediante frecuencias, mientras que las cuantitativas se describieron mediante la media±desviación estándar. Las variables cuantitativas se compararon por medio de la prueba de la Razón de Verosimilitud.
Antes de efectuar comparaciones, se comprobó la normalidad de las variables cuantitativas utilizando la prueba de Kolmogorov-Smirnov. Si los datos presentaban una distribución normal, se aplicó la prueba de t de Student para muestras independientes (2 medias) o el análisis de la varianza, ANOVA (más de 2 medias). En las distribuciones no normales se empleó la prueba de la U de Mann-Whitney o la de Kruskal-Wallis. Para las variables ordinales se utilizó la prueba de Wilcoxon.
Las correlaciones se evaluaron por medio del coeficiente de correlación de Spearman (ρ) y los correspondientes coeficientes de determinación (ρ2).
ResultadosEl éxito técnico de la implantación fue del 100%. No hubo muertes inmediatas ni complicaciones importantes debidas al procedimiento.
Aunque la mayoría de animales fueron sacrificados el día 90, 8 animales (80%) del grupo SA fallecieron (media: 31,4días postintervención), al igual que 2 animales (20%) del grupo NiTi (media: 39,5días) y 4 animales (40%) del grupo SLF (media: 14,5días). Todas las muertes se debieron a causas relacionadas con el stent, tales como estenosis o infecciones.
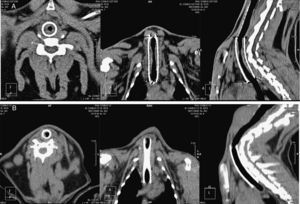
Estudio con tomografía axial computarizadaGrado de estenosisEn la tabla 2 se presentan la estenosis traqueal máxima (%) y su localización en los días 30 y 90. En el grupo de stent de acero, la estenosis traqueal máxima se localizó en el extremo proximal, mientras que en el grupo nitinol el segmento más afectado fue el central (fig. 2). En la tabla 3 se resumen las puntuaciones de estenosis en cada uno de los grupos. Los grupos SA y SLF obtuvieron puntuaciones más altas en ambos días, aunque no estadísticamente significativas.
Evaluación de la estenosis en el estudio con tomografía axial computarizada (TAC)
| Estenosis traqueal máxima (%) y su localización (días 30 y 90) | ||||
|---|---|---|---|---|
| Grupo | Día 30 | Día 90 | ||
| Media±DE | Segmento | Media±DE | Segmento | |
| Control | 0,00±0,00 | - | 0,00±0,00 | - |
| SA | 15,54±25,95 | P | 13,63±19,28 | 0 |
| NiTi | 2,86±6,91 | 2 | 3,45±5,14 | 2 |
| SLF | 11,28±13,98 | 2 | 16,88±13,82 | 2 |
| Longitud de la estenosis (mm) en los escáneres de TAC (días 30 y 90) | ||||||||
|---|---|---|---|---|---|---|---|---|
| Grupo | Día 30 | Día 90 | ||||||
| n | Media±DE | min | max | n | Media±DE | min | max | |
| SA | 6 | 6,57±6,54a | 0,0 | 16,5 | 2 | 14,55±12,52a | 5,7 | 23,4 |
| NiTi | 8 | 5,84±12,43a | 0,0 | 36,0 | 8 | 8,19±11,64a | 0,0 | 34,7 |
| SLF | 8 | 20,51±14,08b | 0,0 | 39,2 | 6 | 21,62±3,94a | 16,0 | 28,2 |
| pa | 0,043 | 0,065 | ||||||
NiTi: grupo de stent de nitinol; P: tejido inmediatamente craneal respecto al extremo proximal del stent; SA: grupo de stent de acero; SLF: grupo de stent de nitinol liberador de fármaco; 0: extremo proximal del stent; 2: parte central del stent.
Estenosis de la luz traqueal (puntuaciones, máxima=25)
| Día 30 | Día 90 | ||||
|---|---|---|---|---|---|
| n | Media±DE | n | Media±DE | p* | |
| Control | 10 | 0,00±0,00a | 9 | 0,00±0,00a | > 0,999 |
| SA | 6 | 3,00±3,22c | 2 | 2,50±2,12b | 0,180 |
| NiTi | 8 | 0,63±1,06ab | 8 | 1,00±1,07a | 0,180 |
| SLF | 8 | 2,38±1,92bc | 6 | 2,83±1,33b | 0,357 |
| p** | 0,006 | < 0,001 | |||
Los valores con el mismo superíndice indican diferencias estadísticas entre ellos, según el test de la U Mann-Whitney.
Treinta días después de la implantación, el grupo SLF presentó estenosis significativamente más largas que las de los otros 2 grupos. La longitud de la estenosis aumentó el día 90 en todos los grupos, pero en los grupos SA y NiTi su longitud se incrementó más que en el grupo SLF (tabla 2). No hubo diferencias estadísticamente significativas entre grupos el día 90, ni entre los días 30 y 90 dentro de un mismo grupo.
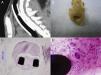
Formación de granulomasTodos los grupos parecieron presentar granulomas, que se localizaron en los segmentos 0 y/o 2 (fig. 3). Las mayores intensidades de estas sospechas de granuloma se observaron en los escáneres del grupo SLF. El porcentaje de casos con granulomas obvios en el grupo SLF fue estadísticamente significativo en el segmento 2 el día 30 (50%, p=0,010) y en el segmento 0 el día 90 (50%, p=0,018). En los otros grupos no hubo diferencias estadísticamente significativas.
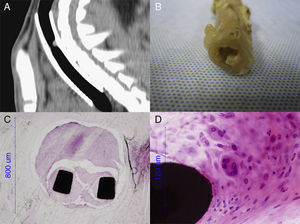
Imágenes de una sospecha de granuloma. A) Imagen de TAC, proyección sagital con aspecto de granuloma. B) Visión macroscópica de un granuloma. C) Visión microscópica (10 aumentos) de un granuloma alrededor de la estructura del stent. D) Visión microscópica (60 aumentos) de una célula gigante.
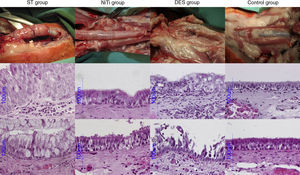
En la tabla 4 se resumen todas las puntuaciones AP, y en la figura 4 se presentan las imágenes AP.
Evaluaciones de los parámetros histológicos (puntuaciones)
| Engrosamiento del epitelio (máximo=15) | n | Media±DE | min | max |
| Control | 10 | 0,00±0,00a | 0 | 0 |
| SA | 10 | 5,50±1,77b | 3 | 8 |
| NiTi | 10 | 2,13±2,75c | 0 | 8 |
| SLF | 10 | 3,67±1,21c | 2 | 5 |
| pa | < 0,001 | |||
| Engrosamiento subepitelial (máximo=15) | ||||
| Control | 10 | 0,10±0,32a | 0 | 1 |
| SA | 10 | 7,56±2,7b | 4 | 11 |
| NiTi | 10 | 2,38±2,83ac | 0 | 7 |
| SLF | 10 | 4,00±3,74c | 0 | 12 |
| pa | < 0,001 | |||
| Formación de granulomas (máximo=10) | ||||
| Control | 10 | 0,00±0,00a | 0 | 0 |
| SA | 10 | 1,11±0,78b | 0 | 2 |
| NiTi | 10 | 0,25±0,70a | 0 | 2 |
| SLF | 10 | 0,30±0,67a | 0 | 2 |
| pa | < 0,001 | |||
Los valores con el mismo superíndice indican ausencia de diferencias estadísticamente significativas entre ellos, según el test de la U Mann-Whitney para valores pareados.
El resultado AP del grupo SA en su conjunto se caracterizó por un engrosamiento de la pared traqueal y una significativa neovascularización. Se observó un aumento de células caliciformes y una menor cantidad de células ciliadas. El porcentaje de casos de metaplasia escamosa a lo largo de la tráquea fue estadísticamente más elevado en este grupo (p<0,001). La formación de granulomas, observados principalmente en los extremos del stent, también fue estadísticamente mayor en este grupo (44,4% de los casos). De hecho, este fue el único grupo en que se evidenció más de un granuloma en un mismo segmento (11,1% de los casos). En este grupo también se observó inflamación aguda y crónica, pero solamente la puntuación de inflamación aguda fue estadísticamente mayor respecto a los otros grupos (p<0,001). La frecuencia de formación de neovasos también fue estadísticamente mayor en el grupo SA (entre el 22,2 y el 55,6% de los casos; p<0,001), en comparación con los otros grupos.
Grupo stents de nitinolEl stent de nitinol provocó menos casos de engrosamiento epitelial y subepitelial, aparentemente leve y moderado pero no grave. Las proporciones de células caliciformes y ciliadas se mantuvieron en la mayoría de casos, y cuando se detectaron alteraciones, la desproporción fue leve, localizándose principalmente en los extremos del stent. En un 25% de los casos observamos metaplasia escamosa en el segmento 4, aunque no fue estadísticamente significativa. En este grupo se detectaron menos granulomas (12,5 y 10%, en los segmentos 4 y D, respectivamente), así como menos inflamación y neovascularización.
Grupo stents liberadores de nitinolLos SLF provocaron la destrucción de la estructura traqueal en 7 animales (70%), observándose el relieve del stent a través de la pared traqueal y adherencias al tejido circundante. El epitelio estaba destruido en un número significativo de casos (40% en el segmento proximal, 60% en el segmento distal y 30% en los segmentos en contacto con el stent). Aunque en el grupo SLF el epitelio no era tan grueso como en el grupo SA, tenía un grosor mayor que en el grupo NiTi y la alteración del epitelio fue estadísticamente mayor debido a su destrucción (p<0,001). En general, la metaplasia escamosa no fue tan importante en el grupo SLF como en el grupo SA, aunque fue significativamente más pronunciada en el segmento central (40% de los casos, p=0,020). En un 10% de casos se detectaron granulomas en el segmento 0, así como en los segmentos 4 y D, con la misma proporción que en el grupo NiTi. La inflamación se componía principalmente de linfocitos e histiocitos, lo que sugirió una respuesta crónica. La neovascularización también fue mayor en el grupo SLF comparado con el grupo NiTi, pero menor que en el grupo SA.
Correlación entre la tomografía axial computarizada y los estudios histológicosEn un 68,9% de casos se observó una correlación positiva entre el engrosamiento epitelial (observado en el estudio microscópico) y el grado de estenosis (detectado en la TAC) en el día 90. No obstante, la correlación entre ambas técnicas en la detección de granulomas no fue estadísticamente significativa (p=0,880).
DiscusiónEl tratamiento de elección de las lesiones sintomáticas de la vía aérea es la resección quirúrgica, pero algunas veces son necesarias otras alternativas terapéuticas, con o sin implantación de stents de silicona. En las lesiones traqueobronquiales en las que no es posible la cirugía, la colocación de un stent constituye una alternativa. El uso de stents metálicos autoexpandibles o expandibles mediante balón se ha generalizado en el tratamiento de las patologías obstructivas o estenóticas de todo el organismo. Cada vez más, muchos médicos implantan stents metálicos expandibles para tratar a pacientes con distintas patologías endobronquiales13.
El stent autoexpandible de nitinol ha mostrado los mejores resultados tanto en las lesiones benignas del árbol traqueobronquial como en las malignas14,15. Sin embargo, no se han realizado estudios comparativos ni se dispone de series de un tamaño suficiente como para demostrar fehacientemente dichos resultados. En nuestro estudio comparamos stents de 2 tipos distintos de metal (acero y aleación de nitinol) y, dados los resultados favorables de los stents SLF en otras localizaciones anatómicas, se incorporó también un tercer tipo de stent de nitinol recubierto con paclitaxel.
La tráquea del conejo es muy reactiva, por lo que elegimos esta especie para evaluar las respuestas de la pared traqueal a los stents metálicos16. Además, en este modelo animal la implantación percutánea de stents es un procedimiento fácil, rápido y efectivo. Los 5 segmentos distintos que se analizaron en cada muestra resultaron útiles para evaluar la reactividad de la tráquea en su conjunto y de las áreas de estenosis.
Los stents de acero fueron los primeros en utilizarse en el árbol traqueobronquial, y los resultados iniciales fueron favorables, pero enseguida aparecieron sus inconvenientes3,17,18. En el estudio de De Gregorio et al.19, 3 de cada 4 stents de acero que se utilizaron para tratar lesiones benignas de la tráquea tuvieron que ser retirados al cabo de un año de su implantación. En nuestro estudio corroboramos estos resultados. De hecho, la mortalidad más alta fue la del grupo al que se implantaron stents de acero (80%), y se debió a estenosis y a infecciones. La respuesta a la presencia de un cuerpo extraño y la acumulación de mucosidad incrementó las posibilidades de infección. En las necropsias se evidenció neumonía, y como agente causal se aisló Pasteurella multocida, que había proliferado a causa de las condiciones deficientes de la vía aérea de los animales tras la implantación del stent. En el estudio mediante TAC, la estenosis traqueal y los granulomas fueron más significativos en el grupo SA que en el grupo NiTi, como era de esperar.
Los stents autoexpandibles de nitinol no recubiertos mostraron el mejor comportamiento, tanto en lesiones estenóticas benignas como malignas del árbol traqueobronquial. Algunos autores han comunicado resultados aceptables con este tipo de stent8,20-22. Nuestro estudio también demuestra un menor índice de lesiones epiteliales y granulomas en las tráqueas tratadas con stents de nitinol no recubiertos.
La principal causa de reestenosis tras la implantación del stent es el engrosamiento traqueal debido a la formación de granulomas23,24. Nuestra hipótesis inicial era que el SLF liberador de paclitaxel mejoraría los resultados al reducir la reacción epitelial. Sin embargo, de acuerdo con el estudio con TAC, el 50% de los casos de SLF habían desarrollado granulomas en el segmento central del stent en el día 30 (p=0,010) y en el segmento 0 el día 90 (p=0,018). En este grupo también se observó una destrucción epitelial relevante. Estos resultados son comparables a los del estudio in vitro de Arellano et al.25, en el que los SLF provocaron una destrucción celular rápida y notable en los cultivos de fibroblastos.
Se han efectuado pocos estudios con stents SLF para el tratamiento de estenosis de las vías aéreas. Se ha informado del efecto positivo de un stent bioabsorbible liberador de mitomicinaC, implantado en la tráquea de conejos, que se comparó con otros 4 tipos de stents26. Algunos autores han usado también stents liberadores de paclitaxel para el tratamiento de pacientes con enfisema, con el fin de mantener la permeabilidad de la vía aérea27-30. Aunque inicialmente los resultados fueron prometedores, la mejoría solo fue temporal. A excepción de los stents para el bypass de las vías aéreas en el enfisema, los SLF no están indicados clínicamente como prótesis de la vía aérea y los estudios futuros deberán abordar sus problemas, como el modo de evitar los granulomas, reducir la colonización del stent por bacterias y hongos, etc.
Los resultados de nuestro estudio comparativo coincidieron con los resultados publicados de stents de acero y de nitinol no recubiertos, pero en el grupo SLF los hallazgos fueron sorprendentemente negativos. Los SLF provocaron graves alteraciones en todas las capas de la pared traqueal, llegando incluso a afectar al cartílago. Para explicar estos hallazgos hemos postulado la hipótesis de que las condiciones de un SLF difieren según su localización. También es importante que la dosis del fármaco sea la correcta para evitar lesionar los tejidos31. En otro estudio, las concentraciones elevadas de paclitaxel se asociaron a una peor respuesta en la vía biliar32. El conducto biliar y la pared traqueal tienen estructuras histológicas diferentes respecto a las de los vasos sanguíneos, que es el lugar en que los SLF han demostrado ser más efectivos. Por otro lado, el flujo sanguíneo produce un efecto continuo de lavado del fármaco en los vasos, que no está presente en otras localizaciones, lo que podría explicar por qué en nuestro estudio se produjo una sobredosis de paclitaxel en la vía aérea. Las fuerzas radiales que los stents ejercen en la luz de las vías aéreas contra la pared de estas también son un detalle importante en este modelo, pero hay que tener en cuenta que el diseño y el tamaño de los SLF y los stents de NiTi son iguales, por lo que las diferencias son debidas al fármaco.
La limitación principal de este estudio es que se llevó a cabo en animales de laboratorio. La anatomía y la reactividad traqueal en el conejo son similares, pero no idénticas, a las de los humanos. Además, debido al pequeño tamaño, utilizamos stents comercializados para uso vascular, que tienen una concentración fija de fármaco. Los datos del grupo SA del día 90 probablemente no son representativos, debido a la elevada mortalidad previa a ese día (80%).
En conclusión, nuestro estudio confirma los efectos previamente descritos de los stents de acero, que ya habían provocado granulomas y un grado significativo de estenosis. Los stents de nitinol fueron los que menos reacción provocaron de entre todos los evaluados. Los SLF causaron lesiones significativas, con destrucción de todas las capas de la tráquea, lo cual posiblemente estuvo relacionado con la dosis del fármaco.
FinanciaciónEste estudio fue financiado gracias a una beca de investigación del Fondo de Investigación Sanitaria del Instituto de Salud CarlosIII (número PI081424).
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
El garante de este estudio es Miguel Ángel de Gregorio, Investigador Principal del Grupo de Investigación en Técnicas de Mínima Invasión (GITMI) de la Universidad de Zaragoza.