Durante las últimas décadas hemos presenciado un aumento sostenido de la prevalencia de asma y de obesidad en muchos países1. Por ejemplo, en EE.UU., entre los años 1980 y 1996 la prevalencia de asma se incrementó en un 73,9%2, y la de obesidad se elevó del 15,8 al 33,2% en mujeres y del 13,4 al 27,6% en varones durante el período 1960-20003. El incremento paralelo de estas 2 enfermedades ha dado origen a que se postule que ambas podrían estar de algún modo relacionadas.
Camargo et al4 realizaron uno de los primeros estudios longitudinales en adultos y demostraron que las mujeres que ganaban peso después de los 18 años tenían un riesgo mayor de desarrollar asma (incidencia) en los próximos 4 años, independiente de la ingesta calórica o la actividad física. Castro-Rodríguez et al5, en el primer estudio longitudinal en población pediátrica, demostraron que las niñas, pero no los niños, que se volvían obesas o adquirían sobrepeso entre los 6 y los 11 años de edad tenían 7 veces más riesgo de desarrollar asma (incidencia) que aquellas que se mantuvieron eutróficas, independientemente de la actividad física realizada y de la condición alérgica; además, estas niñas obesas o con sobrepeso presentaron una mayor respuesta broncodilatadora (volumen espiratorio forzado en el primer segundo) y mayor variabilidad del flujo espiratorio pico forzado que las eutróficas; esto los llevó a postular que podría haber una anomalía en la regulación del tono bronquial en las mujeres ("el cuarto fenotipo de asma infantil").
En los últimos años más de 20 estudios epidemiológicos, tanto en adultos como en niños, han confirmado la existencia de esta conexión entre la obesidad y la incidencia/prevalencia del asma, principalmente en el sexo femenino e independiente de la dieta, la actividad física o la condición alérgica. Esta influencia de la obesidad ocurre principalmente con el asma y con la hiperreactividad bronquial, pero no con otras enfermedades alérgicas6.
También hay comunicaciones y ensayos clínicos que demuestran que la pérdida de peso (ya sea por dieta o por cirugía de derivación gástrica) mejora los síntomas del asma7,8. Por lo tanto, si, como los estudios epidemiológicos demostraron, la obesidad precede y predice el desarrollo del asma (efecto de temporalidad) y no al revés; si además hay estudios que demuestran que, a mayor obesidad, mayor es el efecto sobre el asma (efecto de dosis-respuesta), y si hay una relación entre la obesidad y fenotipos intermedios de asma (cuarto fenotipo: púberes obesas con menarquia temprana no atópicas), podemos insinuar que la relación obesidad-asma sería de tipo causal.
Sin embargo, la explicación para esta relación es muy compleja y se han postulado al menos 5 posibles mecanismos biológicos:
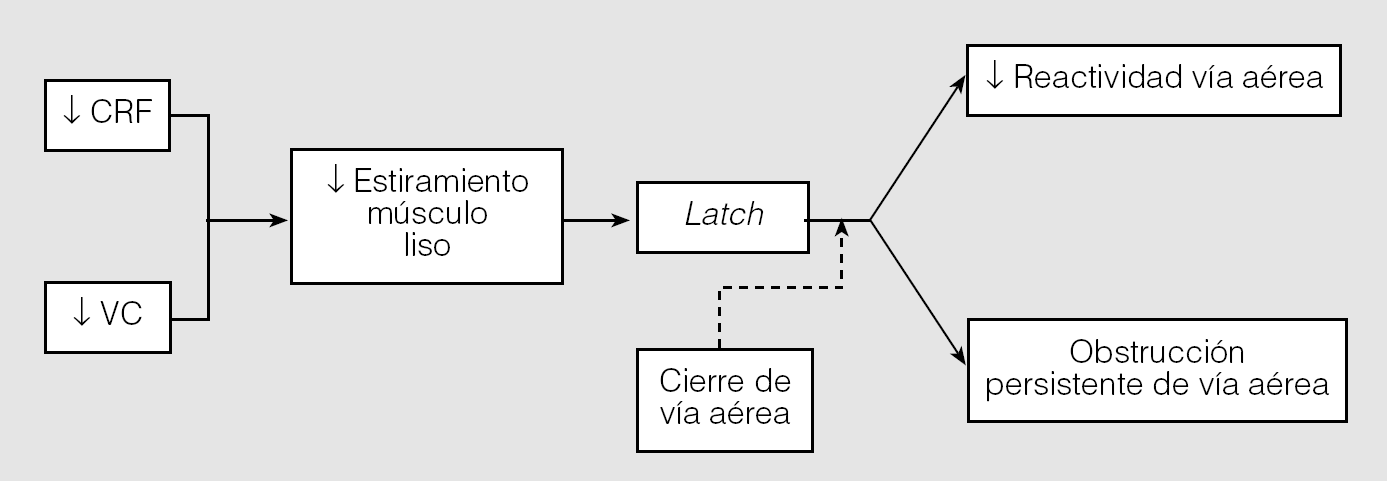
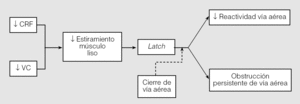
1. Efectos directos sobre la mecánica respiratoria funcional. Los efectos mecánicos de la obesidad sobre el aparato respiratorio parecen ser los más fáciles de entender. La obesidad produce una disminución del volumen corriente y de la capacidad residual funcional; estos cambios tienen como consecuencia una reducción del estiramiento del músculo liso (hipótesis del latching), y de esta forma la habilidad para responder al estrés fisiológico, como el ejercicio, se ve obstaculizada por los pequeños volúmenes corrientes, lo que altera la contracción del músculo liso y empeora la función pulmonar. El músculo liso intrínsecamente tiene un ciclo de excitación y contracción; sin embargo, en los obesos estos ciclos son más cortos, lo que, junto con la capacidad funcional disminuida que los caracteriza, tiene como resultado una conversión de los ciclos rápidos de actina-miosina hacia ciclos más lentos9,10 (fig. 1). Sin embargo, se desconoce la relación de dosis-efecto entre la cantidad y/o distribución de la grasa corporal y los cambios en la mecánica respiratoria.
Fig. 1. La hipótesis del latch: la obesidad causa disminución de la capacidad residual funcional (CRF) y del volumen corriente (VC), lo que da como resultado el latching del músculo liso, que aumenta la hiperreactividad y la obstrucción persistente de la vía aérea. Este efecto se incrementa por el tipo de respiración cercano al volumen de cierre que caracteriza a la obesidad mórbida. (Tomada de Tantisira y Weiss10.)
Otro efecto de la obesidad en la mecánica respiratoria es el aumento del reflujo gastroesofágico, que se observa en quienes la presentan y que también se ha descrito en asmáticos, principalmente adultos. Se sabe que la obesidad está asociada a una relajación del esfínter gastroesofágico, lo que tiene como resultado un reflujo del ácido del esófago a la tráquea/vía aérea. El contacto directo del ácido gástrico con la vía aérea origina broncoconstricción debido a la microaspiración o al reflejo vagal que se produce11.
2. Cambios en la respuesta inmunológica e inflamatoria. Cada vez hay más evidencias de que la obesidad es un estado "proinflamatorio"12. Los estudios iniciales demostraron que existe una asociación entre obesidad y diversos marcadores inflamatorios, como el factor de necrosis tumoral (TNF-α), las interleucinas (IL), como la IL-6, la IL-1β, y la proteína C reactiva. Se ha demostrado que la IL-6 y el TNF-α se expresan en los adipocitos y se relacionan directamente con la grasa corporal total. Por otra parte, el TNF-α también está aumentado en el asma y está relacionado con la producción de IL-4 e IL-5 IL del tipo T helper (Th) 2 por el epitelio bronquial y de IL-6 e IL-1β. Por lo expuesto, se puede inferir que la vía inflamatoria del TNF-α sería la vía común tanto para la obesidad como para el asma.
La leptina, una proteína del gen Lep, es una hormona producida por los adipocitos que actúa sobre el hipotálamo como un indicador de saciedad e incrementando el metabolismo basal. La concentración circulante de leptina se ha relacionado positivamente con la grasa corporal13. Además, se ha demostrado que también cumple una importante función en la estimulación de la liberación de citocinas proinflamatorias como la IL-6 y el TNF-α por el adipocito. La leptina promueve asimismo la respuesta inmunitaria del tipo Th1 con una mayor secreción de proteínas como el interferón gamma (IFN-γ)14. También se ha descrito que existe una relación entre valores elevados de leptina y de IFN-γ, y que la leptina incrementa la expresión y secreción del IFN-γ por las células periféricas mononucleares. Por otra parte, se ha demostrado que en la desnutrición asociada a hipoleptinemia hay una menor respuesta del tipo Th115. En estudios experimentales con ratones con déficit de leptina se observó hipoplasia pulmonar, lo que indica que existiría una relación entre la baja concentración de leptina y una reducción del desarrollo pulmonar16.
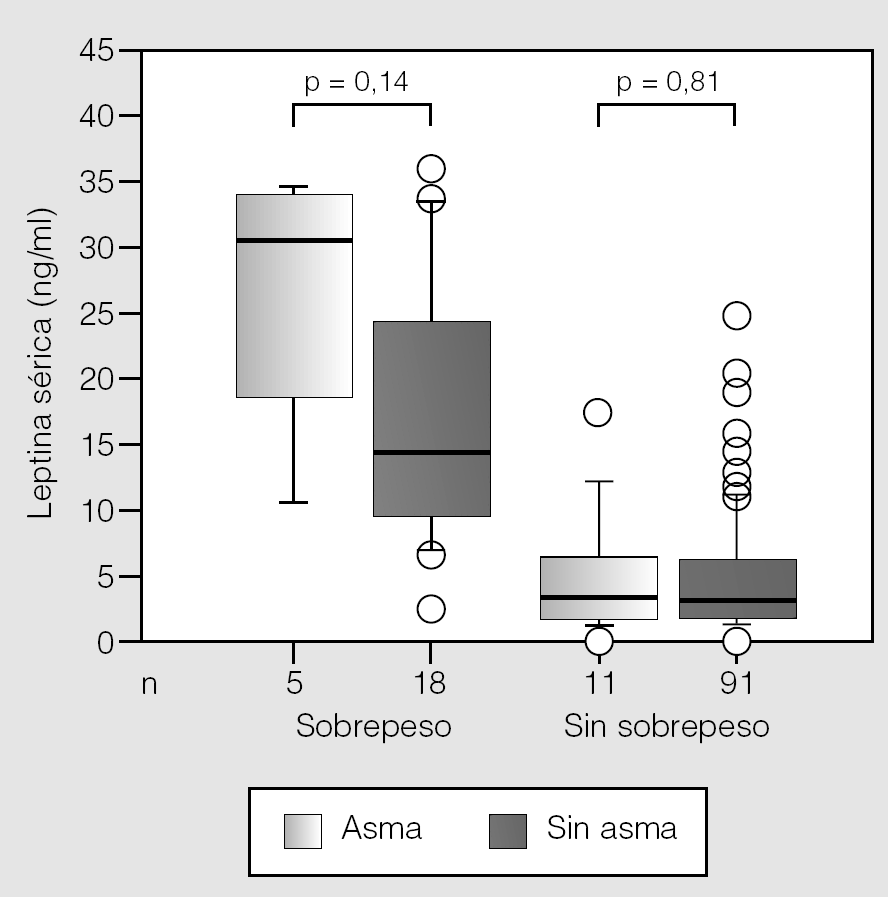
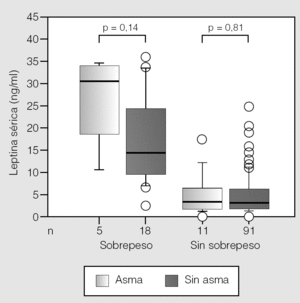
Sin embargo, en la vida posnatal el efecto de la leptina sobre el desarrollo pulmonar es distinto; por ejemplo, en humanos las concentraciones altas de leptina circulante se asociaron con un déficit de la función pulmonar17. Además, los efectos de la leptina pueden variar según las diferentes condiciones de la alimentación; por ejemplo, en el ayuno hay una menor concentración de leptina en los ratones no obesos. La leptina también actúa en la activación del sistema nervioso simpático, específicamente vía activación del metabolismo de la grasa parda. Tanto el sistema nervioso simpático como la grasa parda controlan el metabolismo basal; sin embargo, el sistema nervioso simpático es también crucial en el control del tono y diámetro de la vía aérea, que son marcadores importantes en el asma. Mai et al18 comunicaron que, entre los niños con sobrepeso, en aquéllos con diagnóstico de asma la concentración de leptina sérica fue casi 2 veces mayor que en los eutróficos (fig. 2). Aunque esta diferencia no fue significativa probablemente debido al tamaño de la muestra o a que la obesidad se evaluó con el índice de masa corporal (IMC), estos resultados apuntarían a un papel potencial de la leptina que debe confirmarse en otros estudios. Si bien el IMC es el parámetro más usado para evaluar la obesidad, no se relaciona del todo bien con la grasa corporal, y actualmente se postula que la combinación del IMC y el grosor del pliegue cutáneo puede ser un mejor reflejo de obesidad. Finalmente, hay otras hormonas relacionadas con la obesidad (p. ej., la insulina, la adiponectina y los neuropéptidos) que deben estudiarse en el asma.
Fig. 2. Valores séricos de leptina en pacientes con asma y sin ella, según la presencia de obesidad. (Tomada de Mai et al18.)
3. Activación de genes comunes. Sabemos del pleomorfismo genético, es decir, que los genes tienen muchos efectos, por lo que es biológicamente posible plantear que ciertos genes que están relacionados con una determinada enfermedad también podrían relacionarse con otra. En efecto, se han identificado regiones específicas del genoma humano que están relacionadas tanto con el asma como con la obesidad, como, por ejemplo, los cromosomas 5q, 6, 11q13 y 12q10.
El cromosoma 5q contiene los genes ADRB2 y NR3C1. El gen ADRB2, que codifica para el receptor adrenérgico β2, tiene influencia en la actividad del sistema nervioso simpático y es importante para el control del tono de la vía área, pero también para el metabolismo basal. El gen NR3C1, que codifica para el receptor de glucocorticoides, participa en la modulación inflamatoria tanto en el asma como en la obesidad.
El cromosoma 6 contiene los genes del complejo principal de histocompatibilidad y del TNF-α, que, como señalamos anteriormente, influyen en la respuesta inmunitaria e inflamatoria tanto en el asma como en la obesidad. El cromosoma 11q13 contiene los genes para las proteínas desacopladoras UCP2-UPC3 y para el receptor de la inmunoglobulina E de baja afinidad. Las proteínas UCP2-UPC3 influyen en el metabolismo basal, pero no en el asma. En cambio, el receptor de la inmunoglobulina E de baja afinidad es parte de la respuesta inflamatoria de las células Th, que se incrementan en el asma, pero no en la obesidad. Por último, el cromosoma 12q contiene genes para citocinas inflamatorias relacionadas tanto con el asma (p. ej., IFN-γ, LTA4H, óxido nítrico sintetasa-1) como con la obesidad (p. ej., STAT6, factor de crecimiento insulinoide-1, CD36L1).
4. Influencia hormonal y de sexo. Es algo remarcable que desde los primeros estudios longitudinales se ha evidenciado que el efecto de la obesidad sobre el asma se da más en mujeres que en varones4,5. Sabemos que la enzima aromatasa, responsable de convertir andrógenos en estrógenos, se encuentra presente en el tejido adiposo. En general, en la obesidad se incrementa la producción de los estrógenos, los cuales se asocian con una menarquia precoz en las mujeres y con un retraso de la pubertad en los varones19,20.
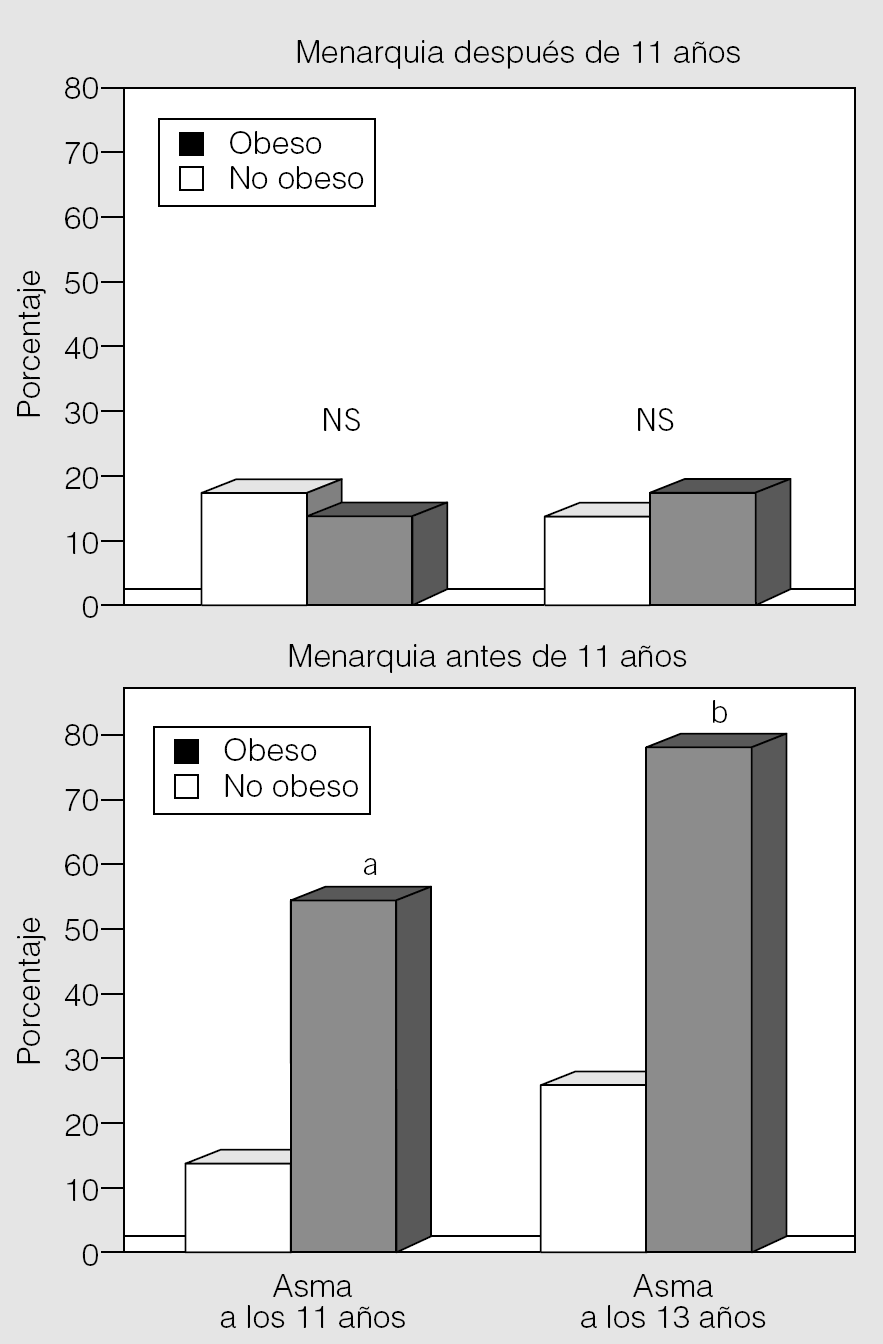
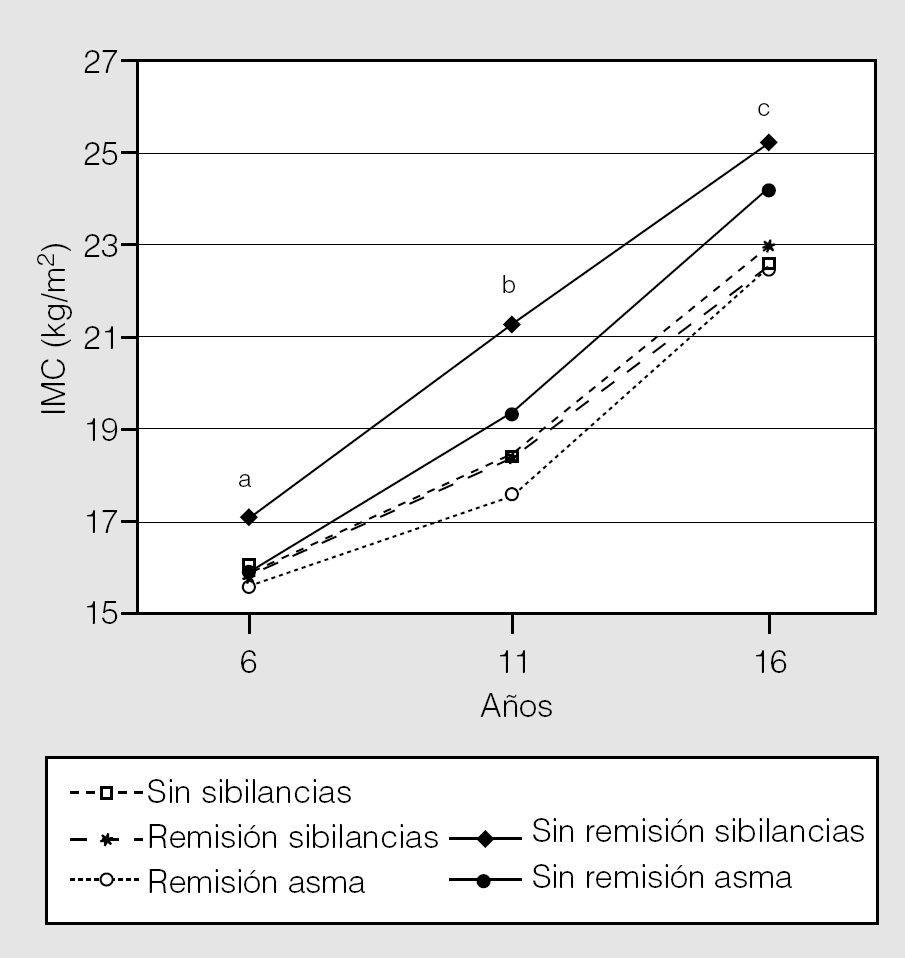
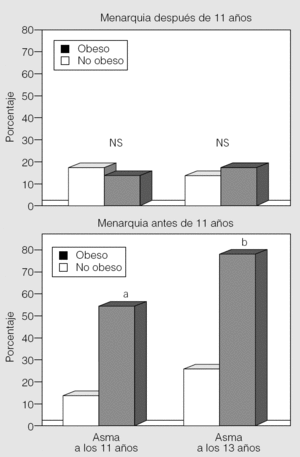
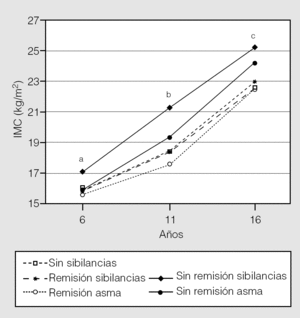
En la cohorte de Tucson, Castro-Rodríguez et al5 observaron que la prevalencia de asma fue mayor entre las niñas obesas que tuvieron menarquia temprana (antes de los 11 años de edad) que entre las que la tuvieron después de esa edad (fig. 3). Esto indicaría que la obesidad altera la producción (o sensibilización periférica) de las hormonas relacionadas con la pubertad en las niñas, y que una producción incrementada de las hormonas femeninas (o su sensibilidad) alteraría el desarrollo pulmonar y la regulación del tono de la vía aérea en las niñas púberes (con una mayor respuesta broncodilatadora, como se explicó anteriormente). Más tarde, en un estudio en adultos realizado en Francia, Varraso et al21 confirmaron este hallazgo, ya que observaron que la asociación entre obesidad y asma fue más evidente entre las mujeres con menarquia temprana. Se ha descrito asimismo que el uso de estrógenos exógenos es un factor de riesgo para una mayor incidencia de asma en mujeres22. El mecanismo por el cual los estrógenos conducen a un incremento de la respuesta en la vía aérea en el asma aún se desconoce, pero no es infrecuente en la práctica clínica ver casos de mujeres con asma grave y refractaria asociada con una obesidad mórbida, y curiosamente el sexo femenino por lo general se asocia también a mayor gravedad de obstrucción fija de los flujos aéreos o enfermedad pulmonar obstructiva crónica. Sin embargo, se desconoce si la resistencia a corticoides inhalados en los casos de asma grave está relacionada con los efectos metabólicos del asma, con el incremento de la inflamación o con efectos estrogénicos. Recientemente Guerra et al23, en la cohorte de Tucson, han comunicado que tanto el sobrepeso/obesidad a los 11 años de edad como la menarquia temprana fueron factores de riesgo para la persistencia de sibilancias después de la pubertad (fig. 4).
Fig. 3. Relación entre obesidad y asma en niñas con menarquia después de los 11 años (arriba) y con menarquia temprana o antes de los 11 años (abajo). ap = 0,01;bp = 0,004. NS: no significativo. (Tomada de Castro-Rodríguez5.)
Fig. 4. Obesidad como factor de riesgo para la persistencia de sibilancias desde los 6 hasta los 16 años de vida. ap = 0,01;bp = 0,0001; cp = 0,04. (Tomada de Guerra et al23.)
5. Influencia de la dieta, de la actividad física y de la "programación fetal". La dieta y la actividad física son 2 factores que influyen en la obesidad y al parecer también en el asma. Se postula que algunos factores que actúan en las mujeres embarazadas probablemente también tienen un considerable efecto en el desarrollo del feto vía peso de nacimiento y programación genética. Estos eventos in útero tendrían una repercusión en el desarrollo ulterior del asma y la obesidad. La fortaleza de esta hipótesis se basa en el reconocimiento de que la mayoría de los casos de asma sucede precozmente en los niños, antes de los 6 años, y que mucho de lo que ocurre después en la vida es sólo recrudescencia de la niñez. Mientras que los estudios prospectivos no han podido demostrar que la actividad física influya en la relación entre obesidad y asma, la actividad física de la madre gestante puede tener importancia en el desarrollo del sistema nervioso simpático in útero. La activación de la grasa parda, que generalmente está regulada por el sistema nervioso simpático, es importante para incrementar la termogenia y el metabolismo basal a través del desacoplamiento de proteínas. Por otra parte, sabemos que los 3 tipos de receptores betaadrenérgicos se expresan en el tejido adiposo.
Además, se ha descrito que una variedad de factores dietéticos tienen relación con la prevalencia del asma en adultos y niños. Por ejemplo, los antioxidantes (vitaminas C y E), el caroteno, la riboflavina y la piridoxina pueden tener un efecto importante aumentando la función inmunológica, reduciendo los síntomas del asma/eccema y mejorando la función pulmonar. Recientemente Romieu et al24 han demostrado que mujeres adultas que consumían frutas y verduras (tomate, zanahorias y vegetales de hoja) tuvieron una menor prevalencia de asma. También el mayor consumo de ácido grasos trans en población pediátrica se ha relacionado con una reducción de la prevalencia del asma25. Sin embargo, es importante recalcar que muchos de los trabajos sobre dieta y asma se realizaron en personas ya diagnosticadas de asma. No se sabe si la composición de la dieta materna durante la gestación puede influir en el desarrollo de obesidad en el hijo, pero es interesante señalar que la relación entre peso al nacimiento, independientemente de la edad gestacional, y el riesgo de asma sigue una curva de tipo U; es decir, tanto el peso bajo al nacer como el alto presentaron mayor riesgo de asma26,27. Asimismo se describe una curva de tipo U en la relación en los varones del bajo y alto IMC con una mayor hiperreactividad bronquial28. Esto indicaría que la "programación fetal" podría tener alguna repercusión en el desarrollo ulterior de la obesidad y del asma.
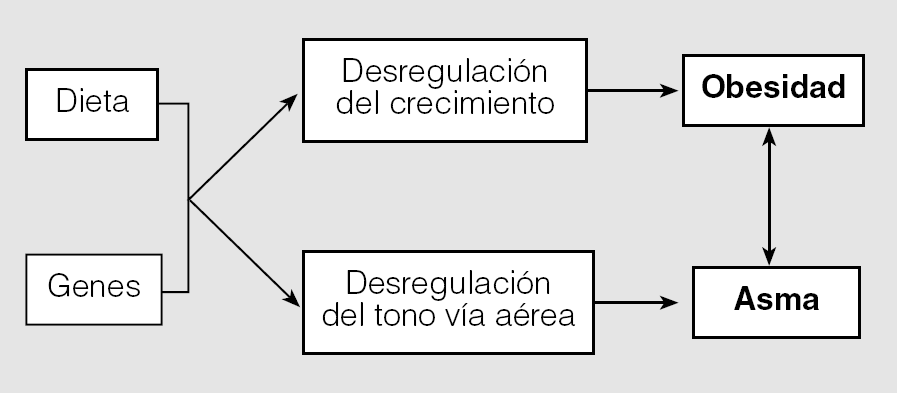
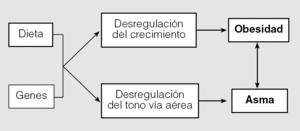
La compleja interrelación entre obesidad y asma es un ejemplo de cómo interactúan los genes y el ambiente en la génesis de ambas entidades, y es muy probable que esté involucrado más de un mecanismo biológico. La obesidad, a través de mecanismos inflamatorios o cambios en el estilo de vida, puede desencadenar los síntomas asmáticos en personas "susceptibles". La interacción dieta-genes puede causar alteraciones en los patrones de crecimiento corporal (originar obesidad) y/o alterar el tono de la vía aérea (originar asma), y pueden producirse múltiples interrelaciones entre la obesidad y el asma (fig. 5).
Fig. 5. Mecanismos de interrelación entre la genética y el medio ambiente que se proponen para explicar la correspondencia existente entre la obesidad y el asma.
Correspondencia:
Prof. J.A. Castro-Rodríguez.
Escuela de Medicina. Pontificia Universidad de Chile.
Lira, 44, 1.er piso, casilla 114-D. Santiago de Chile. Chile.
Correo electrónico: jacastro17@hotmail.com
Recibido: 12-6-2006; aceptado para su publicación: 27-6-2006.