Introducción
La polisomnografía es la prueba de referencia para el diagnóstico del síndrome de apneas obstructivas durante el sueño (SAOS)1. Sin embargo, existe una tendencia, casi universal, a simplificar los métodos diagnósticos a través del uso de diversos monitores portátiles, que se han dividido en tipos II, III y IV en función de la complejidad y del número de señales que registran, cada uno de los cuales tiene diferente rentabilidad diagnóstica cuando se comparan con la prueba de referencia2. Los monitores de tipo IV no están aceptados como método de estudio de diagnóstico definitivo1.
El análisis automatizado de la oximetría de pulso nocturna se considera un estudio de tipo IV y, mediante diferentes algoritmos, se puede medir el índice de desaturaciones (ID), que es el número de desaturaciones que presenta el sujeto por cada hora de registro. Otros monitores de tipo IV utilizan sólo la señal de flujo nasal (presión nasal) para estimar un índice respiratorio basado en el flujo (IRF)3.
Aun cuando los monitores portátiles de tipo IV se desarrollaron como una prueba de cribado en pacientes con sospecha de SAOS, en la actualidad su uso se ha extendido con fines diagnósticos. En este sentido, dichos dispositivos tienen algunas ventajas: son más accesibles, su análisis suele ser automático, no requieren de personal altamente capacitado y el estudio puede realizarse en el domicilio del paciente2,4.
Es indispensable conocer la rentabilidad diagnóstica de los monitores portátiles mediante un proceso de validación en que se comparen con la polisomografía. Vázquez et al5 validaron previamente, a 1.049 m sobre el nivel del mar, el algoritmo del oxímetro de pulso que se utiliza en este trabajo. En dicho estudio, que se llevó a cabo en 241 pacientes, el coeficiente de correlación fue de 0,97, la sensibilidad del 98% y la especificidad del 88%. Los estudios de validación de otros monitores6,7 se han realizado a una altitud menor que la observada en Ciudad de México, lo cual tiene algunos potenciales inconvenientes para los que se basan en la oximetría. La altitud de Ciudad de México (2.240 m) puede afectar el rendimiento de los algoritmos automatizados de los oxímetros de pulso, ya que los habitantes se encuentran cerca de la rodilla de la curva de disociación de la hemoglobina. En esta situación, un cambio dado en la presión arterial de oxígeno ocasiona un mayor cambio en la saturación de oxígeno, por lo que resulta más fácil generar desaturación a partir de pequeñas disminuciones de la presión arterial de oxígeno. De esta manera, es probable que la altitud genere un error de sobrestimación, con un ID mayor que el índice de apneas-hipopneas (IAH).
El objetivo del presente estudio ha sido determinar la correspondencia entre el ID y el IAH, así como entre el ID y el IRF, en adultos con sospecha de SAOS de Ciudad de México.
Pacientes y métodos
Se trata de un estudio de tipo transversal de 2 vertientes. En la primera se compararon el ID y el IAH, y en la segunda, el ID y el IRF. El protocolo de investigación fue aprobado por el Comité Institucional de Ciencia y Bioética, y todos los pacientes firmaron previamente el consentimiento informado.
Vertiente 1 (índice de desaturación frente a índice de apneas-hipopneas)
Se incluyó de manera consecutiva a pacientes mayores de 18 años de edad, remitidos a la Clínica de Sueño del hospital donde se realizó el estudio por sospecha de SAOS. A todos ellos se les realizaron, de manera simultánea y en el medio hospitalario, una polisomnografía estándar nocturna y el registro con el oxímetro de pulso. No se incluyó a pacientes con enfermedad pulmonar grave (volumen espiratorio forzado en el primer segundo o capacidad vital forzada < 50% del valor predicho), enfermedades neuromusculares, hipoxemia diurna, enfermedad cardíaca conocida, insomnio, síntomas indicativos de piernas inquietas, enfermedades psiquiátricas o uso de hipnóticos.
La polisomnografía estándar basal se realizó con un equipo Grass (Grass-Telefactor, Astro Med Inc., West Warwick, RI, EE.UU.), mediante un montaje monopolar en el cual se incluyeron las siguientes señales: 2 canales de electroencefalograma (C3-A2, O1-A2), 2 canales de electrooculografía (O1-A2, O2-A1) y electromiografía (EMGm, EMGp), electrocardiograma y micrófono. Las señales respiratorias que se registraron fueron: 2 canales para pletismografía por inductancia (Respitrace, Ambulatory Monitoring Inc., Ardsley, NY, EE.UU.), 2 para flujo respiratorio (presión nasal y sensor térmico), anhídrido carbónico espirado y oximetría de pulso. Las polisomnografías se estatificaron de acuerdo con los criterios de Rechtschaffen y Kales8. Las señales respiratorias se calificaron de manera manual siguiendo las recomendaciones actuales internacionalmente aceptadas1. Se consideró apnea obstructiva la ausencia o disminución mayor del 50% de la amplitud del flujo aéreo, con una duración mayor de 10 s y persistencia del esfuerzo respiratorio, con o sin desaturación de oxígeno o alertamiento o microdespertar (arousal). Se consideró hipopnea una disminución menor del 50% de la amplitud del flujo aéreo por termistor o punta nasal, con una duración mayor de 10 s, que se asociaba con desaturación del 4% o mayor, o alertamiento de 1,5 s o mayor9.
El monitor portátil que se utilizó para medir el ID (Remmers Sleep Recorder, Sagatech, Calgary, Alberta, Canadá) permite el registro simultáneo de 5 señales: flujo respiratorio, oximetría de pulso, frecuencia cardíaca, posición corporal y ronquido. El algoritmo automatizado de este equipo se basa únicamente en la oximetría, considerando un evento respiratorio el ascenso de la saturación de oxígeno que es precedido por una disminución mayor del 3% del valor basal de la saturación de oxígeno. El valor basal de saturación de oxígeno se define como el promedio de la percentil 5 en los 5 min previos al evento. La rentabilidad diagnóstica de este equipo se determinó previamente en un estudio realizado en la ciudad de Calgary (Alberta, Canadá) a una altura de 1.049 metros sobre el nivel del mar5.
Vertiente 2 (índice de desaturaciones frente a índice respiratorio basado en el flujo)
Se incluyó a pacientes mayores de 18 años de edad con sospecha de SAOS. Estos pacientes fueron distintos de los incluidos en la vertiente 1, aunque se siguieron los mismos criterios de inclusión y exclusión. A estos pacientes se les colocaron, de manera simultánea, 2 monitores: uno para medir el ID y el otro para medir apneas e hipopneas por flujo nasal a través de un sistema monocanal de detección de flujo nasal. El estudio de estos pacientes se llevó a cabo en el hospital.
El ID se obtuvo del mismo modo descrito en la vertiente 1. El IRF se determinó a través de un sistema monocanal de detección de flujo, que se basa en la presión nasal medida por puntas nasales (ApneaLink, ResMed Corp, Poway, CA, EE.UU.). El algoritmo automático para el cálculo del IRF considera una apnea cuando existe una disminución del 80% o más en la amplitud de la señal de flujo, e hipopnea cuando existe una disminución de al menos el 50% de la amplitud de la señal. Además, se llevó a cabo un análisis manual de la señal para eliminar los períodos que presentaban artefactos. No se incluyó para el análisis a los pacientes que hubieran tenido más del 10% del tiempo de registro con una señal de mala calidad o artefactuada. Este monitor se ha validado previamente frente a la polisomnografía en Alemania, a 116 m sobre el nivel del mar6,7.
Análisis estadístico
Los datos se muestran como media ± desviación estándar. La fuerza de la asociación entre el IAH frente al ID y entre el ID frente al IRF se evaluó mediante los coeficientes de correlación de Pearson y Spearman. El análisis de concordancia (también llamada correspondencia) para las mismas variables se realizó mediante el cálculo del coeficiente de correlación intraclase (CCI). Se obtuvo el error de medición al calcular la media y desviación estándar de las diferencias individuales, y se muestran con el gráfico modificado de Bland y Altman. Para la vertiente 1 se calcularon además la sensibilidad, la especificidad y el área bajo la curva, considerando como referencia varios puntos de corte del IAH, que se compararon con varios puntos de corte del ID. Se consideraron significativos los valores de p < 0,05. El análisis de los datos se realizó con el paquete estadístico Stata versión 9,2 (STATATM, StataCorp, College Station, TX, EE.UU.).
Resultados
Vertiente 1
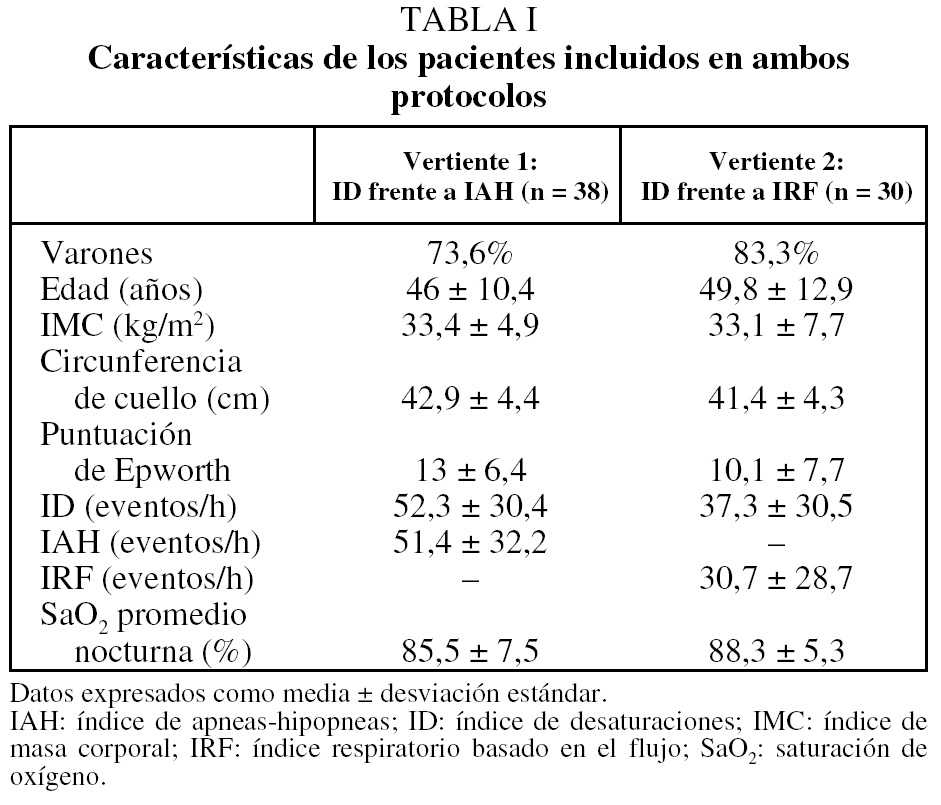
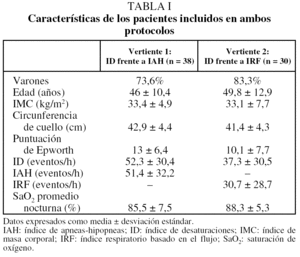
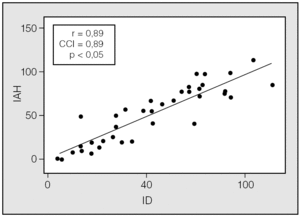
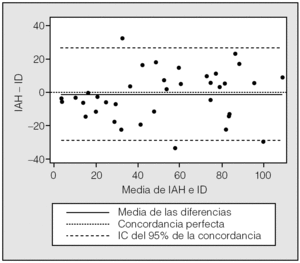
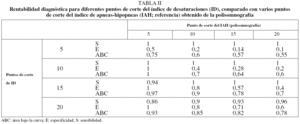
Las características de los pacientes incluidos en ambas vertientes se muestran en la tabla I. Para la vertiente 1 se incluyó a 38 pacientes (28 varones) con una edad media de 46 ± 10,4 años. En la figura 1 se muestra la correlación entre el ID y el IAH. Tanto el coeficiente de correlación de Pearson como el de Spearman fueron de 0,89. El CCI, como indicador de correspondencia entre el ID y el IAH, fue de 0,89, y la media de la diferencias (IAH ID) fue de 0,9, lo que implica que el ID fue ligeramente mayor que el IAH. Sin embargo, en la figura 2 se observa que las diferencias individuales se modificaron ligeramente con los incrementos del IAH. Las diferencias entre el IAH y el ID (al IAH se le resta el ID) fueron uniformemente negativas para un punto de corte de IAH menor de 35, por lo que se calculó el CCI en subgrupos; en aquellos en quienes el IAH era menor de 35 (n = 13), el CCI fue de 0,59 (con media de diferencias IAH-ID de 7,6), en tanto que fue de 0,72 (con media de diferencias IAH-ID de 2,5) para aquellos en quienes el IAH era mayor de 35 (n = 25). En la tabla II se muestra la rentabilidad diagnóstica considerando como referencia 4 puntos de corte del IAH (5; 10; 15, y 20), que se compararon con varios puntos de corte del ID (5; 10; 15, y 20). La mayor área bajo la curva se obtuvo cuando se consideró un punto de corte de ID de 10 y la referencia, de 5.
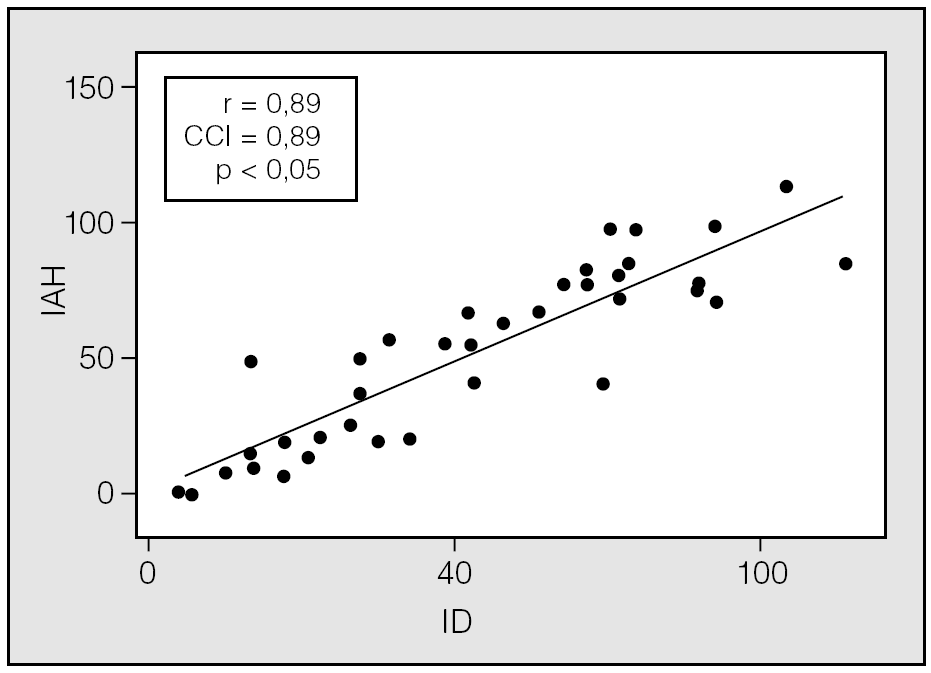
Fig. 1. Correlación entre el índice de desaturaciones (ID) y el índice de apneas-hipopneas (IAH). CCI: coeficiente de correlación intraclase.
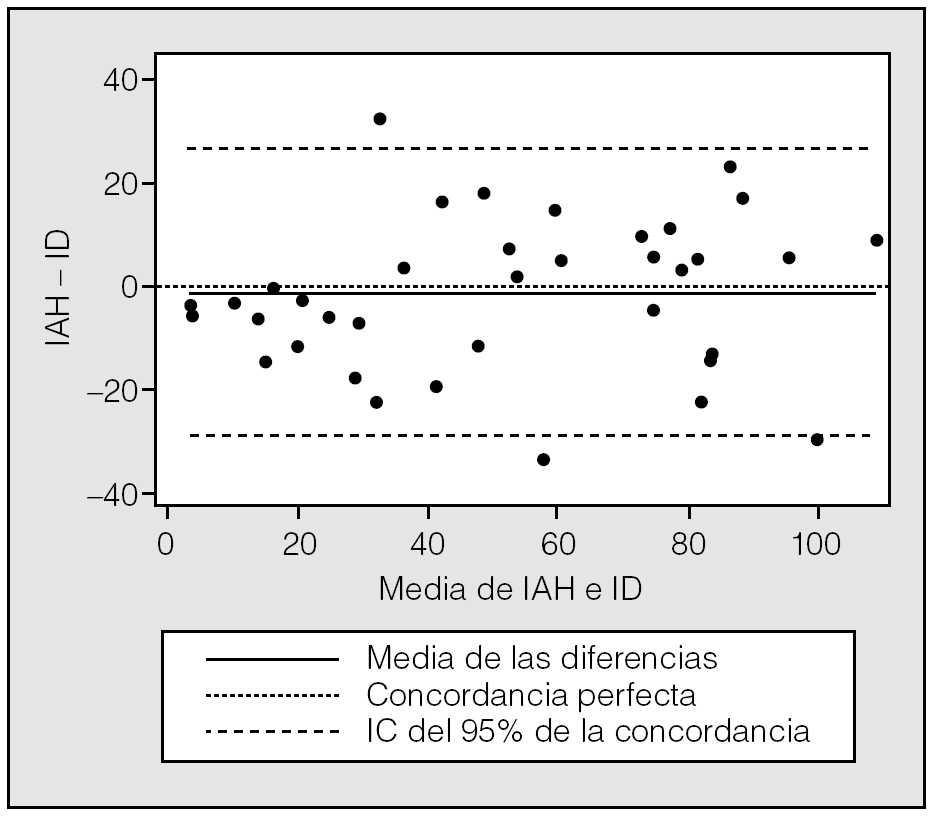
Fig. 2. Gráfico modificado de Bland y Altman que muestra las diferencias, punto por punto, entre el índice de apneas-hipopneas (IAH) obtenido de la polisomnografía y el índice de desaturaciones (ID). IC: intervalo de confianza.
Vertiente 2
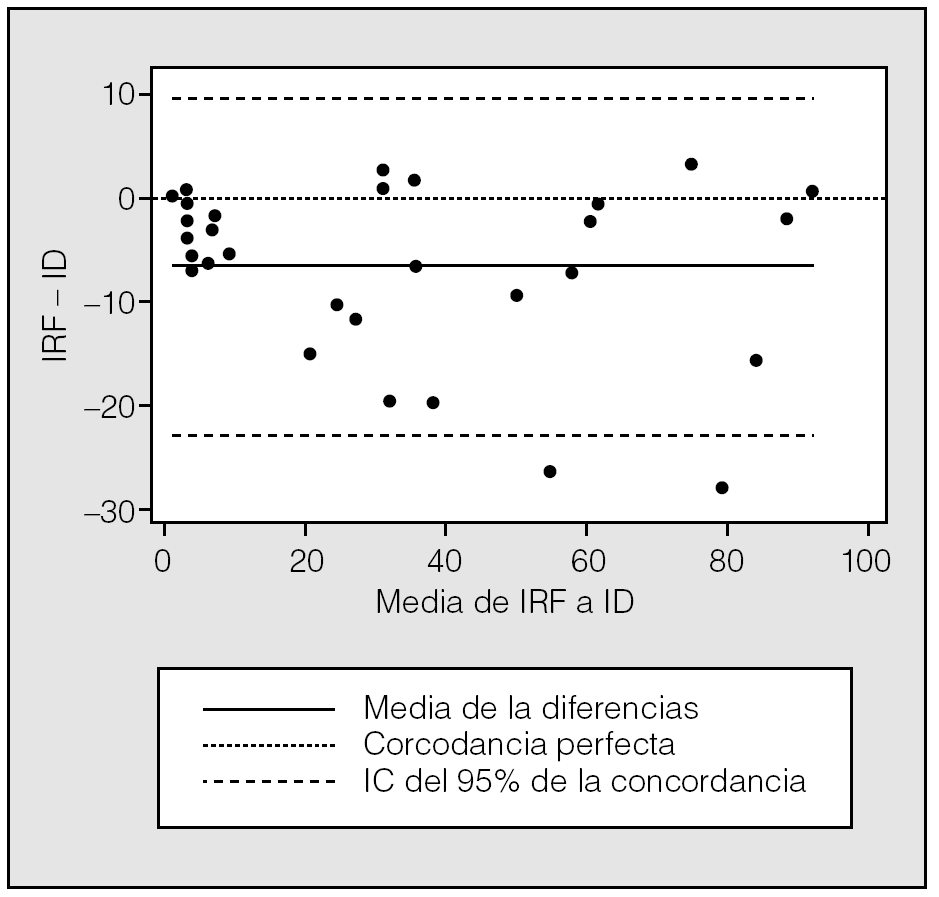
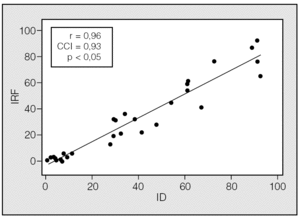
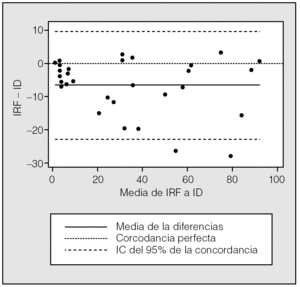
Se incluyó a 30 pacientes (25 varones) con un promedio de edad de 49,8 ± 12,9 años. En la figura 3 se muestra la correlación entre el ID y el IRF. El coeficiente de correlación de Pearson fue de 0,96, y el de Spearman, de 0,94. El CCI fue de 0,93. El promedio de las diferencias (el valor de IRF menos el valor del ID) tuvo un valor negativo (6,6), lo cual significa que el número de desaturaciones excedió al número de apneas e hipopneas basadas en el flujo nasal (fig. 4).
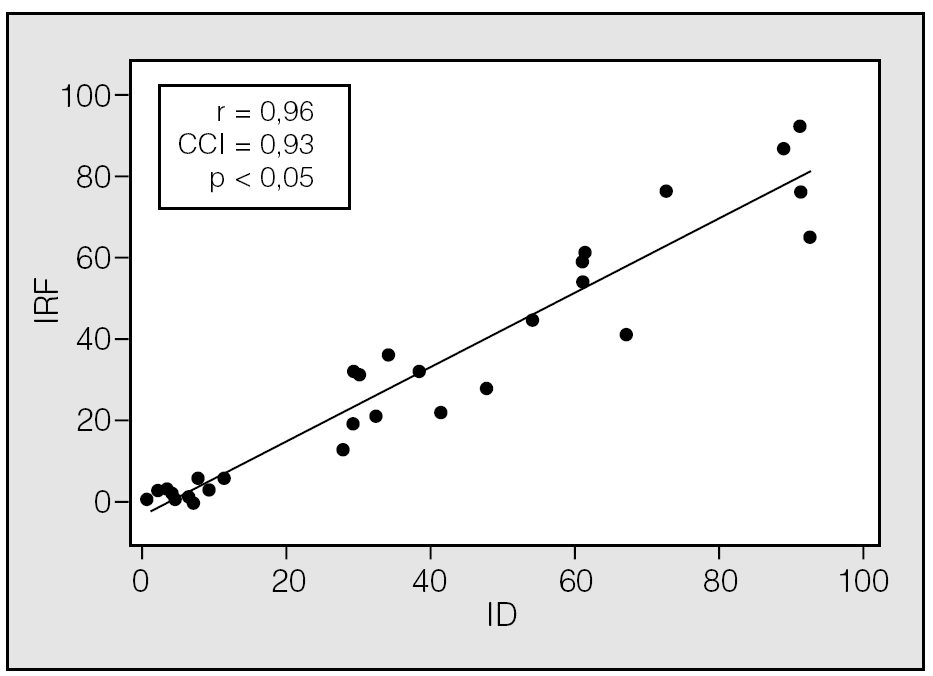
Fig. 3. Correlación entre el índice de desaturaciones (ID) y el índice respiratorio basado en el flujo (IRF). CCI: coeficiente de correlación intraclase.
Fig. 4. Gráfico modificado de Bland y Altman que muestra las diferencias, punto por punto, entre el índice respiratorio basado en el flujo (IRF) y el índice de desaturaciones (ID). IC: intervalo de confianza.
Discusión
El SAOS es un grave problema de salud pública. Su alta prevalencia estimada en un 2 y un 4% en mujeres y varones, respectivamente10,11, junto con el reconocimiento que ha tenido en las últimas décadas, han propiciado un incremento espectacular de la demanda de los estudios de SAOS12. En este sentido, Pellicer-Císcar12 ha señalado recientemente que el SAOS se ha convertido en el diagnóstico más frecuente por el que los pacientes son remitidos a consultas neumológicas. Así pues, dadas la alta frecuencia de la enfermedad y la gran demanda social para estudiar a pacientes con sospecha de SAOS, así como el poco acceso al diagnóstico y al tratamiento13, deben adoptarse medidas más eficientes para atender a un gran número de pacientes. Los monitores portátiles representan una alternativa diagnóstica útil ante los costes que representa la polisomnografía y el número limitado de clínicas de sueño donde se realizan dichos estudios. Sin embargo, los monitores de tipo IV, como el sistema monocanal de flujo y la oximetría, sólo están aprobados como estudios de cribado1.
La creciente tendencia a emplear monitores simplificados no es privativa de economías en desarrollo, sino que también se observa en países desarrollados que encaminan sus esfuerzos a atender a un mayor número de pacientes a un coste menor2,14. Es necesario, por lo tanto, conocer la rentabilidad diagnóstica de cada uno de los monitores disponibles, así como los factores que potencialmente pueden afectar a su rendimiento.
La altitud de Ciudad de México es una variable que, al menos teóricamente, puede influir en la rentabilidad de los oxímetros. Sin embargo, esto no se ha confirmado en el presente este estudio, que compara la medición automatizada de desaturaciones y la medición manual del IAH en la polisomnografía. En las circunstancias descritas, el ID del monitor Remmers es un indicador fiable del IAH en Ciudad de México, al igual que se ha comunicado en otras alturas5. Sin embargo, es necesario aclarar, a través de estudios que incluyan a un número mayor de pacientes, si la elevada concordancia se mantiene en diferentes grupos de sujetos clasificados de acuerdo con la gravedad de la enfermedad. En el presente estudio se observó que, al clasificar a los pacientes por IAH menor de 35, el CCI disminuyó, lo que implica que la rentabilidad diagnóstica del algoritmo del oxímetro pudiera ser diferente en distintos grupos de pacientes (con enfermedad leve, moderada o grave).
El estudio de validación del monitor que mide el ID fue realizado por Vázquez et al5. En dicho estudio la apnea se definió como la ausencia de flujo oronasal durante al menos 10 s, y la hipopnea como una reducción de cuando menos 10 s en el movimiento toracoabdominal, junto con una reducción de la saturación de oxígeno de más del 4%, con o sin alertamiento. Los criterios que se utilizaron en el presente estudio son un poco diferentes, ya que se consideró que había apnea obstructiva ante la ausencia o disminución mayor del 50% de la amplitud del flujo aéreo, con una duración superior a 10 s, y persistencia del esfuerzo respiratorio, con o sin desaturación de oxígeno o alertamiento. La hipopnea, por su parte, se definió como la disminución menor del 50% de la amplitud del flujo aéreo por termistor o punta nasal, con una duración mayor de 10 s, que se asocia con desaturación del 4% o mayor, o tiene alertamiento de 1,5 s o mayor. A pesar de estas mínimas diferencias en los criterios de estadificación, los resultados obtenidos en ambos estudios son muy semejantes al comparar el IAH obtenido con la polisomnografía y el ID del oxímetro. El presente estudio se diseñó como un estudio de correspondencia, no como una prueba diagnóstica; sin embargo, se calcularon las áreas bajo la curva estableciendo como referencia el IAH obtenido en la polisomnografía, que se comparó con varios puntos de corte de ID. Se obtuvo un área bajo la curva de 1 cuando se comparó un punto de corte de 10 en el ID con un punto de corte de referencia de 5, lo que implica que un punto de corte de 10 en el ID no genera errores de clasificación cuando se compara un punto de corte de 5 en la prueba de referencia, criterio que se ha considerado patológico10. Desde el punto de vista clínico, la alta tasa de verdaderos positivos y de verdaderos negativos que se obtuvo con un punto de corte de ID mayor de 10 subsana la correspondencia relativamente baja que se observó entre el ID y el IAH en pacientes en que éste era inferior a 35. Cuando se consideró un punto de corte de IAH de 10 (criterio más estricto de apnea obstructiva del sueño), la mejor área bajo la curva se obtuvo con un punto de corte de ID de 15 eventos/h. Los oxímetros tienen diferentes algoritmos automatizados, pero en general, cuanto mayor es la desaturación de oxígeno que el equipo considera un "evento respiratorio", mayor es la especificidad, aunque disminuye la sensibilidad. Los resultados que mostramos no pueden extrapolarse a otros oxímetros ni a mayores altitudes, para lo cual se requeriría de una confirmación semejante a la mostrada en el presente trabajo.
La comparación realizada entre el ID y el IRF mostró también una alta concordancia. Ambos índices se obtuvieron de manera automatizada de acuerdo con sus algoritmos correspondientes, y el ID fue uniformemente mayor que el IRF en 6,6 eventos/h. Esta diferencia fue creciente a medida que aumentaba la gravedad de la enfermedad (fig. 4). El criterio de estadificación para hipopneas que utiliza el sensor de flujo Apnea Link para estimar el IRF es una disminución mayor del 50% en la amplitud de la señal de flujo. Esto podría explicar, al menos en parte, por qué el IRF es menor que el ID. Dicho de otra manera, la estimación del IRF a través del sensor de flujo no contabiliza (baja sensibilidad) algunas hipopneas con la definición utilizada, ya que no cuenta con el sensor de oxígeno, lo cual podría interpretarse como un inconveniente para el IRF porque, aun cuando este índice se validó originalmente frente a la polisomnografía6, aquel estudio se realizó prácticamente a nivel del mar, donde las hipopneas asociadas a desaturación podrían ser menores en frecuencia por la posición que los sujetos que habitan a esa altitud ocupan en la curva estándar de disociación de la hemoglobina. Es importante señalar esto, porque, aunque la prueba de referencia para determinar las apneas o hipopneas es la señal de flujo (idealmente, el neumotacógrafo), se ha descrito que las desaturaciones de oxígeno, que son la consecuencia, también generan diversos daños a la salud por el fenómeno de la hipoxemia intermitente15-18. En la validación original a 116 m de altitud, la media de las diferencias entre el IRF y el IAH obtenido con la polisomnografía fue de 3,8 (de +11,1 a 3,5). La sensibilidad fue del 100% y la especificidad del 87,5% para un punto de corte de 10, que fue el que se asoció a mayor área bajo la curva (0,95)6. En el presente estudio no se comparó el IRF con el IAH de la polisomnografía; sin embargo, la diferencia observada entre el ID y el IRF (6,6 eventos/h a favor del ID) es poco probable que genere errores de clasificación en la decisión para prescribir presión positiva continua de la vía aérea, ya que la diferencia fue mayor en puntos de corte altos, donde una diferencia de 6 eventos no modifica la decisión del clínico por lo que se refiere a la prescripción de presión positiva continua de la vía aérea (fig. 4).
En conclusión, en adultos con sospecha de SAOS en Ciudad de México se observó una alta correspondencia entre el IAH polisomnográfico y el ID del monitor Remmers, así como entre el ID y el IRF del sistema monocanal de detección de flujo, aunque este último muestra en promedio 6 eventos menos que el ID por hora de registro. La altitud de Ciudad de México no afecta significativamente la rentabilidad diagnóstica del monitor portátil basado en desaturaciones de oxígeno. Es preciso evaluar otros monitores basados en la desaturación de oxígeno en Ciudad de México y en altitudes mayores.
Correspondencia: Dr. L. Torre-Bouscoulet.
Clínica de Trastornos Respiratorios del Dormir.
Instituto Nacional de Enfermedades Respiratorias.
Tlalpan, 4.502. Colonia Sección XVI. Delegación Tlalpan. 14080 México, DF. México.
Correo electrónico: luistorreb2001@yahoo.com.mx
Recibido: 16-8-2006; aceptado para su publicación: 3-4-2007.