Introducción
La EPOC se caracteriza por la presencia de obstrucción crónica y poco reversible al flujo aéreo (disminución del volumen espiratorio forzado en el primer segundo [FEV1] y de la relación FEV1/capacidad vital forzada [FVC]), causada fundamentalmente por una reacción inflamatoria anómala frente al humo del tabaco1. Por tanto, el diagnóstico de la enfermedad requiere la realización de una espirometría que demuestre "escasa" reversibilidad en una prueba broncodilatadora. Esta prueba también se ha usado en la evaluación de la gravedad, así como en la monitorización de la respuesta con diferentes medidas terapéuticas. Si nos atenemos a la propia definición de la EPOC, la respuesta espirométrica con diversos broncodilatadores debería ser modesta. Sin embargo, en la práctica clínica esto no es siempre así, y en los casos en que no se confirman cambios espirométricos significativos, los broncodilatadores siguen siendo el tratamiento sintomático más importante.
Dada la importancia del tono vagal y de los receptores muscarínicos en la vía aérea del paciente con EPOC, resulta sorprendente que la reversibilidad se haya estado valorando con dosis bajas de simpaticomiméticos, los resultados se expresen como incremento respecto al valor basal. Esta forma de actuar, como ha ocurrido en otros aspectos de la EPOC, es el resultado de una simple extrapolación de lo que suele hacerse en el asma, olvidándose de que en la EPOC puede ser necesario utilizar dosis más elevadas de agonistas β22, que puede haber respuestas heterogéneas con simpaticomiméticos o con anticolinérgicos3, que los factores geométricos resultantes de la obstrucción basal pueden condicionar la forma de medir la respuesta4 o que puede haber respuestas clínicamente muy relevantes con respuesta espirométrica negativa5. Estas peculiaridades de la EPOC obligan a replantear la utilidad de la información que aporta una prueba broncodilatadora y mejorar su ejecución con el uso de más de un fármaco, utilizando índices que valoren la reversibilidad de una forma más apropiada, o incluyendo parámetros menos usuales en el análisis de la respuesta, ya sean de la propia espirometría forzada o de otras pruebas de función pulmonar.
Reversibilidad en la EPOC
Un aspecto que define la obstrucción crónica al flujo aéreo es su persistencia a pesar del tratamiento. En pacientes con EPOC, la obstrucción al flujo aéreo puede deberse a un incremento de la resistencia al flujo aéreo por cambios patológicos en las vías aéreas o por pérdida de las propiedades elásticas del pulmón, secundaria a la presencia de enfisema pulmonar. Teóricamente, la limitación al flujo aéreo por obstrucción bronquial puede mejorar relajando el tono del músculo liso o disminuyendo los cambios inflamatorios. Por el contrario, los cambios funcionales secundarios a fibrosis o enfisema pueden considerarse irreversibles, aunque con frecuencia es posible observar en un mismo paciente varios tipos de lesiones, lo que impide establecer puntos de corte categóricos a la hora de predecir el grado de broncodilatación6-8.
Aunque habitualmente se acepta que sólo una pequeña proporción de pacientes con EPOC (15-20%) presenta una respuesta positiva con tratamiento broncodilatador, existen varios aspectos que han podido contribuir a una deficiente valoración del grado de reversibilidad. Por este motivo, para valorar de forma adecuada la reversibilidad tras el tratamiento broncodilatador en la EPOC es necesario tener presente previamente una serie de puntos, ya que no existe ningún "patrón oro" que permita identificar con una sola prueba una respuesta significativa tras el uso de fármacos broncodilatadores o antiinflamatorios.
1. En la EPOC, la presencia de reversibilidad en la obstrucción al flujo aéreo en ocasiones no se acompaña de cambios relevantes en la espirometría forzada. Con frecuencia, los pacientes refieren una clara mejoría clínica sin que se observe un incremento igual o superior al 15% en el FEV1. De hecho, múltiples estudios han demostrado que puede haber cambios en la resistencia de la vía aérea, en la conductancia específica, en la capacidad residual funcional o en el volumen residual, sin una mejoría paralela en los parámetros espirométricos. En estos pacientes el beneficio de un fármaco broncodilatador puede quedar enmascarado por el colapso de la vía aérea o por la compresión del gas intratorácico que se produce en una maniobra espiratoria forzada. En este sentido, Smith et al5 describieron que el 85% de los pacientes que no presentaron una mejoría significativa en los parámetros espirométricos tuvieron respuestas positivas cuando éstas se valoraron como cambios de volumen en maniobras no forzadas. En los casos con respuesta negativa, antes de decidir la exclusión de un tratamiento broncodilatador, es necesario tener en cuenta que existen pacientes con escasa respuesta broncodilatadora en los que es posible detectar una mejoría en la dificultad respiratoria, que se correlaciona con mejorías en la capacidad vital inspiratoria, MIF50%VC, resistencia específica de la vía aérea, y en el grado de atrapamiento aéreo.
2. Cuando la reversibilidad se valora con parámetros espirométricos, con frecuencia la respuesta se analiza tras una única prueba broncodilatadora realizada 10-15 min después de inhalar dosis bajas de simpaticomiméticos9, a pesar de que el pico de broncodilatación, tanto para los agonistas β2 de acción corta como para el ipratropio, ocurre a partir de los 30 min.
3. La respuesta broncodilatadora puede variar en diferentes períodos. La probabilidad de obtener una prueba broncodilatadora positiva es acumulativa, de manera que el 80% de los pacientes con EPOC puede tener una respuesta positiva si se realizan 3 tests independientes10. En un estudio clásico, Anthonisen y Wright11 demostraron que un 30% de los pacientes presentaba una respuesta positiva si el test se repetía, y un 68% tenía al menos una respuesta positiva en el curso de 7 pruebas broncodilatadoras.
4. La probabilidad de tener una respuesta broncodilatadora positiva o negativa dependerá del criterio que se utilice. Aunque la normativa GOLD establece una respuesta positiva cuando se produce un incremento en el FEV1 de 200 ml o del 12% del valor basal; este criterio varía notablemente en diferentes series y guías clínicas, con rangos que oscilan entre el 10 y el 20%. En la práctica, ninguno de estos índices tiene valores aceptables de reproducibilidad. De hecho, en una serie reciente con datos del estudio ISOLDE, la mitad de los pacientes clasificados inicialmente como reversibles con criterios American Thoracic Society/GOLD debieron ser reclasificados con los resultados de una nueva prueba broncodilatadora. Cuando se utilizó el criterio de la ERS, el porcentaje de reclasificación fue del 38%12. Por este motivo, no resulta sorprendente que la prueba bronco-dilatadora no permita valorar la eficacia a largo plazo del tratamiento con broncodilatadores con corticoides inhalados6,7.
5. Existe una notable controversia sobre cuál debe ser el fármaco utilizado para valorar la respuesta y la dosis que obtiene una respuesta máxima. Nisar et al13, estudiando a 127 pacientes con limitación crónica al flujo aéreo, encontraron un grado significativo de reversibilidad en el 56% de los pacientes cuando en la valoración de la reversibilidad se utilizaron dosis altas de β adrenérgicos inhalados y un ciclo de corticoides orales. Por este motivo, para que la valoración de una prueba broncodilatadora sea adecuada, es necesario utilizar una dosis mínima de 0,4 mg de salbutamol o una dosis equipotente de otro agonista β22.
Resulta sorprendente que, a pesar de que nadie discute la importancia de los anticolinérgicos en el tratamiento de la EPOC, habitualmente la prueba broncodilatadora se realice sólo con agonistas β2 de acción corta. De hecho, numerosos estudios han demostrado que en pacientes con EPOC estable, dosis bajas de ipratropio pueden producir más broncodilatación que los agonistas β2, aunque estos resultados no se han confirmado en otras series. De hecho, la heterogeneidad de la EPOC hace posible que un determinado paciente tenga una respuesta más favorable con uno de estos fármacos que con el otro. En otro estudio, Nisar et al3, en un grupo de pacientes con EPOC moderada-grave, observaron que cuando se utilizaban dosis elevadas de agonistas β2 e ipratropio era posible detectar con un solo test una respuesta positiva en el 66% de los pacientes. Repitiendo la prueba en diferentes días e incluyendo una prueba con esteroides era posible incrementar notablemente el número de respuestas positivas. Un aspecto importante de este estudio fue que, aunque aproximadamente un tercio de los pacientes respondió con ambos fármacos, un grupo de pacientes respondió con salbutamol pero no con ipratropio y otro grupo lo hizo con ipratropio pero no con salbutamol.
6. Cuando se quiera valorar la utilidad de los corticoides, especialmente de los inhalados (CI), una única prueba broncodilatadora con fármacos broncodilatadores, e incluso tras un tratamiento con un ciclo corto de corticoides, no permite predecir la eficacia de los CI a largo plazo14,15, por lo que es más adecuado valorar su eficacia analizando la respuesta directamente con CI durante un período mínimo de 6-12 semanas16.
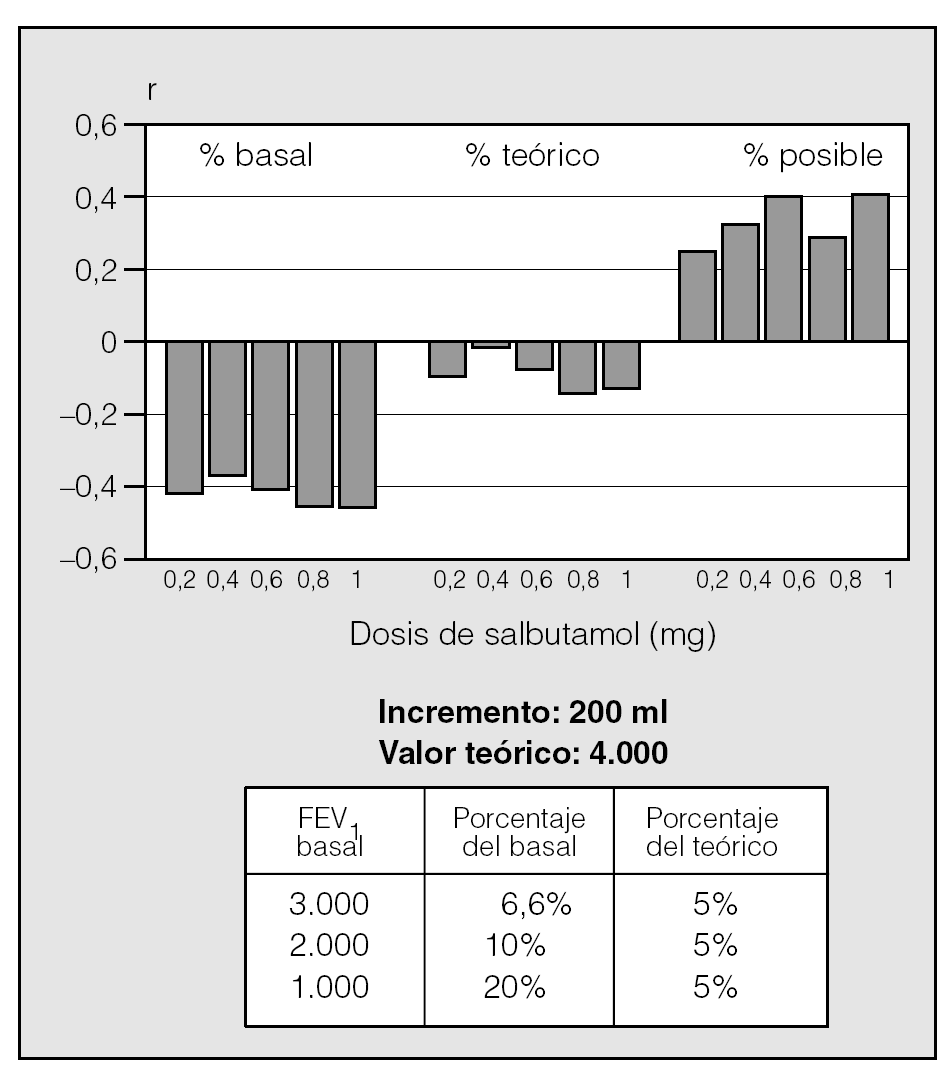
7. Se han descrito varios índices espirométricos para analizar la respuesta broncodilatadora en pacientes con EPOC, aunque el más difundido es el que valora el porcentaje de mejoría sobre el valor basal (post-pre/pre %). Esta forma de análisis sobrevalora la respuesta en pacientes con obstrucción más grave al flujo aéreo. De hecho, una reversibilidad de 200 ml en el FEV1 en un paciente con 3.000 ml de FEV1 supone un incremento del 6,6% del basal, pero en un paciente con un FEV1 de 1.000 ml éste es del 20%. Por este motivo, lo que es positivo cuando se considera un incremento respecto al porcentaje del basal puede ser negativo cuando se utiliza otro criterio de reversibilidad, como el porcentaje del teórico. Adicionalmente, cualquier punto de corte es arbitrario, y no pueden establecerse límites categóricos en una variable que tiene una distribución continua12.
Dompeling et al17, analizando diversos índices en un estudio con un período de seguimiento de 2 años, concluyeron que el porcentaje del posible y el porcentaje del "alcanzable", definido como una mejoría del FEV1 con respecto a la diferencia entre el basal y el máximo conseguido durante el estudio, son los índices más reproducibles y los que muestran un menor grado de dependencia de los valores basales.
Dada la conocida variabilidad del FEV1, cuanto peor resulta una primera medida, más probable será que una segunda la supere, y viceversa. Por este motivo, no se puede descartar que la dependencia que presentan los criterios de reversibilidad respecto al FEV1 inicial se deba a un fenómeno de regresión a la media. Sin embargo, dado que el uso del porcentaje del posible y del alcanzable resulta poco útil en la práctica clínica, y que otros estudios han demostrado que el porcentaje del teórico (post-pre/teórico %)2 también minimiza este posible error, siempre que se realice una prueba broncodilatadora en pacientes con EPOC los resultados deberían expresarse en valores absolutos y estandarizados para edad y talla, como porcentaje del teórico (fig. 1)18.
Fig. 1. En pacientes con EPOC, el incremento en el volumen espiratorio forzado en el primer segundo (FEV1) tras la administración de un fármaco broncodilatador presenta una importante dependencia del valor basal, que se mantiene con diferentes dosis de broncodilatador. Utilizar como criterio de reversibilidad el porcentaje del teórico este problema y permite valorar mejor el grado de broncodilatación con independencia de la obstrucción basal. Como puede verse en el ejemplo, un incremento de 200 ml en un paciente con un valor teórico de 4.000 ml puede interpretarse como positivo o negativo según el criterio utilizado. (Tomado de Fernández Francés e Izquierdo Alonso2.)
8. La finalidad de un test condiciona en gran medida cuál debe ser el criterio que debe utilizarse para valorar la respuesta broncodilatadora. Si, en vez de analizar el grado de reversibilidad, lo que se pretende es discriminar entre asma y EPOC, dada la típica variabilidad de la función pulmonar en el paciente asmático, debería elegirse un criterio reproducible e independiente de la función pulmonar. Sin embargo, los mecanismos que condicionan un aumento en el calibre de la vía aérea tras la administración de un fármaco broncodilatador son complejos4, y no existe una relación lineal entre el incremento de los flujos espiratorios y los cambios en la longitud del músculo liso de la vía aérea. Por este motivo, la prueba de broncodilatación discrimina mal el asma de la EPOC19, por lo que, salvo que se confirme la desaparición de la obstrucción, no debería utilizarse para establecer el diagnóstico diferencial entre ambas entidades. En ocasiones esta normalización no se consigue con una única prueba broncodilatadora, sino con un tratamiento más prolongado. Aunque con frecuencia se ha propuesto un límite del 15% para establecer el diagnóstico de asma o "bronquitis asmática", éste es el valor promedio de mejoría funcional obtenido por Anthonisen et al en un grupo de pacientes con EPOC en quienes cualquier diagnóstico de asma fue un criterio de exclusión11.
Como consecuencia de todas estas limitaciones, cuando se analiza la reversibilidad de la obstrucción con broncodilatadores y tratamiento antiinflamatorio es necesario valorar la respuesta con dosis adecuadas de agonistas β2 y de anticolinérgicos, esperar al menos 30 min para realizar la espirometría posbroncodilatador, medir en algunos casos cambios en los volúmenes con maniobras no forzadas (capacidad vital lenta, capacidad inspiratoria, capacidad residual funcional, etc.)20-22 y utilizar un criterio que sea poco dependiente de los valores basales. A pesar de ello, debemos ser conscientes de que la información que aporta una prueba broncodilatadora tiene una relevancia clínica muy limitada.
Bases teóricas para el uso de anticolinérgicos en la EPOC
En pacientes con EPOC, los mecanismos que conducen a la limitación crónica al flujo aéreo son múltiples. Algunos están relacionados con cambios destructivos y fibróticos que, en términos generales, son poco o nada reversibles con tratamiento farmacológico. Sin embargo, incluso en estos pacientes con escasa reversibilidad, es posible detectar algún grado de broncodilatación, que puede ser clínicamente relevante, especialmente en pacientes con obstrucción grave.
En sujetos sanos y en pacientes con EPOC, el tono colinérgico del sistema parasimpático ejerce un importante control sobre el calibre de la vía aérea. Este factor puede ser especialmente relevante en los pacientes con mayor obstrucción al flujo aéreo, ya sea porque, como han sugerido algunos autores23, el tono colinérgico aumenta a medida que lo hace la gravedad de la obstrucción, o porque la obstrucción producida por los cambios estructurales amplifica el efecto de la relajación-contracción del músculo liso sobre el diámetro de la vía aérea4. En pacientes con EPOC, el grado de contracción del músculo liso ante un estímulo dependerá de la magnitud del estímulo, de la longitud del músculo y su relación con la longitud óptima, y de la carga que debe superar pero, a diferencia de lo que puede observarse in vitro, el aumento del calibre de la vía aérea dependerá no sólo del grado de relajación del músculo liso sino también de factores geométricos (obstrucción basal) o de las características de la propia vía aérea.
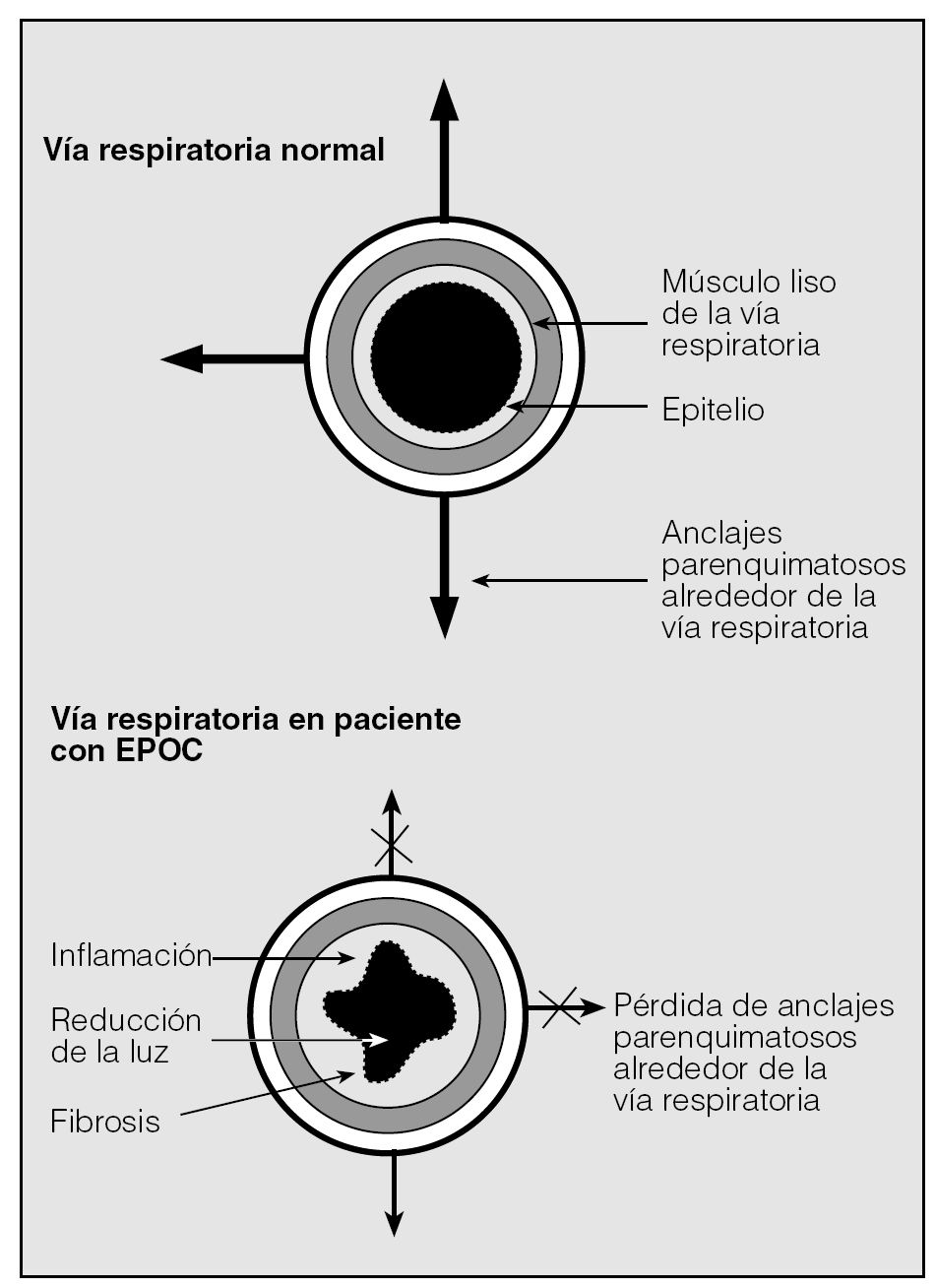
Dado que la resistencia al flujo aéreo es inversamente proporcional a la cuarta potencia del radio, pequeños aumentos en el radio de la vía aérea condicionan importantes reducciones de la resistencia, de manera que si el radio se duplica, la resistencia se reduce 16 veces. Además, en pacientes con EPOC, el grosor de la pared de la vía aérea por dentro de la capa del músculo liso será decisivo a la hora de amplificar la respuesta broncodilatadora con un fármaco o la respuesta broncoconstrictora frente a diversos estímulos. Cuando el engrosamiento de la pared por dentro de la capa muscular es del 20%, una relajación del músculo liso que condicione un alargamiento del 20% produce un descenso de la resistencia al flujo aéreo del 55%. Este mismo grado de alargamiento produce un descenso del 70% en la resistencia cuando el área de la pared de la vía aérea en dicha zona es de un 45%4. Esto es precisamente lo que ocurre en las vías aéreas de algunos pacientes con EPOC, en los que, debido a la presencia de un componente inflamatorio crónico, el grosor de la pared por dentro de la capa del músculo liso está aumentada. Por otro lado, la presencia de cambios patológicos por fuera de la capa muscular podría desacoplar la relación entre el músculo liso y las fuerzas elásticas y viscosas que, originadas por el parénquima pulmonar, actúan como "contrapeso", impidiendo que el músculo liso se contraiga excesivamente (fig. 2). Por este motivo, aunque tanto en sujetos sanos como en pacientes con EPOC existe un tono vagal colinérgico, en ausencia de afección apenas tiene repercusión funcional, pero puede ser decisivo en pacientes con obstrucción crónica al flujo aéreo.
Fig. 2. El engrosamiento de la pared bronquial por dentro de la capa muscular y la pérdida de anclajes parenquimatosos amplificarán la respuesta broncodilatadora para un mismo estímulo sobre el músculo liso. (Véase texto.)
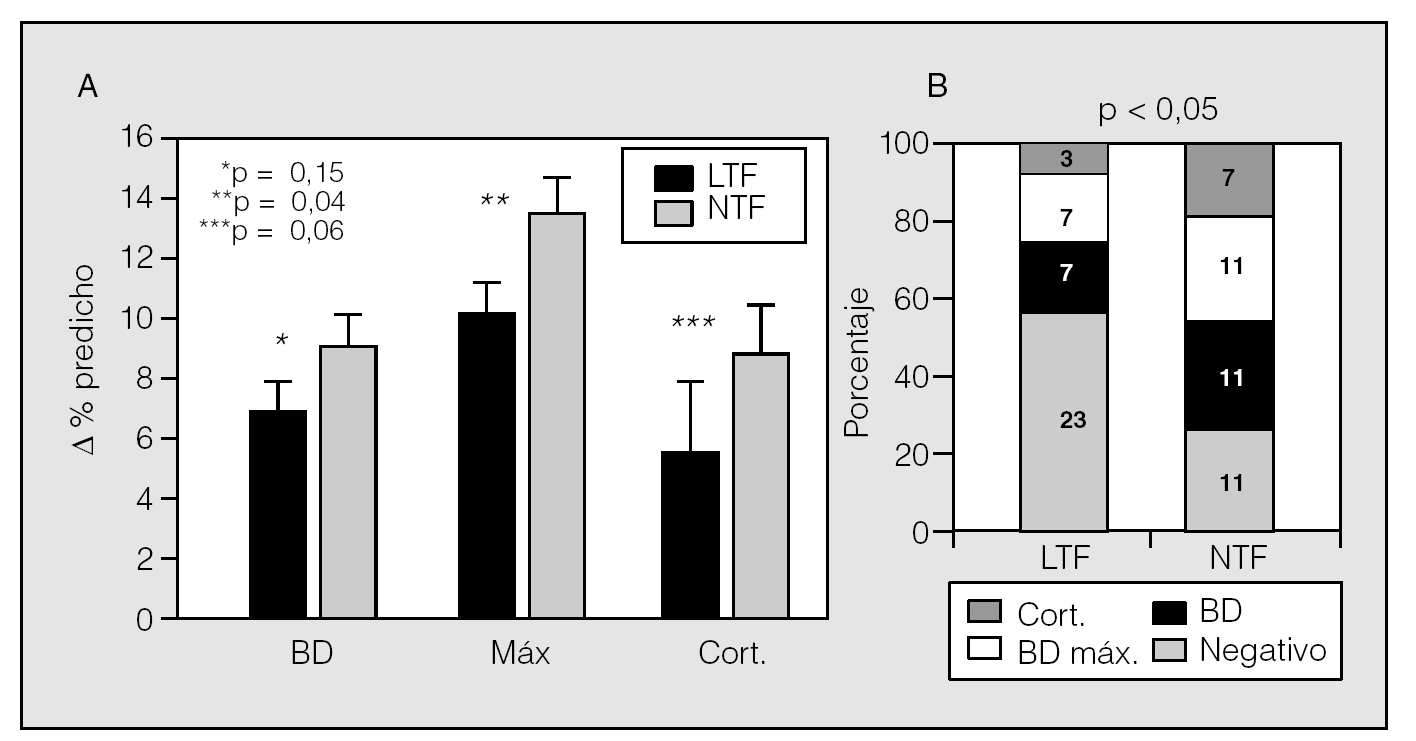
A diferencia de lo que ocurre en el asma, la EPOC engloba lesiones muy heterogéneas que afectan a las vías aéreas y al parénquima pulmonar, con un elevado grado de solapamiento (fig. 3). Esto hace que en estos pacientes la valoración de broncodilatación sea más compleja. De hecho, dada la importancia del tono vagal colinérgico, la valoración del grado de reversibilidad en pacientes con EPOC debería incluir el uso de anticolinérgicos en todos los casos. Además, hay que tener presente que, con frecuencia, los cuadros de broncoconstricción están mediados por mecanismos colinérgicos, por lo que un bloqueo de esta vía puede evitar su presentación. De este modo, en la EPOC los broncodilatadores pueden producir un efecto terapéutico favorable a través de su efecto broncodilatador, que puede valorarse sólo parcialmente con una prueba broncodilatadora, pero también por su efecto protector de la vía aérea frente a estímulos broncoconstrictores.
Fig. 3. La presencia de cambios destructivos en el parénquima pulmonar (LTF) reduce el grado de reversibilidad en relación con los pacientes con lesión fundamentalmente de vía aérea (NTF) (A). También se reduce la posibilidad de obtener una prueba broncodilatadora positiva con dosis estándar de broncodilatadores (BD), con dosis máximas de broncodilatadores (Máx.) o con corticoides (Cort.) (B). La presencia de diferentes grados y tipos de lesión parenquimatosa y/o sobre la vía aérea en diferentes pacientes impide establecer puntos de corte precisos para establecer fenotipos de EPOC en función de la respuesta broncodilatadora. (Tomado de Izquierdo Alonso et al8.) LTF: pacientes con test de difusión reducido; NTF: pacientes con test de difusión normal.
Broncodilatación con tiotropio
Los anticolinérgicos constituyen un tratamiento de primera línea en el tratamiento clínico del paciente con EPOC. Su uso no debe estar condicionado por el resultado de una prueba broncodilatadora, ya que este tipo de análisis no permite predecir el grado de mejoría clínica que se obtiene en un paciente (disnea, tolerancia al esfuerzo, etc.) o si esta mejoría se mantiene en el tiempo26. En la "vida real", puede haber pacientes con escasa reversibilidad en una prueba broncodilatadora en los que el uso de un broncodilatador permite mejorar los síntomas y la calidad de vida, y reducir las exacerbaciones. Por este motivo, desde un punto de vista asistencial, cualquier evaluación de la eficacia de un fármaco en pacientes con EPOC debería analizar su impacto en variables clínicamente relevantes, independientemente del grado de reversibilidad en la prueba broncodilatadora. Esta aproximación, cada vez más utilizada en los ensayos clínicos, no cuestiona el estudio del paciente con variables funcionales como el FEV1, pero en la valoración funcional deberían incluirse otros parámetros espirométricos obtenidos en maniobras más "fisiológicas", como la capacidad vital lenta o la capacidad inspiratoria. Además, para valorar correctamente un tratamiento es necesario analizar su eficacia durante un tiempo suficiente, determinando su impacto, no sólo en la función pulmonar sino también en los síntomas, en las actividades de la vida diaria y en la morbimortalidad.
En un estudio reciente Tashkin et al26 observaron que el 51% de los pacientes con criterios bien definidos de EPOC presentaron una respuesta broncodilatadora positiva (FEV1 ≥ 12% y ≥ 200 ml) con una dosis de 18 μg de tiotropio. Después de un año de seguimiento los pacientes tratados con tiotropio presentaron mejores valores de FEV1 y de FVC que aquellos tratados con placebo, con independencia de la respuesta inicial con la primera dosis de tiotropio. Esta mejoría se observó también en variables clínicas como el grado de disnea, la calidad de vida o la necesidad de medicación de rescate. De hecho, aunque es posible observar una cierta correlación entre la respuesta obtenida en una prueba broncodilatadora y los valores espirométricos tras un período prolongado de seguimiento, esta correlación es pequeña con la disnea y con la calidad de vida, lo que sugiere que los valores de función pulmonar obtenidos tras la administración de una dosis de fármacos broncodilatadores puede predecir (aunque sólo en parte) el grado de mejoría funcional que puede alcanzarse, pero no así del grado de mejoría en otras variables clínicamente muy relevantes26. Los resultados de este estudio son complementarios a los observados por Rennard et al27 que, analizando la eficacia de salmeterol (42 μg dos veces al día) y bromuro de ipratropio (36 µg cuatro veces al día) observaron que la mejoría con ambos fármacos fue superior frente a placebo en los parámetros funcionales (FEV1 valorado como área bajo la curva), tolerancia al esfuerzo (test de marcha de 6 min) y tiempo hasta la primera exacerbación, incluso en los pacientes que no habían respondido de forma positiva en la prueba broncodilatadora con salbutamol.
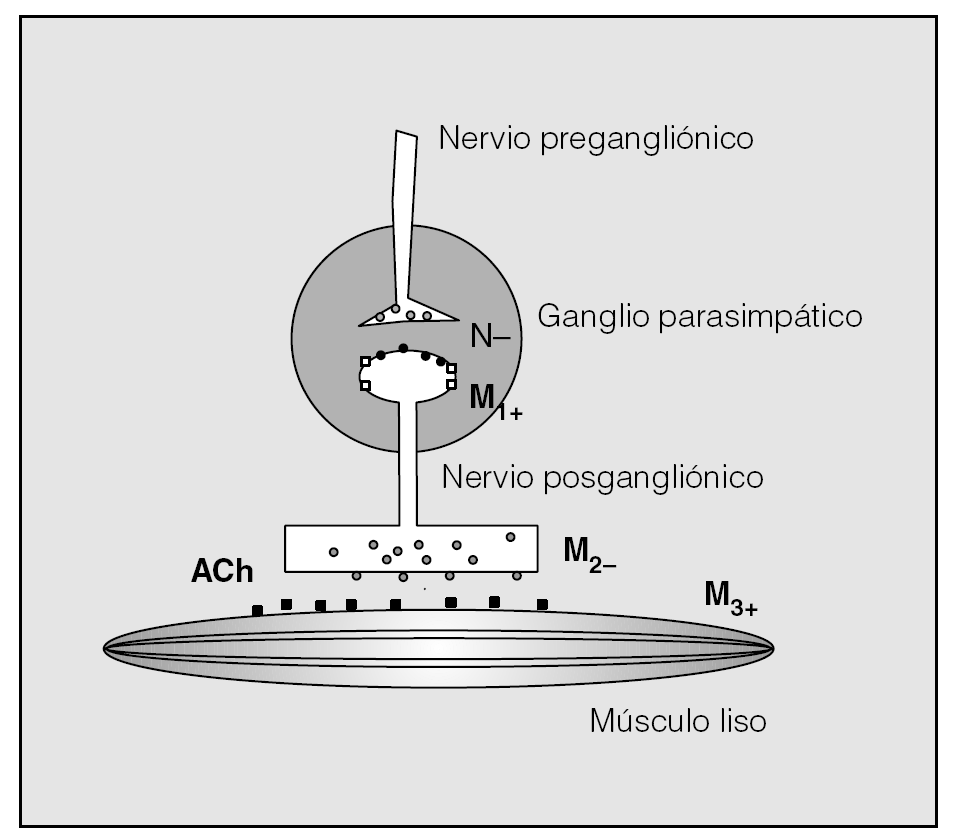
La principal limitación del bromuro de ipratropio es su corta vida media. Tras la administración de una dosis estándar el efecto del fármaco empieza a los pocos minutos, el 80% se alcanza a los 30 min y el efecto máximo a los 90-120 min, y su duración habitual es de 4-6 h. Por este motivo, es necesaria una administración continuada cada 6 h para mantener una broncodilatación sostenida. Además, se comporta como antagonista no selectivo, ya que produce un bloqueo, tanto presinápti-co (M2), como postsináptico (M3). Así, la activación de los receptores M2 hace que sea necesario liberar más acetilcolina tras un estímulo colinérgico, que puede sobrepasar el bloqueo postsináptico, haciendo que el an-tagonismo de los receptores M3 sea menos eficiente (fig. 4).
Fig. 4. Se conocen 5 subtipos de receptores muscarínicos, de los cuales al menos 3 participan en el control del calibre de la vía aérea7. a) Receptores M1: en la vía aérea, la transmisión pre-posgangliónica está mediada por la acetilcolina a través de receptores nicotínicos. Sin embargo, en este ámbito también existen receptores muscarínicos M1, cuyo bloqueo con antagonistas produce una inhibición de la contracción del músculo liso. b) Receptores M2: se localizan en las fibras presinápticas posganglionares de las vías aéreas. La activación de estos receptores inhibe la liberación de acetilcolina, limitando, por lo tanto, la contracción del músculo liso y posiblemente la secreción de las glándulas mucosas. Los antagonistas colinérgicos no selectivos pueden, en ocasiones, producir broncoconstricción actuando a través de los receptores M2. c) Receptores M3: tienen una localización postsináptica en el músculo liso de la vía aérea, en las glándulas submucosas y en los vasos sanguíneos. Su activación produce contracción del músculo liso, vasodilatación y secreción de mucosa.
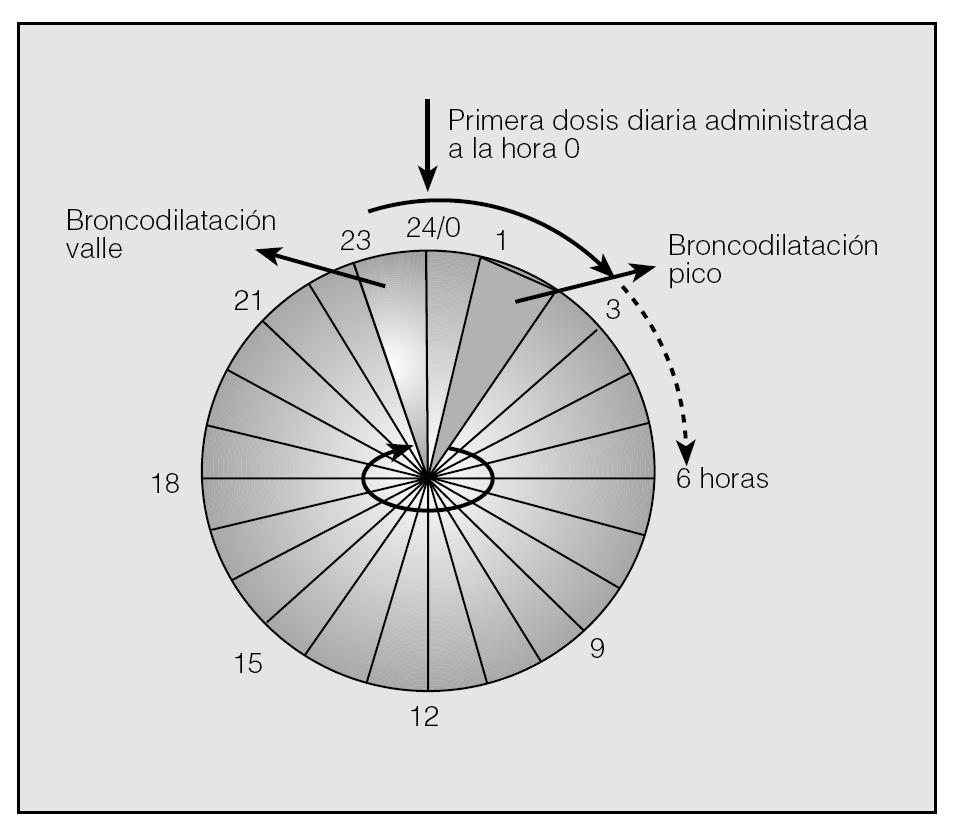
El tiotropio es un compuesto antimuscarínico que tiene una estructura con un amonio cuaternario, lo que le confiere algunas similitudes con el ipratropio, en especial su baja absorción sistémica, pero un efecto broncodilatador que se mantiene durante 24 h y un efecto broncoprotector que es posible confirmar durante más de 36-48 h. Su efecto prolongado y las características farmacológicas están relacionadas con su alta selectividad por los receptores M3 y con su lenta disociación en la unión con este receptor. El tiotropio es aproximadamente 10 veces más potente que el ipratropio en su unión a los receptores muscarínicos, y esta mayor potencia y duración permite no sólo alcanzar una mayor broncodilatación sino también mantenerla durante más tiempo, como lo confirman los valores obtenidos durante el período valle (fig. 5), lo que podría justificar una mayor eficacia clínica en pacientes con síntomas persistentes. Noord et al28 realizaron, en 288 pacientes con EPOC, un estudio comparativo entre 18 μg de tiotropio en dosis única diaria y 40 μg de ipratropio cada 6 h. En este estudio, el tiotropio produjo una mayor mejoría en el flujo espiratorio máximo, tanto matutino como nocturno, en el FEV1, y una menor necesidad de salbutamol de rescate, todo ello con una tasa de efectos secundarios similar.
Fig. 5. En tratamientos prolongados con broncodilatadores, además de valorar su eficacia en una prueba broncodilatadora estándar, el análisis del volumen espiratorio forzado en el primer segundo (FEV1) valle proporciona información sobre la duración del efecto del fármaco. En pacientes con síntomas persistentes, una broncodilatación sostenida puede tener una relevancia igual o superior que el pico máximo.
En todos los estudios realizados con tiotropio, la respuesta broncodilatadora favorable, valorada como mejoría en el FEV1, se confirmó con todas las dosis, aunque con una clara relación dosis-respuesta. Sin embargo, lo que realmente sitúa a este y otros fármacos en el tratamiento de la EPOC, no es sólo su pico de broncodilatación en una prueba estándar, sino los beneficios funcionales (tolerancia al esfuerzo, mantenimiento de la reversibilidad en período valle, etc.) y clínicos, que se traducen en un mejor control de estos pacientes, y que en el caso del tiotropio alcanzan su efecto máximo a los 8 días de tratamiento29,30.
Conclusión
La prueba broncodilatadora continúa siendo una técnica ampliamente extendida en el tratamiento del paciente con EPOC. De hecho, muchos médicos siguen condicionando el tratamiento en función de sus resultados. Sin embargo, las múltiples limitaciones que presenta cuestionan su utilidad en la EPOC. Además de los numerosos interrogantes teóricos para establecer si un test es positivo o negativo, estudios recientes12,31 no han demostrado una relación entre el cambio en el FEV1 en la prueba broncodilatadora y el grado de deterioro funcional. Tampoco se correlaciona con la eficacia del tratamiento con CI ni con broncodilatadores a largo plazo, tanto en las variables espirométricas como en otras más clínicas (calidad de vida, síntomas, exacerbaciones, tolerancia al esfuerzo, etc.).
Por todos estos motivos la prueba broncodilatadora puede ser una fuente de confusión en el tratamiento clínico de la EPOC, como lo ha sido durante muchos años a la hora de diseñar ensayos clínicos en estos pacientes. De hecho, actualmente en Estados Unidos el grado de reversibilidad ya no es un criterio de selección para la inclusión de pacientes con EPOC en ensayos clínicos, pero lo sigue siendo en Europa, donde se genera un sesgo importante a la hora de valorar la eficacia de cualquier medida terapéutica. En la actualidad, la valoración de la broncodilatación en la EPOC debería centrarse en buscar variables con mayor valor predictivo y en analizar la eficacia del tratamiento sobre variables que tengan un impacto en la evolución clínica del paciente, ya que en contra de lo que postula la normativa GOLD16: a) la prueba broncodilatadora estándar tiene una escasa utilidad clínica en el paciente con EPOC si se realiza en una sola ocasión; b) no permite establecer el diagnóstico diferencial con el asma (salvo que normalice la función pulmonar); c) no permite establecer la mejor función pulmonar posible (que puede requerir tratamientos más prolongados); d) carece de valor pronóstico, y e) no debe servir para guiar decisiones clínicas.