El tratamiento oncológico basado en la inmunoterapia ha supuesto una revolución en el tratamiento de algunas neoplasias, y son cada vez más los tumores que se benefician de su uso. Los inhibidores de los puntos de control inmunitario (ICIs) como los anticuerpos monoclonales contra la proteína de control PD-1, estimulan el sistema inmune favoreciendo el ataque contra las células tumorales1. Pero, por otra parte, provocan el aumento de reacciones inmunitarias contra el tejido propio provocando efectos adversos, entre los que destacan los respiratorios.
Se presenta un caso de melanoma metastásico que desarrolló neumonía organizativa fibrinosa aguda (NOFA) asociada al tratamiento con pembrolizumab, un efecto adverso no descrito previamente en la literatura.
Varón de 61 años, exfumador desde hace 10 años, con un consumo acumulado de 90 paquetes/año, sin antecedentes respiratorios. Fue diagnosticado de un melanoma nodular ulcerado en región escapular, que se extirpó con márgenes ampliados en octubre de 2019. En octubre de 2020 comenzó tratamiento con pembrolizumab por progresión subcutánea.
Tras siete meses en tratamiento con pembrolizumab acudió a urgencias por tos seca, disnea de un mes de evolución hasta hacerse de mínimos esfuerzos y molestias torácicas opresivas. Se encontraba afebril, eupneico, con SatO2 94%, con acropaquias incipientes en dedos de las manos y auscultación pulmonar con crepitantes bilaterales.
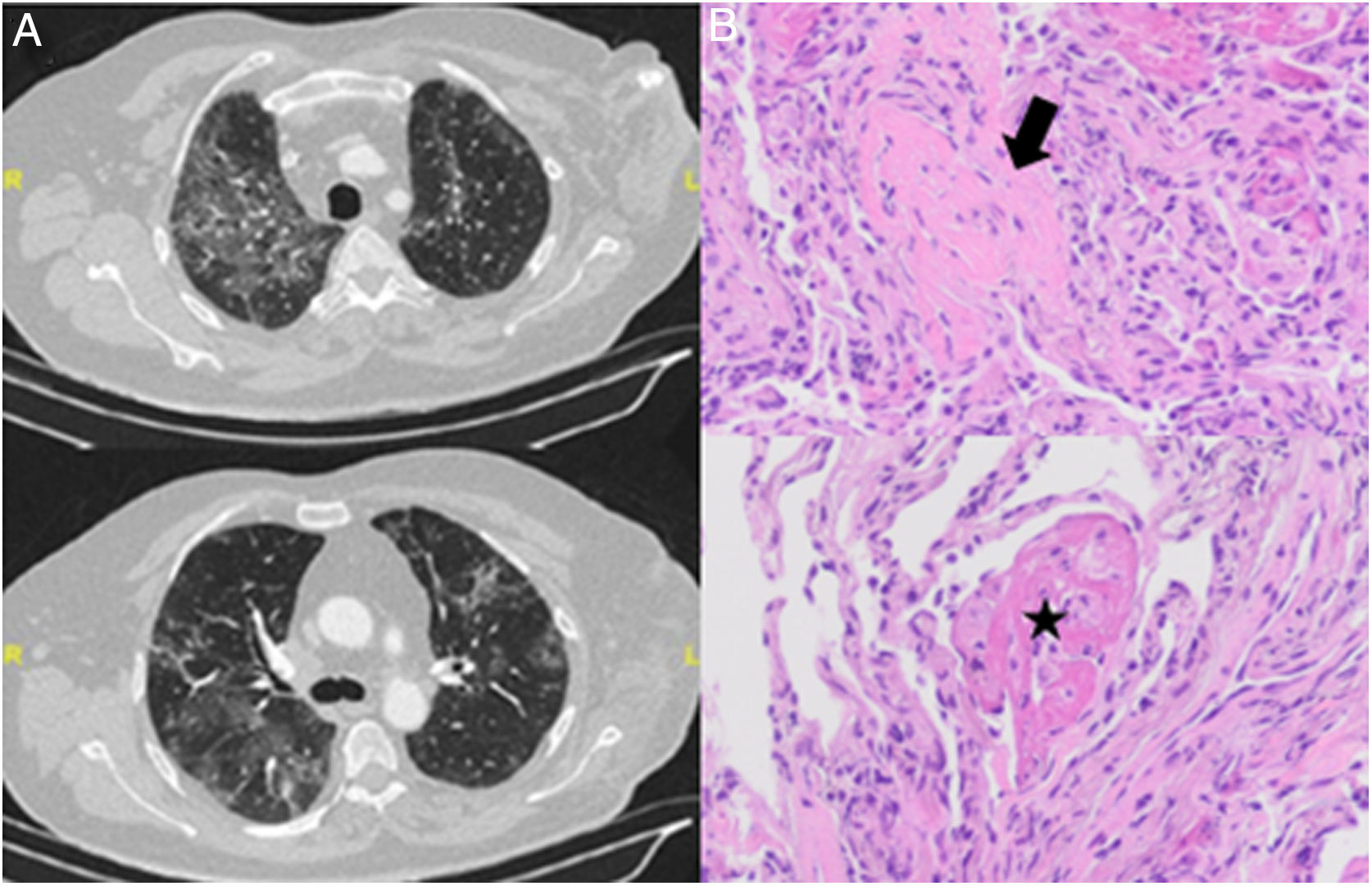
En la radiografía de tórax se objetivó un patrón intersticial bilateral de predominio en campos medios e inferiores. En la tomografía computarizada (TC) se objetivaron infiltrados pulmonares bilaterales extensos con vidrio deslustrado de nueva aparición (fig. 1A).
A) Cortes de TC torácica que muestra infiltrados bilaterales en vidrio deslustrado. B) Muestra de biopsia transbronquial con tinción hematoxilina-eosina con presencia de neumonía organizativa en forma de cuerpos de Masson (flecha) junto con agregados («bolas») de fibrina en organización (estrella). Con ausencia de membranas hialinas e hiperplasia de neumocitos tipo 2 y leve infiltrado inflamatorio intersticial.
En la analítica no presentaba alteraciones relevantes, con IgG específicas normales y espirometría con restricción leve (capacidad vital forzada [FVC] 78%) y descenso leve de la difusión (difusión pulmonar de monóxido de carbono [DLCO] de 65%).
Se realizó fibrobroncoscopia con broncoaspirado y lavado broncoalveolar, sin evidencia de malignidad ni gérmenes oportunistas, así como alveolitis linfocitaria con CD3 51% y cociente CD4/CD8 de 0,36. En la histología de la biopsia transbronquial, se identificó un patrón de neumonía organizativa con focos de NOFA (fig. 1B).
Se inició tratamiento con metilprednisolona 1 mg/kg y se suspendió la inmunoterapia con buena respuesta clínica. Fue dado de alta, con pauta descendente de prednisona y con realización de tomografía computarizada de alta resolución (TCAR) de control al mes, que mostraba desaparición casi por completo de las opacidades pulmonares.
Entre los efectos adversos respiratorios secundarios al uso de ICIs destacan la neumonía organizada (NO), el daño alveolar difuso (DAD), las reacciones granulomatosas sarcoidosis-like, la neumonía eosinofílica (NE) o la NOFA2.
Histológicamente, la NOFA se caracteriza por la presencia de bolas de fibrina intraalveolares y neumonía organizativa con una distribución parcheada y sin membrana hialina, lo que lo diferencia de la NO, en la que no encontramos depósito de fibrina o del DAD que presenta tanto fibrina como membranas hialinas. En la NE destaca el elevado número de eosinófilos3.
Solo un 10,6% de casos de NOFA son secundarios a fármacos, los más frecuentes con abacavir o amiodarona4, con un solo caso descrito con ICIs (nivolumab)5.
En conclusión, es importante vigilar estos efectos adversos, cada vez más frecuentes debido al mayor uso de ICIs. Además, es fundamental la toma de biopsias para el diagnóstico de NOFA, pues apenas hay descritos casos secundarios al uso de ICIs, ninguno secundario al pembrolizumab hasta ahora.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.