Un niño de 4 años de edad fue ingresado por un episodio de infección respiratoria febril aguda caracterizada por rinitis y tos. El paciente presentaba disnea intensa, taquipnea (60 respiraciones/min) y una reducción bilateral del murmullo vesicular con crepitantes difusos. La saturación de oxígeno (SaO2) con el empleo de 4l/min de O2 era del 93% y no se observó respuesta alguna al tratamiento con agonistas beta inhalados. Se administró al paciente claritromicina, amoxicilina-ácido clavulánico y dexametasona, pero su estado se agravó rápidamente, con un aumento del trabajo respiratorio y aparición de un enfisema subcutáneo. El paciente fue trasladado a la unidad de cuidados intensivos de nuestro hospital pediátrico.
Se trataba de un niño nacido a término y sin complicaciones posnatales; había estado completamente bien hasta ese episodio y no tenía antecedentes familiares de enfermedades respiratorias.
A la exploración, el paciente continuaba presentando disnea y la SaO2 era del 92% con 7l/min de O2.
Los análisis de laboratorio mostraron una anemia leve (10,3g/dl) y un recuento leucocitario elevado (18.470/mm3 con un 70% de neutrófilos). La proteína C reactiva, los niveles de inmunoglobulinas, los electrólitos en sangre, la creatinina sérica y las pruebas de la función hepática eran normales.
La radiografía de tórax reveló un engrosamiento tosco del patrón intersticial, múltiples áreas radiotransparentes a causa del enfisema intersticial y opacidades parenquimatosas en el campo medio-basal del pulmón izquierdo.
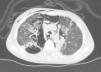
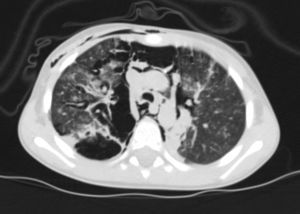
La tomografía computarizada del tórax mostró un neumomediastino difuso con enfisema subcutáneo (fig. 1).
Se colocó un catéter venoso central, para el apoyo nutricional del paciente y para el manejo del tratamiento intravenoso; se mantuvo el aporte de oxígeno, al tiempo que se iniciaban tratamientos antibióticos, antifúngicos, antivirales y antiinflamatorios (corticoides en dosis altas e inmunoglobulinas intravenosas) de forma empírica, a la espera de los resultados de laboratorio. En los hemocultivos y los cultivos de muestras de aspirado hipofaríngeo no crecieron gérmenes. Se descartó una inmunodeficiencia. Las pruebas de VIH y CMV fueron negativas.
La prueba del sudor fue normal.
Durante la hospitalización, el estado respiratorio mejoró y el paciente fue dado de alta a los 10 días con una exploración física normal.
Una semana después, una revisión de seguimiento mostró un buen estado clínico, una normalización del equilibrio ácido-base y una saturación de oxígeno del 98% respirando aire ambiental.
En la radiografía de tórax el neumomediastino se había resuelto por completo.
Después de 2años de seguimiento, el niño mantenía un crecimiento normal. La exploración física no mostró signos de una enfermedad significativa, no se observaron dedos en palillo de tambor y la SaO2 fue del 99% respirando aire ambiental; no se realizó una radiografía de tórax de control porque los padres no dieron su consentimiento.
El precedente de una asociación entre mutaciones de genes de proteínas surfactantes y la neumopatía intersticial más leve1-4 nos llevó a evaluar en este paciente posibles mutaciones genéticas asociadas a un déficit de surfactante.
Las pruebas genéticas para las proteínas surfactantes SPB y SPC no mostraron ninguna variante, pero se observó que el paciente era heterocigoto compuesto para dos variantes de ABCA3: las sustituciones c.863G>A (p.Arg288Lys) y c.875A>T (p.Glu292Val). La sustitución Arg288Lys se ha asociado anteriormente a un síndrome de dificultad respiratoria mortal. Se indicó que afectaba al primer bucle extracelular, que se cree que interviene en las interacciones extracelulares5 y ejerce, por tanto, un efecto grave sobre la función proteica. La sustitución Glu292Val de sentido erróneo se ha descrito de forma asociada a la neumopatía intersticial pediátrica (NIP)2. Basándose en la observación de la mutación Glu292Val en múltiples pacientes con un fenotipo más leve de lo que antes se había apreciado, los autores sugirieron la posibilidad de una correlación genotipo-fenotipo. Demostraron la presencia de una alteración del metabolismo del surfactante en los pacientes con NIP, aun cuando llegaron a la conclusión de que serían necesarios nuevos estudios sobre la histopatología específica asociada a las mutaciones de ABCA3 para una clasificación más exacta. Además, se han propuesto también otras variables genéticas y ambientales importantes para modificar el curso de la enfermedad.
Aun cuando el neumomediastino pueda ser consecuencia de crisis asmáticas, casi nunca se ha descrito durante la bronquitis aguda. El primer caso descrito de neumomediastino grave asociado a mutaciones del gen ABCA3 aporta una nueva evidencia de la variabilidad fenotípica. En la actualidad no podemos predecir la correlación exacta entre las variantes génicas, su efecto combinado y su interacción con otros factores genéticos o ambientales y las manifestaciones clínicas. La mala función de la proteína surfactante puede no solo causar una neumopatía intersticial más leve en los niños sino favorecer también la lesión alveolar, la fuga intersticial y el neumomediastino durante los episodios infecciosos agudos. Serán necesarios más datos para delimitar mejor el mecanismo patogénico que subyace en el espectro clínico del déficit de surfactante. Podría obtenerse una mejor correlación entre genotipo y fenotipo mediante la determinación de la incidencia de las mutaciones del gen ABCA3 en la enfermedad pulmonar.