La dificultad en la desconexión definitiva de la ventilación mecánica y la decanulación tras una ventilación prolongada es bien conocida. La mayoría de los pacientes tienen un destete simple (70%), un 15% un destete difícil y otro 15% un destete prolongado1,2. A este último grupo es importante proporcionarles un manejo global y especializado.
Presentamos el caso de una mujer de 50años ingresada en la unidad de cuidados intensivos (UCI) durante mes y medio tras la resección quirúrgica de una malformación arteriovenosa occipital. Ante la dificultad para el destete en esta unidad, la paciente se trasladó a una unidad de cuidados intermedios respiratorios (UCIR), llevándose a cabo el siguiente protocolo de destete de ventilación mecánica y decanulación3:
Fase 1. Evaluar la situación global
La paciente tuvo una permanencia prolongada en la UCI a causa de un cuadro de epilepsia focal de difícil control tras la cirugía que condicionó una conexión prolongada a ventilación mecánica invasiva (VMI), con realización de traqueotomía quirúrgica a las dos semanas. Como complicaciones presentó una neumonía asociada a VMI4 y una polineuromiopatía grave del enfermo crítico5. Precisó de presiones positivas al final de la espiración (PEEP) elevadas (20-25cmH2O) para mantener un adecuado reclutamiento alveolar. A su llegada a la UCIR se encontraba en situación de dependencia total del respirador, con ventilación en modo presión soporte (PS) (PEEP:12, PS:8, FiO2: 60%).
Fase 2. Evaluar la viabilidad de la ventilación espontánea
Se observó un fracaso de la prueba de ventilación espontánea derivada de un bajo drive respiratorio, una malacia severa con imposibilidad de disminuir la PEEP por colapso, una ausencia de esfuerzo tusígeno y una disfunción diafragmática grave, confirmada mediante ecografía torácica6,7. Se iniciaron técnicas de aclaramiento mucociliar con fisioterapia respiratoria, cambios posturales, sistemas de humidificación activa dirigido a reducir la viscosidad de las secreciones y aspiración de las mismas de forma periódica, 2-3veces cada 8h, utilizando una sonda de aspiración de 12CH8,9.
Fase 3. Elección del modo con ventilación
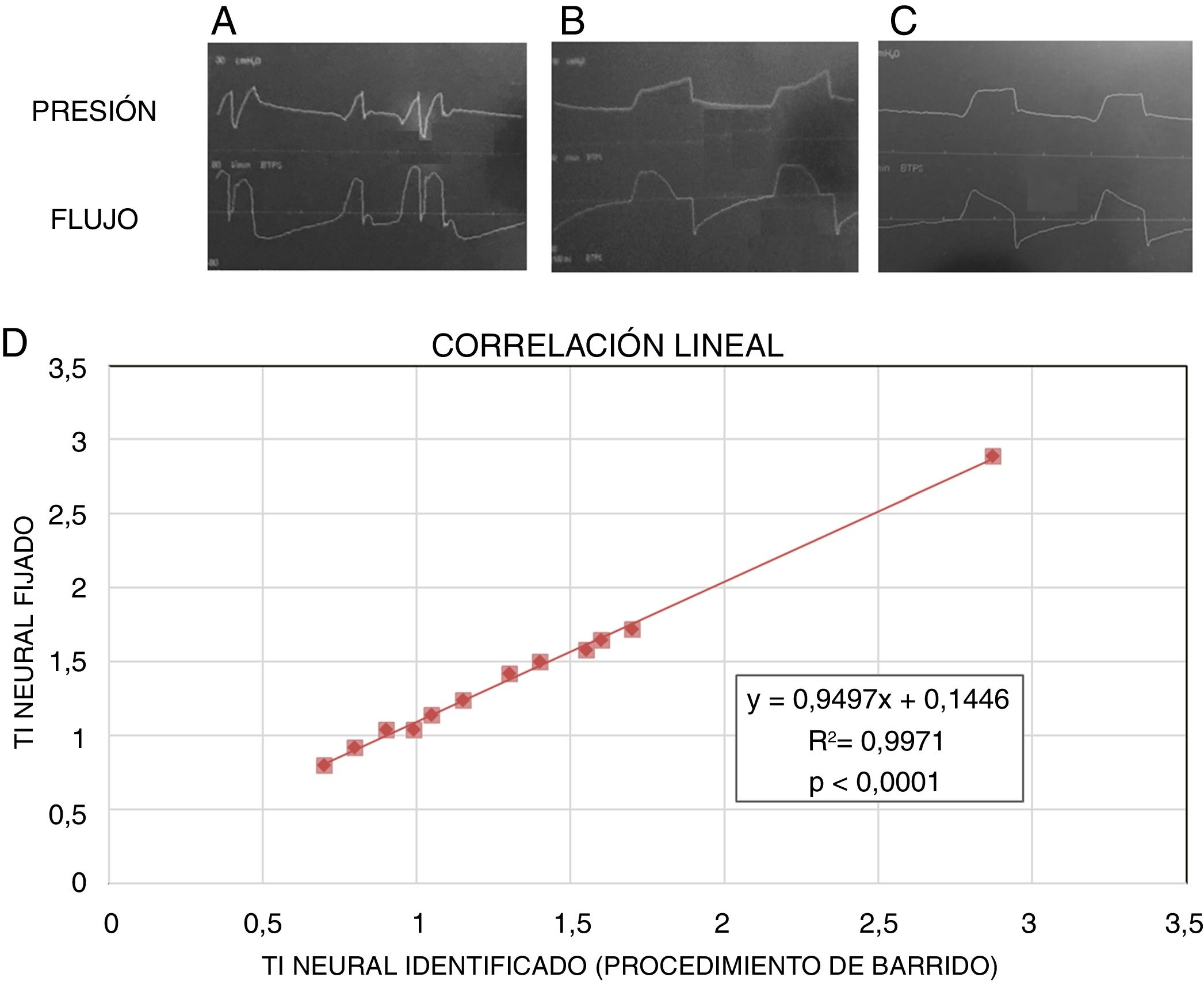
Por lo mencionado anteriormente, se decidió cambiar a modo presión control hasta mejoría del drive respiratorio, necesitando establecer un tiempo inspiratorio (Ti) fijo que se acoplase al Ti neural del paciente10. Con el objetivo de evitar asincronías (inspiraciones prolongadas y dobles trigger) se realizó el procedimiento de barrido, consistente en aumentar y/o disminuir el Ti del respirador hasta encontrar el que mejor se ajuste al paciente (fig. 1A-C).
Procedimiento de barrido para calcular el tiempo inspiratorio (Ti) neural. A)Ti neural mayor que el Ti del ventilador, objetivándose asincronía del tipo doble trigger. B)Ti neural menor que el Ti del ventilador, objetivándose asincronía del tipo inspiración prolongada. C)Ti ajustado con correcto acoplamiento al ventilador. D)Correlación lineal entre el Ti neural y Ti ajustado obtenido con el método de barrido.
Además de la fisioterapia motora y respiratoria, para abordar el problema de la disfunción diafragmática se realizaron sesiones de entrenamiento muscular diafragmático, conectando al paciente durante periodos breves de tiempo a un trigger de presión incremental, dado que este ha demostrado aumentar la carga mecánica frente a los trigger de flujo11. Tras varias sesiones se objetivó una mejoría en la excursión diafragmática, un mayor drive respiratorio y un incremento en la potencia para la tos. Dado el avance clínico y mecánico se decidió progresar y retomar la ventilación en modo presión soporte.
Fase 4. Valorar la integridad de la tráquea realizando test de fugas
Se realizó un test de fugas12 con resultado positivo, mostrando una diferencia del volumen tidal espirado mayor de 130ml.
Fases 4-7: Cambio de cánula y cierre progresivo de la misma
Inicialmente se procedió al cambio por una cánula con fenestra y se realizaron cierres de la misma durante 1-2h. Durante el periodo de cierre se utilizaron gafas de alto flujo, por sus ventajas para controlar la malacia y disminuir las resistencias de la vía aérea. De forma paralela a la mejoría clínica, fue disminuyendo la necesidad de aspirar secreciones hasta alcanzar una tos eficaz.
Fases 8-11. Colocación de hemicánula, cierre y retirada
Tras comprobar la tolerancia al cierre de la cánula durante periodos superiores a 4-6h y confirmar la adaptación y la eficacia a la ventilación mecánica no invasiva (VMNI), se procedió a colocar una hemicánula con tapón, la cual fue retirada a los 3-4días ante la ausencia de complicaciones. Tras finalizar con éxito la aplicación del protocolo, la paciente fue trasladada al Servicio de Neurocirugía, manteniendo sesiones de VMNI sin nuevas incidencias.
El método de barrido utilizado en este caso no está descrito en la literatura científica, por lo que se ha realizado una simulación a doble ciego de este procedimiento. Para ello se utilizó un simulador de pulmón13, al que un primer operador fija un Ti neural y un segundo operador ventila el simulador en modo presión control y realiza el método de barrido para hallar el Ti neural. El procedimiento se repite con diferentes Ti neurales (n=12). La correlación por el método de regresión lineal simple entre los dos Ti fue R2=0,9, con p<0,0001 (fig. 1D). De acuerdo con este resultado, pensamos que este procedimiento permite abrir una novedosa ventana al control neural de la ventilación en los modos controlados.
Además, planteamos la posibilidad de utilizar el alto flujo durante los cierres con traqueotomía para gestionar la malacia traqueal, dadas sus ventajas en la presurización de la vía aérea superior14.
Describimos también una nueva modalidad de entrenamiento diafragmático basado en el uso del trigger de presión, abandonado en la práctica habitual por el incremento del trabajo respiratorio frente al de flujo. Sin embargo, en nuestro paciente aprovechamos este efecto para entrenar el músculo diafragmático, monitorizar su actividad mediante ecografía y controlar así el riesgo de fatiga muscular (esfuerzo ineficaz).
Como conclusiones, destacamos la relevancia del uso del método de barrido en el control neural de la ventilación y resaltamos la importancia de disponer de un entorno altamente especializado donde poder aplicar un protocolo exhaustivo para el manejo de pacientes con problemas respiratorios de alta complejidad, como es el del destete prolongado.