En las últimas 2 décadas la tuberculosis con resistencia a fármacos se ha convertido en una amenaza y un reto para la salud pública mundial. El diagnóstico y el tratamiento de estas formas de tuberculosis es mucho más complejo, y el pronóstico empeora claramente a medida que se incrementa el patrón de las resistencias. Sin embargo, es necesario destacar cómo con el manejo clínico y programático adecuado de estos enfermos se puede conseguir la curación de una mayoría de ellos.
En esta normativa se razonan las bases del diagnóstico y tratamiento de todos los pacientes afectos de tuberculosis, desde aquellos que tienen formas de la enfermedad con sensibilidad a todos los fármacos hasta aquellos que son portadores de los patrones más extensos de resistencia. Asimismo, se dan recomendaciones específicas para cada uno de estos supuestos. También se aborda el papel que ya están teniendo y pueden tener en un futuro inmediato los nuevos métodos moleculares de detección de resistencias, los esquemas acortados de tratamiento de la tuberculosis multi-farmacorresistente (TB-MDR) y los nuevos fármacos con actividad frente a Mycobacterium tuberculosis.
In the last 2 decades, drug-resistant tuberculosis has become a threat and a challenge to worldwide public health. The diagnosis and treatment of these forms of tuberculosis are much more complex and prognosis clearly worsens as the resistance pattern intensifies. Nevertheless, it is important to remember that with the appropriatesystematic clinical management, most of these patients can be cured.
These guidelines itemize the basis for the diagnosis and treatment of all tuberculosis patients, from those infected by strains that are sensitive to all drugs, to those who are extensively drug-resistant. Specific recommendations are given forall cases. The current and future role of new molecular methods for detecting resistance, shorter multi-drug-resistant tuberculosis regimens, and new drugs with activity against Mycobacterium tuberculosis are also addressed.
Tras décadas en las que la tuberculosis (TB) se había transformado en una enfermedad curable en la práctica totalidad de los casos, la aparición de cepas de M. tuberculosis con resistencia a los fármacos (TB-DR) más activos disponibles la han convertido, nuevamente, en una gran amenaza y un reto para la salud pública mundial1. Pero es necesario destacar que todos los enfermos afectos de TB tienen una probabilidad muy importante de curarse, aunque sean portadores de TB con patrones extensos de resistencias, si se garantiza el acceso a un diagnóstico y tratamiento adecuados. El manejo clínico y programático de estos casos es esencial en esta posibilidad de éxito2–9.
La situación actual de la TB multi-farmacorresistente (TB con resistencia, al menos, a H+R, TB-MDR) en el mundo es preocupante, y la respuesta global muy deficiente1,10. Se estima que el 3,9% de los casos nuevos de TB en el mundo padecen TB-MDR, porcentaje que asciende al 21% en los enfermos previamente tratados1. De los 10,6 millones de casos estimados de TB en el año 2015 (1,8 millones de muertes), alrededor de 580.000 podían estar afectos de tuberculosis con resistencia a la rifampicina (TB-RR)/MDR, de los que pudieron morir alrededor de 250.000 personas1. Pero solo menos de 150.000 casos (26% de los estimados) fueron notificados a nivel mundial, con una tasa de curación del 52%1. O sea, que solo se consiguió curar el 10% de los enfermos estimados de TB-MDR en el mundo, respuesta absolutamente ineficaz para controlar la epidemia.
En España, aunque la situación de la TB-MDR es difícil de precisar (subregistro de casos de TB y la no realización sistemática de antibiograma), parece que la situación es más favorable, con un porcentaje de casos de TB-MDR primaria del 0,1% en autóctonos y del 2,2% en inmigrantes, y resistencia primaria a H en 3,4% y 10,2% respectivamente11,12.
Diagnóstico de la tuberculosis con resistencia a fármacosLa base del diagnóstico de la TB sigue recayendo en la sospecha clínica, en la radiología y en las pruebas microbiológicas13. La clínica y la radiología de la tuberculosis con resistencia a fármacos (TB-DR) son indistinguibles de la TB con sensibilidad a fármacos. Por lo tanto, el diagnóstico de la TB-DR debe ser siempre microbiológico y/o molecular6,14,15.
Estudio de sensibilidad a fármacosEn la actualidad, en nuestro país, se debe recomendar que a todo paciente con TB se le realice cultivo y estudio de sensibilidad, como mínimo a isoniacida (H) y rifampicina (R), tanto a enfermos nunca tratados como a los que tienen algún factor de riesgo de TB-DR (tabla 1)3,6,16,17 (recomendación fuerte, alta calidad de evidencia [⊕⊕⊕⊕]).
Factores de riesgo de ser portador de una tuberculosis con resistencia a fármacos3,6,16
| Factores de riesgo elevado |
| Pacientes previamente tratados para TB, especialmente los fracasos a esquemas terapéuticos previos, pero también las recaídas y los abandonos recuperados. |
| Conviviente o contacto íntimo de un paciente que tiene una TB-MDR |
| Factores de riesgo moderado |
| Pacientes con baciloscopia positiva al final del segundo mes con el tratamiento inicial (HRZE) y en los que no se conoce la sensibilidad inicial a fármacos |
| Pacientes procedentes de países con tasas elevadas de TB-MDR inicial |
| Pacientes que viven en instituciones cerradas, como cárceles o albergues donde haya habido casos deTB-MDR |
| Personal sanitario, especialmente aquellos que atienden casos con TB-MDR |
| Pacientes con comorbilidades que puedan conllevar situaciones de malabsorción |
| Infección por VIH |
Si se demuestra resistencia a R, este estudio de sensibilidad se debe extender a la fluoroquinolona (FQ) y al fármaco inyectable de segunda línea (FISL) que se vaya a utilizar en el tratamiento de rescate que se va a ofrecer al enfermo6 (levofloxacino [Lfx]/moxifloxacino [Mfx] y amikacina [Am]/capreomicina [Cm] en el caso de España) (recomendación condicional, moderada calidad de evidencia [⊕⊕
]).La fiabilidad clínica del resultado de una prueba de sensibilidad convencional a todos estos fármacos es muy buena y, por lo tanto, debe orientar en la pauta de tratamiento a recomendar. Por el contrario, la credibilidad clínica de una prueba de sensibilidad a otros fármacos como etambutol (E), pirazinamida (Z), etionamida/protionamida (Eth/Pth), cicloserina (Cs), ácido paraaminosalicílico (PAS), o clofazimina (Cfz) es significativamente inferior y, con frecuencia, pueden confundir más que ayudar en la decisión del posible régimen de tratamiento que necesita el enfermo, por lo que no se recomienda testarlos de rutina, o que en el caso de realizarlos, sus resultados sean tomados con la cautela correspondiente5,6,18 (recomendación condicional, baja [⊕
] a muy baja [] calidad de evidencia).Pruebas de sensibilidad a fármacos fenotípicas y genotípicasLas pruebas de sensibilidad pueden realizarse por métodos fenotípicos o genotípicos. Las primeras precisan micobacterias en fase de crecimiento activo en los medios de cultivo, por lo que los resultados se demoran un mínimo de 2-3 semanas si se utilizan medios líquidos, y hasta 4-8 semanas en el caso de los medios sólidos6. Puede ser un tiempo excesivo en la decisión del tratamiento ideal que debe recibir el enfermo.
Por el contrario, las pruebas moleculares permiten disponer de resultados en 24-48horas, al detectar por técnicas de amplificación genética mutaciones en los genes que codifican la resistencia a fármacos anti-TB. Por este motivo, si el centro tiene acceso a alguna de estas pruebas moleculares se recomienda que se les realice a todos los enfermos diagnosticados de TB (recomendación fuerte, alta calidad de evidencia [⊕⊕⊕⊕]).
Técnicas moleculares específicas: Xpert MTB/RIF (Cepheid) y GenotypeMDRplus (Hain)De entre estas técnicas moleculares es necesario resaltar el Xpert MTB/RIF (Cepheid) que puede detectar resistencia a R en un plazo de 2horas, con una sensibilidad del 95% y una especificidad del 98%14,17. Además, es mucho más sensible que la baciloscopia (es positivo hasta en el 70-90% de los casos con baciloscopia negativa y cultivo positivo), por lo que también supone un avance importante en la detección precoz. Y también el GenotypeMDRplus (Hain) o ensayo de prueba en línea (Line Probe Assay), que puede detectar simultáneamente mutaciones en los genes que codifican resistencia a isoniacida (katG e inhA) y rifampicina (rpoB) en un plazo de 6-24horas19,20.
Ambas técnicas moleculares pueden realizarse en muestra directa, sin que sea necesario esperar al crecimiento en el cultivo. El significado clínico que puede tener la mutación en el gen inhA y/o en el gen katG en la recomendación de utilizar H a pesar de su probada resistencia se detalla en la versión online de esta normativa21–28.
Por otra parte, la versión del ensayo de prueba en línea denominada GenotypeMDRsl (Hain) versión 2, permite detectar resistencia a las FQ (presencia de mutaciones en genes gyrA y gyrB) y a los FISL (identifica mutaciones en los genes rrs y el promotor eis). La especificidad de este método es superior al 98%29–31, tanto para las FQ, como para las de los FISL, por lo que se recomienda que esta información sea seguida en el diseño del esquema de tratamiento32,33 (recomendación condicional, moderada calidad de evidencia [⊕⊕
]).Historia clínica de fármacosEs de suma importancia la historia de fármacos tomados por el paciente en el pasado, en el caso de los enfermos previamente tratados para TB6. Cuando un fármaco haya sido mal administrado durante más de un mes se debe sospechar la posibilidad de resistencia y pensar que su eficacia puede estar disminuida, a pesar de que la prueba de sensibilidad indique lo contrario6,34. Hay modelos sencillos de historia de fármacos que pueden ayudar en este sentido, como el que se expone en la figura 16. También es necesario investigar si el posible caso índice de un paciente tenía una TB-DR.
Modelo para realizar historial de fármacos anti-TB recibidos por el paciente. Adaptado de Caminero et al.6
Esta normativa recomienda: 1) que a todos los enfermos diagnosticados de TB se les realice un test de sensibilidad a H y R, a ser posible un test rápido molecular si se dispone del mismo; 2) si se demuestra resistencia a R y/o a H se recomienda que se realice test de susceptibilidad a la FQ y al FISL que se vaya a utilizar en el esquema de tratamiento posterior, a ser posible el GenotypeMDRsl (Hain) v2; 3) también se deben realizar las técnicas fenotípicas convencionales que, aunque se demoran más tiempo y apoyan menos en la decisión de tratar, pueden resolver algunas discrepancias entre los métodos; y 4) por último, la historia clínica farmacológica es indispensable para diseñar la pauta de tratamiento.
Bases del tratamiento de todas las formas de tuberculosis, tanto sensibles como con resistencia a los fármacosTodo tratamiento de la TB debe cumplir 2 bases bacteriológicas: asociar fármacos para evitar la selección de resistencias y prolongar el tratamiento el tiempo suficiente que asegure la curación y evite las recaídas6,35,36.
Para asegurar al máximo la posibilidad de curación sin recaídas de una TB se recomienda que todo tratamiento asocie al menos 4 fármacos no utilizados previamente, o en los que haya certeza de que M. tuberculosis es sensible a los mismos6,15,36. De ellos, al menos 2 deben ser fármacos «esenciales», que son los que eliminan la mayor parte de la población bacilar y pueden curar al enfermo. De estos fármacos «esenciales», al menos uno debe tener buena actividad bactericida (capacidad de eliminar a los bacilos en fase de multiplicación rápida, que están en las lesiones cavitadas y que son los que producen los síntomas y la transmisión), y al menos otro debe tener buena capacidad esterilizante (capacidad de eliminar los bacilos en fases semilatentes productores de las recaídas). Los otros 2 fármacos son lo que denominamos «acompañantes», cuya misión es la de proteger a los fármacos «esenciales» de la selección de resistencias6,36 (recomendación condicional, moderada calidad de evidencia [⊕⊕
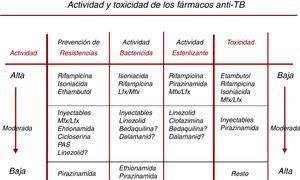
]).Para ayudar en la selección de los fármacos que deben componer un tratamiento de la TB, en la figura 2 se muestra la capacidad bactericida y esterilizante de los diferentes fármacos, así como su capacidad de prevenir la selección de resistencias y su toxicidad36.
Características de los fármacos con actividad frente a Mycobacterium tuberculosis. Adaptado de Caminero et al.36
La prevención de resistencias, la actividad bactericida y la actividad esterilizante se exponen de mayor a menor (actividad alta, moderada y baja) en la tabla, mientras que la toxicidad se expone al revés en la flecha del lado derecho (baja, moderada, alta), para poder poner en la parte superior los mejores fármacos disponibles según todas estas características
En la tabla 2 y tabla 2b se detallan las dosis de los diferentes fármacos con actividad frente a M. tuberculosis, así como la vía de administración y los efectos adversos más frecuentes.
Fármacos activos frente a M. tuberculosis. Dosis recomendadas y efectos adversos más frecuentes. Tabla 2a. Dosis recomendadas para cada uno de los fármacos usados individualmente
| Farmaco | Vía | Dosis | Efectos adversos más frecuentes |
|---|---|---|---|
| Rifampicina | Oral, IV | 10mg/kg. Máx. 600mg | Hepatitis, reacciones de Hipersensibilidad |
| Isoniacida | Oral, IV, IM | 5mg/kg a dosis normales (máx. 300mg) 15mg/kg a dosis elevadas | Hepatitis. Neuritis periférica |
| Pirazinamida | Oral | 25-30mg/kg | Hepatitis. Hiperuricemia |
| Etambutol | Oral | 25mg/kg 15mg/kg en fase de continuación | Neuritis óptica |
| Estreptomicina | IM, IV | 15mg/kg. Máx 1g | Nefrotoxicidad, alteraciones viii par craneal |
| Etionamida/protionamida | Oral | 750-1000mg | Gastroenteritis/hepatitis |
| Cicloserina | Oral | 750-1000mg | Alt. personalidad/depresión |
| Capreomicina | IM, IV | 15mg/kg. Máx. 0,75-1g/día o/48h | Ototoxicidad/nefrotoxicidad |
| Kanamicina | IM, IV | 15mg/kg. Máx. 0,75-1g/día o/48h | Ototoxicidad/nefrotoxicidad |
| Amikacina | IM, IV | 15mg/kg. Máx. 0,75-1g/día o/48h | Ototoxicidad/nefrotoxicidad |
| Levofloxacina | Oral, IV | 15mg/kg → 750mg-1g | Tenosinovitis |
| Moxifloxacina | Oral | 400-800mg | Tenosinovitis |
| PAS | Oral | 10-15g | Gastroenteritis/hepatitis |
| Clofazimina | Oral | 100-200mg | Pigmentación/enteritis eosinófila |
| Linezolid | Oral, IV | 600mg | Pancitopenia/alteraciones gastrointestinales/polineuritis |
| Meropenem | IV | 1g/8 o 12h | Alteraciones hematológicas |
| Bedaquilina | Oral | 400mg/día durante 15 días y después 200mg/3 veces por semana hasta completar un máximo de 6 meses | Intolerancia gástrica, pancreatitis, hepatitis, alteraciones QTc en ECG |
| Delamanid | Oral | 100mg/12h, hasta un máximo de 6 meses | Anemia, naúseas, alteraciones QTc en ECG |
Dosis recomendadas de las asociaciones de fármacos más comunes disponibles en España
| Asociación isonicida+rifampicina (H+R) | |
| Rifinah 300®(H 150mg, R 300mg) | |
| Pacientes de 30-50kg de peso | 1comp./día |
| Pacientes de 50kg o más | 2comp./día |
| Asociación isoniacida+rifampicina+pirazinamida (H+R+Z) | |
| Rifater®(H 50mg, R 120mg, Z 300mg) | |
| En niños menores de 10 años ajustar según dosis | |
| Pacientes de 20-30kg | 2 comp./día |
| Pacientes de 30- 40kg | 3 comp./dia |
| Pacientes de 40-49kg | 4 comp./dia |
| Pacientes de 50-64kg | 5 comp./día |
| Pacientes de 65kg o más | 6 comp./día |
| Asociación isoniacida+rifampicina+pirazinamida+etambutol (H+R+Z+E) | |
| Rimstar®(H 75mg, R 150mg, Z 400mg, E 275mg) | |
| Pacientes de 30-39kg | 2 comp./día |
| Pacientes de 40-54kg | 3 comp./día |
| Pacientes de 55-70kg | 4 comp./día |
| Pacientes de 70kg o más | 5 comp./día |
Para ayudar en la selección de los 4 fármacos que deben formar parte de todo tratamiento de la TB en su fase inicial, se recomienda clasificarlos en 5 grupos diferentes (tabla 3), empezando por el grupo 1, que serían los que tienen la mayor actividad, y siguiendo con los grupos en orden decreciente de eficacia y tolerancia3,8,37,38. Se ha de ir bajando en estos grupos hasta poder completar la máxima de al menos 4 fármacos nuevos o con muy probable sensibilidad, que incluyan al menos un fármaco bactericida y otro esterilizante. Las directrices para la introducción de cada uno de los fármacos incluidos en estos grupos se exponen en la tabla 3 (recomendación condicional, moderada calidad de evidencia [⊕⊕
]).Clasificación racional y uso secuencial que se debería hacer de los fármacos antituberculosos a la hora de diseñar un esquema de tratamiento para la TB, tanto sensible como resistente a fármacos
| Fármacos de primera línea de administración orala |
| Fármacos esenciales: isoniacida, rifampicina, pirazinamida |
| Fármaco acompañante: etambutol |
| Fluoroquinolonasb |
| Altas dosis de levofloxacino, o moxifloxacino todos son esenciales |
| Fármacos inyectables de segunda líneab |
| Estreptomicinac, kanamicina, amikacina, capreomicina todos son esenciales |
| Grupo mixto de fármacos esenciales con poca evidencia y fármacos acompañantes menos eficacesd |
| Fármacos esenciales: linezolid, bedaquilina, delamanid |
| Fármacos acompañantes: etionamida/protionamida, clofazimina, cicloserina/terizidona |
| Otros fármacos con menor experiencia clínica, o menos eficaces y más tóxicose |
| Carbapenemes (meropenem/imipenem)+amoxicilina/clavulánico, PAS, tioacetazona |
Fuentes: World Health Organization4; Caminero et al.6; World Health Organization8; Caminero et al.37; Caminero et al.38
Utilizar solo uno de ellos, pues su diana genética es la misma. Considerarlo como fármaco activo en los casos con TB-MDR. En los casos TB-XDR, añadir una fluoroquinolona y/o un inyectable si se mantiene sensibilidad in vitro a alguno de estos fármacos, y siempre intentando que sea diferente al utilizado previamente. En cualquier caso, en TB-XDR no se deberían contar entre los 4 fármacos activos del régimen.
Evitar estreptomicina por su elevada tasa de resistencia asociada a isoniacida, pero puede considerarse si se demuestra su sensibilidad en el antibiograma y no ha sido utilizada previamente en el enfermo.
El grupo 1 lo forman los denominados «fármacos orales de primera línea» debido a que se utilizan en primera instancia en la práctica totalidad de los enfermos que padecen TB con sensibilidad a los fármacos. Como conjunto son los más eficaces, mejor tolerados y más baratos37,38. Es necesario diferenciar los fármacos que pueden ser denominados «esenciales» por su capacidad bactericida (H y R), o esterilizante (R y Z), de los denominados «acompañantes» (E)6,36.
El grupo 2 lo forman las FQ (altas dosis de Lfx o Mfx), que son también fármacos «esenciales» con actividad bactericida y esterilizante y escasa toxicidad6,37,38. Además, si pueden ser utilizadas marcan claramente el pronóstico en el tratamiento de la TB-MDR6,39,40. Aunque no se ha estudiado parece que la resistencia cruzada entre estas 2 FQ puede ser considerable.
El grupo 3 lo forman los inyectables de segunda línea, también fármacos «esenciales» por su capacidad bactericida, pero con escasa o nula capacidad esterilizante y mucho más tóxicos que las FQ6,37,38. Esta toxicidad acumulativa y la necesidad de administrarlos inyectados limitan mucho su uso.
El denominado grupo 4 estaría integrado por 6 fármacos diferentes, que podrían darse conjuntamente pues su diana de ataque a M. tuberculosis es diferente3,4,6,37,38. Este es un grupo mixto formado tanto por fármacos que podrían etiquetarse como «esenciales» por su actividad, pero aún con poca evidencia acumulada (linezolid, bedaquilina y delamanid), como por otros donde la evidencia es mayor pero con moderada o escasa actividad (etionamida/protionamida y cicloserina/terizidona) y que se comportarían como «acompañantes», y otro como la clofazimina, con posible buena actividad esterilizante. La selección de unos u otros va a depender de la disponibilidad de cada uno de ellos y sus posibles efectos adversos.
Linezolid puede considerarse un fármaco «esencial», con capacidad bactericida y esterilizante38. Varias publicaciones38,41–43 han demostrado su buen papel en el tratamiento de la TB-MDR y TB-XDR. Solo tiene 2 inconvenientes, su precio elevado y su perfil de toxicidad cuando se administra durante más de 6-8 semanas, con frecuentes alteraciones hematológicas y polineuropatías. El problema de la toxicidad va muy ligado a la dosis38, y es relativamente fácil de manejar dada la dosis baja recomendada para TB-MDR38,41 y el precio es menor desde la comercialización de la molécula genérica en 2016.
Bedaquilina también se puede considerar fármaco «esencial» por su actividad bactericida y esterilizante38,44. Dos ensayos clínicos han demostrado su eficacia en el tratamiento de la TB-MDR45,46, especialmente en la TB extensamente-fármaco-resistente (TB-MDR más resistencia al menos a una FQ y a un FISL [kanamicina, amikacina, capreomicina], TB-XDR), y se está utilizando en muchos países.
Por último, el delamanid y el pretomanid son derivados del metronidazol con actividad bactericida y esterilizante38,47–51. Dos ensayos clínicos aleatorizados han demostrado el buen papel del delamanid en el tratamiento de la TB-MDR48,49, especialmente de la TB-XDR.
Tanto linezolid como bedaquilina y delamanid están destinados a ocupar un papel relevante en el tratamiento de la TB-MDR en un futuro muy cercano38, y podrían tenerlo en el desarrollo de un esquema de tratamiento para la TB sensible.
A estos 3 fármacos les seguirían en actividad las tioamidas (etionamida/protionamida), que pueden llegar a tener ligera actividad bactericida6, pero con potencial resistencia cruzada con H (mutación gen inhA, detectable por GenotypeMDRplus) y tienen mala tolerancia gástrica6. Le seguiría en actividad la clofazimina, que está desempeñando un papel importante en los esquemas acortados de tratamiento de la TB-MDR por su posible actividad esterilizante8,26,52. Y, por último, la cicloserina (la terizidona es similar y tiene la misma acción), con buena tolerancia oral, pero con actividad limitada y con efectos adversos psiquiátricos potencialmente graves6,53.
En un hipotético grupo 5 quedarían los carbapenemes (imipenem o meropenem) asociados a ácido clavulánico (como no existe en forma separada obliga a darlo junto con amoxicilina), probablemente bastante activos, pero aún con poca evidencia6,54; el PAS, muy poco eficaz y muy mal tolerado a nivel gástrico6,37, y la tioacetazona, muy débil, potencialmente tóxica en pacientes con virus de la inmunodeficiencia humana (VIH) y muy difícil de conseguir37.
Tratamiento de la tuberculosis según el patrón de resistenciasEn función de las posibles resistencias, su dificultad de tratamiento y el diferente pronóstico que puede conllevar, la TB se podría clasificar en 5 grandes grupos, escalando siempre en el nivel de dificultad55 (tabla 4).
Esquemas básicos recomendados para los pacientes con TB sensible y mono-polirresistencia
| Casos TB iniciales con sensibilidad a todos los fármacosa,b,c |
| 2HRZE/4(HR) |
| Casos TB con resistencia a H (mono o polirresistencia), pero con sensibilidad a Rd,e |
| 9HRZE, o 2FQ-REZ/7FQ-RE o 2RZE/10RE |
| Casos con resistencia a R (mono o polirresistencia), pero con sensibilidad a H, o si no se conoce la sensibilidad a H |
| Mismo tratamiento que la TB-MDR, que se aborda en la tabla 5, añadiendo H al régimen, pero sin contarla entre los 4 fármacos nuevos |
No hay unanimidad respecto a la duración de este tratamiento en los pacientes infectados por VIH, y algunos grupos y sociedades científicas recomiendan prolongar el tratamiento hasta completar 9 meses, con la finalidad de reducir la tasa de recaídas.
No cambiar a la fase de continuación (4HR) hasta que no se dé una de las 2 siguientes circunstancias: que ya la baciloscopia sea negativa, o que se sepa que existe sensibilidad a H y R.
Prolongar el tratamiento por encima de los 6 meses en aquellos pacientes en los que la negativización de las baciloscopias y/o cultivos se demora por encima de los 2 meses6. Como referencia, a estos pacientes se prolongará el tratamiento con H+R hasta un mínimo de 4 meses después de que se negativicen los cultivos.
La FQ (Lfx/Mfx) solo se debe introducir en el régimen si se administra desde un inicio con el resto de los fármacos. No se debe añadir si el resultado de resistencia a la H se recibe después de 3-4 semanas de tratamiento, por el posible riesgo de realizar una monoterapia encubierta. En ese caso utilizar 9HRZE.
El régimen de tratamiento ideal para los casos nuevos de TB en los que se presume sensibilidad a todos los fármacos sería 2HRZE/4HR, con las consideraciones expuestas en la tabla 46,13,15,36,56 (recomendación fuerte, alta calidad de evidencia [⊕⊕⊕⊕]). Para disminuir la posibilidad de errores y de posible selección de resistencias, estos fármacos deben administrarse siempre en dosis fijas combinadas (tabla 2) y bajo tratamiento directamente observado en los pacientes que tienen factores de riesgo de mal cumplimiento terapéutico15.
Tratamiento de la tuberculosis con resistencia a isoniacida (mono o polirresistencia), pero con sensibilidad a la rifampicinaEsta situación se da con relativa frecuencia. En estos casos se recomienda tratar con 9HRZE (en este caso valorar altas dosis de H)23, realizando estudio de sensibilidad al resto de fármacos de primera línea (recomendación condicional, baja [⊕
] a muy baja () calidad de evidencia). Un régimen con 2FQ-REZ/7FQ-RE también se podría valorar (realizando estudio de sensibilidad a la FQ), pero la FQ (Lfx/Mfx) solo se debe introducir en el régimen si se administra desde un inicio con el resto de los fármacos. No se debe añadir si el resultado de resistencia a la H se recibe después de 3-4 semanas de tratamiento, por el posible riesgo de realizar una monoterapia encubierta. Consultar las consideraciones expuestas en la tabla 44,6,15. Una tercera posibilidad es 2RZE/10RE, que está de acuerdo con las recomendaciones vigentes de SEPAR y que se ha utilizado con éxito en los tratamientos estándar en los que se ha tenido que retirar H por intolerancia.Tratamiento de la tuberculosis con resistencia a rifampicina (mono o polirresistencia), pero con sensibilidad a isoniacidaComo estos casos de resistencia aislada a R son muy poco frecuentes en la práctica clínica, y como la R es la que condiciona el pronóstico en los enfermos con TB-MDR, se debe enfocar estos enfermos como pacientes TB-MDR, y tratarlos como tal, por supuesto añadiendo al esquema H, porque si se confirma su sensibilidad va a ser una importante aportación al tratamiento5,6 (recomendación condicional, baja [⊕
)] a muy baja [] calidad de evidencia).Tratamiento de la tuberculosis multi-farmacorresistente, con sensibilidad a las fluoroquinolonas e inyectables de segunda líneaSiguiendo con el razonamiento expuesto en esta normativa, el régimen ideal para estos enfermos llevará una FQ (Mfx, o altas dosis de Lfx), un inyectable de segunda línea (al menos hasta la negativización de los cultivos), y 2 fármacos a seleccionar del denominado grupo 4 en esta normativa. Además, se asociará Z por su posible actividad en este esquema si fuese sensible, y teniendo en cuenta que su test de sensibilidad no es fiable (recomendación condicional, muy baja [
] calidad de evidencia). Siempre se deben valorar las consideraciones expuestas en la tabla 5.Esquemas básicos recomendados para los pacientes con TB-MDR
| Casos con TB-MDR, pero sin resistencia a fármacos de segunda línea |
| Esquema acortado: 4a (Cm/Am+Mfxb+Pth/Eth+Cfz+E+Z+Hc)/5 (Mfxb+Cfz+E+Z) |
| Esquema convencional |
| Fase intensiva (Cmd+Mfx/Lfx+Z+2 fármacos del grupo 4e)/fase continuación (Mfx/Lfx+Z+2 fármacos del grupo 4e) |
| Casos con TB-MDR y resistencia añadida a las FQ, FISL, a ambos, o incluso patrones más amplios de resistencia de la TB-XDR |
| Consultar con expertos y diseñar un esquema que siga todas las recomendaciones efectuadas en esta normativa, buscando un mínimo de 4 fármacos nuevos, siguiendo la clasificación racional expuesta (grupos 1 a 5) y tratando de que el esquema lleve el máximo número de medicamentos bactericidas y esterilizantes |
FC: fase continuación: Hasta completar 21 meses de tratamiento; FI: fase intensiva. Hasta la negativización de los cultivos, o hasta 6 meses si existen lesiones extensas. Mantener un mínimo de 4 meses si el paciente no expectora y no se pueden realizar exámenes de esputo de control.
Fuentes: Caminero et al.6; World Health Organization8; Caminero55.
Es mucho más controvertido la duración total que debería tener este esquema de 4 fármacos nuevos más la Z. Los esquemas de 21 meses recomendados tradicionalmente3,4,8,9 no han conseguido tasas de éxito superiores al 55-70%, sobre todo por la elevada tasa de abandonos que tiene40,57,58, en clara relación con la extensa duración del mismo, y en parte por su mala tolerancia y toxicidad. Por ello, esta normativa recomienda que se dé prioridad al esquema de 9-12 meses recomendado recientemente por la OMS8, para todos los pacientes afectos de TB con resistencia a la R, o con TB-MDR que no hayan recibido previamente FQ ni FISL para el tratamiento de la TB, o que se demuestre que hay sensibilidad in vitro a estas 2 clases de antibióticos (recomendación condicional, muy baja [
] calidad de evidencia). Este esquema consta de una fase inicial de 4 meses (o hasta negativizar la baciloscopia) con kanamicina (podría ser Am o Cm en nuestro país), moxifloxacino a altas dosis, clofazimina, etionamida/protionamida, pirazinamida, etambutol y altas dosis de H. La fase de continuación será de 5 meses con moxifloxacino a altas dosis, clofazimina, etambutol y pirazinamida. Se debe realizar un control muy cercano de posibles efectos adversos, principalmente de la posible prolongación del espacio QTc en el electrocardiograma, sobre todo por las dosis elevadas de moxifloxacino que recomienda este esquema.Tratamiento de los pacientes con tuberculosis multi-farmacorresistente y resistencia añadida a las fluoroquinolonas, a los fármacos inyectables de segunda línea, a ambos, o incluso a patrones más amplios de resistenciaEstas formas de TB ya son de muy difícil manejo, tanto clínico como programático5,6. Serán tratados por personal muy experto en el tema y en unidades que puedan garantizar una buena supervisión del tratamiento y el abordaje adecuado de sus reacciones adversas. Los posibles regímenes a dar a la gran mayoría de estos pacientes se exponen en la tabla 5.
Papel de la cirugíaLa cirugía también puede contribuir al éxito del tratamiento de la TB-MDR6,8,59, aunque solo se considerará para los pocos pacientes que cumplan las 3 condiciones siguientes6: 1) lesión bastante localizada, susceptible de ser resecada; 2) reserva respiratoria que permita tolerar la cirugía y el postoperatorio; y 3) falta de medicamentos para diseñar un esquema curativo para el paciente6. Basados en esta última premisa, quizás se considerará la cirugía en los pacientes con TB-MDR y resistencia a las FQ, o con un patrón de resistencias aún más amplio (recomendación condicional, muy baja [
] calidad de evidencia).Control a lo largo del tratamiento y evaluación de resultadosSe debería realizar un mínimo de un control mensual durante la fase intensiva del tratamiento, y cada uno o 2 meses en la fase de continuación. Los aspectos a valorar en cada uno de estos controles se pueden ver en la tabla 6 y los criterios para evaluar los resultados del tratamiento se describen detalladamente en la tabla 760.
Controles necesarios a realizar a lo largo del tratamiento de la TB
| Controles | M0 | M1 | M2 | M3 | M4 | M5 | M6 | M7 | M8 | M9 | M10 | M11 | +M12 |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Visita médica | X | X | X | X | X | X | X | X | X | X | X | X | X |
| Baciloscopia (×2-3) | X | X | X | X | X | Xa | X | Xa | X | Xa | X | Xa | X |
| Cultivo (×2-3) | X | X | X | X | X | Xa | X | Xa | X | Xa | X | Xa | X |
| Análisis de sangre | X | X | X | X | X | X | X | X | X | X | X | X | X |
| EKG | X | Xb | Xb | Xb | Xb | Xb | Xb | Xb | Xb | Xb | Xb | Xb | Xb |
| ORL Audiometría | X | Xc | Xc | Xc | Xc | Xc | Xc | Xc | Xc | Xc | Xc | Xc | Xc |
| Rx tórax | X | X | X | X | X | ||||||||
| Oftalmológico | X | Xd | Xd | Xd | Xd | Xd | Xd | ||||||
| Psiquiátrico | Xe | Xe | Xe | Xe | Xe |
Criterios para evaluar los resultados del tratamiento de los pacientes afectos de TB, siguiendo las recomendaciones de la OMS
| Resultado | Definición |
|---|---|
| Resultados de tratamiento de pacientes con TB que no están afectos de TB con resistencia a rifampicina o TB-MDRa | |
| Curado | Paciente con TB con bacteriología confirmada al inicio del tratamiento y que tiene baciloscopia o cultivo negativo en el último mes de tratamiento y al menos en una ocasión anterior |
| Tratamiento completo | Paciente con TB que completó el tratamiento sin evidencia de fracaso, pero sin constancia de baciloscopia o cultivo de esputo negativo en el último mes de tratamiento y en al menos una ocasión anterior, ya sea porque las pruebas no se hicieron, o porque los resultados no están disponibles |
| Fracaso al tratamiento | Paciente con TB cuya baciloscopia o cultivo de esputo es positivo en el mes 5 o posterior durante el tratamiento |
| Fallecido | Paciente con TB que muere por cualquier razón antes de comenzar o durante el curso del tratamiento |
| Pérdida en el seguimiento | Paciente con TB que no inició tratamiento o interrumpió el tratamiento durante 30 días consecutivos |
| No evaluado | Paciente con TB que no se le ha asignado el resultado de tratamiento. Incluye los casos «transferidos» a otra unidad de tratamiento, y los casos en los que se desconoce el resultado del tratamiento |
| Resultados de pacientes con TB con resistencia a la rifampicina, o TB-MDR/XDR, que son tratados con medicamentos de segunda línea | |
| Curado | Tratamiento completo según lo recomendado por la política nacional sin evidencia de fracaso y 3 o más cultivos negativos consecutivos con un intervalo de por lo menos 30 días, después de la fase intensiva |
| Tratamiento completo | Tratamiento completo según lo recomendado por la política nacional sin evidencia de fracaso, pero sin constancia de 3 o más cultivos negativos consecutivos con al menos 30 días de intervalo después de la fase intensiva |
| Fracaso al tratamiento | Tratamiento suspendido o necesita cambio permanente de esquema o por lo menos de 2 fármacos anti-TB debido a: falta de conversiónb «al final de la fase intensiva», o reversiónc bacteriológica «en la fase de continuación después de la conversión» a negativo, o evidencia de resistencia adicional adquirida a las fluoroquinolonas o fármacos inyectables de segunda línea, o reacciones adversas a medicamentos |
| Fallecido | Paciente con TB que muere por cualquier razón antes de comenzar o durante el curso del tratamiento |
| Pérdida en el seguimiento | Paciente con TB que no inició tratamiento o interrumpió el tratamiento durante 30 días consecutivos |
| No evaluado | Paciente con TB que no se le ha asignado el resultado de tratamiento. Incluye los casos «transferidos» a otra unidad de tratamiento, y los casos en los que se desconoce el resultado del tratamiento |
Fuente: World Health Organization60.
Basados en la evidencia disponible, si un contacto de un caso con TB-MDR acaba padeciendo TB, en espera de las pruebas de sensibilidad, recibirá el mismo esquema de tratamiento que el caso índice, con posible ajuste posterior al recibir el resultado de estas pruebas. Si no hubiese confirmación microbiológica del caso secundario, como puede ocurrir en niños, formas paucibacilares o TB extrapulmonar se ha de continuar con el esquema del caso índice. No se aconseja prescribir de forma sistemática tratamiento de la infección tuberculosa a los contactos de TB-MDR si estos no tienen otro factor de riesgo para TB3,4,6,61.
Conclusiones- 1.
A pesar de que las resistencias en TB complican el tratamiento y las posibilidades de éxito, con unas reglas básicas de manejo se pueden conseguir tasas aceptables de curación en la gran mayoría de los enfermos. Estas reglas básicas, que resumen prácticamente toda la normativa, se exponen en la tabla 8.
Tabla 8.Resumen de buenas prácticas en el manejo de TB-MDR
Pasos Consideraciones 1. Diagnóstico Tener en cuenta:
Historia de fármacos: un mes de monoterapia, o el añadir un solo fármaco a un régimen de tratamiento que no está siendo eficaz es un indicador importante de posible resistencia a este fármaco, o de su posible menor eficacia
Prueba sensibilidad a fármacos (PSF): muy fiable para R y H; bastante fiable para inyectables de segunda línea y FQ; menos fiable para S, E y Z; muy poco fiable para Eth/Pth, Cs y PAS. Aún por investigar el método exacto y la credibilidad para Lzd, Bdq, Dlm, Cfz y carbapenemes
Realizar test de VIH2. Número de medicamentos Al menos 4 medicamentos efectivos: nunca usados en el pasado o con sensibilidad demostrada por PSF, teniendo en cuenta fiabilidad de PSF comentada en punto 1 y posibles resistencias cruzadas
Al menos 2 fármacos esenciales (al menos uno con alta capacidad bactericida y al menos otro con capacidad esterilizante) y 2 fármacos acompañantes para proteger a los esenciales3. Selección de medicamentos Introducción racional según tabla 3
En el caso de TB-MDR, tratar de utilizar medicamentos de primera línea si todavía son efectivos. Pero, en este caso, no contarlos entre los «4 fármacos efectivos»
Altas dosis de levofloxacino o moxifloxacino
Un fármaco inyectable de segunda línea, o S si mantiene sensibilidad y no se ha usado previamente
Usar fármacos grupo 4 hasta completar 4 fármacos efectivos
Valorar altas dosis de H4. Duración del tratamiento Esquema acortado: 9 meses. Fase intensiva 4 meses o hasta negativización de la baciloscopia. Fase continuación: 5 meses
Esquema convencional: 21 meses. Fase intensiva: al menos hasta la negativización de baciloscopia y cultivo; y siempre con un mínimo de 6 meses. Aún mayor duración si no hay 3 medicamentos efectivos en la fase de continuación, o hay sospechas de resistencias a FQ. Fase de continuación: al menos hasta completar 21 meses de tratamiento total y 12 meses con cultivos negativos
Siempre con tratamiento directamente supervisado5. Cirugía Considerar solo si se cumplen estas 3 condiciones
1) Menos de 4 fármacos efectivos; 2) lesiones localizadas; y 3) reserva respiratoria suficiente tras la resección
Valorar sobre todo en TB-XDR y pre-TB-XDR por resistencia a FQ6. Régimen ideal Estandarizado: si solo ha recibido esquemas estandarizados en el pasado, tanto de primera como de segunda línea.
Individualizado: si ha habido uso de medicamentos de segunda línea fuera de los tratamientos estandarizados, o en contactos de pacientes MDR que los han usado. En este último caso tratar con el régimen que fue efectivo en el caso índiceSiempre es aconsejable consultar con un experto a la hora de diseñar un esquema de tratamiento para estos pacientes.
Adaptada de: Caminero y Scardigli38.
- 2.
En cualquier caso, siempre es aconsejable consultar con un experto a la hora de diseñar un esquema de tratamiento para estos pacientes. Con tal finalidad se recomienda la organización de grupos de expertos a nivel estatal promovidos por las autoridades sanitarias y/o las sociedades científicas.
- 3.
La primera prioridad seguirá siendo dar un buen tratamiento a los pacientes con TB sensible para evitar la aparición de estas resistencias.
Los autores declaran no tener conflicto de intereses.