Introducción
La reacción alérgica, una vez instaurada en el pulmón, parece persistir durante tiempo y, probablemente, de por vida en la mayoría de pacientes asmáticos. Bien distinto es que presente siempre síntomas. Por consiguiente, la clínica depende de factores no del todo conocidos que permiten en los sujetos asmáticos asintomáticos la persistencia de una inflamación eosinofílica de la mucosa bronquial, demostrable por biopsia1, mientras que otros pacientes a los que se han administrado dosis altas de glucocorticoides (GC) refieren síntomas de asma grave, concomitantes con alteraciones histológicas que pueden considerarse leves2.
De acuerdo con las recomendaciones nacionales e internacionales al respecto, el abordaje terapéutico considera la persistencia o la intermitencia del asma exclusivamente a través de la valoración de los síntomas presentados por el paciente, su función pulmonar y el consumo de fármacos broncodilatadores requerido. El hecho de que la relación entre la inflamación bronquial en el asma, los síntomas y la función pulmonar sea laxa e imprecisa, conlleva que el significado del concepto mismo de persistencia clínica del asma sea muy poco concreto, aunque la presencia o no de las manifestaciones de esta enfermedad sea fácil de determinar.
Asma persistente
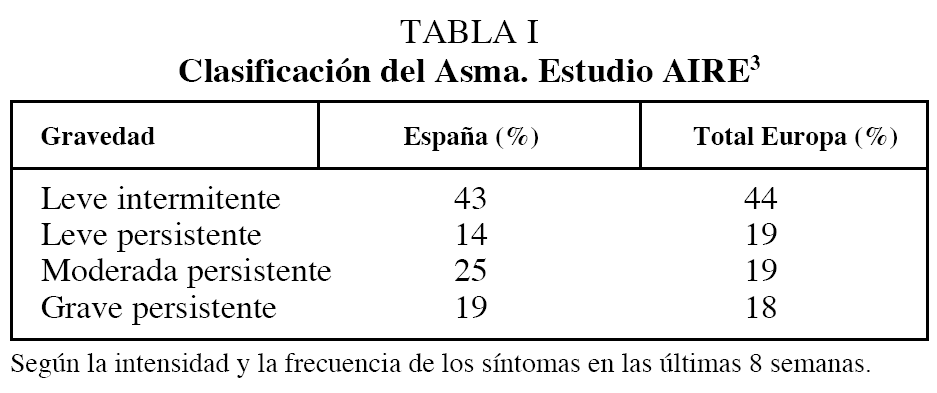
Se dispone de poca información sólida sobre la frecuencia de la persistencia clínica en el conjunto de enfermos con asma. Los datos del estudio AIRE3, basado en una encuesta telefónica realizada en una amplia muestra de hogares europeos, pueden ayudar a estimar la frecuencia de la persistencia clínica. Las cifras ofrecidas por dicho estudio para la proporción de asmáticos que referían síntomas con una frecuencia calificable de persistente pueden apreciarse en la tabla I. En el conjunto de grados de intensidad del asma, la persistente supone aproximadamente el 58% del total en España, y el 56% en el conjunto europeo. Los datos ponen de manifiesto, además, que la persistencia es un fenómeno independiente de la gravedad, pues afecta a los 3 grados.
Causas de persistencia
Desde el punto de vista clínico, un factor de confusión, y a la vez determinante, en el concepto de persistencia es la respuesta al tratamiento, que con mucha frecuencia convierte las manifestaciones clínicas de un asmático de diarias en ocasionales. Es precisamente la inadecuada respuesta al tratamiento, la que ha dado lugar al concepto de asma difícil o resistente4. El concepto en sí es también difícil de definir e incluye los aspectos de la enfermedad y su gravedad, los relativos a las características del enfermo y los problemas relacionados con el tratamiento y su fracaso. Así, el asma difícil (resistente) se refiere al asma no controlada, con una función pulmonar alterada, el asma grave y el asma con respuesta disminuida o nula a los GC. La combinación variable de los 3 elementos (enfermedad, pacientes y su tratamiento), interviene en la dificultad y da lugar a problemas diferentes que complican sobremanera el abordaje terapéutico. Por ejemplo, cuando la enfermedad tiene una gran intensidad o responde escasamente a los GC, el tratamiento se hace difícil, aunque el paciente colabore y el médico sepa lo que debe hacer. Si el asma es menos grave, pero el paciente no cumple con las pautas prescritas, éste seguirá presentando síntomas y su función pulmonar será inferior de lo normal. Puede ocurrir también que en el mismo paciente asmático coincidan otras enfermedades, como la sinusitis y las bronquiectasias, o el tabaquismo con un desarrollo de la limitación crónica del flujo respiratorio, o que su hiperrespuesta bronquial sea muy intensa. Hay pacientes en los que puede documentarse una variación caótica de su función pulmonar, habitualmente determinada por el flujo espiratorio máximo (FEM)5. De esta denominada asma frágil (brittle asthma), según describió Turner-Warwick5, hoy día se distinguen 2 tipos de cuadro clínico: a) pacientes con ataques de asma graves y repetidos, que habitualmente muestran una gran variabilidad del registro diario del FEM pese a recibir abundante medicación que incluye GC, y b) pacientes con asma estable, bien controlada con tratamiento y con una función pulmonar preservada, que sufren repetidamente ataques súbitos y graves, con riesgo vital a causa del asma. Este último subgrupo de pacientes es un buen ejemplo de que la gravedad del asma no es necesariamente sinónimo de mal control6.
En un paciente con manifestaciones de asma intensa, el control deficiente derivado del mal tratamiento o del incumplimiento de un tratamiento correcto, el cuadro clínico y la función pulmonar podrán corresponderse con la apreciación de asma grave. En el extremo opuesto, el asma inicialmente evaluada como persistente y grave, más tarde bien controlada con tratamiento adecuado, puede pasar a manifestarse clínicamente como asma ocasional si no se considera el consumo de fármacos en la evaluación.
En la intensidad y la persistencia del asma intervienen también factores constitucionales. Así, por ejemplo, el pequeño diámetro de las vías respiratorias del niño se ha invocado como determinante de la propensión a desarrollar sibilancias durante la infancia, que en muchos casos desaparecen más tarde al crecer. Por la misma razón, las mujeres parecen estar algo más predispuestas que los varones a desarrollar sibilancias7. También se ha demostrado una relación positiva entre sobrepeso y asma8, y se ha comprobado la mejoría clínica y funcional del asma con el adelgazamiento9. Por tanto, el factor anatómico puede tener un papel en la persistencia de síntomas. La información sobre la importancia de factores genéticos en el desarrollo del asma está acumulándose rápidamente en los últimos años, aunque los datos relativos a la determinación genética de la gravedad del asma son todavía preliminares10.
Los estudios sobre la heterogeneidad de la estructura de los receptores de los GC y de los receptores β2 apuntan a posibles mecanismos de persistencia del asma y su resistencia al tratamiento. En este sentido, se orienta la identificación de formas α y β en el receptor de los GC y el aumento de la variante β en células T de asmáticos con resistencia a GC11, aunque la aceptación de este mecanismo no acaba de ser unánime12. También se ha implicado, y quizás con mayor consenso, a determinados polimorfismos del receptor adrenérgico β2. En concreto, la variante arginina-arginina en la posición 16 de la cadena de aminoácidos del receptor β afecta a la regulación del mismo y se asocia con la disminución del flujo máximo13 y el aumento del número de exacerbaciones14 con el uso regular del salbutamol. Estos hechos darían soporte al empeoramiento del asma crónica atribuido al uso pautado de fenoterol15 y salbutamol16. No obstante, dicho empeoramiento no ha sido comprobado en otros estudios17.
Otro aspecto de potencial trascendencia en el asma persistente y difícil se refiere a la estructura espacial (quiral) de los fármacos, en particular del salbutamol, disponible actualmente en forma racémica, que incluye los 2 isómeros (enantiómeros) dextro (R) y levo (S) al 50%. La forma R de los agonistas β2, concretamente del salbutamol, es análoga a la adrenalina y responsable de los efectos broncodilatadores del fármaco. Por el contrario, la forma S es la opuesta y no se une al receptor β2; su eliminación del compuesto puede reducir los efectos secundarios. La administración de las 2 conjuntamente (salbutamol racémico) muestra pocas diferencias de broncodilatación con la del salbutamol R puro. Pero la vida media de la forma S es muy superior a la de la R y su retención pulmonar también. Este hecho puede tener importancia en el paciente con asma grave, que requiere mayores y más frecuentes dosis. A las 3-4 h de una sola dosis de salbutamol racémico, la forma R disminuye mucho su concentración, pero la degradación de S es muy lenta y permite su acumulación, con lo que su concentración va en aumento18. Las dosis siguientes no harán sino empeorar el problema, en particular si la administración es inhalada y pautada. No obstante, estos posibles efectos del S-salbutamol siguen siendo objeto de debate19.
La importancia de la hiperrespuesta bronquial en la frecuencia y la intensidad de los síntomas es indudable. La hiperrespuesta es un elemento asociado a la inflamación bronquial20, aunque la correlación entre la intensidad de los 2 fenómenos no es muy consistente21. No obstante, la valoración de la intensidad de la hiperrespuesta se ha usado con éxito para optimizar el tratamiento del paciente asmático22.
La aparición de limitación del flujo aéreo de carácter irreversible es un hecho que debe considerarse en el paciente con asma persistente pese al tratamiento correcto. Los datos proporcionados por el Copenhagen City Heart Study23 muestran que el asma puede generar una obstrucción crónica, irreversible, independientemente de otros factores causales, como el tabaco. Además, la disminución irreversible del volumen espiratorio máximo en el primer segundo (FEV1) es más rápida en los pacientes con asma no alérgica24. La prevalencia de la obstrucción fija se ha estimado en un 49% en un grupo de 132 asmáticos no fumadores con asma grave tratada con GC inhalados25. En estos pacientes, la obstrucción se asoció con la mayor edad, el comienzo tardío del asma, la mayor hiperrespuesta bronquial y, particularmente, la eosinofilia en el esputo.
Inflamación neutrofílica. En diversas ocasiones, y en parte por motivos farmacológicos, se ha intentado definir el asma como una inflamación eosinofílica. Por la dependencia de los eosinófilos respecto de las células T y las citocinas TH2, como IL-5 e IL-4, la hipótesis patogénica prevalente hasta hoy se centra en la persistencia de mecanismos TH2 para explicar la inflamación alérgica en la mayoría de pacientes con asma. Sin embargo, un número creciente de autores cuestiona actualmente la universalidad de dicha hipótesis: unos basándose en pruebas no directas, de diversas fuentes26, y otros en sus propias observaciones2,27-29. Douwes et al26 propugnan la importancia de la inflamación neutrofílica como fenotipo inflamatorio diferenciado en cerca de la mitad de los casos de asma. Otros autores se refieren sólo a la asociación de neutrofília en el lavado broncoalveolar (LBA)2 o el esputo28 con la mayor gravedad del asma, las exacerbaciones30 o la muerte por esta enfermedad31. En conjunto, estos estudios, y en particular el de Pavord et al32, ligan la inflamación neutrofílica a la persistencia y la gravedad de los síntomas, además de explicar el fracaso o la menor eficacia del tratamiento convencional con GC inhalados en un número significativo de asmáticos.
Muy recientemente, la publicación del estudio ENFUMOSA33 puso de manifiesto la posibilidad de que el asma persistente grave, que requiere dosis altas de GC inhalados y orales para su tratamiento sea, en realidad, una enfermedad diferente del asma no grave, la que responde al tratamiento convencional. El estudio analizó los datos de 163 pacientes con asma grave y los comparó a los de 158 pacientes con asma controlada con dosis bajas de GC inhalados. El grupo de asma grave se distinguía por un predominio de mujeres en una relación de 4:1, con menor atopia, mayor frecuencia de intolerancia a la aspirina, sinusitis, inflamación bronquial neutrofílica, mayor índice de masa corporal (sólo en las mujeres), mayor obstrucción --como era esperable-- y grado de hiperinflación, y menor capacidad de difusión. Las diferencias reflejadas en estas variables no representaban fenómenos de todo o nada. Pero, al igual que la notable menor respuesta a los GC, el conjunto se caracterizaba por ser claramente distinto de otras formas menos graves de asma. La observación permite hipotetizar la presencia de uno o varios fenotipos diferenciados que conformarían el asma persistente grave como entidad particular. Al mismo tiempo, desde el punto de vista de la actuación médica y el tratamiento, destaca la importancia de elementos como la intolerancia a los antiinflamatorios no esteroideos y la asociación con sinusitis, frecuentes en este grupo de pacientes.
Factores psicológicos y emocionales. La angustia y la depresión son frecuentes entre los pacientes con asma persistente grave. El estrés es un factor emocional bien reconocido como intensificador de los síntomas, aunque por mecanismos desconocidos y la posibilidad de efectos inconsistentes o paradójicos34,35. Determinados tipos de personalidad llevan a los pacientes a no aceptar o infravalorar la gravedad de su enfermedad. El término "alexitimia" se aplica a la dificultad mostrada por algunas personas para percibir y expresar sensaciones físicas y emociones. La dificultad para percibir la disnea podría inducir a algunos asmáticos a subestimar la gravedad de sus síntomas, y hacerles aceptar una mayor gravedad y persistencia de su enfermedad sin tomar las medidas terapéuticas oportunas. La alexitimia propiciaría así una mayor frecuencia y gravedad de las exacerbaciones.
Todos estos factores hacen menos probable la adhesión del paciente al tratamiento y las recomendaciones del médico. El incumplimiento es particularmente frecuente e importante en el uso de GC, por la corticofobia tan frecuente entre los pacientes36. Los problemas familiares y sociales actúan también muy negativamente sobre el cumplimineto terapéutico37,38. El síndrome de hiperventilación o ventilación disfuncional39 puede simular el asma o, lo que es más complicado, coincidir con el asma genuina en un mismo paciente. La definición de respiración disfuncional no es precisa y se refiere a un patrón ventilatorio anómalo que puede ocasionar disnea, tirantez torácica, parestesias, ansiedad y mareo. Algunos autores la han observado hasta en el 30% de las mujeres asmáticas y en el 20% de los varones40. La coincidencia puede aparentar una mayor intensidad y persistencia del asma y un fracaso terapéutico, con el probable resultado de un exceso de prescripción de fármacos. Otra disfunción, la de las cuerdas vocales, puede simular el asma, y en este caso con una característica falta de respuesta al tratamiento. El problema es especialmente complicado cuando se presenta asociada con el asma verdadera41. La complicación puede simular un empeoramiento del asma, con una menor respuesta al tratamiento, sin que la enfermedad empeore realmente.
Otros factores clínicos. Entre los problemas clínicos adicionales que pueden contribuir a la disminución de la respuesta al tratamiento, merecen mención la persistencia de la exposición alergénica, particularmente a hongos, o de otras noxas, como el tabaco y diversos irritantes, además de la intensa contaminación atmosférica. Los procesos concomitantes, como la sinusitis crónica, las bronquiectasias, la fibrosis quística, la aspergilosis y el reflujo gastroesofágico, requieren un adecuado tratamiento, con frecuencia enérgico, por su interferencia con la consecución del control clínico del asma. Por último, no puede olvidarse la posibilidad de error diagnóstico, en particular el relacionado con la disnea y tos persistentes.
Posibles mecanismos farmacológicos explicativos para el asma "resistente"
El núcleo del tratamiento del asma lo ocupan actualmente los GC, generalmente administrados por inhalación. Los GC ejercen su acción terapéutica por represión de genes proinflamatorios, a través de un mecanismo de secuestro de proteína por proteína, con la inhibición directa de factores de transcripción, como la proteína-1 de activación y el factor nuclear κB, que aumentan la expresión de citocinas, quimiocinas y moléculas de adhesión, enzimas y receptores participantes en la inflamación42. Para actuar, los GC comienzan por ligarse a un receptor de corticoide, predominantemente localizado en el citoplasma de la célula diana. Al unirse el GC, el receptor se traslada al interior del compartimiento nuclear, donde se ligará a los citados factores de transcripción para inhibir sus efectos. Dada su reconocida eficacia terapéutica en el asma, la explicación de un fracaso terapéutico de los GC en un paciente asmático que cumple correctamente el tratamiento no es sencilla. Basándose en la escasa información disponible, Corrigan43 propone varios posibles mecanismos:
El más obvio sería, quizás, la hipotética capacidad de metabolizar o depurar el GC inhalado más rápido de lo necesario para llevar a cabo su acción terapéutica. Pero los escasos datos disponibles indican muy poca variabilidad en la depuración del GC entre pacientes sensibles y resistentes a los GC44. Los estudios in vitro sobre la capacidad de las células T para metabolizar el GC muestran también muy poca variabilidad entre estos 2 tipos de pacientes45.
La información sobre la dependencia de los efectos de los GC respecto a su dosis, es decir, la relación dosis-respuesta, es deficiente, aunque permite dibujar una curva sigmoidea que alcanza la meseta de efectos antiasmáticos alrededor de los 1.000 μg (beclometasona o budesonida inhaladas), con una acentuación de los efectos sistémicos por encima de esa dosis46,47. Algunos de los datos obtenidos con fluticasona (tabla II) indican que la curva dosis-respuesta terapéutica comienza a aplanarse entre 100 y 200 μg/día, alcanza el máximo a los 500 μg/día, y la mayor eficacia entre 150 y 250 μg/día. Los aumentos de efecto entre los 100 y 500 μg/día son más eficaces que la adición de un agonista adrenérgico β2 de acción prolongada; no así por encima de los 500 μg/día. Además, estas dosis mayores sólo son recomendables en asmáticos "dependientes" de GC oral48. Estas observaciones obligan a considerar la posibilidad de que la sobredosificación sea un hecho frecuente en la práctica clínica actual del tratamiento del asma. Por otro lado, como ocurre con otros fármacos, el espectro de la relación dosis-respuesta de los GC incluye individuos con gran respuesta, junto a otros con una respuesta mucho menor o nula. Son estos últimos, en el extremo inferior de la distribución de respuestas, los que constituirían el grupo de asma resistente. Con toda probabilidad, estos individuos son pocos y el asma resistente a los GC es infrecuente; su prevalencia se ha estimado entre uno por 1.000 y uno por 10.000 asmáticos49. Dadas las implicaciones en su tratamiento, es importante asegurar el diagnóstico con una prueba de prednisona a 30-40 mg diarios durante 2-3 semanas, con la monitorización del FEM o del FEV1, que en estos pacientes no deberán aumentar más del 15% respecto a su valor inicial. Además, para distinguir al asma resistente de la enfermedad pulmonar obstructiva crónica, en los casos de duda deberá establecerse la falta repetida de respuesta espirométrica al broncodilatador50.
La mayoría de pacientes "resistentes" a los GC muestra una concentración plasmática de cortisol en el margen de referencia, y las funciones endocrinas y metabólicas de los GC endógenos, no disminuidas51. La falta de respuesta parece afectar fundamentalmente a la acción antiinflamatoria. Así pues, la administración de dosis altas de GC en busca de efectos terapéuticos se acompañará de un aumento de los efectos adversos secundarios, lo que fuerza a la limitación de la administración.
Junto a los individuos "resistentes" a los GC se sitúan los pacientes denominados "dependientes" de los GC. El asma dependiente de GC se define como la que requiere para su control el uso frecuente o continuo de GC en administración oral. Por definición, es grave y persistente, pero muestra respuesta a los GC, aunque sólo a dosis altas. Los mecanismos implicados en la dependencia o resistencia relativa son inciertos, pero la biopsia bronquial de estos pacientes demuestra que la inflamación persiste en ellos, pese a las dosis altas de GC, y hay un aumento de neutrófilos en los bronquios, cuyo significado es también incierto2. Es posible que el tratamiento con dosis muy altas de GC permita superar la resistencia relativa y restaure, en parte, la sensibilidad. Parece, pues, aconsejable administrar dosis altas en ciclos cortos y reducirlas después, para mantener el control con dosis inferiores. La resistencia relativa y su fluctuación también pueden estar relacionadas con el empleo de altas dosis de agonistas adrenérgicos β252 que, al reducirse, disminuyen también la necesidad de dosis altas de GC53.
Enfoque terapéutico
En un paciente que se presenta con asma difícil o persistente se deben seguir una serie de pasos (tabla III), que comienzan por certificar el diagnóstico de asma y, llegado el caso, determinar la sensibilidad y la necesidad de administrar GC, la conveniencia de añadir otros fármacos antiinflamatorios (antileucotrienos, anticuerpo monoclonal anti-IgE) y broncodilatadores (agonistas adrenérgicos β2 de acción prolongada, antifosfodiesterasas, anticolinérgicos) y, en ocasiones, considerar los inmunosupresores como alternativa a los GC. Es muy aconsejable realizar este plan diagnóstico y terapéutico con el paciente hospitalizado. Ello permite controlar los posibles factores adversos, asegurar la correcta dosificación y administración, y comprobar la respuesta clínica, funcional e incluso histológica, si se requiere. Es decir, el esquema de actuación debe comenzar por comprobar el carácter persistente del asma y sus posibles causas, en el extremo de las cuales se encontraría la verdadera resistencia al tratamiento.