Adaptar al español y analizar la fiabilidad y la validez de la versión española del cuestionario OSA-18 de calidad de vida (CVRS) en el síndrome de apnea-hipopnea del sueño (SAHS) infantil.
MétodoSe incluyeron niños con sospecha de SAHS a los que se practicó polisomnografía (PSG) pre y post adenoamigdalectomía (AA). Se analizó: edad, género, clínica, PSG, datos antropométricos, grados de Brodsky y Mallampati. Se administró OSA-18 basal y entre 3-6meses post AA. Tras la traducción-retrotraducción por personas bilingües se evaluaron la consistencia interna, la fiabilidad, la validez de constructo, la validez concurrente, la validez predictiva y la sensibilidad a los cambios.
ResultadosSe evaluaron 45 niños y 15 niñas: IMC18±4, cuello 28±5, Brodsky (0: 7%; <25%: 12%; 25-50%: 27%; >50 a <75%: 45%; >75%: 6%), IAH: 12±7 pre AA. El alfa de Cronbach del global fue 0,91. Las correlaciones entre dominios fueron significativas salvo para aspectos emocionales, aunque el global se correlacionó con todos los dominios (0,50-0,90). El análisis factorial mostró una estructura prácticamente idéntica al original. En la validez concurrente, el global mostró buena correlación (0,2-0,45). En su validez predictiva, diferenció adecuadamente los niveles de gravedad según Mallampati (ANOVA p=0,002) e índice apnea-hipopnea (ANOVA p=0,006). La sensibilidad al cambio fue excelente, tanto en el global (p<0,001) como en cada dominio (p<0,001), así como la fiabilidad test-retest.
ConclusionesLa adaptación española del OSA-18 es comprensible y sus características psicométricas sugieren que la versión española es equivalente a la original y puede ser empleada en países de habla hispana.
To analyze the reliability and validity of the Spanish version of the OSA-18 quality of life questionnaire in children with apnea-hypopnea syndrome (SAHS).
MethodChildren with suspected SAHS were studied with polysomnography (PSG) before and after adenotonsillectomy (AA). Age, gender, clinical data, PSG, anthropometric data, and Mallampati and Brodsky scales were analyzed. OSA-18 was administered at baseline and 3-6months post AA. After translation and backtranslation by bilingual professionals, the internal consistency, reliability, construct validity, concurrent validity, predictive validity and sensitivity to change of the questionnaire was assessed.
ResultsIn total, 45 boys and 15 girls were evaluated, showing BMI 18±4, neck 28±5, Brodsky (0: 7%; <25%: 12%; 25-50%: 27%; >50 to <75%: 45%; >75%: 6%), AHI 12±7 pre AA. Global Cronbach alpha was 0.91. Correlations between domains were significant except for emotional aspects, although the total scores correlated with all domains (0.50 to 0.90). The factorial analysis was virtually identical to the original structure. The total scores showed good correlation for concurrent validity (0.2-0.45). With regard to predictive validity, the questionnaire adequately differentiated levels of severity according to Mallampati (ANOVA P=.002) and apnea-hypopnea index (ANOVA P=.006). Test-retest reliability was excellent, as was sensitivity to change, both in the total scores (P<.001) and in each domain (P<.001).
ConclusionsThe Spanish adaptation of the OSA-18 and its psychometric characteristics suggest that the Spanish version is equivalent to the original and can be used in Spanish-speaking countries.
El síndrome de apnea-hipopnea del sueño (SAHS) en la infancia es una patología altamente prevalente que afecta del 2 al 4% de niños entre los 2 y los 6 años1,2. La hipertrofia amigdalar y adenoidea, las malformaciones craneofaciales, la obesidad, las enfermedades neurológicas, como la parálisis cerebral infantil, las enfermedades neuromusculares, el reflujo gastroesofágico y la obesidad, son algunos de los factores de riesgo que con mayor frecuencia se presentan en la infancia2. El SAHS pediátrico está asociado a una importante morbilidad que afecta fundamentalmente al sistema nervioso central provocando trastornos neurocognitivos (memoria, inteligencia general, funciones ejecutivas, etc.) y conductuales, y al sistema cardiovascular, dando lugar a disfunción autonómica, arritmias cardíacas, hipertensión arterial3, remodelado ventricular4 y afectación endotelial5,6, además de comorbilidad endocrinometabólica7,8.
Las enfermedades crónicas como el SAHS pueden modificar la sensación de bienestar del paciente al afectar su entorno psicosocial. Esta alteración se puede medir y cuantificar por medio de cuestionarios de calidad de vida relacionados con la salud (CVRS). Para ello se precisa disponer de cuestionarios validados específicos, ya que presentan una mayor sensibilidad para los cambios tras alguna actuación terapéutica y son capaces de discernir las modificaciones9-11. La percepción subjetiva de mejoría tras tratamiento (principalmente cuando es necesaria la presión positiva continua en la vía respiratoria) se relacionará con la adherencia del paciente al mismo12. Un reciente metaanálisis mostró que los niños con SAHS tienen un peor estado de salud que los niños sanos13. Al igual que en los adultos, se han empleado cuestionarios genéricos, y ejemplo de ellos son el Glasgow Children's Benefit Inventory14, el Youth Quality of Life Instrument15 y otros13.
El desarrollo de cuestionarios dirigidos a la infancia y la adolescencia es reciente y tiene particularidades específicas, diferentes al adulto, por lo que es más necesaria aún la evaluación de sus propiedades psicométricas16. En el caso del SAHS infantil, los cuestionarios desarrollados están dirigidos a evaluar la CVRS por parte de los padres o cuidadores. Todos han sido elaborados para ser administrados en un entorno cultural anglosajón. Para poder ser aplicados en nuestro ambiente han de ser traducidos y adaptados a nuestra cultura17-20. Para ello hay que seguir unos pasos: comprobar que el concepto que se ha de medir existe en la cultura que se adapta, traducirlos de la lengua original a la cultura de la población diana, valorar las propiedades métricas del cuestionario adaptado y medir sus propiedades psicométricas (validez y fiabilidad)21.
Los cuestionarios específicos diseñados para SAHS infantil son muy escasos, siendo el cuestionario OSA-18, descrito en el año 2000 por Franco et al.22, el que se ha empleado en varios trabajos para evaluar los cambios posquirúrgicos, mostrándose fiable y sensible a los cambios postratamiento23-25.
En contraste con el amplio desarrollo de la medicina del sueño en adultos, hasta la fecha no existe en la literatura un cuestionario específico para SAHS infantil validado al español. Por ello, el objetivo de nuestro estudio fue analizar la fiabilidad y la validez de la versión española del cuestionario de CVRS OSA-18, para ser empleado en la evaluación inicial y en el seguimiento de niños con SAHS.
MétodoPara la adaptación del OSA-18 se siguieron las directrices generales de la Comisión Internacional de Test26 y las guías propuestas para la adaptación de cuestionarios de CVRS27. El proceso de adaptación se basó en el método de traducción y retrotraducción por profesionales y un estudio piloto con pacientes en distintas etapas28.
Periodo de estudioEnero de 2014 a marzo de 2015.
Primera fase: traducción al españolTras la autorización de los autores del OSA-18, se procedió a su traducción al español por 2 expertos bilingües, con lengua española como materna. Se unificaron las 2 versiones según consenso entre traductores y grupo investigador y se pasó inicialmente a los padres o cuidadores de niños con SAHS para comprobar la comprensión de las preguntas, adaptando comentarios para facilitar su lectura. El texto final se pasó a un experto traductor, bilingüe, de lengua nativa inglesa, para realizar la retrotraducción, y tras las correcciones pertinentes se adaptó a la traducción final al español. Los traductores puntuaron la dificultad de la traducción y la retrotraducción de cada ítem según escala de 1 (mínima) a 10 (máxima). El grupo investigador valoró igualmente la naturalidad-corrección de cada ítem de la versión española de 1 (mínimo) a 10 (máximo). Por último se realizó la equivalencia conceptual tras la retrotraducción en 3 apartados: A (totalmente equivalente), B (bastante equivalente, alguna expresión dudosa) y C (equivalencia dudosa).
Segunda fase: validación de los cuestionariosPara valorar si la versión traducida cumplía las mismas condiciones psicométricas que la versión original se evaluó la fiabilidad o la consistencia interna con el coeficiente α de Cronbach para cada una de las escalas, que mide el coeficiente de correlación media de cada ítem con el total de la escala y con su número total de ítems. Se consideró satisfactoria cuando fue >0,4 entre grupos y ≥0,8 individual (miden una única dimensión). La cohesión del instrumento se valoró mediante la correlación entre subescalas y entre subescala y el total. Para analizar la validez concurrente (constructo) se utilizaron los valores de correlación de Pearson o Spearman en función de la normalidad de distribución de las variables, de los diferentes dominios del cuestionario de forma global y por subescalas, con el índice de apnea-hipopnea (IAH) y otras variables respiratorias y antropométricas. La validez convergente correlacionó cada ítem con su dominio, y la validez divergente, cada ítem con otros dominios. La validez predictiva se analizó comparando los grupos de pacientes con distintos niveles de gravedad del SAHS según el punto de corte en el IAH mediante una prueba t de Student para medias independientes. Para evaluar la fiabilidad test-retest se efectuó un análisis de concordancia mediante el coeficiente de correlación intraclase (CCI) del cuestionario inicial y a la semana, por ítems y total, en las mismas condiciones. Se consideró una buena concordancia para valores del CCI superiores a 0,71 y moderada para valores entre 0,51 y 0,7029.
Se realizó un análisis descriptivo de las distintas variables con un estudio de su distribución para valorar el estadístico paramétrico o no paramétrico adecuado, y se valoró el efecto «techo» (porcentaje de respuestas con el máximo de puntuación), el efecto «suelo» (porcentaje con el mínimo de puntuación), así como el porcentaje de ítems no contestados y el porcentaje de ítems no aplicables.
Tercera fase: sensibilidad al cambioUna tercera fase valoró los cambios en la calidad de vida mediante OSA-18, en respuesta al tratamiento, comparando los valores de todos los dominios del cuestionario antes y después del tratamiento mediante una prueba t de Student para medias repetidas.
Población- •
Criterios de inclusión. Niños entre 2 y 14 años remitidos a la Unidad de Sueño, diagnosticados de SAHS mediante polisomnografía (PSG).
- •
Criterios de exclusión. Imposibilidad para completar el seguimiento por razones de lejanía, inmunodepresión (niños gravemente malnutridos, con inmunodeficiencias primarias y sida), rechazo de los padres a participar en el estudio, historia previa de cirugía de vía aérea o de otro tipo de intervención, como cauterización o termoplastia).
El protocolo diagnóstico consistió en obtención de medidas antropométricas (peso, talla, IMC, percentil de IMC, perímetro del cuello), cuestionario de síntomas relacionados con el SAHS30, escala de Mallampati31, grado de hipertrofia amigdalar mediante escala de Brodsky, realización de PSG nocturna hospitalaria vigilada, evaluación basal de cuestionarios OSA-18 administrados a los padres o cuidadores el mismo día de la prueba. Tras la PSG los niños fueron remitidos al servicio de ORL en caso de considerarse susceptibles de tratamiento quirúrgico. Los pacientes fueron evaluados con nueva PSG entre 3 y 6meses tras la cirugía para evaluar los cambios en los parámetros respiratorios tras el tratamiento. El mismo día se obtuvieron los datos antropométricos, los cuestionarios de síntomas y se repitió el test OSA-18.
Estudio polisomnográficoPara el diagnóstico se empleó un sistema de PSG Alice 5 (Philips Respironics) con monitorización de EEG, EOG, flujo nasal (sonda de presión), EMG mentoniano, movimientos torácicos y abdominales, ECG y EMG tibial de ambas piernas. Para definir los eventos respiratorios se emplearon los criterios del documento de consenso del síndrome de apnea-hipopnea durante el sueño en niños1. Los registros poligráficos fueron interpretados y corregidos manualmente por el mismo observador. Se clasificaron los distintos niveles de gravedad como SAHS leve: IAH<5, SAHS moderado: IAH de 5 a 10, y SAHS grave: IAH>101.
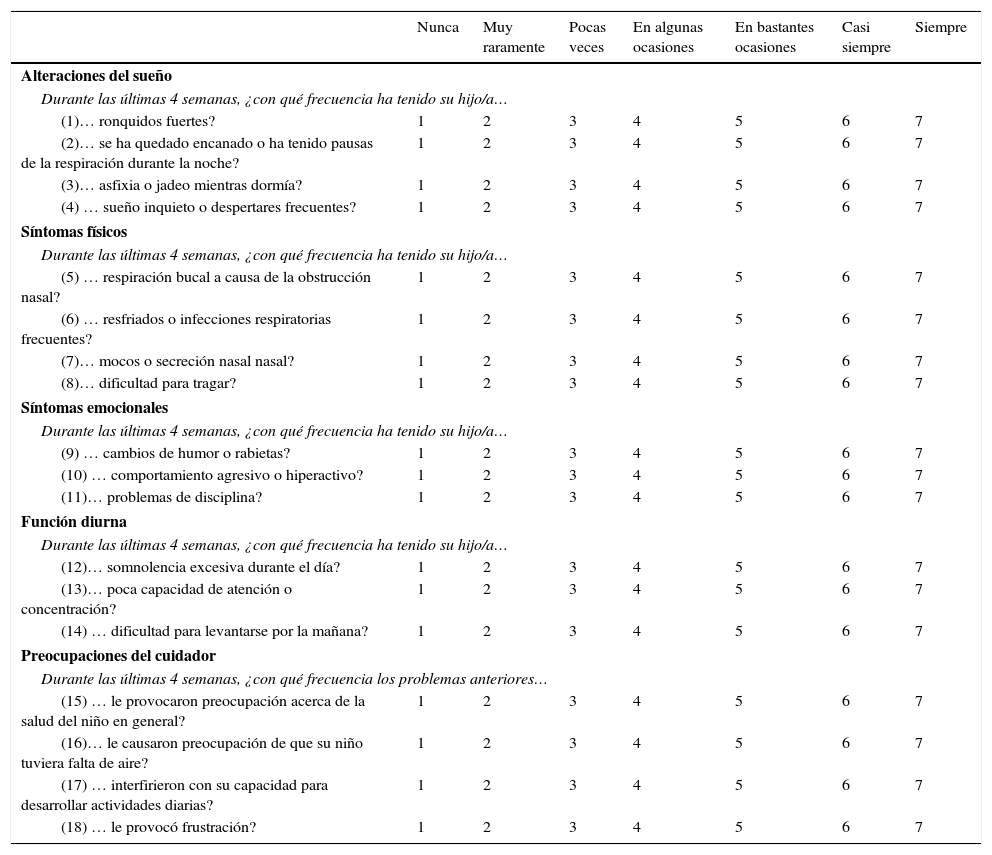
Cuestionario OSA-18El cuestionario incluye 18 ítems agrupados en 5 dominios, siendo puntuados cada uno de los ítems en una escala ordinal de 7 puntos.
Los dominios del OSA-18 contienen las siguientes puntuaciones:
- a)
Trastorno del sueño (4 ítems con puntuaciones entre 4 y 28).
- b)
Sufrimiento físico (4 ítems con puntuaciones entre 4 y 28).
- c)
Sufrimiento emocional (3 ítems con puntuaciones entre 3 y 21).
- d)
Problemas diarios (3 ítems con puntuaciones entre 3 y 21).
- e)
Preocupación de los padres o cuidadores (4 ítems con puntuaciones entre 4 y 28).
La puntuación total OSA-18 puede oscilar entre 18 y 126. El cuestionario OSA-18 permite clasificar el impacto sobre la calidad de vida en leve (puntuación menor de 60), moderado (puntuación entre 60 y 80) y grave (puntuación por encima de 80).
Cálculo del tamaño muestralPara el estudio inicial se calculó un nivel de confianza o seguridad (1-α): 95%; precisión (d): 3%; proporción (valor aproximado del parámetro a medir): 5%, calculando así una muestra necesaria (n) inicial de 80 niños. Ajustando el tamaño muestral a las pérdidas, con una proporción esperada (R) de un 15%, la muestra total se calculó en 60 individuos.
Para el cálculo del número de pacientes necesarios para determinar la fiabilidad test-retest y la sensibilidad al cambio calculamos un tamaño de muestra de 20 pacientes. El criterio utilizado para la estimación del tamaño de la muestra viene dado por los requerimientos estadísticos necesarios para poder calcular el coeficiente de fiabilidad, suponiendo un valor esperado del coeficiente de fiabilidad ≥0,85, con esa muestra y un intervalo de confianza ±0,10 para una Zα2=1,96.
EstadísticaSe efectuó un análisis descriptivo de las variables cuantitativas, expresadas como media y desviación estándar, o mediana y rango, según el tipo de distribución. Se analizó la normalidad de las distribuciones mediante la prueba de Kolmogorov-Smirnov. Además de los cálculos empleados para la validación de los cuestionarios, se empleó el test de ANOVA para medidas repetidas o el de Kruskal-Wallis y el test de comparación múltiple de medias para valorar los cambios en las puntuaciones de cada uno de los cuestionarios. El nivel mínimo exigido para todos los cálculos fue una p<0,05. Los cálculos estadísticos se efectuaron mediante el programa SPSS versión 18.
Aspectos éticosSe obtuvo consentimiento informado a los padres y cuidadores para realizar el estudio. El proyecto respetó los principios fundamentales establecidos en la Declaración de Helsinki, en el Convenio del Consejo de Europa relativo a los derechos humanos y la biomedicina, en la Declaración Universal de la UNESCO sobre el genoma humano y los derechos humanos, así como los requisitos establecidos en la legislación española en el ámbito de la investigación biomédica, la protección de datos de carácter personal y la bioética.
ResultadosSe incluyeron 60 pacientes consecutivos, aceptando los padres la participación en todos los casos. Se evaluaron 45 niños y 15 niñas, con una edad de 6±3 años, un IMC de 18±4kg/m2 y un perímetro de cuello medio de 28±5cm. El índice de Brodsky fue 0 en un 7%, menor del 25% en un 12%, entre 25 y 50% en un 27%, entre 50 y 75% en un 45%, y más de 75% en un 6%. El IAH medio tras la PSG fue de 12±7h−1.
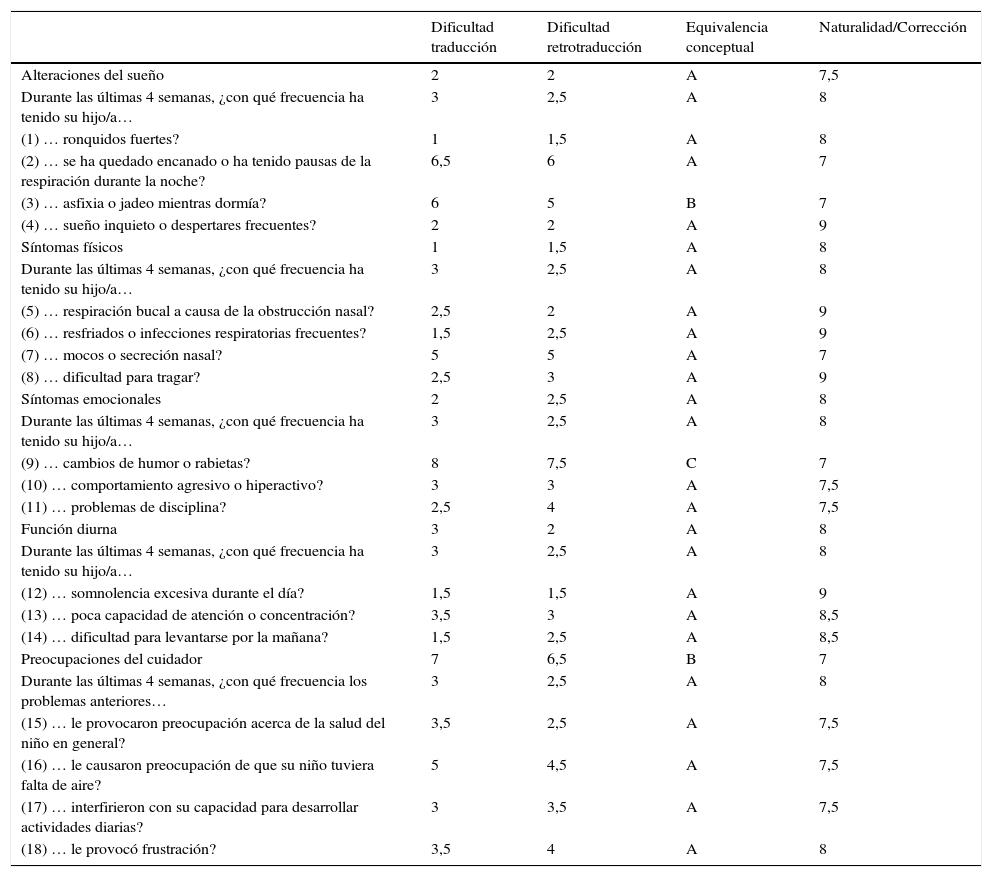
La dificultad de traducción fue superior a 5 en 3 ítems (11%) y un dominio (4%). Tras la retrotraducción se consideraron 2 ítems (7%) de tipo B y uno de tipo C (4%). Se discutieron las dudas de equivalencia (B y C) y las expresiones equivalentes, pero poco naturales o gramaticalmente incorrectas en 2 reuniones, de investigadores y traductores. Se obtuvo una expresión final consensuada que se incluyó en una segunda versión. La versión final alcanzó puntuaciones >7 en todos los ítems y dominios. La nueva versión fue administrada a los padres de 10 niños entre 2 y 14 años diagnosticados de SAHS por PSG, consensuando la versión definitiva del cuestionario (tabla 1).
Traducción y retrotraducción del cuestionario OSA-18
| Dificultad traducción | Dificultad retrotraducción | Equivalencia conceptual | Naturalidad/Corrección | |
|---|---|---|---|---|
| Alteraciones del sueño | 2 | 2 | A | 7,5 |
| Durante las últimas 4 semanas, ¿con qué frecuencia ha tenido su hijo/a… | 3 | 2,5 | A | 8 |
| (1) … ronquidos fuertes? | 1 | 1,5 | A | 8 |
| (2) … se ha quedado encanado o ha tenido pausas de la respiración durante la noche? | 6,5 | 6 | A | 7 |
| (3) … asfixia o jadeo mientras dormía? | 6 | 5 | B | 7 |
| (4) … sueño inquieto o despertares frecuentes? | 2 | 2 | A | 9 |
| Síntomas físicos | 1 | 1,5 | A | 8 |
| Durante las últimas 4 semanas, ¿con qué frecuencia ha tenido su hijo/a… | 3 | 2,5 | A | 8 |
| (5) … respiración bucal a causa de la obstrucción nasal? | 2,5 | 2 | A | 9 |
| (6) … resfriados o infecciones respiratorias frecuentes? | 1,5 | 2,5 | A | 9 |
| (7) … mocos o secreción nasal? | 5 | 5 | A | 7 |
| (8) … dificultad para tragar? | 2,5 | 3 | A | 9 |
| Síntomas emocionales | 2 | 2,5 | A | 8 |
| Durante las últimas 4 semanas, ¿con qué frecuencia ha tenido su hijo/a… | 3 | 2,5 | A | 8 |
| (9) … cambios de humor o rabietas? | 8 | 7,5 | C | 7 |
| (10) … comportamiento agresivo o hiperactivo? | 3 | 3 | A | 7,5 |
| (11) … problemas de disciplina? | 2,5 | 4 | A | 7,5 |
| Función diurna | 3 | 2 | A | 8 |
| Durante las últimas 4 semanas, ¿con qué frecuencia ha tenido su hijo/a… | 3 | 2,5 | A | 8 |
| (12) … somnolencia excesiva durante el día? | 1,5 | 1,5 | A | 9 |
| (13) … poca capacidad de atención o concentración? | 3,5 | 3 | A | 8,5 |
| (14) … dificultad para levantarse por la mañana? | 1,5 | 2,5 | A | 8,5 |
| Preocupaciones del cuidador | 7 | 6,5 | B | 7 |
| Durante las últimas 4 semanas, ¿con qué frecuencia los problemas anteriores… | 3 | 2,5 | A | 8 |
| (15) … le provocaron preocupación acerca de la salud del niño en general? | 3,5 | 2,5 | A | 7,5 |
| (16) … le causaron preocupación de que su niño tuviera falta de aire? | 5 | 4,5 | A | 7,5 |
| (17) … interfirieron con su capacidad para desarrollar actividades diarias? | 3 | 3,5 | A | 7,5 |
| (18) … le provocó frustración? | 3,5 | 4 | A | 8 |
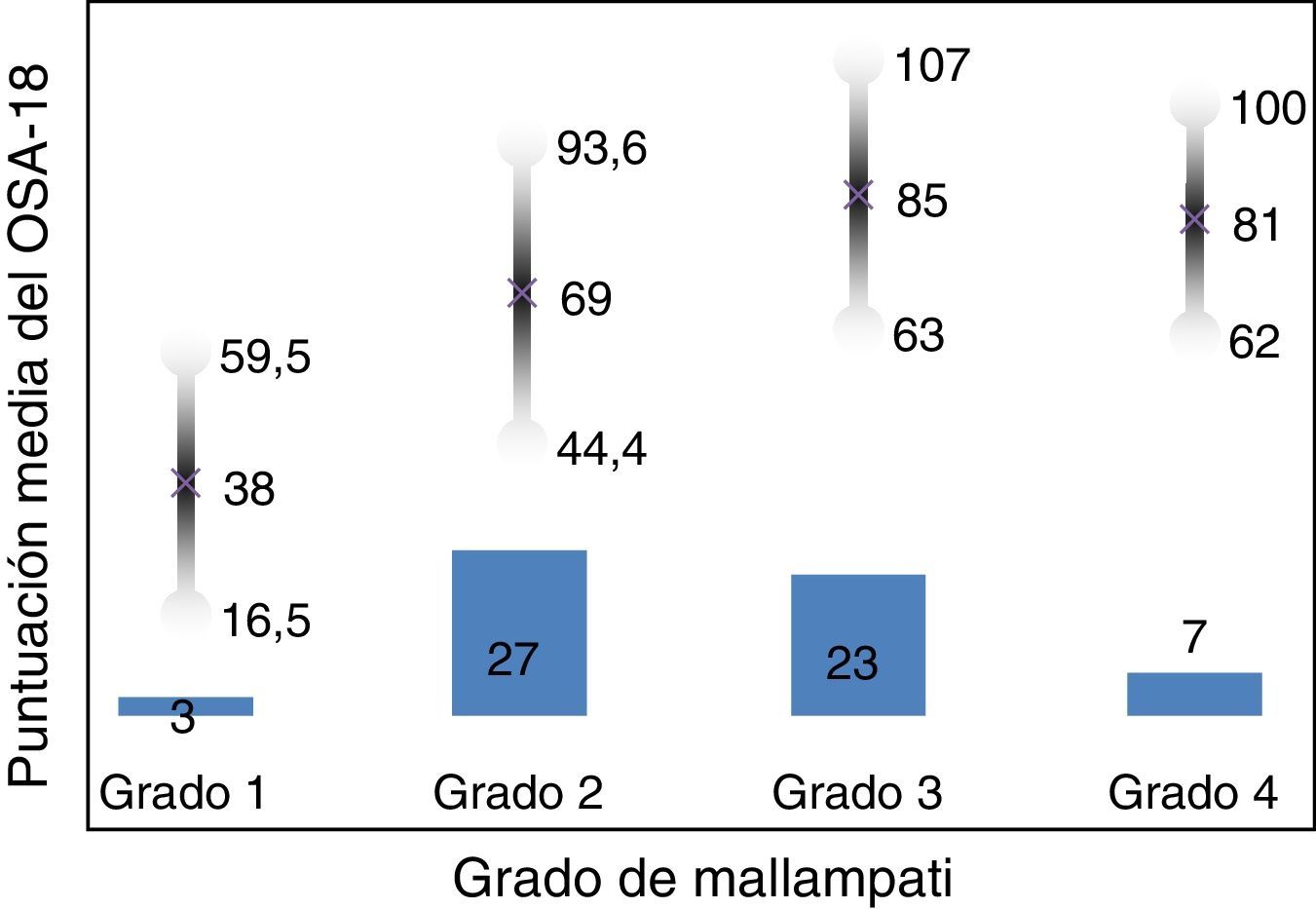
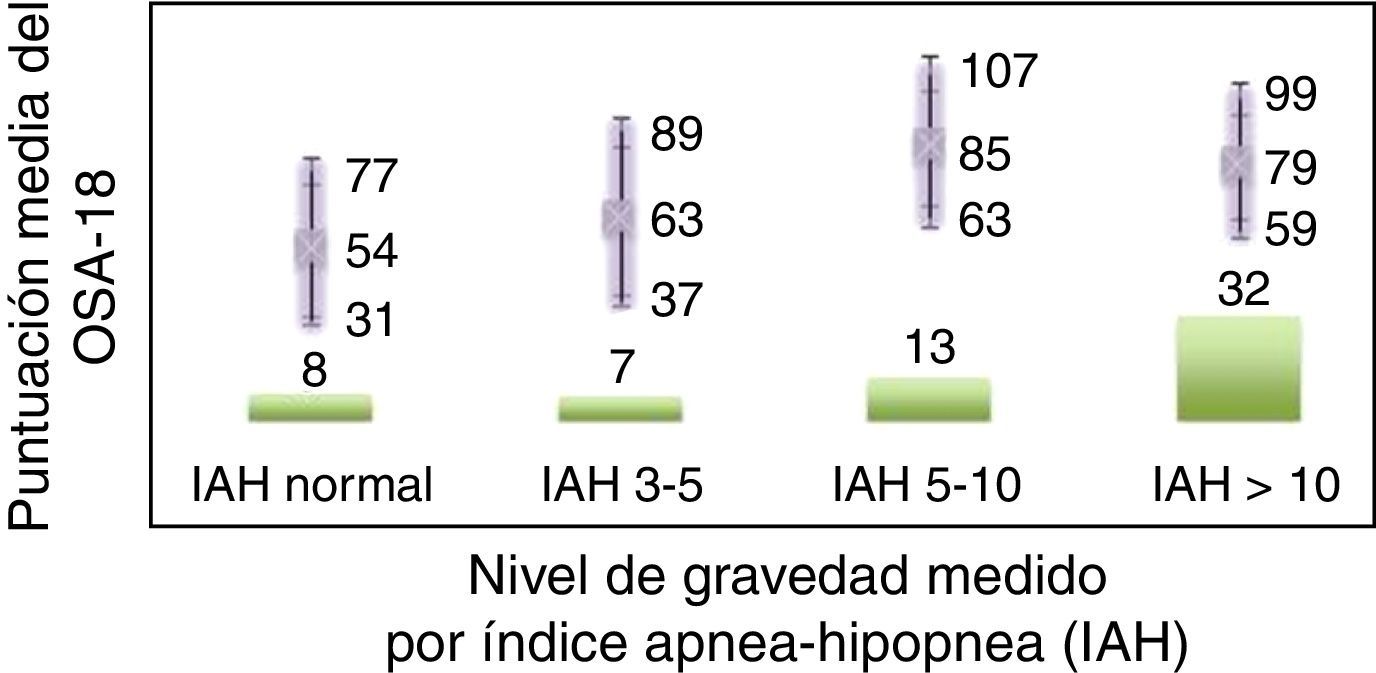
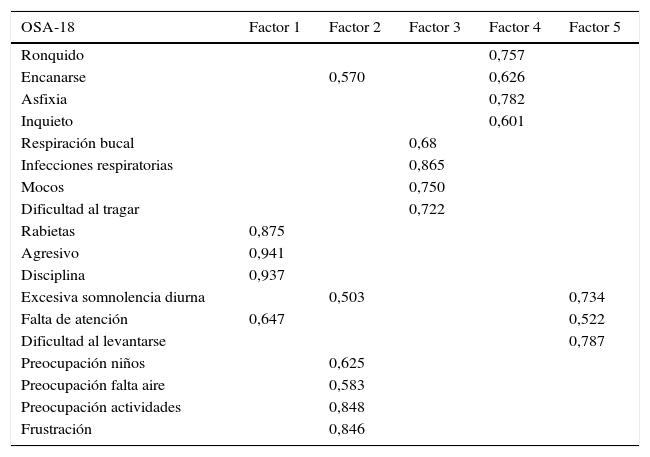
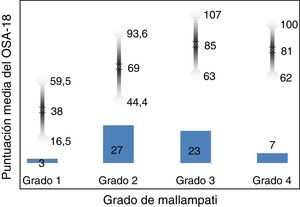
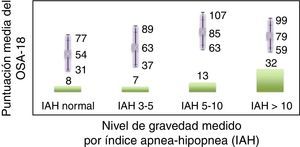
La consistencia interna o fiabilidad analizada mediante el alfa de Cronbach, de forma global fue de 0,91, lo que expresa excelente fiabilidad, así como el de cada dominio, sin variaciones significativas al excluir cada ítem de un determinado dominio, o un dominio del global (tabla 2). Las correlaciones entre dominios fueron significativas salvo para el de aspectos emocionales, aunque el valor global se correlacionó con todos los dominios. Los ítems mostraron una distribución normal, sin presentar efecto techo en ningún dominio (máximo 10% de pacientes en D5), ni tampoco efecto suelo, tan solo en D3 (30% pacientes). Al analizar el cuestionario de forma global, presentó 0% en el efecto suelo y en el efecto techo. El valor del cuestionario global se correlacionó con todos los dominios de forma significativa. La validez de constructo mediante análisis factorial de componentes principales con rotación varimax y forzando una estructura de 5 componentes correspondientes a las 5 dimensiones del cuestionario se muestra en la tabla 3, donde se presentan solo las saturaciones mayores de 0,5. Se observa que la forma de estructurarse el cuestionario en su versión castellana es prácticamente idéntica a la forma de estructurarse el cuestionario original. Los ítems se agrupan de la misma forma y saturan en los componentes a los que pertenecen. Tan solo hay una excepción: el ítem «falta de atención basal», que en el cuestionario original pertenece al dominio de función diaria, satura mejor en este cuestionario en el dominio emocional, lo cual es explicable dadas las características del ítem en cuestión y del dominio. En la validez concurrente, el análisis global mostró buena correlación (0,2-0,45), con la mayoría de variables con las que correlacionan los dominios y de los dominios con aquellas variables que miden. De forma individual, D1 con ronquidos, apneas, asfixia presenta correlaciones entre 0,32-0,46; D2 con obstrucción nasal y síntomas nasales, entre 0,2-0,28; D3 presenta las peores correlaciones (p.ej., con hiperactividad o timidez) pero muestra buena correlación con rendimiento escolar (0,35); D4 correlaciona con rendimiento escolar e hipersomnia (0,2-0,3), y D5 correlaciona con síntomas y rendimiento escolar de forma significativa (0,24-0,35). Al valorar la validez predictiva, el cuestionario diferenció adecuadamente los niveles de gravedad según el Mallampati (ANOVA p=0,002) y el IAH (ANOVA p=0,006) (figs. 1 y 2). La sensibilidad al cambio fue excelente, tanto en el global (p<0,001) como en cada dominio (p<0,001) (tabla 4). La repetibilidad test-retest fue asimismo excelente, tanto en el global como en cada dominio (tabla 5).
Validez de constructoa
| OSA-18 | Factor 1 | Factor 2 | Factor 3 | Factor 4 | Factor 5 |
|---|---|---|---|---|---|
| Ronquido | 0,757 | ||||
| Encanarse | 0,570 | 0,626 | |||
| Asfixia | 0,782 | ||||
| Inquieto | 0,601 | ||||
| Respiración bucal | 0,68 | ||||
| Infecciones respiratorias | 0,865 | ||||
| Mocos | 0,750 | ||||
| Dificultad al tragar | 0,722 | ||||
| Rabietas | 0,875 | ||||
| Agresivo | 0,941 | ||||
| Disciplina | 0,937 | ||||
| Excesiva somnolencia diurna | 0,503 | 0,734 | |||
| Falta de atención | 0,647 | 0,522 | |||
| Dificultad al levantarse | 0,787 | ||||
| Preocupación niños | 0,625 | ||||
| Preocupación falta aire | 0,583 | ||||
| Preocupación actividades | 0,848 | ||||
| Frustración | 0,846 |
a Solo se tabulan las saturaciones > 0,50.
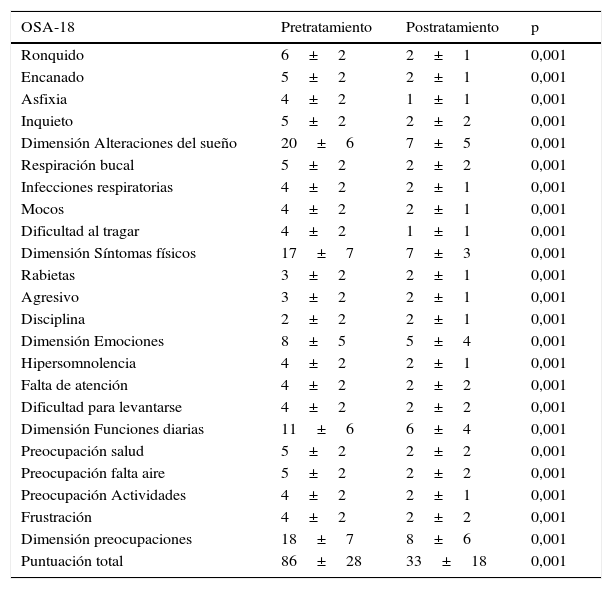
Sensibilidad al cambio
| OSA-18 | Pretratamiento | Postratamiento | p |
|---|---|---|---|
| Ronquido | 6±2 | 2±1 | 0,001 |
| Encanado | 5±2 | 2±1 | 0,001 |
| Asfixia | 4±2 | 1±1 | 0,001 |
| Inquieto | 5±2 | 2±2 | 0,001 |
| Dimensión Alteraciones del sueño | 20±6 | 7±5 | 0,001 |
| Respiración bucal | 5±2 | 2±2 | 0,001 |
| Infecciones respiratorias | 4±2 | 2±1 | 0,001 |
| Mocos | 4±2 | 2±1 | 0,001 |
| Dificultad al tragar | 4±2 | 1±1 | 0,001 |
| Dimensión Síntomas físicos | 17±7 | 7±3 | 0,001 |
| Rabietas | 3±2 | 2±1 | 0,001 |
| Agresivo | 3±2 | 2±1 | 0,001 |
| Disciplina | 2±2 | 2±1 | 0,001 |
| Dimensión Emociones | 8±5 | 5±4 | 0,001 |
| Hipersomnolencia | 4±2 | 2±1 | 0,001 |
| Falta de atención | 4±2 | 2±2 | 0,001 |
| Dificultad para levantarse | 4±2 | 2±2 | 0,001 |
| Dimensión Funciones diarias | 11±6 | 6±4 | 0,001 |
| Preocupación salud | 5±2 | 2±2 | 0,001 |
| Preocupación falta aire | 5±2 | 2±2 | 0,001 |
| Preocupación Actividades | 4±2 | 2±1 | 0,001 |
| Frustración | 4±2 | 2±2 | 0,001 |
| Dimensión preocupaciones | 18±7 | 8±6 | 0,001 |
| Puntuación total | 86±28 | 33±18 | 0,001 |
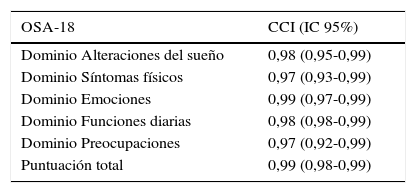
Análisis de repetibilidad test-retest
| OSA-18 | CCI (IC 95%) |
|---|---|
| Dominio Alteraciones del sueño | 0,98 (0,95-0,99) |
| Dominio Síntomas físicos | 0,97 (0,93-0,99) |
| Dominio Emociones | 0,99 (0,97-0,99) |
| Dominio Funciones diarias | 0,98 (0,98-0,99) |
| Dominio Preocupaciones | 0,97 (0,92-0,99) |
| Puntuación total | 0,99 (0,98-0,99) |
CCI (IC 95%): coeficiente de correlación intraclase con su intervalo de confianza al 95%.
El concepto de salud en niños/as y adolescentes no solo considera los aspectos físicos, psicológicos y sociales, sino también la habilidad para realizar actividades apropiadas para su edad. En el caso de los niños/as y adolescentes, las dimensiones que generalmente se tienen en cuenta están relacionadas con su capacidad para realizar actividades diarias (movilidad y cuidado personal), las adquisiciones cognitivas (memoria, habilidad para concentrarse y aprender), las emociones (positivas y negativas), la percepción de sí mismo, las relaciones interpersonales (con los amigos y familiares) y con el medio que los rodea (cohesión familiar, apoyo social). La mayoría de los instrumentos de CVRS en edad pediátrica están concebidos según el modelo psicométrico que se basa en la capacidad del individuo para discernir entre estímulos de diferente intensidad recogiendo las respuestas en escalas (generalmente de tipo Likert).
En algunas unidades se emplea el Pediatric Sleep Questionnaire, desarrollado por la Universidad de Michigan, como cribado previo de pacientes con SAHS infantil, para evitar la PSG, o como cuestionario de síntomas. La versión española validada no parece que sea correcta en su dimensión de comportamiento diurno y somnolencia respecto al original32,33, dimensiones que sin duda son de extraordinaria importancia en el SAHS infantil.
El cuestionario OSA-18 ha sido adaptado a otros idiomas34-36, mostrando su utilidad en el abordaje del SAHS infantil. Algunos autores lo han empleado como cribado para valorar si puede sustituir la PSG, aunque el cuestionario no fue diseñado con este objetivo37.
El cuestionario OSA-18 presenta una excelente consistencia interna. La validez predictiva es buena-excelente, si bien sería mejorable si los grupos de gravedad estuvieran más balanceados respecto al número (hay una tendencia a una importante gravedad del SAHS), y la validez concurrente es asimismo buena. El dominio más problemático en cuanto a sus características psicométricas es el emocional. El constructo es prácticamente idéntico al del cuestionario original. Además, se ha observado que este cuestionario es un muy buen predictor al ser comparado con la escala de Mallampati y con la gravedad del SAHS medida por el IAH.
En conclusión, los resultados sugieren que la versión española del cuestionario OSA-18 es equivalente a la original y puede ser empleada en países de habla hispana (Anexo 1).
FinanciaciónFinanciado en parte por una beca de la Fundación Valenciana de Neumología (2013) y Beca SEPAR 2014.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
| Nunca | Muy raramente | Pocas veces | En algunas ocasiones | En bastantes ocasiones | Casi siempre | Siempre | |
|---|---|---|---|---|---|---|---|
| Alteraciones del sueño | |||||||
| Durante las últimas 4 semanas, ¿con qué frecuencia ha tenido su hijo/a… | |||||||
| (1)… ronquidos fuertes? | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| (2)… se ha quedado encanado o ha tenido pausas de la respiración durante la noche? | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| (3)… asfixia o jadeo mientras dormía? | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| (4) … sueño inquieto o despertares frecuentes? | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| Síntomas físicos | |||||||
| Durante las últimas 4 semanas, ¿con qué frecuencia ha tenido su hijo/a… | |||||||
| (5) … respiración bucal a causa de la obstrucción nasal? | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| (6) … resfriados o infecciones respiratorias frecuentes? | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| (7)… mocos o secreción nasal nasal? | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| (8)… dificultad para tragar? | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| Síntomas emocionales | |||||||
| Durante las últimas 4 semanas, ¿con qué frecuencia ha tenido su hijo/a… | |||||||
| (9) … cambios de humor o rabietas? | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| (10) … comportamiento agresivo o hiperactivo? | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| (11)… problemas de disciplina? | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| Función diurna | |||||||
| Durante las últimas 4 semanas, ¿con qué frecuencia ha tenido su hijo/a… | |||||||
| (12)… somnolencia excesiva durante el día? | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| (13)… poca capacidad de atención o concentración? | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| (14) … dificultad para levantarse por la mañana? | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| Preocupaciones del cuidador | |||||||
| Durante las últimas 4 semanas, ¿con qué frecuencia los problemas anteriores… | |||||||
| (15) … le provocaron preocupación acerca de la salud del niño en general? | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| (16)… le causaron preocupación de que su niño tuviera falta de aire? | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| (17) … interfirieron con su capacidad para desarrollar actividades diarias? | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| (18) … le provocó frustración? | 1 | 2 | 3 | 4 | 5 | 6 | 7 |