Historia de la oxigenoterapia
La vida humana no puede entenderse sin la presencia de la molécula de oxígeno. Su ausencia es sinónimo de muerte; su presencia, de vida. La existencia del oxígeno se descubrió el 1 de agosto de 1774, gracias al trabajo del científico británico J. Priestley1. Éste lo definió como un "aire puro que sin duda se convertiría en un artículo de lujo". Paralelamente, sin conocer la existencia de dicho trabajo, el químico sueco C.W. Scheele2 aisló también la molécula de oxígeno, aunque fue el primero al que la historia reservó la gloria. Años más tarde, este nuevo "aire" adquirió su denominación definitiva: A. Lavoisier, amigo de Priestley, y por tanto conocedor de sus experimentos, lo bautizó con el nombre de "oxygene"3. El oxígeno se introdujo en la práctica médica durante el siglo xix. El primer documento escrito que demuestra su eficacia terapéutica en el tratamiento de las enfermedades respiratorias se remonta a 1885, cuando el Dr. G. Holtzapple lo usó con éxito en un joven neoyorquino que presentaba un cuadro de distrés respiratorio secundario a una neumonía4, aunque antes de esa fecha los médicos de la época lo usaban con fines muy diversos.
A principios del siglo XX el fisiólogo inglés J.S. Haldane5 fue el primero en demostrar los efectos de la hipoxemia (cefalea matutina, taquicardia y taquipnea)5, afirmando que pronto el uso del oxígeno se extendería por los hospitales para tratar los citados síntomas. Este hecho comenzó a ser realidad en años posteriores gracias, entre otros, a los trabajos publicados por el Dr. A. Barach, considerado el padre de la oxigenoterapia moderna. En 1922 este autor publicó un artículo en el que se racionalizaba el uso del oxígeno para el tratamiento de la neumonía ("oxigenoterapia aguda")6. En años posteriores, con los conocimientos adquiridos en un laboratorio de fisiología pulmonar durante la Segunda Guerra Mundial, Barach desarrolló un sistema, a partir de las mascarillas de los pilotos de aviones, que permitía la administración de oxígeno de manera continua ("oxigenoterapia crónica"). Aún fue más ingenioso cuando, a mediados de los años cincuenta, diseñó un sistema de pequeñas bombonas alrededor de la cintura, con el objetivo de administrar el oxígeno también fuera del domicilio ("oxigenoterapia en deambulación")7. En 1956 Cotes y Gilson8 publicaron un artículo en el que demostraban la mejoría clínica de los pacientes que utilizaban oxígeno durante el ejercicio.
La administración controlada de oxígeno se introduce en los años sesenta, cuando Campbell9, aplicando el efecto Venturi, diseñó unas mascarillas de oxígeno que permitían regular la fracción inspiratoria de oxígeno (FiO2) proporcionada. Su objetivo era obtener un mayor control del oxígeno administrado a los pacientes con enfermedad pulmonar obstructiva crónica (EPOC), dado que algunos presentaban complicaciones secundarias a la administración de flujos altos. En esos mismos años, diversos grupos de investigadores, entre los que destacaba el liderado por el Dr. T. Petty, realizaron los primeros estudios sistemáticos con oxigenoterapia crónica. Describieron una mejoría en la tolerancia al ejercicio y una reducción tanto de la eritrocitosis como de la hipertensión pulmonar10,11. En años posteriores la evidencia acumulada indicaba asimismo una disminución de la hospitalización y mortalidad de los pacientes tratados con oxígeno12,13. De esta inquietud nacieron los estudios, ya clásicos, Nocturnal Oxygen Therapy Trial (NOTT)14 y el del British Medical Research Council (MRC)15. El primero, norteamericano, estudiaba a pacientes con EPOC y oxígeno continuo (una media de 17,4 h/día) frente a oxígeno nocturno (12 h/día). En cambio, el estudio del MRC analizaba a pacientes con EPOC que no recibían oxigenoterapia, frente a los que sí la recibían (una media de 15 h/día). Ambos estudios demostraron el aumento de la supervivencia en los pacientes con oxigenoterapia, supervivencia que era mayor cuantas más horas de oxígeno recibían. Estos estudios sentaron las bases de la oxigenoterapia crónica domiciliaria en pacientes con EPOC, indicaciones que, por extensión, se aplican a las otras enfermedades pulmonares crónicas, aunque su utilidad no se haya demostrado suficientemente16.
Fuentes de oxígeno
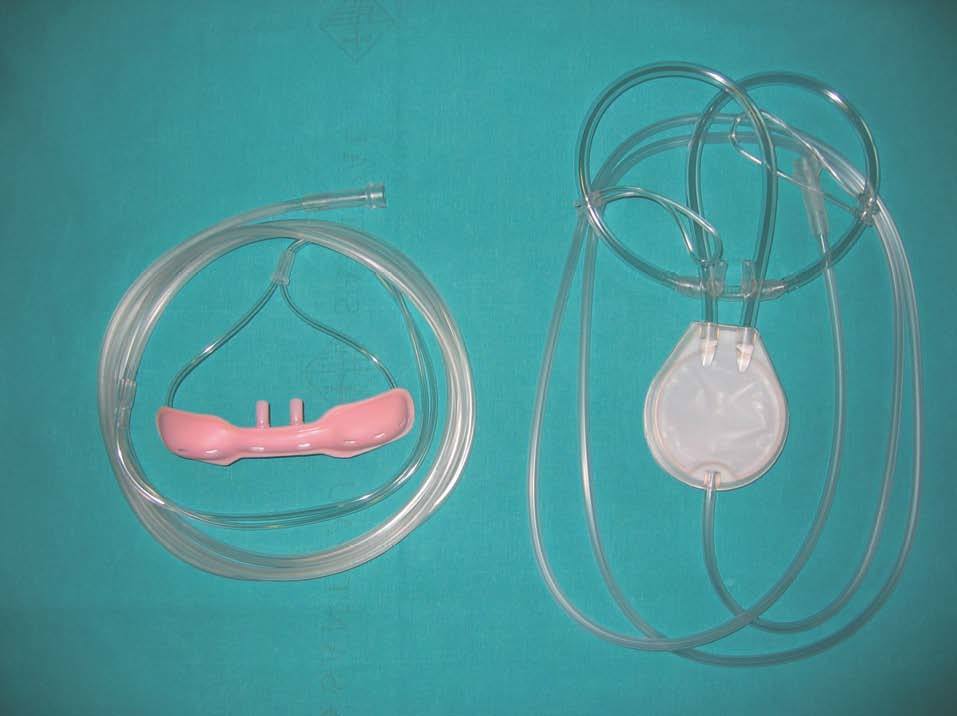
Las principales fuentes de oxígeno son el gas comprimido, el concentrador y el oxígeno líquido. Las características principales de cada uno se exponen en la tabla I.
La primera fuente de oxígeno que se utilizó fueron las bombonas de gas comprimido. Ampliamente extendidas, su principal inconveniente surge de su tamaño y peso, que suponen una importante limitación para el paciente, dado que dificultan su movilidad incluso dentro del domicilio; problema que puede solventarse parcialmente con el uso de bombonas portátiles. El concentrador aparece a principios de los años setenta. Su funcionamiento consiste en concentrar el oxígeno del aire ambiente separándolo del nitrógeno mediante unos filtros. Tiene la ventaja de ser un sistema autónomo (no es necesario rellenar una unidad base cada cierto tiempo, como en los anteriores), aunque su gran limitación estriba en que es preciso que esté conectado a la red eléctrica para funcionar, lo que impide los desplazamientos del paciente. El oxígeno líquido se introdujo para su uso doméstico en 1965. Union Carbide, trabajando con Petty, desarrolló un pequeño sistema portátil que tenía el peso y el tamaño adecuados a las necesidades de los pacientes17. Además, podía rellenarse desde una unidad de base. Aunque la autonomía de este sistema es limitada (dependiendo sobre todo del flujo prescrito), permite a los pacientes asegurar una correcta saturación de oxihemoglobina mientras realizan sus actividades cotidianas, dentro y fuera del domicilio.
El oxígeno líquido ha demostrado mejorar la calidad de vida de los pacientes que reciben oxigenoterapia crónica domiciliaria al permitir mayor movilidad y autonomía en las actividades cotidianas dentro y fuera del domicilio18. Un reciente metaanálisis de la biblioteca Cochrane concluye que el oxígeno ambulatorio mejora el rendimiento del ejercicio en las personas con EPOC moderada a grave19. Además, también se ha demostrado que los pacientes con EPOC sin hipoxemia diurna grave (presión arterial de oxígeno > 60 mmHg) que realizan un programa de rehabilitación pulmonar pueden aumentar la capacidad de entrenamiento si reciben oxígeno20. A pesar de esta evidencia, y dado que el coste del oxígeno líquido es mayor que el de las otras fuentes estáticas de administración, los proveedores de equipos médicos prefieren el uso de los concentradores de oxígeno y, en menor medida, las bombonas de gas comprimido, para reducir los gastos, relegando así al oxígeno líquido a un papel secundario21,22. Esta actitud es, además, abiertamente agradecida por la economía de los sistemas sanitarios nacionales.
Sistemas de ahorro de oxígeno
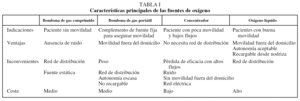
Con el objetivo de aumentar la autonomía de las fuentes de oxígeno portátiles mediante la disminución del gasto de oxígeno, a mediados de los años ochenta aparecieron los sistemas de ahorro. Los principales métodos disponibles actualmente son el catéter transtraqueal, las cánulas reservorio y los sistemas a demanda23. Dado que se admite que las cánulas nasales convencionales son un sistema ineficiente, pues sólo un 15-20% del oxígeno administrado participa en el intercambio gaseoso24, los sistemas de ahorro se concibieron para utilizar menos oxígeno, pero de una manera más eficiente. Así, se estima que pueden aumentar la autonomía de un pequeño cilindro hasta 3 veces más que con oxígeno continuo utilizando las gafas nasales convencionales25. Esto permite optimizar la administración de oxígeno, además de conseguir una mayor competitividad económica de las fuentes portátiles. En la tabla II se resumen sus principales características.
Catéter transtraqueal
El catéter transtraqueal proporciona oxígeno directamente en la tráquea a través de un pequeño catéter de 1,6-2 mm de diámetro, que se introduce por vía percutánea, a la altura del segundo-tercer anillo traqueal. De esta manera se evita el espacio muerto creado por la cavidad orofaríngea y, además, la vía aérea superior actúa como reservorio, con lo que aumenta la FiO2 y se consigue mantener saturaciones de oxihemoglobina similares al las del sistema convencional, pero con menores flujos de oxígeno. Se estima que el catéter transtraqueal puede producir un ahorro de oxígeno de un 50% en reposo y de un 30% en ejercicio, aproximadamente26. Además, ha demostrado producir una disminución del trabajo respiratorio y de la disnea que presenta el paciente, gracias a la reducción de la ventilación27,28. También se ha demostrado una mejoría en la función hemodinámica29. Todo ello con un impacto significativo en la calidad de vida relacionada con la salud del paciente.
El uso del catéter transtraqueal está indicado principalmente para ahorro de oxígeno en pacientes que utilizan fuentes portátiles para la deambulación. Christopher et al30 también demostraron su utilidad en pacientes con hipoxemia refractaria. A pesar de que estéticamente no representa un inconveniente, ya que puede ocultarse bajo la ropa, los pacientes suelen rechazar su prescripción, sobre todo por ser un método invasivo, que además comporta un entrenamiento y una educación en su cuidado, y porque es preciso recambiarlo cada 60-90 días en ámbito hospitalario. Las principales complicaciones del catéter31 son locales, en la zona de inserción (enfisema subcutáneo, celulitis, hemorragia, etc.). Su uso está contraindicado de manera absoluta en pacientes con estenosis subglótica, parálisis de cuerda vocal, coagulopatía grave, acidosis respiratoria o incapacidad para mantener los cuidados, y relativamente contraindicado en estados que dificulten la correcta cicatrización o en pacientes con hipersecreción bronquial31.
No obstante, aunque el catéter transtraqueal fue introducido en la práctica médica hace más de 20 años por el Dr. Heimlich32, su prescripción sigue siendo muy infrecuente en la actualidad. Este hecho se debe fundamentalmente a 2 factores. Por un lado, tiene poca aceptación por parte de los pacientes, tal como demuestra el estudio de Díaz-Lobato et al33, en el que se utilizó el catéter transtraqueal para el tratamiento de la insuficiencia respiratoria y en el que sólo el 9% de los pacientes lo aceptaron para uso domiciliario. Por otro lado, los médicos tienen la sensación de que es un método que presenta muchas complicaciones, a pesar de que estudios recientes han demostrado que es un sistema de administración seguro34.
En conclusión, numerosos grupos señalan que el catéter transtraqueal es el medio ideal para la administración de oxígeno continuo durante 24 h en pacientes con actividad conservada (en ausencia de contraindicaciones para su prescripción).
Cánulas reservorio
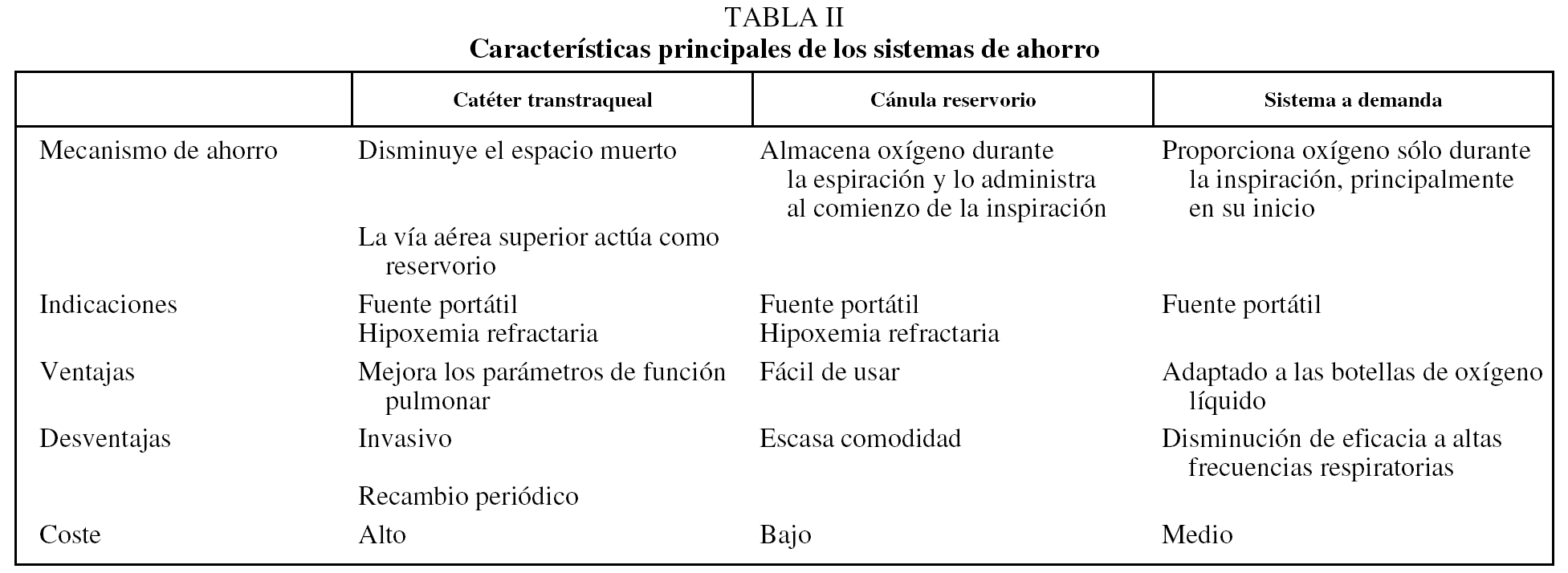
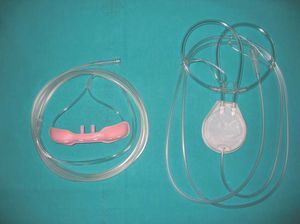
Las cánulas reservorio nacieron a mediados de los años ochenta con la intención de aumentar la eficacia de las cánulas nasales convencionales. Para ello, aumentan el volumen de oxígeno administrado al inicio de la inspiración, hecho que representará una mayor FiO2 en la fracción de volumen corriente que realmente participa en el intercambio gaseoso. El reservorio dispone de una membrana que se desplaza durante la espiración, lo que permite el almacenamiento de unos 30-40 ml de oxígeno proveniente de la fuente (y que normalmente se desperdiciaría), el cual se administra como un bolo al comienzo de la inspiración. Se dispone de 2 modelos: Oxymizer, en el que el reservorio se coloca directamente en la nariz, y el Oxymizer Pendant, en el cual el reservorio se sitúa en el pecho y se conecta a la nariz por medio de 2 cánulas nasales de mayor grosor que las convencionales (fig. 1). Usando este sistema se puede mantener una saturación de oxígeno adecuada, con un menor flujo administrado35, lo que produce el ahorro de oxígeno deseado. Su uso está indicado tanto para aumentar la autonomía de las fuentes portátiles como para optimizar el tratamiento de pacientes que utilicen fuentes fijas, dado que éstas, a veces, no pueden alcanzar el flujo necesario con los sistemas de administración convencionales. No obstante, las cánulas reservorio presentan el problema de que, a elevada frecuencia respiratoria, como ocurre en las enfermedades restrictivas, los pacientes utilizan más la boca para respirar, lo que disminuye su eficacia36, por lo que hay que concienciar a los pacientes para que respiren siempre por la nariz. A pesar de ser más efectivas, en un estudio clásico de Clairbone et al37 algunos pacientes rechazaron su uso argumentando una pérdida de comodidad respecto a las cánulas convencionales (molestias en la nariz y las orejas, por ser más pesadas y gruesas), así como por ser un método menos estético. Los estudios de Arlati et al36, Soffer et al38 o Collard et al39 ya demostraron la eficacia de las cánulas reservorio para ahorrar oxígeno, manteniendo una adecuada saturación. Sin embargo, a pesar de ser un método bastante similar al convencional y, por lo tanto, sin grandes complicaciones para los pacientes, su uso está poco introducido entre los pacientes de nuestro medio.
Fig. 1. Cánulas reservorio: Oxymizer (izda.) y Oxymizer Pendant (dcha.).
Sistemas a demanda
Los sistemas a demanda se desarrollaron a principios de los años ochenta. Quizá sea el sistema de conservación de oxígeno más extendido. Al igual que las cánulas reservorio, los sistemas a demanda se diseñaron con la intención de mejorar la eficacia de las cánulas nasales convencionales racionando el oxígeno durante las diversas fases del ciclo respiratorio. El flujo de oxígeno se controla mediante una válvula que se activa (y permite el paso a su través) cuando detecta la presión negativa que se genera durante la inspiración (fig. 2). Así se administra oxígeno sólo durante esta fase del ciclo respiratorio, suprimiendo el oxígeno desperdiciado durante la espiración. Además, con la intención de reducir el oxígeno acumulado en el espacio muerto y favorecer el intercambio gaseoso (al igual que ocurre con las cánulas reservorio), se perfeccionaron los sistemas mediante 2 tipos de estrategias: una que sólo proporciona un bolo de oxígeno predeterminado al inicio de la inspiración aumentando en volumen según una gradación numérica, y otra que utiliza también el bolo (de menor cuantía), seguido de un flujo continuo el resto de la inspiración, generalmente de menor cuantía que los empleados en los sistemas convencionales (y que también aumentan en volumen según una gradación numérica). Esto significa, en contra de lo que muchos médicos han considerado siempre, que con estos sistemas no se administra un flujo continuo, como hacen los sistemas convencionales, sino un volumen de oxígeno equivalente (estimado) al que participa en el intercambio gaseoso a dicho flujo. Gracias a esto, los sistemas a demanda consiguen ahorrar oxígeno manteniendo unos valores de saturación adecuados.
Fig. 2. Sistemas a demanda: válvula integrada en una bombona de oxígeno líquido (izda.) y válvula independiente (dcha.).
Su principal indicación es en pacientes que usan fuentes portátiles para la oxigenoterapia. Sus grandes ventajas son que estéticamente no presenta problemas y que hoy día se dispone de modelos de botellas de oxígeno líquido que incorporan este sistema (fig. 2), lo que permite reducir su tamaño y peso sin variar la autonomía, con el consiguiente beneficio que eso supone para el paciente. Su principal inconveniente reside en que no son válidos si el paciente precisa un elevado flujo de oxígeno para corregir la hipoxemia. La sensibilidad de la válvula, la frecuencia respiratoria y la respiración bucal son 3 factores que también pueden aumentar la ineficacia del sistema. Diversos estudios han puesto de manifiesto que estos sistemas son eficaces tanto en reposo como durante el ejercicio o el sueño40-45. Asimismo, Cuvelier et al46 demostraron que durante el sueño, en pacientes con EPOC moderada-grave, no había diferencias significativas en los parámetros ventilatorios ni neurofisiológicos cuando se administraba oxígeno con el sistema a demanda respecto a los sistemas convencionales. Los sistemas a demanda son eficaces, cómodos y fáciles de manejar; por lo tanto, resultan idóneos para los pacientes que reciben oxígeno en deambulación.
Prescripción de los sistemas de ahorro
La prescripción de un sistema de ahorro implica el reajuste de todos los parámetros establecidos. Dado que la prueba de 6 min de marcha se ha establecido como el mejor reflejo de la desaturación al esfuerzo47, debería realizarse con el nuevo sistema de administración para ajustar los valores en deambulación. Asimismo, cuando los utilicemos para la oxigenoterapia crónica domiciliaria (ya sea con oxígeno líquido o para optimizar una fuente fija), debemos obtener los parámetros adecuados durante el día y la noche para corregir la desaturación.
Los sistemas a demanda presentan la singularidad de que, al ser de diferentes empresas proveedoras, no utilizan volúmenes de oxígeno similares. Johann et al48 demostraron que la presión arterial de oxígeno alcanzada por 3 modelos diferentes variaba de manera significativa. Este hecho se confirma en un estudio reciente publicado por Bliss et al49, quienes compararon los diversos modelos a demanda existentes en el mercado utilizando un modelo artificial que simulaba el aparato respiratorio. Los autores comprobaron que el oxígeno administrado variaba según los diferentes modelos, demostrando que no hay equivalencia entre ellos. Por lo tanto, cuando se cambia de sistema y de modelo es necesario adecuar el sistema a cada paciente, reajustando todos los parámetros de oxigenación tanto en reposo como en actividad o durante el sueño.
Una realidad olvidada
Los sistemas de ahorro de oxígeno constituyen una alternativa eficaz para la administración de oxígeno frente a los sistemas convencionales, principalmente en pacientes con movilidad conservada, dado que aumentan la autonomía de las fuentes portátiles. La otra indicación principal es la optimización de la oxigenoterapia en la hipoxemia refractaria. Debido a sus diferentes características, cada sistema presenta ventajas e inconvenientes, que se deben valorar antes de elegir el más adecuado. Para su correcta prescripción se debe ajustar el flujo de oxígeno tanto en reposo como durante el ejercicio o el sueño mediante las pruebas pertinentes.
Sin embargo, la prescripción de los sistemas de ahorro es un hecho poco usual en nuestro país. Las causas de este "olvido" son varias y complejas, algunas culturales y otras de carácter práctico. En nuestro medio habitual todos los pacientes en general, y aquéllos con enfermedades respiratorias en particular, tienen una escasa movilidad. Con gran dificultad salen de su domicilio, y es excepcional ver a pacientes con enfermedades respiratorias crónicas que realicen normalmente sus actividades diarias con oxigenoterapia de deambulación50. No es ésta la situación que se da en otros países. En EE.UU. los enfermos y discapacitados, por ejemplo, disponen de carritos con suplemento de oxígeno en los grandes supermercados, tienen un mayor grado de actividad pública, salen solos de su domicilio, viajan, etc. En nuestra realidad, actividades como desplazarse en avión presentan serias dificultades para los pacientes con oxigenoterapia51. El paciente con una enfermedad respiratoria crónica, en nuestro medio, tiene, pues, una franca tendencia a la inmovilidad y como consecuencia, los dispositivos que facilitan el manejo del oxígeno ambulatoriono son tan demandados. Del mismo modo, también influye el hecho de que al principio estos sistemas de ahorro de oxígeno se percibiesen como ineficaces y complicados, lo que configuró la sensación general de inutilidad. Otro aspecto influyente es el económico. Las fuentes fijas, especialmente el concentrador, resultan más atractivas para los proveedores, dado que requieren menos apoyo asistencial; y para los sistemas sanitarios, por ser más económicas. Sin embargo, la realidad es que los sistemas de ahorro reducen los costes de las fuentes portátiles (oxígeno líquido, principalmente) y puesto que su uso repercute significativamente en la calidad de vida de determinados pacientes, su comercialización debería ser obligatoria en cada uno de los sistemas sanitarios de nuestro país.
Se trata, pues, de una realidad olvidada. Por un lado, tenemos a nuestra disposición una serie de equipos, más o menos fáciles de utilizar, que, aunque requieren un cierto aprendizaje, redundarían en una mejor calidad de vida del paciente y, además, en un ahorro económico nada despreciable. Por el contrario, los motivos expuestos de tendencia al sedentarismo de nuestra cultura y el poco esfuerzo de divulgación. El resultado: su uso es prácticamente inexistente. Hará falta un gran esfuerzo de educación, tanto de los propios médicos como de los pacientes, así como de las compañías suministradoras y de la Administración sanitaria, para modificar estas pautas de conducta. En nuestra opinión, este esfuerzo debería realizarse. Y lo más pronto posible.
Correspondencia:
Dr. D. Castillo.
Departamento de Neumología. Hospital de la Santa Creu i Sant Pau.
Sant Antoni M.a Claret, 167. 08025 Barcelona. España.
Correo electrónico: dcastillo@santpau.es
Recibido: 11-4-2006; aceptado para su publicación: 16-5-2006.