Introducción
El desarrollo de modelos animales que pueden reproducir una enfermedad, bien sea parcialmente o en su totalidad, ha sido siempre una herramienta de trabajo imprescindible para profundizar en el conocimiento de los diferentes aspectos de ésta. Más aún, cuando se trata de reproducir enfermedades que se desarrollan en un período muy prolongado. En estos casos, el modelo cobra mayor interés por la potencialidad que ofrece, al favorecer disponibilidad y accesibilidad a los mecanismos que puedan participar en su desarrollo.
La enfermedad pulmonar obstructiva crónica (EPOC) se caracteriza por la presencia de una obstrucción crónica y poco reversible del flujo aéreo, asociada a una reacción inflamatoria anómala, principalmente frente al humo del tabaco1, que cursa con disnea, tos, expectoración y aparición de exacerbaciones. Tiene una evolución progresiva y presenta la peculiaridad de que sólo una pequeña parte de la población de fumadores llega a desarrollar la enfermedad, aproximadamente entre el 15 y el 20%2, lo que indica que pueden haber factores genéticos participantes en la susceptibilidad individual de riesgo. Entendido como tal, no existe hasta la fecha ningún modelo de esta enfermedad que permita reproducir fielmente los aspectos que la definen. No se ha identificado un modelo que se acompañe de un descenso progresivo del valor del volumen espiratorio forzado en el primer segundo (FEV1), que se presente con tos y disnea, y que se acompañe de exacerbaciones. Por ello, los esfuerzos se han encaminado a abordar algunas de las características de esta enfermedad, en unas ocasiones para estudiar aspectos patogénicos, en otras para aspectos morfometricofuncionales y, en otras, para aspectos terapéuticos. Todos ellos son importantes y han servido para comprender mejor esta enfermedad, pero ninguno ha podido reproducirla; por ello, suele cambiarse el nombre del modelo, y en vez de EPOC se habla de modelos de enfisema, en un intento de justificarlo, sobre la base de los hallazgos anatomopatológicos y ante la dificultad de reproducir los datos clínicos de la enfermedad.
Los diferentes mecanismos de abordaje existentes pueden clasificarse sobre la base del fin perseguido; en este sentido, existen modelos que podrían denominarse morfométricos, que tratan como objetivo final únicamente reproducir una anatomía patológica de enfisema, independientemente del método empleado. Suelen ser modelos de inducción rápida, producidos generalmente mediante la administración de proteasas, aisladas o en combinación con otros agentes tóxicos. Reproducen una macroscopia de enfisema, con predominios de uno u otro tipo, que puede servir de aplicación para estudiar la sensibilidad de pruebas diagnósticas, como las de imagen o determinadas pruebas funcionales acordes con el hallazgo morfométrico encontrado. Con diferente objetivo se plantean los modelos que podrían denominarse patogénicos, que tratan de explicar alguna de las vías patogénicas implicadas en el desarrollo de la enfermedad y que generalmente se basan en la exposición aguda o crónica al humo del tabaco. Sin embargo, hasta la fecha no se ha conseguido desarrollar verdaderos modelos de EPOC que incluyan características evolutivas y que permitan predecir o ayuden a estudiar el curso de esta enfermedad.
Modelo de EPOC por exposición a humo de tabaco
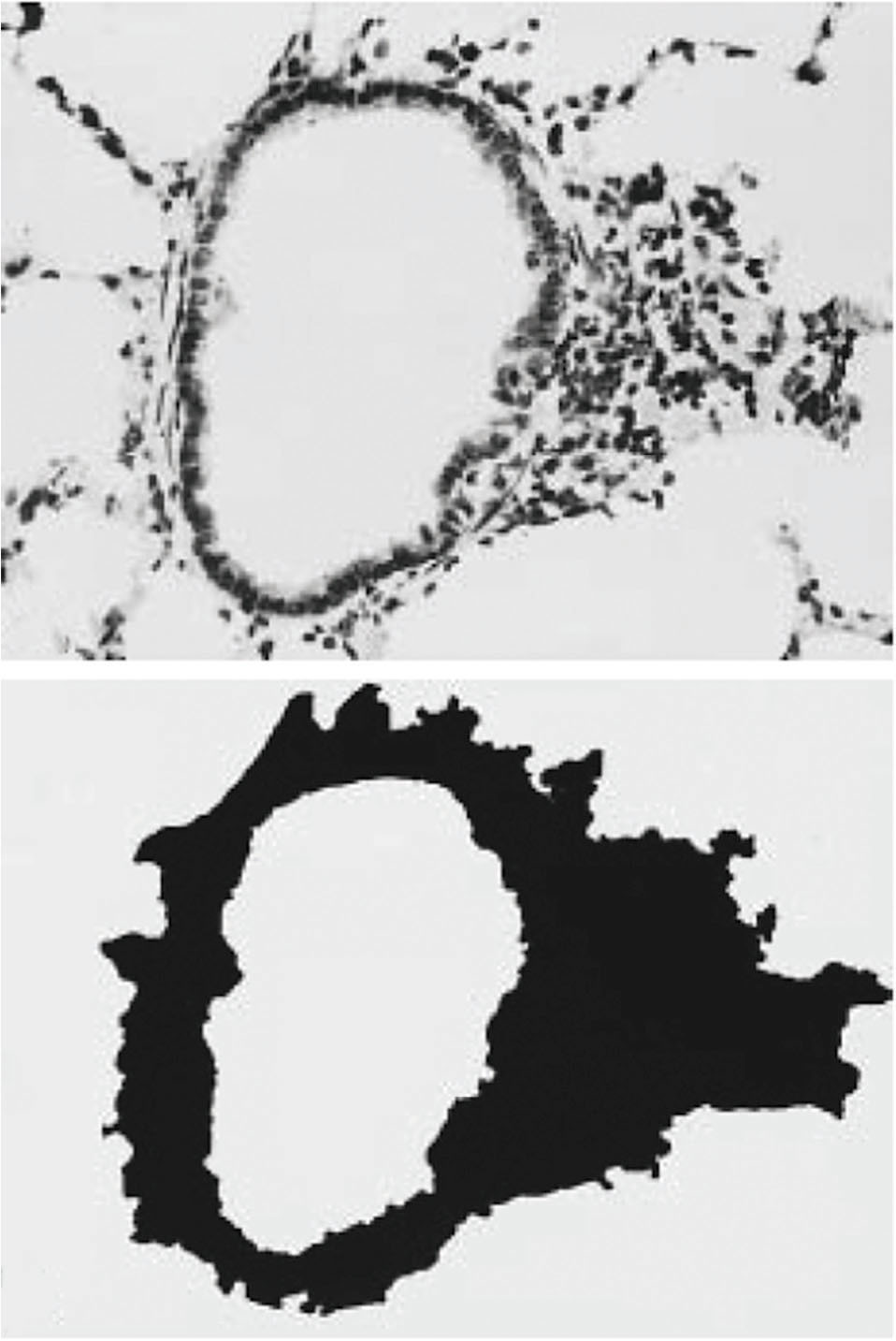
El modelo de EPOC producido mediante exposición a humo de tabaco se ha intentado aplicar a numerosas especies animales, como perros, cobayas, conejos, ratas y ratones. De ellas, los cobayas y los ratones se han mostrado las especies más susceptibles para desarrollar enfisema pulmonar tras exposiciones prolongadas3,4, aunque los ratones muestran una gran variabilidad en la susceptibilidad, que depende de la cepa, de modo que pueden encontrarse desde cepas muy resistentes a cepas muy susceptibles4. En cambio, las ratas son especialmente resistentes a desarrollar enfisema, incluso tras períodos prolongados de exposiciones. No obstante, esta especie animal puede llegar a presentar alteraciones morfométricas en la vía aérea periférica, con infiltrado inflamatorio y con un agrandamiento significativo del grosor de la pared de estas vías aéreas, en concordancia con una alteración en los parámetros funcionales específicos de la periferia pulmonar, como el nitrograma, sin otra alteración funcional ni evidencia morfométrica de enfisema5 (fig. 1).
Fig. 1. Imagen de un bronquio de rata tras ser expuesta a humo de tabaco durante 10 semanas. El análisis morfométrico del grosor de la pared permite cuantificar un incremento de la misma, comparado con el grupo control (imagen 3100)
Los primeros modelos de enfisema inducidos por exposición a humo de tabaco se describieron en los cobayas, especie que desarrolló un incremento estable del tamaño de los espacios aéreos distales, correspondientes a enfisema, analizado mediante los correspondientes análisis morfométricos3. Posteriormente, este animal se ha seguido utilizando como modelo de EPOC para describir algunos aspectos patogénicos de la enfermedad, como la presencia de infiltrado inflamatorio de neutrófilos, linfocitos y macrófagos6 o la presencia de alteraciones sistémicas en el músculo esquelético7. Más recientemente, se ha mostrado que el perfil de respuesta inflamatoria y de liberación de mediadores en cobayas expuestos crónicamente a humo de tabaco reproduce el perfil descrito en los pacientes con EPOC8.
Con todo, los animales más utilizados en los modelos de EPOC han sido los ratones, por la elevada susceptibilidad que tienen de desarrollar esta enfermedad algunas de las cepas existentes en esta especie animal9. Los datos encontrados en los modelos de EPOC inducidos en diferentes cepas de ratones por exposición a humo de tabaco y la amplia posibilidad de disponer de variantes genéticas han mostrado la potencialidad de esta especie. La EPOC es una enfermedad heterogénea con variabilidad de fenotipos morfológicos y fisiológicos; por ello, la caracterización fenotípica del modelo de EPOC, con definición del grado de obstrucción, de distensibilidad, de tipo morfológico de enfisema y de respuesta inflamatoria, deben estar presentes en el modelo. En este sentido, se ha podido diferenciar entre cepas resistentes, como la NZWLac/J, cepas moderadamente susceptibles, como las de C57BL6/J, A/J y SJ/L, y cepas muy susceptibles, como la AKR/J, que además de desarrollar mayor grado de enfisema, puede reproducir el patrón de infiltración de células inflamatorias presente en los pacientes con EPOC y acompañarse de un comportamiento funcional con incremento de la distensibilidad, acorde con la presencia de enfisema4. La aplicación del modelo de exposición a humo de tabaco sobre los ratones y la disponibilidad actual existente para obtener múltiples variantes genéticas de cepas con ausencia de la expresión de algunos componentes, como factores, citocinas o receptores, ha facilitado el análisis de muchos de estos mediadores en lo que respecta a su posible participación durante la patogenia de la enfermedad. El perfil general de respuesta de los ratones a la exposición crónica al humo del tabaco ha sido bien definida10.
En ausencia de expresión del receptor CCR6, la capacidad de desarrollar enfisema en respuesta al humo del tabaco quedaba muy limitada por un menor desarrollo de la respuesta inflamatoria y de la presencia de proteasas, hecho que permitía concluir que la interacción del receptor CCR6 con su ligando participa en la patogenia de la EPOC11. Esta misma técnica se ha utilizado para estudiar la participación de los receptores toll-like en los modelos de exposición aguda y crónica al humo del tabaco, donde se demostraba su importancia en el desarrollo de la respuesta inflamatoria, pero no tanto en la del desarrollo del enfisema12. La participación del factor de necrosis tumoral a (TNF-α) en la patogenia de la EPOC también ha podido definirse, al menos parcialmente. En ausencia del receptor del TNF-α, los ratones no desarrollan infiltrado inflamatorio tras una exposición aguda al humo del tabaco, pero tras una exposición crónica la respuesta cambia, la inhibición ya no es completa y parte de la respuesta sigue estando presente, aunque se reduce muy significativamente el desarrollo de enfisema y la expresión de las proteasas de matriz (MMP)13. En esta misma línea, pero inhibiendo por separado los receptores R1 y R2 del TNF-α pudo comprobarse que ambos receptores participan en el desarrollo de la EPOC, pero que el R2 tiene mayor participación en el desarrollo de los efectos sistémicos encontrados en el modelo14.
La técnica del estudio de los perfiles de expresión génica mediante microarrays en animales que son genéticamente uniformes15, como sucede con las diferentes cepas de ratones, abre una nueva posibilidad de estudio en los modelos de EPOC que permitirá describir los diferentes perfiles y susceptibilidades a la exposición al humo de tabaco. Utilizando esta técnica, se ha encontrado la existencia de una sobreexpresión de MMP12, una metaloproteasa de matriz, implicada en la degradación de tejido conectivo tras exponer la cepa AKR/J a humo de tabaco junto a LPS16.
Los modelos de EPOC inducidos por exposición a humo de tabaco llegan a reproducir muchas de las características de la EPOC en humanos, con una morfometría y una inflamación crónica similares, que están siendo útiles para estudiar algunos aspectos celulares y moleculares presentes en el desarrollo de la enfermedad. Los modelos de exposición a humo de tabaco en ratones también han mostrado el desarrollo de estrés oxidativo en el pulmón y en otros órganos, como el corazón y el hígado17.
Modelos de EPOC por inhalación de gases irritantes:
Lejos de las posibilidades que ofrece la exposición crónica al humo del tabaco, existen otros productos que, administrados por inhalación, pueden reproducir la enfermedad. Gases irritantes, como el dióxido de azufre (SO2) o de nitrógeno (NO2), pueden reproducir algunas de las características de la EPOC de manera aislada. La exposición crónica de ratas a SO2 es capaz de producir un infiltrado inflamatorio polimorfonuclear y mononuclear en las vías aéreas, hipersecreción mucosa e hiperreactividad bronquial18. Sin embargo, el cuadro histopatológico que desarrolla es una destrucción intensa, más similar a la de un enfisema terminal que a una verdadera EPOC19. El NO2 es otro gas irritante que puede reproducir algunas de las lesiones de la EPOC en exposiciones crónicas de baja intensidad, ya que su elevada toxicidad produce daño pulmonar agudo grave en exposiciones intensas20. Al igual que sucede con la exposición al humo de tabaco, el desarrollo de modelos de EPOC con NO2 sigue también un comportamiento de susceptibilidad genética, con una mayor expresividad de la enfermedad en la cepa de ratones C57BL/621.
Modelos de EPOC por administración de proteasas
Desde los experimentos iniciales de Gross et al22, que demostraron la producción de enfisema mediante la instilación intratraqueal en ratas de la proteasa vegetal Papaína, los investigadores han instilado diversas enzimas elastolíticas, incluyendo elastasa pancreática, elastasa neutrofílica y proteinasa 3, que han dado lugar a un agrandamiento de los espacios aéreos por proteólisis, que seguida de reparación ineficaz reproduce un enfisema de tipo panacinar, muy parecido al que presentan los pacientes con déficit de alfa-1 antitripsina23,24. Este tipo de enfisema va acompañado, además, de metaplasia de las células secretoras, de anormalidades de la función pulmonar y de hipoxemia e hipertrofia ventricular derecha, todas ellas características de la EPOC. Estos modelos pueden determinar si una determinada proteasa tiene la capacidad de causar enfisema, pero no pueden identificar qué proteasas están implicadas en la patogenia del enfisema producido por el consumo de cigarrillos, ni tampoco pueden ser usados para descifrar los episodios que ocurren antes de la liberación de estas proteasas. No obstante, el modelo de la elastasa sigue usándose por su simplicidad y porque es muy útil para el estudio de los mecanismos que tienen lugar después, fundamentalmente los mecanismos de reparación tisular, para la aplicación de diferentes métodos diagnósticos, el análisis de las correlaciones morfometricofuncionales y el desarrollo de diferentes ensayos terapéuticos.
Modelos de EPOC por administración de agentes profibróticos
El cloruro de cadmio (CdCl2), constituyente del humo de los cigarrillos, da lugar en un principio a fibrosis intersticial peribronquiolar, que secundariamente origina un agrandamiento de los espacios aéreos distales, que se asemejan al enfisema de tipo centroacinar25. Este agente también puede administrarse junto con el agente latírico β-aminopropionitrilo (BAPN), que actúa inhibiendo la maduración de las fibras de colágeno y elastina, limita la reparación que sigue al daño pulmonar y provoca un mayor aumento de los cambios que se producen en este tipo de enfisema centroacinar24,26,27.
Otros contaminantes
El polvo del carbón y del silicio también pueden dar lugar al desarrollo de enfisema de tipo focal, con un aumento de roturas del tejido conectivo y a un aumento también de células polimorfonucleares (PMN) y macrófagos28.
Modelos de EPOC por administración de toxinas bacterianas
La administración repetida de endotoxinas bacterianas, como lipopolisacáridos (LPS) por vía endotraqueal, provoca enfisema mediante el reclutamiento de neutrófilos y la activación de macrófagos29. Se trata de un modelo inflamatorio que actúa a través de los mediadores que liberan los neutrófilos y macrófagos que reclutan. La administración intratraqueal de lipopolisacáridos bacterianos (LPS) produce una respuesta inflamatoria que también se acompaña de fiebre, hipersecreción mucosa y broncoconstricción30. Se sabe, además, que la administración de LPS puede producir activación de mediadores, como TNF-α, intereucina (IL) 1, interferón (IFN) Υ, MCP1 e IL-8, y potenciar la lesión tóxica del oxígeno en pulmones de la rata31. Recientemente, se ha descrito que los receptores de inmunidad innata toll-like de los linfocitos (TLR) podrían actuar como señalizadores de la activación de los LPS32. La administración crónica en hámsteres ha permitido producir enfisema a través de la infiltración de polimorfonucleares, que podía inhibirse administrando un inhibidor de la elastasa neutrofílica o anti-TNF-α, que podía reducir la presencia de estas células33. Si los lipopolisacáridos se administran de manera crónica junto al humo del tabaco se llega a potenciar la respuesta inflamatoria presente en el modelo, por lo que esta asociación se ha sugerido como posibilidad de reproducir modelos de EPOC con exacerbación34.
Otro modelo de interés reciente ha sido el desarrollado mediante la administración intravascular de un inhibidor del receptor 2 del factor de crecimiento endotelial, que genera enfisema de tipo no inflamatorio, mediado por un proceso apoptótico que se acompaña de pérdida del lecho capilar pulmonar35.
Modelos transgénicos de EPOC
El ratón es un animal que puede desarrollar mutaciones espontáneas secundarias a anomalías genéticas que provocan el desarrollo de enfisema espontáneo. Algunas de estas mutaciones constituyen las líneas de ratones conocidas, entre otros, con los nombres de tight skin, que afecta al ensamblamiento de la fibras elásticas y desarrolla agrandamientos en los espacios aéreos de una manera progresiva con la edad; beige, que ofrece unos resultados controvertidos acerca de si produce valores normales de proteasas séricas y de si tiene la capacidad de desarrollar enfisema; blotchy, que se acompaña de un proceso anormal del ARN del gen Menke del cromosoma X y causa enfisema por vías desconocidas, o pallid, que desarrolla enfisema leve y muy tardío, pero que se utiliza porque responde intensamente a la exposición al tabaco36. En estos casos, las anomalías genéticas se han determinado claramente; en cambio, no se conocen los mecanismos fisiopatológicos, por los que se desarrolla enfisema, aunque en el caso del ratón pallid se sabe que se debe al déficit de la enzima alfa-1 antitripsina.
Gracias a las posibilidades que ofrecen los ratones para la manipulación genética, se han podido desarrollar múltiples modelos, con deficiencias proteínicas concretas que han permitido conocer las funciones concretas de una determinada proteína en el desarrollo de una enfermedad. Existen numerosas variantes de déficit enzimáticos, algunas ya descritas previamente en los modelos de exposición crónica al humo del tabaco, y otras muchas, entre las que cabe destacar las de deficiencias en colagenasa, IL-11, PDGF-B, Klotho, PDGF-A, o FGFR-3 -/- XFGFR-4 -/-, entre otras36.
Modelos de EPOC como herramienta para estudios fisiológicos y de diagnóstico
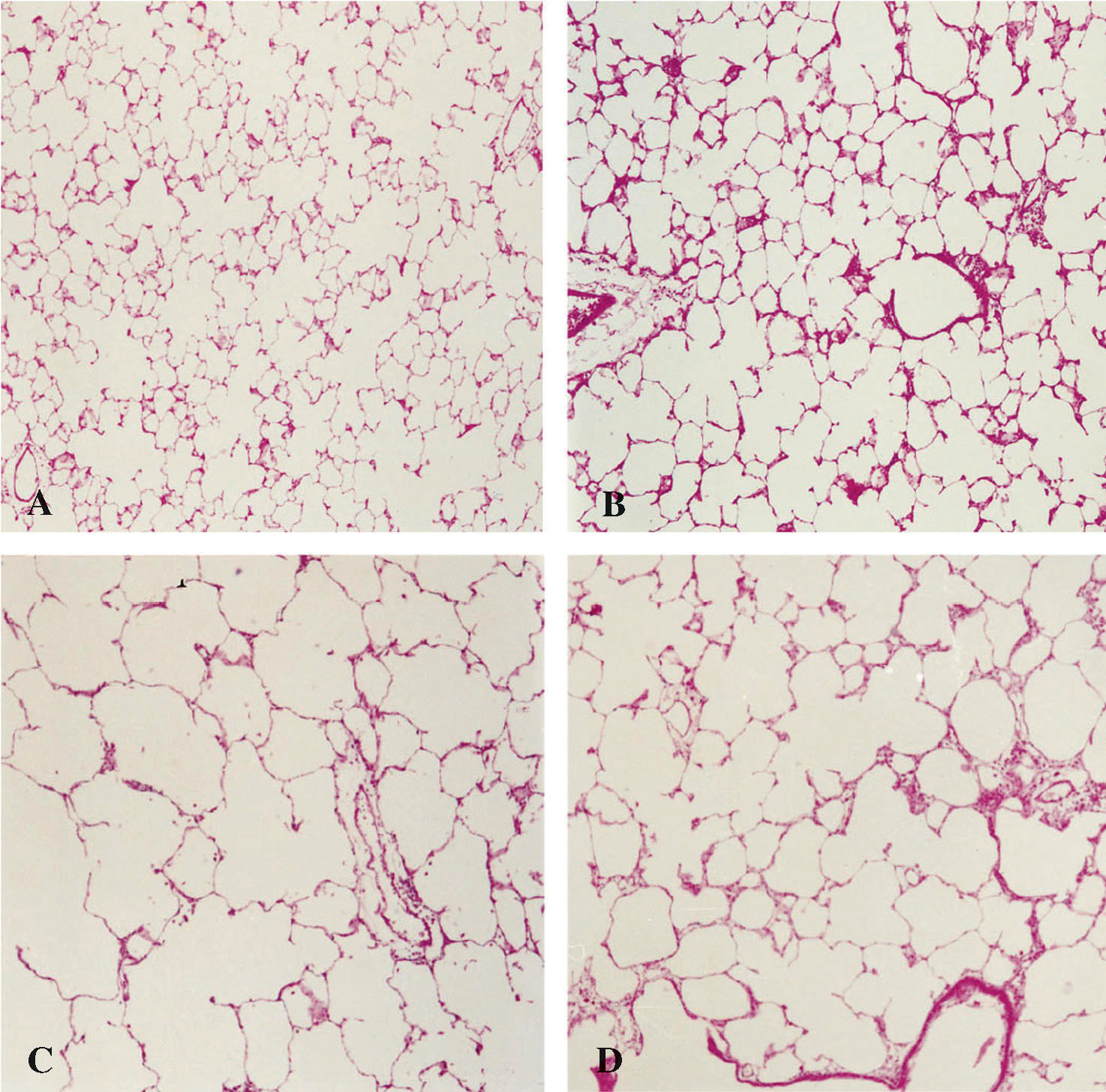
Los modelos animales de enfisema tienen como ventaja que permiten obtener enfisema de tipo panacinar o centroacinar puro (fig. 2). Se ha visto que el enfisema panacinar inducido con elastasa y el centroacinar inducido con cloruro de cadmio y un inhibidor de la maduración del tejido conectivo presentan patrones de alteraciones funcionales distintos y característicos de estas 2 variantes de enfisema24, similares a los descritos para humanos37.
Fig. 2. Cortes histológicos con tinción de hematoxilina-eosina (x40) de pulmones de rata control (A); modelo de efisema centrolobulillar mediante administración de Cloruro de Cadmio (B); modelo de efisema panacinar mediante instilación elastasa (C); y centrolobulillar intenso mediante la combinación de Cloruro de Cadmio y beta-amino-propionitrilo (D). (Tomado de Rubio et al24.)
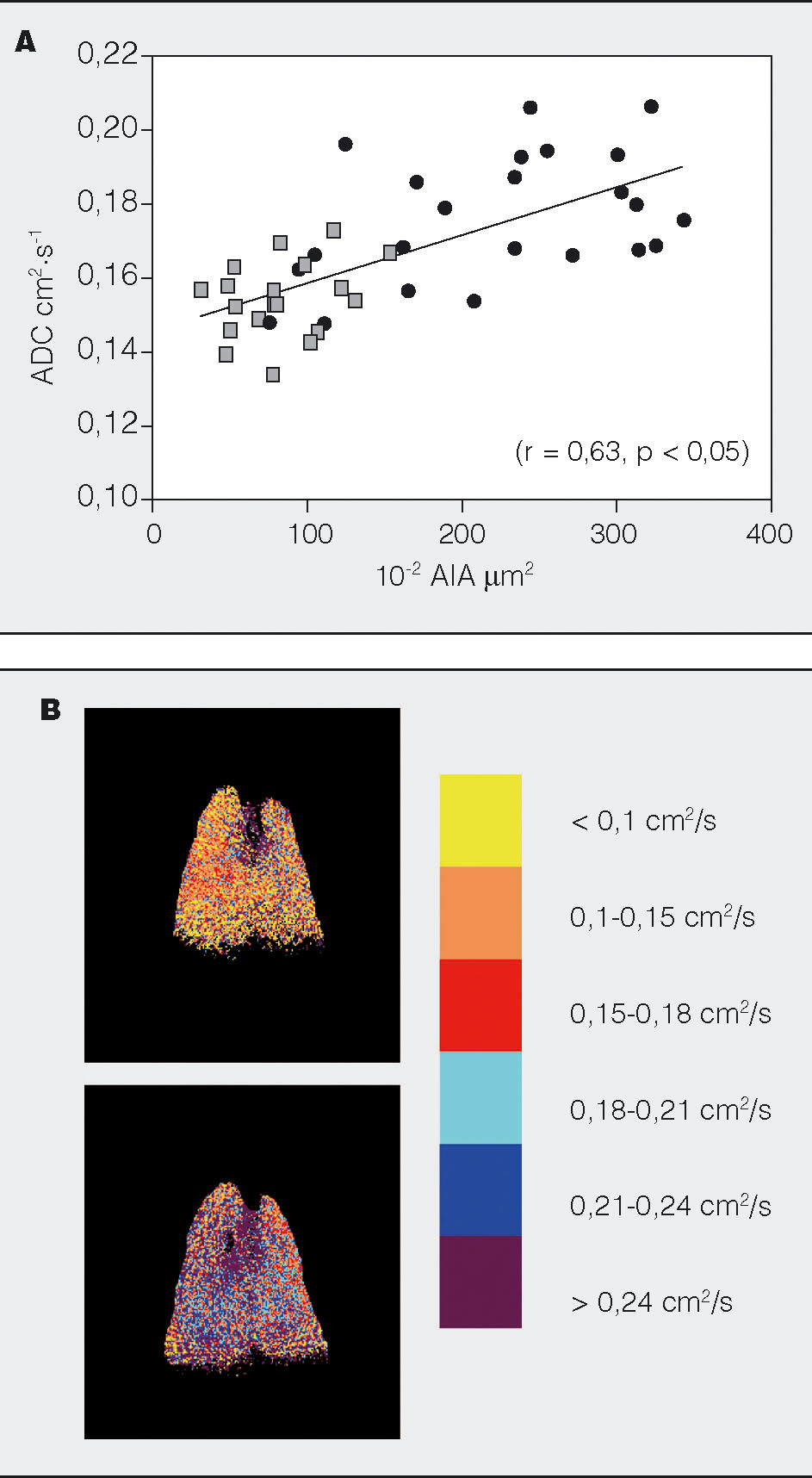
Las técnicas de imagen también han aprovechado las ventajas ofrecidas por los modelos de EPOC para evaluar la resolución en la capacidad de identificar lesiones. La resonancia magnética con 3He hiperpolarizado permite estimar las medidas de los espacios aéreos distales, mediante el análisis de los coeficientes aparentes de difusión (ADC), una medida que depende del tamaño del espacio aéreo donde el gas se está difundiendo38. Aplicándolo a un modelo de enfisema leve inducido por elastasa en ratas, el mapa de valores de ADC mostró una resolución muy elevada, con una excelente correlación con los datos morfométricos medidos por microscopía óptica (fig. 3). Las técnicas de función pulmonar no han llegado, por ahora, a detectar el enfisema incipiente y la tomografía computarizada (TC), aunque proporciona excelentes imágenes, tiene por ahora una capacidad de resolución espacial limitada para la definición de los espacios aéreos más distales39,40 y pierde sensibilidad en la detección del enfisema leve41. Sin embargo, se han publicado algunos datos experimentales realizados con micro-TC que ofrecen una calidad de imagen y una resolución excelente, aunque con sistemas no aplicables por ahora en la clínica42.
Fig. 3. A) Correlación entre el área alveolar (A/A) medido por morfometría y los valores de ADC, calculados por resonancia magnética de helio-3 en un modelo de enfisema panacinar leve, inducido con bajas dosis de elastasa. B) Representación del mapa de valores de ADC, determinados píxel a píxel en un caso de pulmón normal (arriba), y de pulmón con enfisema inducido con elastasa. Puede apreciarse la predominancia de píxeles de mayor tamaño en el modelo de enfisema.
Modelos de EPOC como desarrollo de ensayos terapéuticos
Las características propias de la EPOC, como enfermedad de desarrollo muy lento producida por una respuesta inflamatoria anómala y continuada frente al humo del tabaco1, dificulta el estudio de ensayos terapéuticos que, de plantearse, debe hacerse bajo el concepto de un seguimiento muy prolongado. Ello ha favorecido que los modelos de EPOC también se hayan desarrollado para la aplicación de diferentes pruebas terapéuticas.
El tratamiento de la EPOC debe plantearse como un fenómeno que debe ir más allá del mero efecto antiinflamatorio y debe plantearse también para contrarrestar las consecuencias de esta inflamación continuada, como los fenómenos de remodelado y de destrucción asociados. El desarrollo de antagonistas de la respuesta inflamatoria tiene por tanto elevado interés y, por ahora, sólo son aplicables en estos modelos. Los inhibidores de las proteasas y los activadores de las antiproteasas serían potencialmente útiles en restaurar el equilibrio proteasa-antiproteasa y, por tanto, útiles en el tratamiento de la EPOC, aunque conservando similares limitaciones a las de los antiinflamatorios en cuanto a que estarían potencialmente actuando sobre el desarrollo de la enfermedad, no sobre su regeneración. La enzima alfa-1 antitripsina tiene un efecto sólo parcial en pacientes con déficit congénito de esta enzima43 y no hay evidencia de eficacia en pacientes con concentraciones normales de ésta. Existen, sin embargo, algunos datos experimentales que aplicados sobre modelos de EPOC podrían estar apuntando hacia una posible restitución del parénquima pulmonar como el ácido retinoico, los antioxidantes y algunos factores de crecimiento, entre otros.
Ácido retinoico
Tras las primeras evidencias de que el ácido retinoico era capaz de prevenir la reducción del número de alvéolos en ratas recién nacidas tratadas con dexametasona, que actuaba como inhibidor de la formación de alvéolos44, este producto se utilizó como prueba terapéutica en el modelo de enfisema panacinar inducido en ratas con elastasa45. En este primer estudio, se demostró que la administración de ácido retinoico restituía las anomalías anatómicas del enfisema reduciendo el tamaño de los espacios aéreos distales e incrementando el número de alvéolos de tamaño normal. Estos cambios indujeron a la interpretación por parte de los autores de la existencia de una regeneración del pulmón enfisematoso. Estudios posteriores no han demostrado la misma eficacia y, en cambio, evidencian una completa ausencia de mejoría funcional en los flujos, distensibilidad o capacidad de difusión, esperables si realmente hubiera regeneración alveolar46. Incluso estudios experimentales posteriores, aplicados sobre modelos murinos de enfisema inducido con elastasa, llegaron a encontrar un empeoramiento provocado por el tratamiento con ácido retinoico47.
Antioxidantes
La N-acetilcisteína es un precursor del glutatión y tiene propiedades antioxidantes y antiinflamatorias. Se ha probado como agente terapéutico en pacientes con fibrosis pulmonar48 y en modelos animales de fibrosis pulmonar. También ha sido demostrada su capacidad de atenuar la infiltración celular y la deposición de colágeno en el modelo de fibrosis inducida por bleomicina49. En el modelo de enfisema pulmonar inducido con elastasa, este antioxidante produjo una mejoría que pudo cuantificarse en términos morfométricos de medida de los espacios aéreos distales y en términos funcionales, con mejoría de los flujos espiratorios forzados50.
También se han probado otros antioxidantes, como la superóxido dismutasa humana, cuya sobreexpresión inducida genéticamente en ratones previene la respuesta inflamatoria y el desarrollo de enfisema en el modelo de exposición crónica a humo de tabaco51.
Factores de crecimiento
Tras una neumonectomía se desarrolla un fenómeno de crecimiento en el pulmón contralateral, que se acompaña de incremento de masa, de volumen y de área de intercambio52. El factor de crecimiento del hepatocito (HGF) se ha implicado como uno de los principales causantes de esta respuesta, porque se acompaña de un incremento temporal de su expresión en el pulmón, el incremento de sus valores en suero, la inhibición del crecimiento por anticuerpos anti-HGF y la aceleración de la respuesta con su administración exógena53. El factor de crecimiento de transformación b (TGF-β) es, en cambio, un inhibidor de su expresión. El TGF-β es un potente factor fibrogénico, también presente en el enfisema y posiblemente causante del componente fibrótico que acompaña a esta enfermedad. Existen también otros factores de crecimiento, como el factor de crecimiento epidérmico y el factor de crecimiento similar a la insulina, que también se han implicado en otros estudios en el crecimiento compensatorio posneumonectomía54. El factor de crecimiento de hígado (LGF), distinto del HGF, compuesto por un complejo albúmina-bilirrubina55 tiene gran capacidad antifibrótica y regenerativa. Su actividad como LGF ha sido bien corroborada, y sus receptores se han encontrado, además de en el hígado, en otros órganos, incluido el pulmón56. El efecto del LGF se ha estudiado en el modelo de cloruro de cadmio, administrando el tratamiento una vez que la lesión se hubo establecido. De esta manera, pudo encontrarse una mejoría que se hizo manifiesta en los parámetros de función pulmonar, de morfometría y en la reducción de la presencia de fibrosis57.
Otros factores de crecimiento, como el factor de crecimiento del queratocito y los factores de crecimiento del fibroblasto (FGF-7 y 10) también pueden estimular la proliferación de células epiteliales alveolares y de células endoteliales, sin estimular la proliferación de fibroblastos58. La regeneración del enfisema requiere de la formación de estructuras alveolares y de la eliminación del componente de fibrosis depositado. Partiendo de acciones en otros ámbitos, estos factores plantean un hipotético efecto terapéutico regenerador del enfisema pulmonar que, por ahora, no ha podido establecerse, pero la potencialidad que ofrecen los modelos animales de EPOC puede permitir avanzar en estas aplicaciones.
Ácido hialurónico
Administrado por vía inhalada en un modelo de EPOC inducido por tabaco en ratones, el ácido hialurónico fue capaz de reducir el tamaño de los espacios aéreos y la destrucción de fibras elásticas, cuantificado por la reducción de la presencia de desmosina e isodesmosina, en el lavado broncoalveolar, lo que proporciona un potencial uso terapéutico de este fármaco en el futuro59.
Antagonistas
Administrando un antagonista específico de CXCR2 en un modelo de exposición aguda a humo de tabaco en ratas, se pudo comprobar que se reducía la respuesta inflamatoria neutrofílica60. También se ha comprobado a nivel experimental que un inhibidor de amplio espectro de las metaloproteasas de matriz pudo inhibir parcialmente las lesiones destructivas inducidas por la exposición crónica al humo del tabaco en cobayas61. El roflumilast, un inhibidor de la fosfodiesterasa 4, también ha demostrado ser eficaz en la prevención del desarrollo del enfisema inducido por exposición crónica al humo del tabaco en ratones62.
Conclusiones
En conclusión, no podemos decir que se disponga de verdaderos modelos de EPOC, porque hasta la fecha ninguno de ellos ha permitido reproducir todas las características de esta enfermedad. Sin embargo, dentro de las limitaciones existentes, los modelos descritos están ayudando a comprender la participación de algunos mediadores en la patogenia de la enfermedad, sirven para la aplicación de nuevas pruebas diagnósticas y permiten aplicar nuevos ensayos terapéuticos que serían impracticables sin la ayuda de estos modelos.
Correspondencia:
Dr. G. Peces-Barba.
Servicio de Neumología. Fundación Jiménez Díaz-CAPIO.
Avda. Reyes Católicos, 2. 28040 Madrid. España.
Correo electrónico: gpeces@fjd.es