El tabaquismo es una enfermedad crónica de carácter adictivo y recidivante. Es la primera causa evitable de muerte en el mundo. Todos los profesionales sanitarios están obligados a diagnosticar y tratar correctamente a los fumadores para ayudarles a dejar de serlo1,2. En los últimos años se ha publicado un número amplio de recomendaciones y guías sobre la intervención en fumadores dirigidas a los distintos profesionales sanitarios1-5. En España, en el año 2002 un grupo de sociedades científicas publicó el primer documento de consenso sobre el diagnóstico y tratamiento del tabaquismo6. En 2003 la Sociedad Española de Neumología y Cirugía Torácica (SEPAR) publicó una actualización de lo que hasta entonces habían sido sus recomendaciones para el tratamiento del tabaquismo7,8.
Todas estas guías coinciden en considerar que el tratamiento del tabaquismo es diferente para cada fumador y depende fundamentalmente de la motivación que éste tenga para abandonar de forma definitiva el consumo del tabaco. Así, parece claro que los fumadores que se encuentren en fase de preparación deben recibir 2 tipos de intervención: a) conductual, encaminada a combatir la dependencia psíquica que pudieran presentar, y b) farmacológica, para aliviar la dependencia física por la nicotina. Esta consideración tiene un grado de evidencia A1-8.
El tratamiento farmacológico del tabaquismo se ha desarrollado mucho en la última década. Han aparecido nuevos fármacos para ayudar a los fumadores a dejar el tabaco, se han modificado las formas de utilización y dosis de los ya existentes o incluso se han variado ligeramente las indicaciones de unos y otros. Por otro lado, la irrupción en el campo terapéutico de los tratamientos farmacológicos para dejar de fumar ha abierto un importante debate sobre la necesidad de su financiación por el sistema sanitario público9,10.
Los objetivos principales de estas nuevas recomendaciones sobre el tratamiento farmacológico del tabaquismo son 2: por un lado, analizar los fármacos que han sido aprobados por las autoridades sanitarias españolas para su empleo como tratamientos farmacológicos del tabaquismo; por otro, realizar propuestas razonadas y basadas en la evidencia científica para la financiación pública de este tipo de tratamientos.
A lo largo del artículo se exponen las bases neurofisiológicas que explican la dependencia a la nicotina y la adicción al tabaco, y se justifica, sobre la base de la evidencia científica, la necesidad de que los fumadores que quieran hacer un serio intento de abandono del consumo de tabaco y en los que esté indicado reciban tratamiento farmacológico. Asimismo se revisan el mecanismo de acción, las dosis, indicaciones y contraindicaciones de cada uno de los fármacos disponibles en nuestro país para ayudar a los fumadores a dejar de serlo: chicles, comprimidos y parches de nicotina, bupropión y vareniclina. Igualmente se analizan los resultados y las conclusiones de un nuevo planteamiento del tratamiento del tabaquismo: la reducción progresiva del consumo del tabaco, utilizando chicles de nicotina, como paso previo a su abandono definitivo. Por último, se exponen propuestas para la financiación por parte del sistema sanitario público de los tratamientos farmacológicos para dejar de fumar.
Dependencia a la nicotina. Adicción al tabacoLa nicotina ejerce su acción sobre receptores acetilcolinérgicos situados en las membranas de neuronas del área tegmental ventral del mesencéfalo. Los receptores nicotínicos están constituidos por 5 cadenas polipeptídicas. Los más numerosos están formados por 2 cadenas α4 y 3 cadenas β211. Hoy día se sabe que la estimulación de estos receptores por parte de la nicotina conduce a un incremento de la liberación de dopamina en el núcleo accumbens. Esta respuesta es la causante de la sensación de recompensa que experimentan los fumadores cuando utilizan esta droga y explica su autoadministración11,12. Por otro lado, se ha demostrado que la autoadministración de nicotina se facilita y potencia cuando el suministro de la droga se asocia a estímulos externos11-14.
Se puede concluir que la administración de nicotina mediante el consumo del cigarrillo produce lesiones orgánicas en las neuronas del área tegmental ventral del mesencéfalo: incremento del número y de la función de los receptores nicotínicos α4 y β2. Estas lesiones convierten al fumador en dependiente de la nicotina y esta dependencia produce alteraciones físicas y psíquicas en el fumador (síndrome de abstinencia). Este síndrome conduce a la búsqueda "incontrolada e insana" de la nicotina a través del consumo continuado de cigarrillos. Por ello se debe entender que la dependencia de la nicotina conduce a la adicción a los cigarrillos o, lo que es lo mismo, a la adicción al tabaco inhalado. Sin duda la administración de nicotina mediante el consumo de cigarrillos o puros es la forma más rápida y determinante de llegar a ser dependiente de esta droga. Por el contrario, no es frecuente hacerse dependiente de la nicotina si ésta se consume de otra forma (p. ej., tratamiento sustitutivo con nicotina)11-14.
Tratamiento sustitutivo con nicotinaEl tratamiento sustitutivo con nicotina (TSN) está reconocido como farmacoterapia de primera línea y se utiliza con éxito desde hace muchos años en el tratamiento del tabaquismo. Durante los últimos años se han desarrollado nuevas aplicaciones, como el tratamiento sustitutivo a altas dosis o, más recientemente, el TSN para la reducción del consumo como paso previo al abandono completo. A continuación se comentan las preparaciones farmacéuticas de TSN que están disponibles en España.
Chicle de nicotinaEs una pieza de goma de mascar que contiene 2 o 4mg de nicotina. Mediante la masticación la nicotina se libera al interior de la cavidad bucal y es absorbida a través de la mucosa geniana, alcanza la sangre y desde allí estimula los receptores nicotínicos de las membranas de las neuronas del área tegmental ventral del mesencéfalo. Con ello evita que el fumador que está dejando de serlo presente los síntomas del síndrome de abstinencia.
En la última revisión Cochrane se muestra que la odds ratio (OR) para la abstinencia utilizando chicles de nicotina es de 1,66 (intervalo de confianza [IC] del 95%, 1,52-1,81) y se recoge con un grado de evidencia A15. Hay también pruebas suficientes para recomendar los chicles de 4mg de nicotina, frente a los de 2mg, en fumadores con alta dependencia física; la OR es en este caso de 2,20 (IC del 95%, 1,85-3,25) y el nivel de evidencia A15.
El chicle es una forma de administración de nicotina relativamente rápida. Ésta es una de sus características diferenciales. Por un lado, puede utilizarse de forma puntual con el objetivo de controlar situaciones de deseo compulsivo (craving) intenso, y por otro, puede administrarse de forma pautada para conseguir valores continuos de nicotinemia que ayudarán a aliviar los síntomas del síndrome de abstinencia que experimente el fumador.
En la tabla I se especifican la dosis, los efectos adversos y las contraindicaciones para este tipo de tratamiento1-8,15-17.
Chicle de nicotina
| Eficacia |
| Odds ratio=1,66 (intervalo de confianza del 95%, 1,52-1,81) |
| Dosis |
| Debe ajustarse al grado de dependencia física del fumador En fumadores de menos de 20 cigarrillos diarios o que encienden su primer cigarrillo trancurridos 30min después de levantarse, se recomiendan chicles de 2mg a dosis de una pieza cada 1 o 2h mientras estén despiertos |
| Los fumadores de 20 o más cigarrillos diarios, o que consumen el primer cigarrillo antes de transcurridos 30min después de levantarse, utilizarán chicles de 4mg de nicotina con similar pauta |
| Duración del tratamiento: entre 8 y 12 semanas |
| En los fumadores menos dependientes se recomienda la utilización de chicles durante 8–10 semanas |
| En los de mayor grado de dependencia es aconsejable prolongar el tratamiento hasta 3 meses, si bien es cierto que en éstos la utilización de chicles puede llegar hasta los 6–12 meses |
| La dosis se irá reduciendo progresivamente a partir de las 4–8 semanas de tratamiento |
| Efectos adversos* |
| Dolor de la articulación temporomandibular (4-12%) |
| Mal sabor de boca (2-20%) |
| Molestias orofaríngeas (1-5%) |
| Meteorismo (3-15%) |
| Náuseas (3-8%) |
| Pirosis (3-14%) |
| Hipo (2-14%) |
| Contraindicaciones |
| Absolutas |
| Infarto de miocardio de menos de 4 semanas de evolución |
| Angina inestable |
| Arritmias cardíacas graves |
| Relativas |
| Embarazo |
| Lactancia |
Se trata de unos comprimidos que contienen 1 o 2mg de nicotina. Su mecanismo de absorción y su farmacocinética son relativamente similares a los chicles de 2 o de 4mg, respectivamente. La eficacia de esta forma de TSN se ha comprobado en un estudio doble ciego y controlado con placebo. Se observó que los fumadores que utilizaron pastillas con nicotina tenían el doble de posibilidades de dejar de fumar que aquellos que utilizaron placebo18.
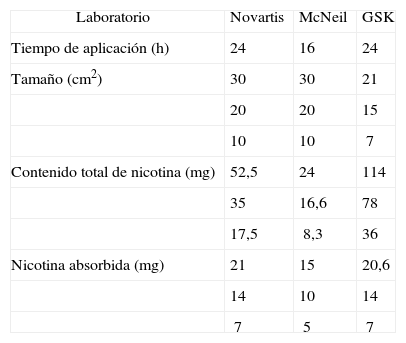
Parche de nicotinaEl parche es un dispositivo cargado de nicotina que está preparado para liberarla a través de la piel cuando se adhiere a ella. En el mercado español hay 3 tipos de parches de nicotina, que se diferencian entre sí por las concentraciones de nicotina que tienen y liberan, por su diferente tiempo de liberación y porque consiguen distintos valores de nicotinemia. En la tabla II se recogen sus características19.
El último metaanálisis demuestra que la OR para la abstinencia con parches de nicotina, en comparación con los controles, fue de 1,81 (IC del 95%, 1,63-2,02), correspondiente a un nivel de evidencia A15. Los parches de 24h son tan eficaces como los de 16h15. Un estudio reciente ha mostrado un leve incremento de la eficacia de los parches de nicotina al cabo de la primera semana de tratamiento como consecuencia de su utilización durante los 15 días previos al día de abandono del tabaco20. El parche representa una forma de administración de nicotina lenta y progresiva.
Para su correcta utilización conviene seguir las siguientes recomendaciones1-8,15-21:
- –
Deben utilizarlos fumadores con una dependencia física de la nicotina leve-moderada. En fumadores con dependencia importante (≥ 7 puntos en el test de Fagerstrom), usados por sí solos, no han demostrado incrementar el porcentaje de éxitos. Las bajas concentraciones de nicotina en sangre que se alcanzan con ellos podrían explicar este hecho. Por ello, en algunos casos es muy recomendable emplear 2 parches al mismo tiempo.
- –
Deben utilizarse durante un período no inferior a 6- 8 semanas y no superior a 12. La interrupción precoz del tratamiento con parches de nicotina, antes de las 6–8 semanas, facilita la recaída, y su prolongación más allá de 12 semanas no incrementa las posibilidades de éxito.
- –
Los parches deben emplearse a dosis altas durante las primeras 4–6 semanas. En el caso de los parches de 16h, la dosis alta recomendada es de 25mg/día; esta dosis se consigue utilizando conjuntamente un parche de 15mg y otro de 10mg. Para el parche de nicotina de 24h la dosis alta es de 21mg/día.
En la tabla III se muestran los efectos adversos y las contraindicaciones de este tratamiento1-8,15-21.
Parche de nicotina
| Eficacia |
| Odds ratio=1,81 (intervalo de confianza del 95%, 1,63-2,02) |
| Efectos adversos |
| Localesa |
| Eritema |
| Exantema |
| Prurito |
| Eccema |
| Sistémicosb |
| Cefalea |
| Insomnio. Sueños vívidos |
| Náuseas. Hipo |
| Mal sabor de boca |
| Palpitaciones |
| Mareos |
| Parestesias |
| Mialgias |
| Contraindicaciones |
| Absolutas |
| Infarto de miocardio de menos de 4 semanas de evolución |
| Angina inestable |
| Arritmias cardíacas graves |
| Relativas |
| Embarazo |
| Lactancia |
Un metaanálisis reciente muestra que la OR para la abstinencia con los diferentes tipos de TSN, comparada con los controles, es de 1,77 (IC del 95%, 1,66-1,88), con un nivel de evidencia A15. Esta eficacia no sólo se observa cuando es un profesional sanitario quien, en el contexto de un programa de deshabituación, ofrece y controla el TSN, sino que también se mantiene cuando se ofrece como medicamento de venta sin receta, sin proporcionar ningún tipo de apoyo psicológico. En los últimos años se han realizado varios estudios con el objetivo de obtener un incremento significativo de la eficacia de este tratamiento. Para ello se han seguido 3 líneas de investigación. Mientras que algunos análisis han intentado buscar un incremento de la eficacia mediante el aumento de la dosis de nicotina, otros han preferido tratar de mejorar la forma de administración de ésta con el propósito de conseguir picos de nicotinemia más altos y rápidos22. En otros estudios se ha optado por analizar la eficacia de la combinación de diferentes vías de administración de la nicotina23.
Reducción del consumo del tabaco como paso previo al abandono completo utilizando tratamiento sustitutivo con nicotinaConcepto. Se define como reducción del consumo de tabaco la disminución del número de cigarrillos diarios en al menos el 50%, disminución que ha de mantenerse como mínimo durante 4 meses. La reducción debe verificarse por un descenso sostenido de los valores de monóxido de carbono en el aire espirado24.
Eficacia y seguridad del tratamiento sustitutivo con nicotina en la reducción del consumo de tabaco como paso previo a la cesación. Durante los últimos años se ha realizado un gran número de estudios y ensayos clínicos en los que se han analizado la eficacia y seguridad de la reducción del consumo de tabaco como paso previo a su abandono25-27. De los resultados de la mayoría de ellos se deduce que reducir el número de cigarrillos consumidos al día no sólo incrementa la motivación para realizar intentos de abandono definitivo del tabaco, sino que también aumenta las posibilidades de conseguirlo. Además, todos estos estudios concluyen que es seguro utilizar TSN (fundamentalmente chicles de nicotina) conjuntamente con el consumo de cigarrillos25-27. Los efectos adversos que aparecen son similares a los que se manifiestan en los estudios en los que el TSN se emplea sin consumo de tabaco y, además, en ningún caso se observaron signos o síntomas de intoxicación nicotínica25-27. Recientemente el Ministerio de Sanidad y Consumo español ha aprobado la utilización de chicles de nicotina para reducir progresivamente el consumo de cigarrillos como paso previo a la cesación completa.
Indicaciones de la reducción del consumo de tabaco como paso previo a la cesación. Hay 3 tipos de fumadores en los que estaría indicado un planteamiento terapéutico de esta índole: los que no quieren dejar de fumar pero se muestran proclives a reducir significativamente el número de cigarrillos consumidos al día; los que, queriendo dejar de fumar, encuentran muchas dificultades para conseguirlo y se sienten frustrados ante la idea de abandonar de forma brusca el consumo de tabaco, y por último, los que quieren dejar de fumar pero no de forma brusca y prefieren reducir progresivamente el número de cigarrillos diarios.
Consideraciones clínicas. Es importante tener en cuenta las siguientes consideraciones en el manejo clínico de los fumadores en proceso de reducción progresiva del consumo de tabaco28:
- 1.
El fumador iniciará el tratamiento para reducir el número de cigarrillos que consume diariamente, pero sabiendo que el objetivo final será el abandono definitivo.
- 2.
Se recomienda que el proceso se realice en 3 fases:
- –
La primera fase se desarrolla desde el día que se inicia la reducción del consumo de tabaco hasta que se alcanza el 50% de éste. Debe durar entre 8 y 10 semanas. Es imprescindible que el fumador utilice chicles de nicotina para ayudarse en este proceso. Se recomienda que sustituya 2 cigarrillos por una pieza de chicle.
- –
La segunda fase se extiende hasta el día en que se abandona por completo el tabaco. Debe durar entre 8 y 10 semanas. Igualmente se deben utilizar chicles de nicotina. En esta fase se recomienda que cada cigarrillo se sustituya por una pieza de goma de mascar.
- –
La última etapa se corresponde con el tiempo en el cual el sujeto ya no consume tabaco y va abandonando progresivamente los chicles de nicotina. En general, tiene una duración de 2 a 3 meses.
- –
- 3.
Se recomienda que los fumadores que consumen más de 20 cigarrillos diarios o tienen un alto grado de dependencia física a la nicotina utilicen chicles de 4mg, y que los que fuman 20 cigarrillos o menos, o tienen un grado de dependencia moderado o bajo, utilicen los chicles de 2mg.
- 4.
Validación de la reducción. En todo proceso de reducción ésta debe ser correctamente validada. Una buena forma de validar químicamente la reducción del consumo de tabaco es recurriendo a la cooximetría. A este respecto es necesario saber que las reducciones del número de cigarrillos diarios se acompañan de reducciones de los valores de monóxido de carbono en el aire espirado, aunque estas reducciones son siempre menos intensas que las del número de cigarrillos.
- 5.
Si al cabo de 2 a 3 meses de utilización concomitante de chicles de nicotina y cigarrillos no se hubiera producido una reducción significativa y validada químicamente de al menos el 50% del consumo basal, está indicado dar por fracasado el intento e interrumpir el tratamiento.
El bupropión es un polvo blanco y amargo que se expende en forma de comprimidos de liberación sostenida que contienen 150mg de sustancia activa. No se conoce con exactitud cuál es el mecanismo de acción de este fármaco. Se sabe que actúa en el núcleo accumbens inhibiendo la recaptación neuronal de dopamina; este efecto explicaría la reducción del craving que los fumadores experimentan cuando lo utilizan. También inhibe la recaptación neuronal de noradrenalina en el núcleo cerúleo, con lo que consigue una reducción significativa de la intensidad de los síntomas del síndrome de abstinencia a la nicotina29. En recientes estudios in vitro30 se ha observado que el bupropión es un inhibidor funcional no competitivo de los receptores nicotínicos de acetilcolina. Esta actividad antinicotínica puede contribuir a su eficacia en el tratamiento de la dependencia nicotínica.
Un metaanálisis demostró que el bupropión a dosis de 300mg/día durante un período de 7 semanas se asociaba con un incremento significativo de la abstinencia continua al final del tratamiento, con una OR de 2,71 (IC del 95%, 1,88-4,07); a los 12 meses de seguimiento la OR fue de 2,10 (IC del 95%, 1,62-2,73)31. Más recientemente otro metaanálisis que ha evaluado la eficacia del bupropión en 19 ensayos clínicos ha encontrado una OR de 2,06 (IC del 95%, 1,77-2,40)32.
En la tabla IV se indican la dosis, los principales efectos adversos y las contraindicaciones del bupropión1-8,29,31,32.
Bupropión
| Eficacia |
| Odds ratio=2,06 (intervalo de confianza del 95%, 1,77-2,40) |
| Dosis |
| Debe utilizarse durante un período de 7–9 semanas a dosis de 300mg diarios en 2 tomas de 150mg cada una |
| El tratamiento se iniciará de 7–15 días antes de abandonar definitivamente el consumo del tabaco |
| Durante la primera semana el paciente tomará sólo un comprimido de 150mg cada día y después de este período se incrementará la dosis a 2 comprimidos de 150mg |
| Conviene tomar un comprimido a primera hora de la mañana, en el momento de levantarse, y el segundo 8h después |
| En fumadores de 65 años o más, con insuficiencia renal o hepática significativa o con bajo peso (< 45kg) se recomienda bajar la dosis a la mitad |
| Efectos adversos* |
| Sequedad de boca (7-12%) |
| Insomnio (10-31%) |
| Inestabilidad (3-8%) |
| Cefalea (3-17%) |
| Náuseas (3-5%) |
| Manifestaciones alérgicas cutáneas (2-14%) |
| Convulsiones (0,1%) |
| Contraindicaciones |
| Epilepsia |
| Trastornos convulsivos |
| Bulimia o anorexia nerviosa |
| Uso simultáneo de inhibidores de la monoaminoxidasa |
| Cirrosis hepática |
| Trastorno bipolar |
| Precauciones de uso |
| Debe utilizarse con precaución en las siguientes circunstancias: |
| Fumadores en situaciones que reducen el umbral convulsionante (antecedentes de alcoholismo, antecedentes de traumatismo craneoencefálico, fumadores en proceso de retirada de benzodiacepinas, etc.) |
| Fumadores que están utilizando medicación que reduce el umbral convulsionante (antipsicóticos, teofilina, corticoides sistémicos, quinina, antidepresivos, antidiabéticos orales, etc.) |
La vareniclina ha sido recientemente aprobada por la Food and Drug Administration estadounidense y por la Agencia Europea del Medicamento como tratamiento específico para dejar de fumar. En España está disponible con la misma indicación desde enero de 2007.
La vareniclina es un fármaco específicamente desarrollado para ayudar a los fumadores a dejar de fumar. Actúa como agonista parcial selectivo de los receptores nicotínicos de las neuronas del área tegmental ventral del meséncefalo. Al ser agonista parcial cumple características de los agonistas y de los antagonistas. Por ser un agonista tiene la capacidad de estimular el receptor nicotínico y por ello es capaz de controlar el craving y el síndrome de abstinencia, pero como antagonista es capaz de bloquear los efectos que la nicotina produce sobre el receptor; por ello su utilización cuando se está dejando de fumar facilita que las recaídas no se acompañen de sensación placentera y recompensa, y por ello este fármaco ayuda a evitar que una recaída se convierta en fracaso. Otra de sus características definitorias es que se elimina casi en su totalidad a través de la orina sin metabolización hepática. Esto hace que no presente problemas de interacción con otros medicamentos33.
El más reciente metaanálisis que la Cochrane Library ha realizado señala que la utilización de vareniclina en un intento por dejar de fumar multiplica por 3 las posibilidades de éxito al cabo del año de seguimiento, en comparación con la utilización de placebo (OR=3,22; IC del 95%, 2,43-4,27). Igualmente se encontró que este fármaco ayudó a más fumadores a dejar de serlo que el bupropión (OR=1,66; IC del 95%, 1,28-2,16). Las náuseas fueron el efecto adverso más común, aunque la mayor parte de las veces fueron de intensidad leve y con tendencia a la autolimitación en el tiempo34.
En la tabla V se recogen la dosis, los principales efectos adversos y las contraindicaciones de la vareniclina34.
Vareniclina
| Eficacia |
| Frente a placebo: OR=3,22 (IC del 95%, 2,43-4,27) |
| Frente a bupropión: OR=1,66 (IC del 95%, 1,28-2,16) |
| Dosis |
| Primera semana: los sujetos podrán fumar y deberán utilizar el fármaco a dosis de 0,5mg una vez al día durante los 3 primeros días, y después a dosis de 0,5mg 2 veces al día hasta completar la primera semana |
| Pasado este tiempo, deberán abandonar el consumo de tabaco y comenzar a utilizar el fármaco a dosis de 1mg 2 veces al día, hasta completar 12 semanas de tratamiento |
| Efectos adversos |
| Náuseas* (28%) |
| Flatulencia (2-5%) |
| Insomnio (13-15%) |
| Sueños anormales (11-13%) |
| Contraindicaciones |
| Hipersensibilidad a vareniclina |
IC: intervalo de confianza; OR: odds ratio.
La vareniclina es un fármaco con un mecanismo de acción diferente del TSN y del bupropión. La información disponible la sitúa como un tratamiento farmacológico de primera línea, eficaz y seguro para ayudar a los fumadores a dejar el tabaco y para prevenir las recaídas.
Financiación de los tratamientos farmacológicos del tabaquismoDiversas guías realizadas en distintos países sobre el tratamiento de la dependencia al tabaco establecen con el nivel de evidencia más alto (A) que hay tratamientos farmacológicos eficaces para ayudar a los fumadores a dejar de serlo1-8. Además señalan, con el mismo grado de evidencia, que la relación coste/efectividad de este tipo de tratamientos es significativamente mejor que la de otros tratamientos de otras enfermedades crónicas como la hipertensión arterial o la hipercolesterolemia. También refieren con el mismo nivel de evidencia (A) que el tratamiento para el abandono del tabaco es la intervención "por excelencia" de todas las intervenciones preventivas1-8. Resulta, pues, sorprendente observar cómo los tratamientos de la hipertensión arterial o la hipercolesterolemia están financiados por los sistemas de salud, tanto públicos como privados, mientras que se exponen numerosos obstáculos a la financiación de los tratamientos para dejar de fumar.
La evidencia científica señala que cuando se financian, pública o privadamente, los tratamientos farmacológicos para dejar de fumar se consigue que un mayor número de fumadores realicen un serio intento de abandono, con lo cual se incrementa el número de exfumadores y, además, aumentan ligeramente las tasas de abstinencia prolongada sin demasiada elevación del gasto (nivel de evidencia B)1,35.
A continuación exponemos 2 propuestas de financiación de los tratamientos farmacológicos del tabaquismo que creemos debería considerar el sistema sanitario público.
Una de las posibles soluciones al problema de la financiación puede pasar por la realización de contratos de riesgo compartido entre la industria farmacéutica y los sistemas de salud en cuanto a los medicamentos para dejar de fumar. Creemos que, dada la incertidumbre sobre el impacto que en los presupuestos públicos podría tener una posible financiación de los tratamientos farmacológicos del tabaquismo, un contrato de este tipo entre la industria y el sistema nacional de salud podría ser una solución. En dicho contrato tanto la industria como el sistema sanitario público tendrían que aceptar sus propias responsabilidades. La industria farmacéutica debería aceptar un compromiso firme con los objetivos de sostenibilidad presupuestaria, la devolución del gasto en caso de prescripción inadecuada y el establecimiento de diferentes precios para distintos grupos poblacionales. El sistema sanitario público, por su parte, debería aceptar un precio sobre la base de la innovación incremental del producto, y que cualquier renegociación del precio debería realizarse de forma bilateral entre el sistema y la industria.
Otra posible solución pasaría por el establecimiento de condiciones que debería cumplir el fumador, e incluso el profesional sanitario prescriptor. El tratamiento farmacológico sería financiado con las siguientes condiciones:
- 1.
El tratamiento sólo debería prescribirse cuando el fumador expresa su compromiso de dejar de fumar y fija una fecha para hacerlo.
- 2.
Con el fin de optimizar los recursos disponibles se podría identificar en la población de fumadores a algunos colectivos prioritarios. Entre ellos cabría destacar los siguientes:
- –
Pacientes con enfermedades producidas por el tabaquismo, cuya historia natural es susceptible de revertir o detenerse, como la enfermedad pulmonar obstructiva crónica, enfermedades cardiovasculares de diferente índole de manifestación o el cáncer con perspectivas de remisión.
- –
Pacientes con enfermedades no producidas por fumar, pero que se ven agravadas por el consumo de tabaco, como sucede con el asma bronquial, la diabetes, las bronquiectasias, la insuficiencia respiratoria crónica de cualquier etiología, el síndrome de apneas durante el sueño, etc.
- –
Fumadores que, aun sin presentar enfermedad, manifiestan deseos serios de dejar de fumar, han realizado intentos previos y no son capaces de controlar su consumo, bien sea por la intensidad de la dependencia o por presentar comorbilidad psiquiátrica.
- –
Profesionales vistos como modélicos por la influencia que su profesión ejerce sobre las conductas de la población, como los profesionales sanitarios o los docentes.
- –
- 3.
Se utilizarían sólo los tratamientos farmacológicos que han demostrado ser eficaces y seguros y que se recomiendan en las distintas guías nacionales e internacionales de tratamiento del tabaquismo. Para la prescripción y la forma de uso se seguirían las indicaciones de estas guías.
- 4.
A fin de optimizar la utilización del tratamiento farmacológico, éste se entregaría al fumador de forma paulatina según acudiese a las consultas de seguimiento. En ningún caso se le entregaría toda la medicación al inicio del tratamiento.
- 5.
En caso de fracaso en el intento, no se volvería a financiar gratuitamente otro tratamiento hasta pasados 6 meses desde la fecha del fracaso anterior.
La puesta en marcha de cualquiera de estas 2 opciones de financiación supondría un reconocimiento del tabaquismo como enfermedad crónica susceptible de ser tratada por el sistema sanitario público, a la vez que contribuiría a que un mayor número de fumadores realizaran serios intentos de abandono del tabaco y con ello se incrementarían sensiblemente sus posibilidades de éxito. Asimismo queremos destacar que el colectivo de profesionales sanitarios de la neumología está perfectamente formado para el cumplimiento de todas las recomendaciones que se han realizado y que pueden contribuir adecuadamente a la optimización de los recursos necesarios para la financiación de los tratamientos para dejar de fumar.