La proteinosis alveolar pulmonar (PAP) es una enfermedad pulmonar poco frecuente, en la que se acumula material lipoproteináceo en los espacios alveolares1,2. Se han descrito 3 tipos: congénita, secundaria y adquirida. La PAP secundaria se asocia a menudo con enfermedades hematológicas malignas y con inmunodeficiencia3. Describimos el caso de un paciente inmunodeprimido con PAP secundaria e infección por citomegalovirus.
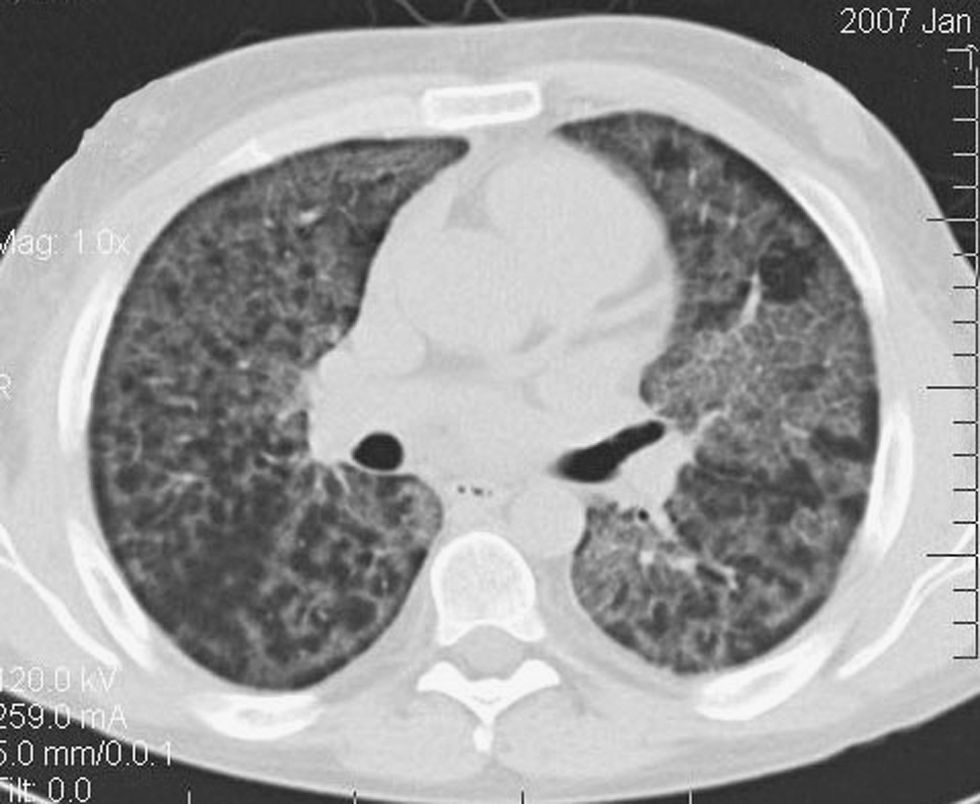
Un varón de 26 años de edad acudió a nuestro centro con disnea. No presentaba fiebre, expectoración ni hemoptisis. Había recibido 7 años antes un trasplante alogénico de células madre hematopoyéticas por anemia resistente, y 3 años antes, un trasplante de riñón por insuficiencia renal crónica relacionada con enfermedad del injerto contra huésped de carácter crónico. En el examen, el paciente presentaba anemia, pero ninguna otra anomalía. Los datos de laboratorio incluían el recuento de leucocitos, que era de 5.230/μl, con un 77% de neutrófilos, un 18% de linfocitos, un de 3% monocitos y un 2% de eosinófilos. La presión arterial de oxígeno era de 58mmHg. Las radiografías de tórax mostraban patrones reticulares bilaterales de mayor opacidad sin afectar a los ángulos costofrénicos. La tomografía computarizada de alta resolución (fig. 1) mostró áreas dispersas de atenuación en vidrio deslustrado, con superposición de engrosamiento septal intra e interlobular (patrón en empedrado). Dado el resultado de los estudios de imagen, se realizó un lavado broncoalveolar mediante fibrobroncoscopia. El líquido del lavado broncoalveolar presentaba a la vista un aspecto lechoso, y microscópicamente contenía macrófagos cargados de lípidos y una gran cantidad de material positivo a la reacción del ácido peryódico de Schiff y resistente a la diastasa. Además, se encontró una concentración elevada de ADN de citomegalovirus en sus células, detectado mediante la técnica de reacción en cadena de la polimerasa en tiempo real. Una vez confirmado el diagnóstico de PAP, se realizó un lavado pulmonar completo. El paciente experimentó una gran mejoría, por lo que se decidió que se llevaría a cabo tratamiento ambulatorio y que se programaría otro lavado pulmonar si estaba indicado. La infección por citomegalovirus se trató con fármacos antivíricos e inmunoglobulina anticitomegalovirus.
La PAP secundaria se desarrolla en el contexto de una deficiencia funcional o de una reducción del número de macrófagos alveolares4 en situaciones tales como los trastornos hematológicos (p. ej., leucemia o linfoma) o los trastornos de la inmunodeficiencia (p. ej., el sida), o bien después de un trasplante de órgano2,3. Las infecciones micobacterianas, por citomegalovirus o por Pneumocystis jiroveci, se han asociado asimismo a la PAP2. La PAP secundaria es también una complicación poco frecuente que ocurre de forma tardía tras un trasplante de células madre hematopoyéticas5.
En nuestro paciente, la PAP secundaria se desarrolló asociada a inmunodeficiencia y a una reactivación de citomegalovirus. La neumonía intersticial por citomegalovirus es una complicación grave en huéspedes inmunocomprometidos, como los pacientes que han recibido un trasplante. Se ha planteado que la reactivación de citomegalovirus, que afecta a los macrófagos alveolares, podría inducir la PAP6, si bien otros estudios indican que las infecciones oportunistas se solapan con una PAP ya existente2. La infección es una característica común en el curso de la PAP, pero en su modalidad secundaria no está claro si es la causa o el efecto de la infección. La tomografía computarizada de alta resolución muestra un patrón en empedrado. Aunque esta característica radiológica no es patognomónica de la PAP, es sumamente indicativa de ella. Los hallazgos radiográficos típicos de citomegalovirus (nódulos pequeños o mal definidos y consolidaciones densas) no estaban presentes en nuestro paciente, aunque no podemos descartar que la atenuación en vidrio deslustrado pudiera deberse a la infección por citomegalovirus.
En conclusión, este caso destaca la importancia de contemplar el diagnóstico de PAP como causa de infiltraciones pulmonares difusas en un paciente con inmunodepresión.