Introducción
El nódulo pulmonar periférico sigue siendo un reto frustrante para el broncoscopista. La rentabilidad diagnóstica de la biopsia transbronquial es muy limitada en estos casos y no supera el 15-30% en lesiones de tamaño inferior a 2 cm, sobre todo si éstas se encuentran en el tercio distal de la vía aérea1. Lo mismo podría decirse de la punción transbronquial de adenopatías mediastínicas, por diferentes razones. En este caso, la frustración suele aparecer por la dificultad que entraña reproducir la rentabilidad diagnóstica de centros con gran experiencia2 y sobre todo de aquellos que, como el nuestro, gozan del lujo de un patólogo presente durante la exploración.
Ninguna de las técnicas complementarias desarrolladas hasta el momento, entre ellas la biopsia guiada por endoscopio o por tomografía computarizada (TC)3, ha conseguido un aumento significativo de la rentabilidad diagnóstica. Todas ellas se ven limitadas por la dificultad para acceder con un instrumento rígido a una lesión periférica. En general, cuanto menor es la lesión, menor es la rentabilidad diagnóstica. Tan sólo el ecoendoscopio parece capaz de garantizar el éxito de la punción transbronquial del mediastino4,5, ya que permite visualizar en tiempo real las adenopatías subsidiarias de punción, pero requiere una inversión elevada y un largo aprendizaje.
La introducción de la navegación electromagnética permite realizar con gran precisión una biopsia tanto de nódulos periféricos de pequeño tamaño como de adenopatías mediastínicas utilizando un broncoscopio terapéutico convencional. El éxito de esta técnica novedosa se basa en 3 pilares: a) la planificación virtual previa con una TC multicorte; b) la navegación en tiempo real, y c) la disponibilidad de una sonda electromagnética dirigible que permite sortear los giros y bifurcaciones de la vía aérea que llevan hasta una lesión remota.
Métodos
Descripción de la técnica
El sistema Broncus® (superDimension, Europe, Düsseldorf, Alemania) se compone de 4 elementos fundamentales: a) un campo electromagnético que rodea el tórax del paciente; b) una sonda electromagnética dirigible, confeccionada y calibrada manualmente; c) un canal de trabajo extensible y reforzado con titanio en su extremo distal para facilitar la obtención de material diagnóstico, y d) el software capaz de planificar la intervención y proporcionar una guía visual en tiempo real de la localización de la sonda. Todas las intervenciones se realizan utilizando un videobroncoscopio flexible terapéutico (el canal de trabajo de éste debe ser de 2,8 mm para facilitar la inserción del canal extensible) bajo sedación o, en algunos casos, mediante anestesia general. En nuestro centro utilizamos una combinación de midazolam y fentanilo o propofol junto con anestesia tópica.
Todos los pacientes precisan la realización de una TC con cortes de 2-3 mm e intervalos de 1-1,5 mm en formato DICOM. La información de la TC se graba en un CD, que a su vez permite la planificación de la intervención mediante una reconstrucción virtual del árbol bronquial.
Registro, navegación y obtención de la muestra
La reconstrucción del árbol bronquial permite marcar puntos de referencia virtuales, generalmente de fácil acceso, como la carina principal, que a su vez permiten al sistema triangular la posición de la sonda dentro del campo electromagnético y, por ende, dentro del tórax del paciente durante la intervención. Se marcan asimismo una o varias dianas (un nódulo pulmonar y/o adenopatía mediastínica) y en ocasiones varios puntos de referencia intermedios (p. ej., carinas subsegmentarias) que facilitarán la búsqueda sistemática del recorrido endobronquial hasta la diana. Durante la broncoscopia se introducen el canal extensible y la sonda en el árbol bronquial, y se registran los mismos puntos de referencia seleccionados durante la planificación. Este proceso se consigue tocando suavemente cada punto de referencia (p. ej., la carina principal) con el extremo distal de la sonda y oprimiendo un pedal. El software se encarga entonces de comparar las 2 imágenes, la virtual y la real, e indicar el grado de divergencia entre ambas (p. ej., carina principal virtual frente a carina principal real), que en condiciones óptimas no debe superar los 4 mm. Una vez completado el proceso de registro comienza la navegación. Durante el proceso el operador dispone en todo momento de una reconstrucción en 3 proyecciones del escáner del paciente. La situación de la sonda en este mundo virtual depende de su posición dentro del campo electromagnético. Es fácil comprobar que todo está en orden al colocar la sonda en cualquier punto visible del árbol bronquial, asegurando al hacerlo que la ubicación de la sonda en el mundo virtual de la pantalla se corresponde con su ubicación real (p. ej., un bronquio segmentario del lóbulo inferior derecho). La navegación se realiza avanzando, al mismo tiempo y sin forzar, el canal extensible y la sonda hasta que se alcanza la lesión. El sistema permite comprobar en todo momento si la sonda se aproxima a la lesión o si, por el contrario, se aleja. De ser así, el operador puede reconducir la sonda guiándose por las 3 proyecciones, y rectificar a cada paso si es necesario, hasta alcanzar el bronquio que lleva hasta la diana. La navegación hasta un ganglio mediastínico es mucho más sencilla, ya que no requiere adentrarse en el árbol bronquial. En ambos casos, el software advierte de la distancia y dirección hasta el centro de la diana tomando como referencia la punta de la sonda.
Una vez alcanzado el nódulo o la adenopatía, se fija el canal extensible y se retira la sonda. Posteriormente se introduce la pinza de biopsia o una aguja citológica y se obtienen las muestras. En nuestro centro este proceso se realiza con la presencia del anatomopatólogo para asegurar el éxito de la intervención y comprobar que el material obtenido es adecuado para establecer un diagnóstico. Algunos centros obtienen biopsias con escopio, pero en nuestro caso no lo creemos necesario.
Indicaciones
La navegación electromagnética está indicada en el diagnóstico de todo tipo de nódulos pulmonares y adenopatías mediastínicas. Resulta particularmente útil cuando un nódulo es de difícil acceso para la punción guiada por TC o de pequeño tamaño (< 2,5 cm). También resulta de utilidad en la punción de adenopatías pequeñas o en aquellas en que tradicionalmente es difícil obtener muestras, como las hiliares, paratraqueales altas etc.
Limitaciones
Las limitaciones del sistema radican fundamentalmente en el límite de tamaño, en torno a los 8-10 mm, del nódulo diana que puede biopsiarse. Algunas lesiones, como las de los lóbulos superiores, son de más difícil acceso. Existe, como es lógico, una curva de aprendizaje, en torno a 10 intervenciones, y un coste sobreañadido, además de una prolongación de la intervención, por lo general inferior a 10 min. Otras limitaciones del sistema incluyen la necesidad de utilizar un broncoscopio terapéutico con un canal de trabajo de 2,8 mm, la imposibilidad de aspirar secreciones o sangre durante la navegación y el imperativo de obtener un escáner con solapamiento y cortes concretos para optimizar la planificación. Por último, algunos nódulos (probablemente en torno al 10%) son inalcanzables por su localización o lejanía.
Contraindicaciones
Las contraindicaciones son las propias de cualquier broncoscopia. Además, debe tenerse en cuenta el riesgo hipotético de una interferencia del campo electromagnético con dispositivos como marcapasos o desfibriladores, si bien la magnitud de dicho campo es inferior al de la tierra.
Observación clínica
El nódulo periférico
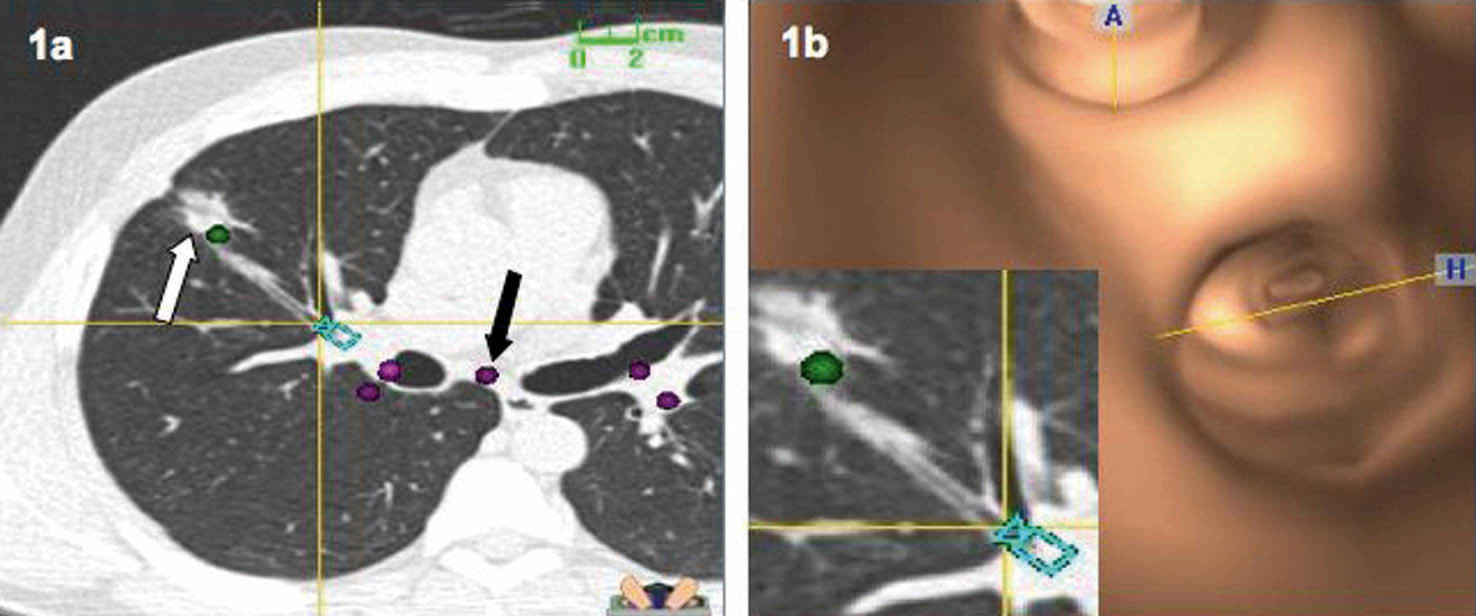
Varón de 45 años de edad, exfumador, sin antecedentes personales de interés, que acudió a nuestro centro para valoración de una masa pulmonar. Había comenzado con hemoptisis franca en abril de 2006. En la radiografía de tórax se detectó una lesión en el lóbulo superior derecho. La TC confirmó la presencia de un nódulo cavitado espiculado de 2 cm en esa localización, motivo por el que se realizaron tanto broncoscopia como punción guiada por TC, sin éxito. Ante la incertidumbre diagnóstica, sus médicos le plantearon una intervención quirúrgica. El paciente se negó y permaneció asintomático hasta julio, cuando presentó hemoptisis de nuevo. Acudió a nuestro centro refiriendo molestias vagas en el hombro y hemitórax derecho, y expectoración matutina crónica, sin fiebre, pérdida de peso o disnea. La exploración física fue normal. En nuestro centro se planteó repetir la broncoscopia con navegación electromagnética, previa realización de una TC de planificación (fig. 1). Se obtuvieron 3 biopsias y varias punciones tras lograr navegar con la sonda electromagnética hasta 5 mm de distancia del nódulo. El anatomopatólogo, presente durante la exploración, confirmó la presencia de inflamación extensa, motivo por el que se envió material de una de las punciones al Laboratorio de Microbiología. En el cultivo se aislaron Prevotella melaninogenica, Peptostreptococcus micros y Streptococcus salivarius, y en el informe de las biopsias se refería inflamación crónica. Se inició tratamiento antibiótico con Augmentine® y se desestimó la cirugía. El nódulo desapareció con el tratamiento antibiótico pautado.
Fig. 1. La planificación previa(a) permite marcar puntos de referencia como la carina principal (flecha negra) y el nódulo diana (flecha blanca), que facilitan la navegación con gran precisión. La reconstrucción virtual del árbol bronquial del paciente (b)identifica el bronquio que lleva hasta la lesión. Se obtuvieron biopsias, punciones y cultivos, todos ellos indicativos del diagnóstico de absceso pulmonar.
La adenopatía hiliar
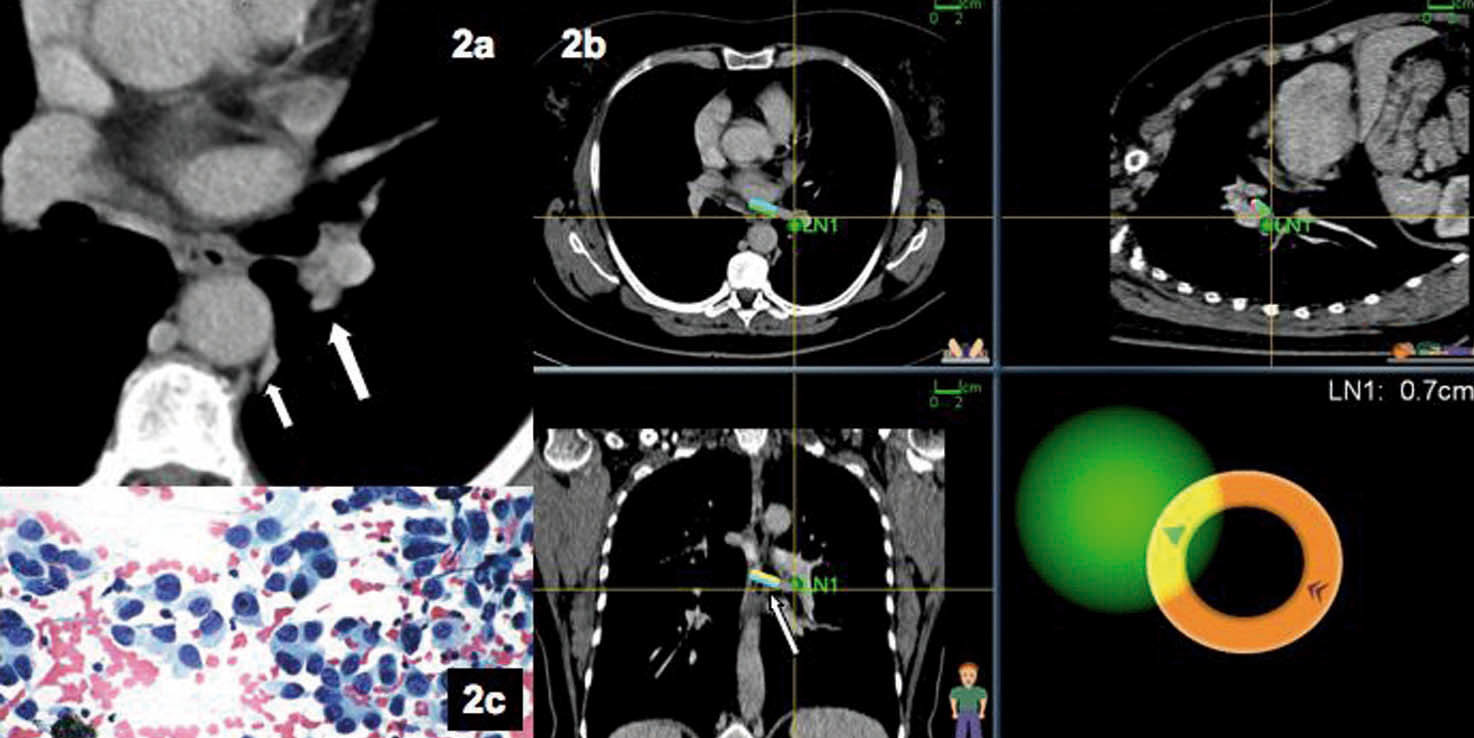
Mujer de 52 años de edad, no fumadora, que acudió a consulta para valoración de un nódulo pulmonar. Se le había diagnosticado recientemente de artritis reumatoide seronegativa y presentaba enfermedad de Von Willebrand. Se realizó una TC torácica sin contraste, motivada por un cuadro de tos y disnea persistente. En el escáner se objetivó una pequeña lesión de 1 cm de tamaño, paraaórtica, sin adenopatías visibles (fig. 2). En nuestro centro se realizó una tomografía por emisión de positrones, que evidenció captación no sólo del nódulo pulmonar ya conocido, sino también de la región hiliar izquierda. Por este motivo se planteó la realización de una broncoscopia diagnóstica con navegación electromagnética, previa administración profiláctica de desmopresina. Se efectuaron 3 punciones con aguja citológica y el anatomopatólogo estuvo presente durante la exploración (fig. 2). Se diagnosticó un adenocarcinoma de probable origen pulmonar.
Fig. 2. Imagen de tomografía computarizada convencional(a), que iden-tifica la presencia de un nódulo pulmonar paraaórtico inaccesible (flecha pequeña) y un ligero engrosamiento hiliar izquierdo (flecha gruesa) que resultó hipercaptante por tomografía por emisión de positrones. Imagen de navegación(b)con la sonda (flecha) a 0,7 cm de la adenopatía, que permite realizar una punción transbronquial. El anatomopatólogo, presente durante la exploración, confirmó que se trataba de un adenocarcinoma (c).
Discusión
El sistema de navegación de Superdimension permite la obtención de biopsias tanto de adenopatías mediastínicas como de nódulos pulmonares periféricos de pequeño tamaño. Su fiabilidad y precisión han sido demostradas recientemente en un ensayo de la Cleveland Clinic6. La media de tamaño de los nódulos biopsiados en ese estudio era de 22,8 mm, y el de las adenopatías, de 28,1 mm. La rentabilidad diagnóstica de la broncoscopia en ambos casos fue del 74 y el 100%, respectivamente. Tan sólo se objetivaron 2 neumotórax en un total de 60 pacientes como única complicación, y los tiempos de navegación fueron realmente cortos: no superaron la media de 7 y 2 min, respectivamente. En nuestro centro comunicación enviada a la Sociedad Española de Neumología y Cirugía Torácica (SEPAR) hemos realizado 8 intervenciones en poco tiempo, con el resultado de 6 diagnósticas y 2 no diagnósticas (un carcinoide, un absceso, una tuberculosis, 2 adenocarcinomas y un carcinoma escamoso). El tamaño medio de los nódulos biopsiados en nuestro centro es de 2,5 cm y no se produjo ningún neumotórax.
La planificación previa de la intervención, que habitualmente se realiza con un ordenador portátil, es fundamental a la hora de acortar el procedimiento. La sonda goza de la peculiaridad de ser dirigible, propiedad que permite sortear giros y bifurcaciones hasta alcanzar el nódulo diana. Esto es imposible de conseguir con instrumentos rígidos como el fórceps o la aguja citológica. Por último, la presencia de un anatomopatólogo durante la exploración permite confirmar el diagnóstico in situ, asegurando el éxito de la intervención. En este caso, consideramos que el sistema Bronchus® puede ser particularmente útil en centros que no disponen de este servicio, ya que permite realizar punciones mediastínicas con una fiabilidad y precisión que rivalizan con las que se obtienen con el ecoendoscopio.
A pesar de que el sistema impone ciertas limitaciones, su versatilidad promete revolucionar el manejo del nódulo pulmonar solitario e implicar definitivamente al broncoscopista como actor fundamental no sólo en la toma de decisiones, sino también en la obtención de material diagnóstico. En cuanto al coste que supone la adquisición del sistema y cada sonda individual, parece muy asumible7, ya que el sistema evita en algunos casos intervenciones quirúrgicas de carácter diagnóstico mucho más costosas.
Correspondencia: Dr. L.M. Seijo.
Departamento de Neumología. Clínica Universitaria de Navarra.
Avda. Pío XII, 36. 31008 Pamplona. Navarra. España.
Correo electrónico: lmseijo@unav.es
Recibido: 31-10-2006; aceptado para su publicación: 18-12-2006.