Introducción
La prevalencia global de la enfermedad pulmonar obstructiva crónica (EPOC) en nuestra área de referencia es del 7,2%. Un 1% tiene un volumen espiratorio forzado en el primer segundo (FEV1) menor del 50% y en un 0,4% es inferior al 35%1. El gasto sanitario aumenta progresivamente tanto por el incremento de la esperanza de vida de la población como por la necesidad de cuidados crónicos2.
Con la organización asistencial actual de la medicina en nuestro país, son los médicos de asistencia primaria quienes controlan a la mayoría de los pacientes afectados de EPOC de grado leve o moderado, pero no existe un modelo claro de cómo enfocar la atención sanitaria en los casos de EPOC grave. Actualmente la atención de estos pacientes puede realizarse de 3 maneras: a) control del paciente en asistencia primaria, con consultas esporádicas al neumólogo hospitalario; b) control mixto entre asistencia primaria y hospital, y c) control casi único por el neumólogo de hospital. En la práctica, debido a la ausencia de barreras de acceso al sistema sanitario, estos pacientes pueden consultar a cualquier nivel.
En 1920, el informe Dawson ya aconsejaba enfocar el diseño y la organización de los servicios asistenciales, la distribución de recursos y la formación de los médicos a partir de criterios de base epidemiológica3. Desde entonces, los países de la Europa occidental han ido desarrollando su sistema sanitario para encontrar modelos de atención adecuados desde el punto de vista clínico y lo menos costosos posible. Por este motivo, parece razonable, como un primer enfoque del problema, cambiar el modelo asistencial por otro en el que las poblaciones comparadas sean superponibles y que permita realizar un estudio de minimización de costes.
Los objetivos principales de nuestro estudio han sido evaluar la repercusión, sobre la clínica y calidad de vida de los pacientes, de un nuevo modelo de asistencia sanitaria para pacientes con EPOC grave e insuficiencia respiratoria crónica basado en una consulta monográfica (CM) hospitalaria, así como cuantificar los costes económicos para el suministrador de servicios (hospital) y para el financiador (Servei Català de la Salut [SCS]) que ello comporta.
Pacientes y métodos
Se ha realizado un estudio observacional con control histórico en la Corporació Parc Taulí (CPT), hospital de Sabadell que dispone de 752 camas y una población de referencia de 350.000 habitantes. El tiempo de seguimiento de los pacientes estudiados fue de un año. En todos ellos se evaluaron las mismas variables durante el año anterior a su inclusión en la CM (control histórico). Los datos históricos de los pacientes, así como los datos económicos, se obtuvieron de la Unidad de Programación, del Servicio de Epidemiología, del Servicio de Planificación y de la Unidad de Contratación y Facturación de la CPT.
Pacientes
Se definieron los siguientes criterios de inclusión: a) EPOC grave (FEV1 ≤ 50% del valor predicho); b) presión arterial de oxígeno (PaO2) ≤ 65 mmHg; c) estabilidad clínica, gasométrica (variación en la PaO2 ≤ 5 mmHg) y espirométrica (variación del FEV1 posbroncodilatación < 15%) durante los 3 meses anteriores a su inclusión. Los criterios de exclusión fueron los siguientes: a) historia clínica de asma; b) alteración ventilatoria restrictiva; c) síndrome de apneas-hipopneas durante el sueño; d) tratamiento con analépticos respiratorios o fármacos en investigación, y e) enfermedad maligna.
Para el cálculo del tamaño muestral se consideraron las variables indicativas de efectividad clínica (número de consultas a urgencias y de hospitalizaciones). Ante la carencia de datos bibliográficos orientativos en este tipo de servicios, se consideró válida y fiable la experiencia del grupo investigador4, que había observado una disminución del número de ingresos hospitalarios similar a la comunicada por otros autores. Skawarska et al5 y Cotton et al6 han encontrado en estudios prospectivos resultados similares, si bien la gravedad de los pacientes estudiados no es tan importante como la de nuestra población. Farrero et al7, en un estudio prospectivo con 2 niveles de intervención distintos de los evaluados en el nuestro (tratamiento domiciliario y control convencional) pero con pacientes con una gravedad de la EPOC e insuficiencia respiratoria crónica similar a la de nuestra muestra, han conseguido disminuir aproximadamente un 50% el número de ingresos en el grupo controlado en el domicilio. Por ello, el cálculo del número de pacientes a evaluar para valorar las consultas en urgencias y hospitalizaciones se realizó finalmente partiendo de los resultados previos del grupo investigador.
- Cálculo del valor de N para valorar el número de urgencias: aceptando un riesgo alfa de 0,05 y un riesgo beta de 0,10 en un contraste bilateral se precisan 86 sujetos para detectar una diferencia igual o superior a 0,44 consultas a urgencias. Se asume una desviación estándar de 1,25. Se ha estimado una tasa de pérdidas de seguimiento del 1%.
- Cálculo del valor de N para valorar el número de hospitalizaciones: aceptando un riesgo alfa de 0,05 y un riesgo beta de 0,10 en un contraste bilateral, se precisan 71 sujetos para detectar una diferencia igual o superior a 0,35 ingresos hospitalarios. Se asume una desviación estándar de 0,9. Se ha estimado una tasa de pérdidas de seguimiento del 1%.
Métodos
El reclutamiento de los pacientes se realizó entre los remitidos y admitidos en la CM que aceptaron voluntariamente participar en el estudio.
La intervención terapéutica consistió en la creación de una CM destinada a tratar de manera exclusiva a estos pacientes de acuerdo con el siguiente protocolo: a) en la primera visita se efectuaban la historia clínica completa, exploración física, espirometría forzada con prueba broncodilatadora (EF; se utilizaron como valores de referencia los de la población mediterránea)8, la gasometría arterial (GA), la determinación de carboxihemoglobina, la pulsioximetría nocturna, el test de calidad de vida mediante el Chronic Respiratory Disease Questionnaire, elaborado por Guyatt (CRQ)9, el electrocardiograma, la radiografía de tórax y la analítica general de sangre; b) en las visitas de seguimiento trimestrales se evaluaron el curso clínico, la EF, la GA, la determinación de carboxihemoglobina, y c) en la visita final se siguió el curso clínico y se realizaron la exploración física, la EF, la GA, la determinación de carboxihemoglobina y el CRQ.
Se evaluaron prospectivamente las siguientes variables clínicas: datos antropométricos, EF, GA, valores de carboxihemoglobina y calidad de vida. Se analizaron retrospectivamente (control histórico) y prospectivamente las siguientes variables: número de ingresos en urgencias, número de ingresos en planta y días de hospitalización.
Las variables económicas estudiadas fueron: coste medio de las visitas en urgencia, coste medio de hospitalizaciones para el SCS y la CPT, coste medio de las visitas en consultas externas, coste de ambulancias para el SCS durante el seguimiento en la CM, coste para la CPT de las EF durante el seguimiento, coste medio total por paciente para el SCS y la CPT, y coste agregado para el SCS y la CPT. Nuestro estudio evalúa costes directos, no costes indirectos o intangibles.
En cuanto a la financiación del proveedor del servicio (CPT), se realizó según el convenio de la CPT con el SCS. Entre las particularidades de facturación que afectan al proveedor cabe citar las siguientes: a) el coste de las EF y GA estaba incluido en el pago por visita o asistencia en planta, por lo que las EF se han contabilizado únicamente en el apartado de pérdidas del hospital, no como gastos del SCS; b) el coste por visitas de seguimiento se establecía de manera fija por paciente y año, por lo cual este flujo de dinero se contabilizó tanto en el cómputo del coste acumulado para el SCS como en ingresos de la CPT; c) el coste por ingreso se establecía de manera fija por paciente y mes, y d) el SCS abonó directamente al Consorci del Transport Sanitari de Catalunya los costes de ambulancia.
El coste agregado que la asistencia de estos pacientes generó a la CPT se calculó del siguiente modo:
Beneficio o pérdida por ingreso - coste de EF + pago de segundas visitas en consultas externas + precio de asistencia en urgencias.
El coste agregado para el SCS se calculó con la fórmula:
Coste asistencia en urgencias + coste de ingreso en planta + coste de segundas visitas en consultas externas + coste del traslado en ambulancias.
Análisis estadístico
El análisis estadístico se realizó con el programa SPSS para Windows, versión 10. Como criterio de significación estadística, se consideró significativo p < 0,05. Se llevó a cabo una explotación descriptiva de todos los datos mediante listados de frecuencias de las variables cualitativas y haciendo la descriptiva de las cuantitativas. Se utilizaron métodos no paramétricos para las distribuciones que no seguían una distribución normal. Se empleó la prueba de rangos de Wilcoxon bilateral para determinar si había diferencias entre los valores antes y después del control ambulatorio monográfico durante un año.
El comité de ética del hospital aprobó la realización del estudio.
Resultados
Pacientes
Se incluyó a los primeros 124 pacientes (105 varones y 19 mujeres) que terminaron el seguimiento de un año. Su edad media ± desviación estándar era de 69 ± 7 años y el índice de masa corporal de 26,8 ± 5,2 kg/m2. Se practicaron 543 EF, 721 GA y 709 determinaciones de carboxihemoglobina. La prevalencia de tabaquismo activo al inicio del control fue del 12,9% y un 26% de pacientes mostró poliglobulia.
Variables clínicas
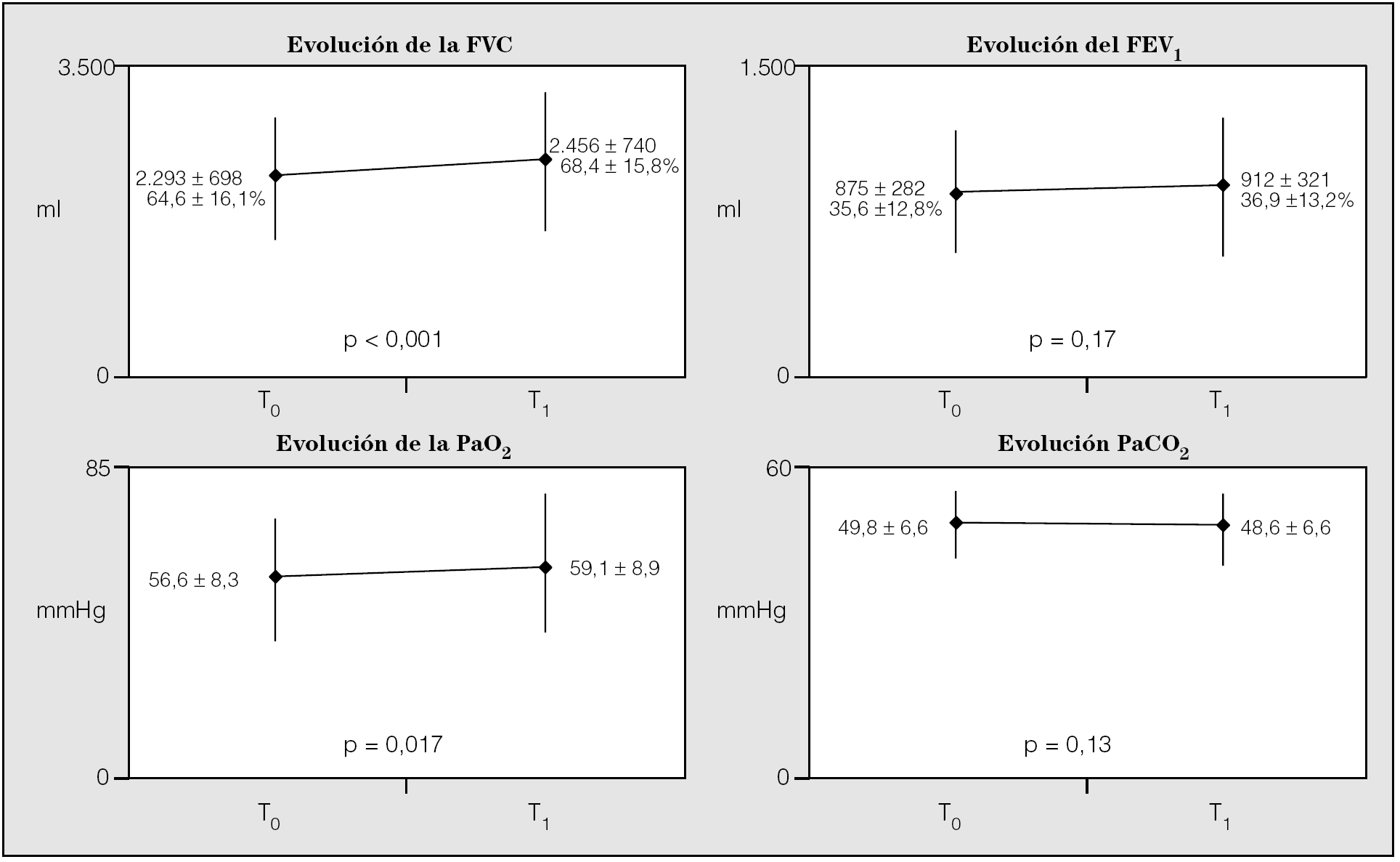
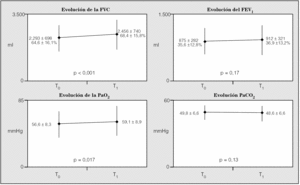
No hubo cambios significativos en los valores antropométricos. Al final del seguimiento mejoraron de manera significativa la capacidad vital forzada y la PaO2, mientras que el FEV1 y la presión arterial de anhídrido carbónico mejoraron de manera no significativa (fig. 1).
Fig. 1. Evolución de la función ventilatoria y gasometría arterial. FVC: capacidad vital forzada; FEV1: volumen espiratorio forzado en el primer segundo; PaO2: presión arterial de oxígeno; PaCO2: presión arterial de anhídrido carbónico; T0: control histórico; T1: seguimiento.
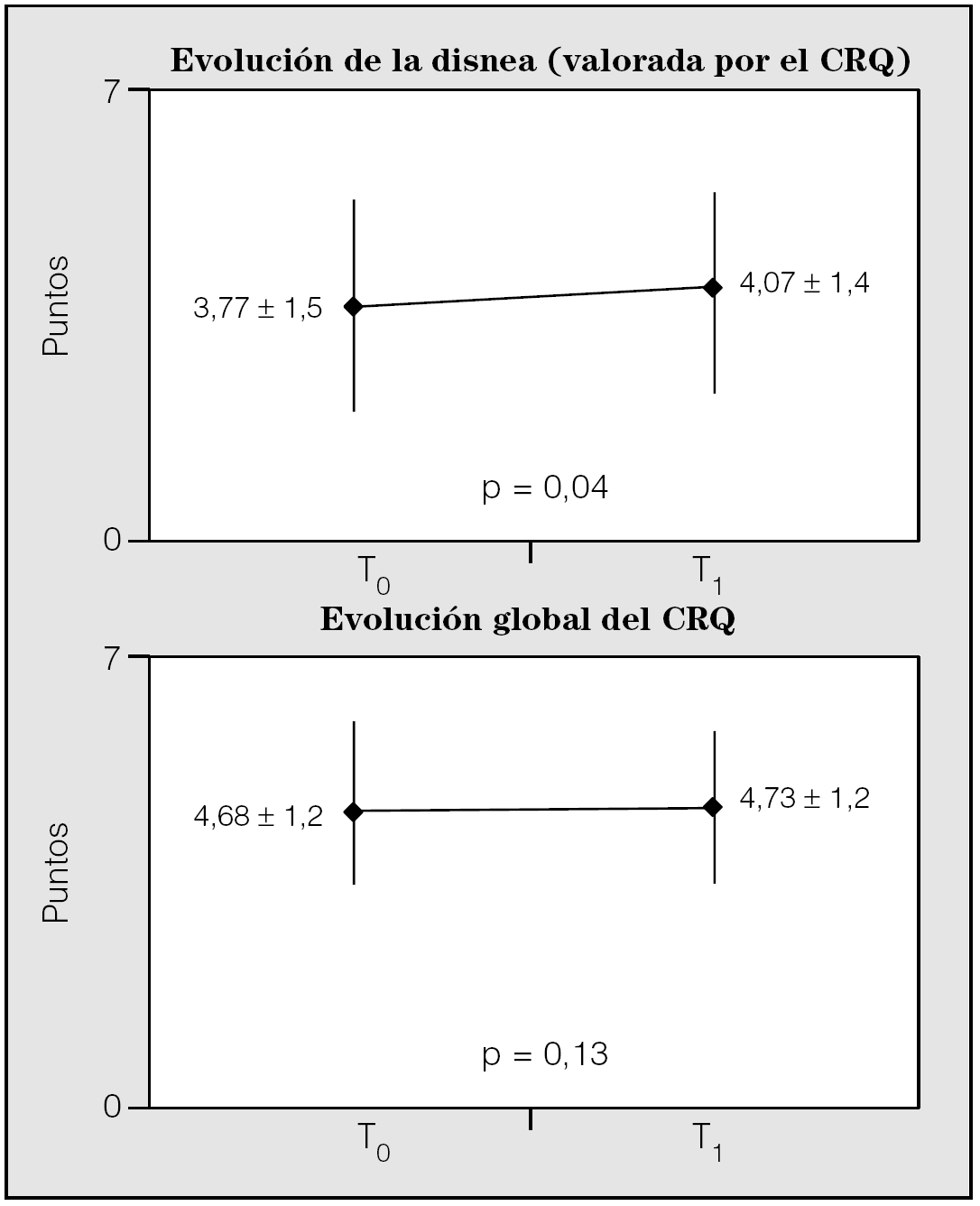
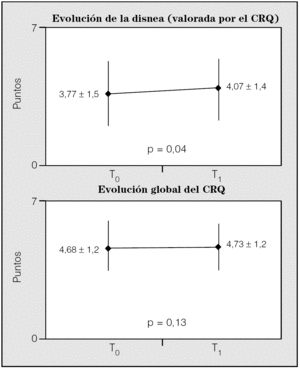
La calidad de vida, medida mediante el CRQ y evaluada en 44 pacientes al inicio y al final del estudio, mostró una mejoría no significativa de la puntuación total y sólo la dimensión disnea mejoró de manera significativa (fig. 2).
Fig. 2. Evolución de la calidad de vida global y de la dimensión disnea en el Chronic Respiratory Disease Questionnaire (CRQ). T0: control histórico; T1: seguimiento.
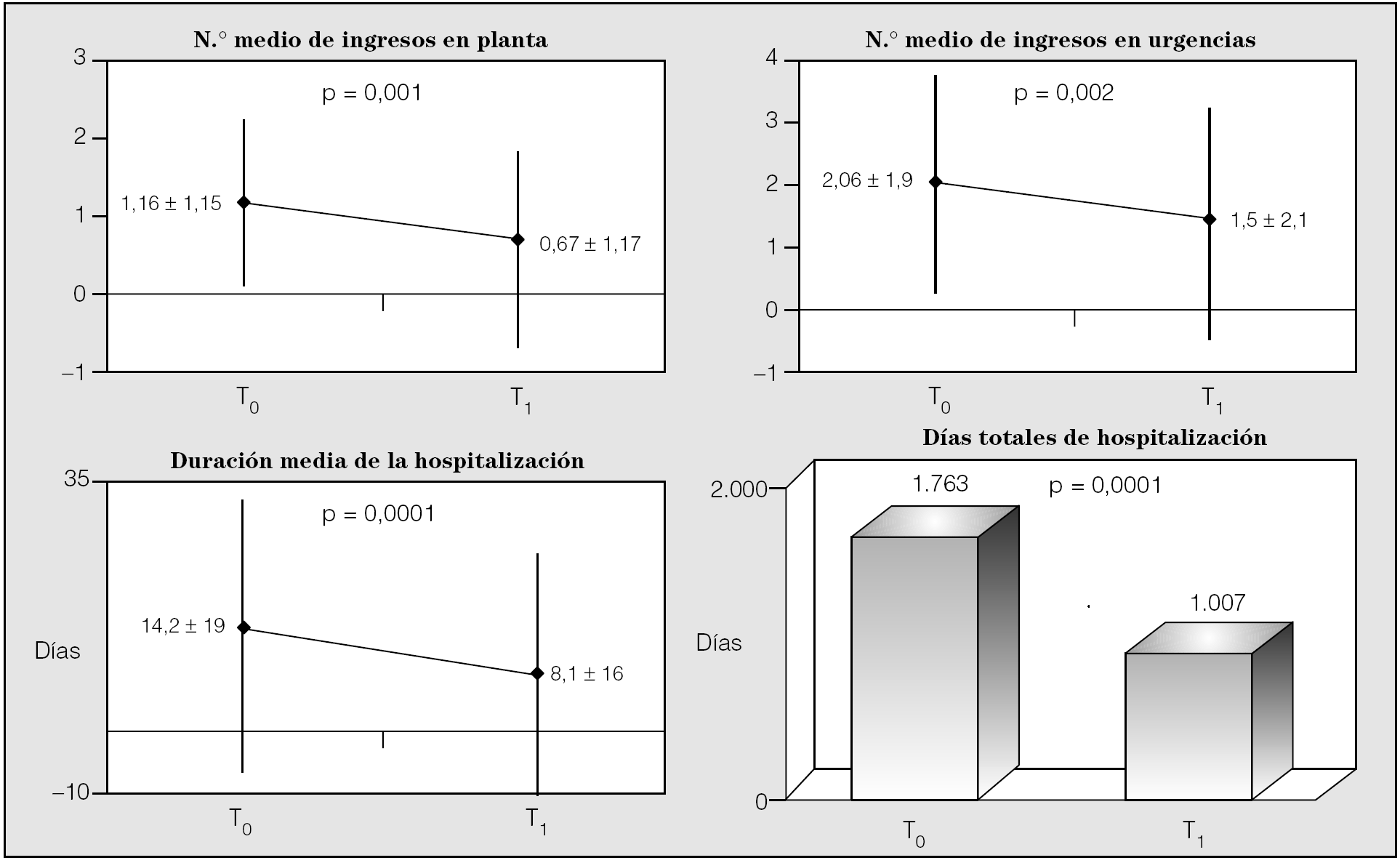
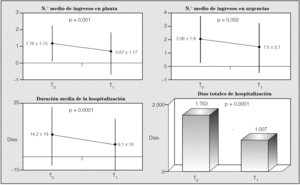
En la comparación del número de ingresos en urgencias, planta y días de hospitalización (fig. 3) se observó una disminución significativa de los 3 índices estudiados durante el período de seguimiento en la CM. Se produjeron 65 visitas menos en urgencias, 60 ingresos hospitalarios menos y se evitaron 756 días de hospitalización, el equivalente a tener 2 camas ocupadas durante todo el año. El análisis por subgrupos en función de la gravedad espirométrica y gasométrica mostró que los resultados seguían siendo favorables a la fase de seguimiento frente al control histórico (tablas I y II).
Fig. 3. Evolución del número de ingresos en planta, urgencias, duración media de hospitalización y días totales de hospitalización. T0: control histórico; T1: seguimiento.
Observamos, además, que 26 pacientes mejoraron y dejaron de cumplir los criterios gasométricos de insuficiencia respiratoria al final del período de seguimiento y 14 empeoraron. En el grupo que mejoró se observó una mejoría significativa de la función respiratoria, así como una disminución significativa tanto del número de asistencias en urgencias como del número de ingresos en planta. En el grupo que empeoró no se observaron cambios ni en la EF ni en el número de ingresos en planta y urgencias.
Variables económicas
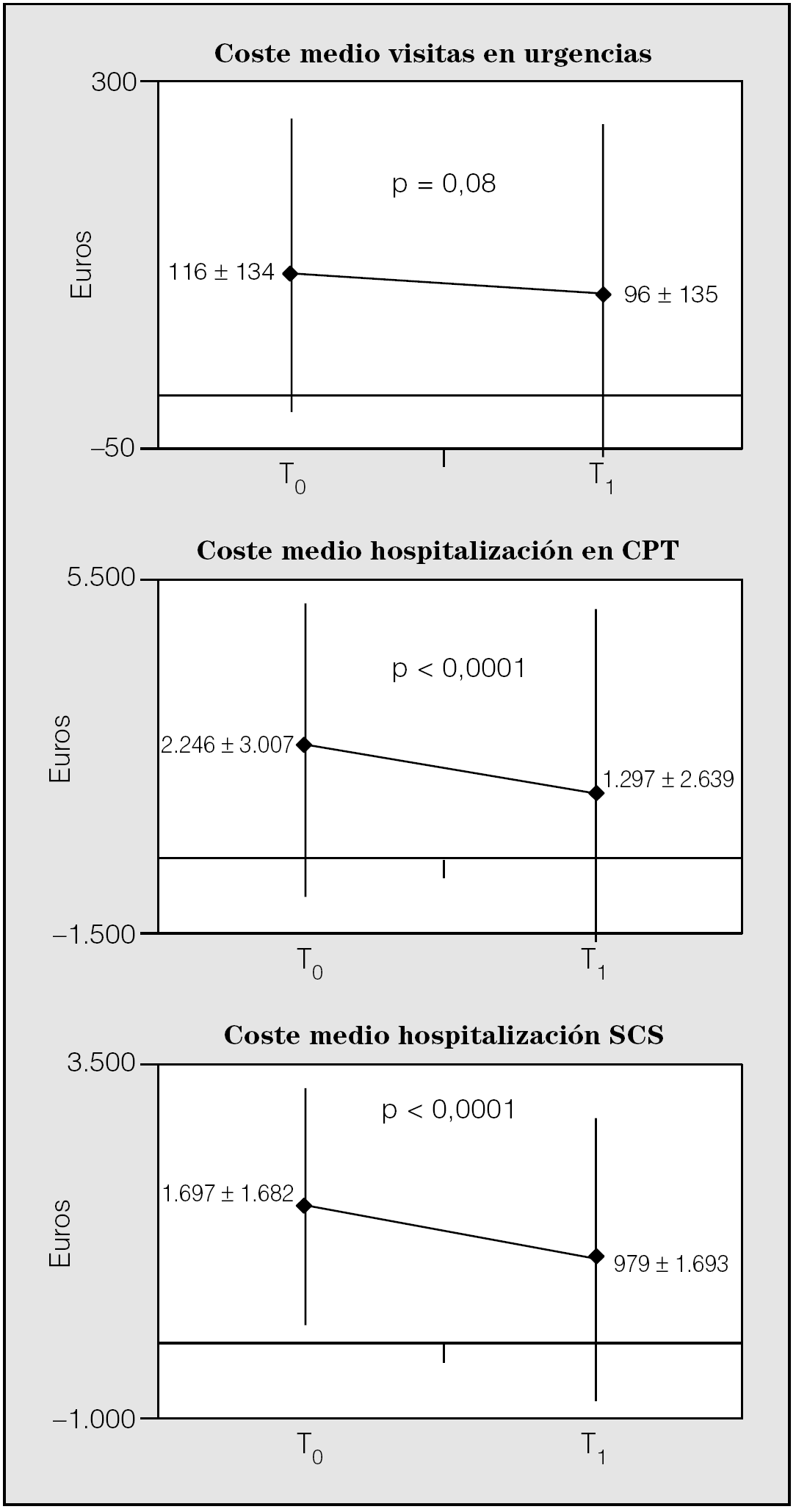
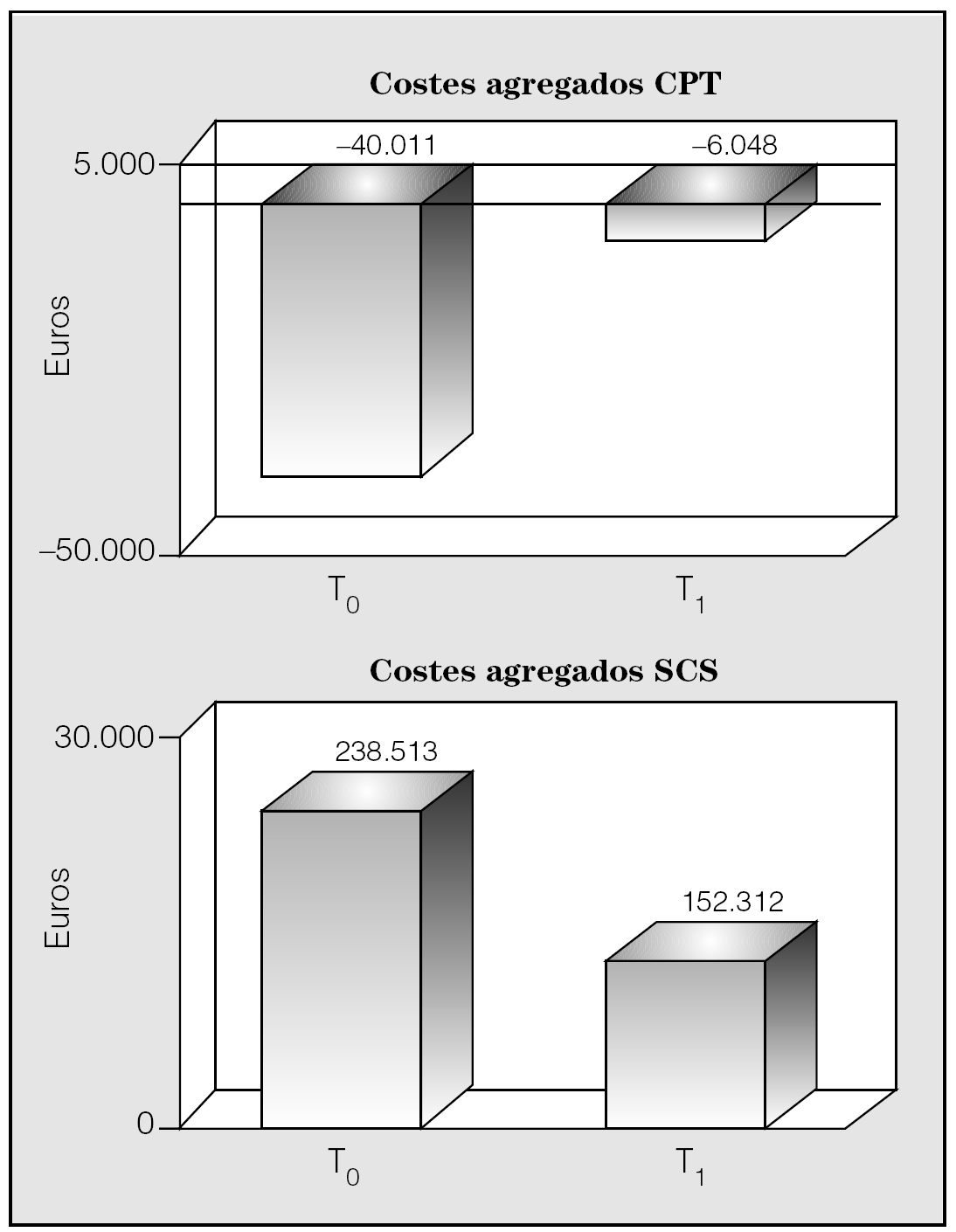
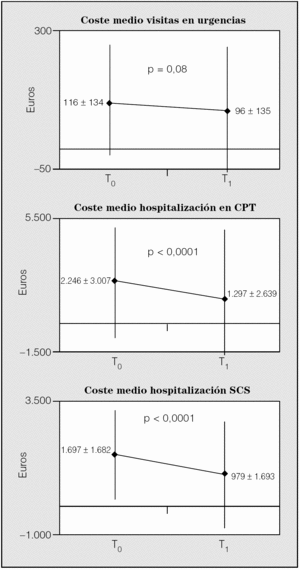
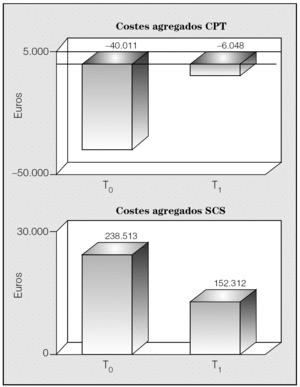
En la figura 4 se muestra el coste medio durante el control histórico y el seguimiento de las visitas en consultas externas, urgencias y costes de hospitalización para el SCS y la CPT. Obsérvese la mejoría estadísticamente significativa de todos los indicadores. La valoración de los costes agregados mostró que durante la fase de seguimiento se produjo un notable ahorro para el SCS; en el caso de la CPT, se consiguió prácticamente equilibrar el presupuesto (fig. 5). El coste medio total por paciente para el SCS y la CPT pasó de 1.923 ± 1.748 a 1.220 ± 1.794 € y de -322 ± 1.846 a -48 ± 1.439 €, respectivamente.
Fig. 4. Evolución de los costes medios de visitas en urgencias y costes medios de hospitalización para la Corporació Parc Taulí (CPT) y el Servei Català de la Salut (SCS). T0: control histórico; T1: seguimiento.
Fig. 5. Costes agregados para la Corporació Parc Taulí (CPT) y el Servei Català de la Salut (SCS). T0: datos del control histórico; T1: seguimiento.
Discusión
En la actualidad, el Estado español destina cerca del 9% del producto interior bruto a gasto sanitario (cantidad superior a los 24.040.484.175,35 €)10. De este montante total, el médico, en el ámbito de la microgestión sanitaria o gestión clínica, asigna el 70% de los recursos sanitarios a sus decisiones terapéuticas11,12. Por tanto, para mejorar la asignación de recursos sanitarios es preceptivo reducir las diferencias entre eficacia y efectividad, atacando los factores vulnerables de las diferentes enfermedades.
Cumpliendo los consejos del informe Dawson, el diseño del trabajo parte de estudios epidemiológicos previos llevados a cabo en el área de referencia del hospital desde 1990 hasta 1995. La originalidad del diseño radica en 2 aspectos distintos pero complementarios: a) el diseño de un nuevo modelo asistencial introduciendo barreras de acceso al sistema concebidas a partir de la racionalidad, y b) la evaluación clínica y económica (efectividad y eficiencia) de las mejoras que ofrece el sistema. Por tanto, se ha procedido a la implementación de un nuevo modelo asistencial a partir de los datos obtenidos con el método de la medicina basada en la evidencia y a la evaluación, en condiciones reales (no ideales), de la respuesta clínica de la población de pacientes tratados y del comportamiento económico del modelo.
La efectividad se puso de manifiesto en todos los indicadores estudiados. Se produjo una mejoría del FEV1 que, si bien no fue estadísticamente significativa, sí resulta relevante desde el punto de vista clínico, y se constató una mejoría significativa en el valor de la capacidad vital forzada, que indica una disminución del volumen residual o, lo que es lo mismo, una disminución del atrapamiento aéreo de estos pacientes. El valor medio de la PaO2 diurna mejoró de manera estadísticamente significativa y la retención de anhídrido carbónico disminuyó ligeramente. Además, es importante destacar que al final del año de seguimiento 26 pacientes mejoraron lo suficiente para dejar de estar en insuficiencia respiratoria. La evolución a la baja de la carboxihemoglobina indica que la mejoría de la oxigenación se mantuvo también durante la noche.
La prevalencia de tabaquismo al inicio y al final del seguimiento fue del 12,9 y el 10,5%, respectivamente. Por tanto, la CM no consiguió modificar de manera sustancial el hábito tabáquico. Debe señalarse que la única intervención para disminuirlo fue el consejo médico, repetido en cada consulta, y que no se diseñó (ni por tanto se pretende evaluar) ninguna variable en este sentido.
En lo que a demanda asistencial se refiere, hubo un descenso significativo del número de consultas a urgencias, ingresos en planta y número de días de hospitalización. La disminución de este último parámetro puede deberse a 2 motivos distintos: por un lado, a que los pacientes no ingresaran en situación clínica alarmante y, por otro, al hecho de disponer de una consulta que permitía el drenaje rápido y ágil de los pacientes ingresados. No hemos evaluado este punto, pero en ambos casos el resultado beneficioso sería debido a la puesta en práctica del nuevo modelo asistencial. Es muy llamativo también que se consiguiera ahorrar 756 días de ingreso hospitalario, lo cual significa aumentar aproximadamente un 10% la capacidad de la planta de hospitalización del Servicio de Neumología, que dispone de 22 camas, sin incremento de recursos económicos. Debemos señalar además que para esta evaluación consideramos que el número de urgencias en asistencia primaria en el control histórico fue de cero, con lo que voluntariamente infravaloramos las demandas asistenciales de estos pacientes durante el control histórico con el fin de ser lo más estrictos posible en la comparación de datos.
Uno de cada 3 ciudadanos consulta una vez al año un servicio de urgencias13 y el 80% de estas consultas son debidas a decisión propia de los pacientes14. Entre todas las consultas a estos servicios, las enfermedades respiratorias representan en algunos casos hasta el 34% de los diagnósticos al alta15. Un problema sobreañadido es el de los reingresos en urgencias, cuya cifra oscila entre el 3,416 y el 9,36%15. Para solventarlo se crearon las áreas de observación de pacientes adscritas a los servicios de urgencias. Precisamente son los pacientes neumológicos los que presentan una mayor tasa de utilización de estas unidades, que en algunos casos llega a ser del 11%17. Por tanto, con nuestra intervención contribuimos a disminuir las consultas a urgencias y las estancias en las salas de observación de estos servicios. Además, dado que en la mayoría de los casos los pacientes consultan a estos servicios por voluntad y decisión propias, el cambio de actitud de la población estudiada, consistente en reducir las consultas a urgencias y sustituirlas por el control en la CM, evidencia un cambio cualitativo de la demanda asistencial, que obedece al menos en parte a la mejoría clínica experimentada y a la satisfacción con el modelo implementado.
En la bibliografía no existen datos referentes a este tipo de modelo asistencial que permitan comparar de manera fidedigna el implementado en nuestro hospital. Farrero et al7 han publicado un estudio en el que comparan 2 grupos de pacientes con EPOC seguidos de manera prospectiva. Las características de éstos son similares a las de nuestra población y el número de ingresos evitados también. Debe plantearse, sin embargo, si es más útil crear programas de atención domiciliaria nuevos con sede hospitalaria o modelos con sede hospitalaria que colaboren con la red de asistencia primaria ya existente. En la bibliografía anglosajona18 se ha publicado un estudio que incide en el tratamiento domiciliario de descompensaciones de los pacientes con EPOC. Si bien se trata de un estudio algo diferente del nuestro, debemos señalar que la atención que nosotros ofrecimos implica que un porcentaje elevado de estas descompensaciones se trataron ambulatoriamente a domicilio y que nuestros pacientes presentaban un grado de EPOC e insuficiencia respiratoria crónica más grave, por lo que creemos que la duda sobre cómo atender a estos pacientes debe plantearse en casos con enfermedad más grave que los estudiados por Gravil et al18.
En cuanto a la calidad de vida, es preciso resaltar que no realizamos ninguna intervención para modificarla en nuestros pacientes, a excepción del cambio de modelo asistencial y los beneficios que de éste se derivan, como es la disminución de las consultas a urgencias, aspecto que sí se relaciona con la calidad de vida de estos pacientes19. Tan sólo la dimensión disnea mejoró estadísticamente, lo cual se corresponde con la mejoría de la función respiratoria observada20. De todos modos, la adherencia de los pacientes al nuevo modelo asistencial traduce sin duda un cierto grado de satisfacción. En otras palabras, podríamos decir que la actitud de los pacientes ilustra la conversión de un bien de confianza, como suele ser la consulta a un médico especialista, en un bien de experiencia. En términos de mercado competitivo, las premisas de que el individuo es racional, que revela sus preferencias con sus acciones y que es el mejor juez de su bienestar también apoyarían un supuesto beneficio en la calidad de vida de este grupo de pacientes derivados del control hospitalario especializado.
A fin de valorar adecuadamente la eficiencia de la CM de EPOC debemos tener en cuenta que, para minimizar la crítica metodológica que todo estudio con control histórico suscita, no hemos contabilizado en el control histórico los gastos en asistencia primaria derivados de visitas por el médico de cabecera, la atención urgente en asistencia primaria o domiciliarias y las EF solicitadas por médicos de cabecera. Estos gastos deberían haberse cargado como costes para el SCS. Una visión panorámica muestra que la mejoría de la efectividad se acompaña de una mejoría de la eficiencia. Se contribuyó a disminuir el déficit que estos pacientes generan a la CPT y el ahorro para el SCS fue notable. Además, se "liberaron" 2 camas de hospitalización a lo largo de todo el año. Este punto puede valorarse de distintos modos: se puede considerar que con los mismos recursos es posible aumentar el nivel asistencial del hospital, o bien cabe pensar, si contabilizamos únicamente el concepto de ahorro, que el déficit hospitalario que existía se ha convertido en beneficio para la CPT, o que el beneficio para el SCS es mucho mayor que el supuesto en primer lugar.
En general, se acepta hoy día que muchas decisiones clínicas son fruto de hábitos o rutinas organizativas. Por tanto, cuanto más acotado esté el terreno de actuación, menor sea la disgregación de profesionales que atienden ciertas enfermedades y mejor se cumplan las normativas internacionales, menor será la variabilidad de actuación. Por otro lado, cuanto más se desplazan hacia abajo las decisiones clínicas, con mayor rapidez responde la organización, lo que en términos médicos suele significar mayor efectividad. Es evidente que estos puntos fomentan que las decisiones se tomen con mayor información y que los niveles superiores de decisión sufran una menor sobrecarga administrativa. La alta especificidad de la información clínica e investigadora es de transmisión costosa y aconseja que las decisiones se tomen allá donde se posea mayor información. Es evidente que todos estos requisitos los cumple una CM controlada por un solo médico especializado en la enfermedad susceptible de ser atendida.
Un problema sin duda importante en medicina es la variabilidad de la práctica médica, que se define como las variaciones sistemáticas (es decir, no aleatorias) en las tasas estandarizadas para determinados tratamientos (o procedimientos diagnósticos) a un determinado nivel de agregación de la población21. Para McPherson (creador de la definición de variabila médica), desde el punto de vista epidemiológico pueden identificarse 3 causas de variaciones sistemáticas: incertidumbre en casos de investigación insuficiente; ignorancia clínica por insuficiente divulgación de la investigación, o que se trate de la manifestación de preferencias informadas. En el caso de la CM no se cumple ninguno de estos 3 puntos, puesto que permite realizar investigación (en caso de que fuera insuficiente), disminuye la probabilidad de ignorancia clínica del facultativo que trabaja de manera continuada en un tema y evita la manifestación de preferencias fácilmente rebatibles por los resultados de la medicina basada en la evidencia.
La diferencia entre eficacia y efectividad radica en que en el primer caso las condiciones de evaluación de la práctica médica son las ideales y en el segundo son las reales. Se entiende por calidad la diferencia entre eficacia y efectividad. Esta última disminuye a medida que aumenta la extensión del uso de un servicio o dispositivo. En nuestra CM hemos mejorado los resultados respecto al control histórico, por lo que hemos mejorado la calidad de nuestra asistencia médica. Por otro lado, segmentamos claramente la población a tratar, lo que ha contribuido a limitar la pérdida de efectividad de la CM.
¿Cómo encaja en la bibliografía nuestro estudio? Algunos trabajos6,19 concluyen que es posible tratar precozmente en el domicilio mediante soporte sanitario variable a los pacientes con EPOC afectados de una descompensación. Postma22 se pregunta qué pacientes con EPOC descompensada son candidatos a beneficiarse de un modelo asistencial basado en la atención domiciliaria precoz y recalca que, para tomar decisiones apropiadas, es imprescindible disponer de información fidedigna sobre su situación basal. Además esta información, para que el modelo sea relevante desde un punto de vista epidemiológico, debe estar disponible también para los médicos de asistencia primaria, que con frecuencia son los primeros en decidir la actitud a seguir23. Nosotros hemos tratado a una población de pacientes con EPOC más grave que la incluida en la mayoría de estudios, por lo que hemos avanzado sobre el tipo de pacientes que pueden beneficiarse de este modelo asistencial.
En cuanto a la evaluación global de la eficiencia de la CM de EPOC, debemos empezar por realzar la importancia de incluir, junto a la evaluación clínica, una evaluación económica. Hace casi 30 años Cochrane24 afirmaba que, si la eficacia se había investigado más bien poco, la eficiencia apenas se había estudiado25,26. Señalaba a continuación que, desde el punto de vista terapéutico, había 3 tipos de ineficiencia: a) el empleo de tratamientos ineficaces y el uso de tratamientos eficaces cuando no deben utilizarse; b) un lugar incorrecto de tratamiento, es decir, la inadecuación del entorno en el que se decide tratar a un paciente, y c) la duración incorrecta de la estancia hospitalaria. Una CM como la nuestra, que intenta seguir las normativas internacionales (cuyo seguimiento suele ser bajo27), incide claramente sobre el primer punto. Además, podemos adecuar mejor la prescripción farmacológica y por tanto racionalizar el gasto farmacéutico28. Por otro lado, podemos decidir cómo, dónde y cuándo tratar una descompensación, con lo cual el segundo punto también es claramente vulnerable. La influencia sobre el tercero es menos evidente, pues la CM no permite condicionar directamente la estancia hospitalaria de manera individual, pero sí controlar el número de candidatos a ingresar y, por consiguiente, influir en los resultados agregados del número de días de ingreso, con lo cual contribuye a reducir uno de los componentes que más encarecen la asistencia de estos pacientes26,29.
En resumen, podemos concluir que de la evaluación de los resultados se desprende que el modelo diseñado cumple con las directrices recomendadas30 y se comporta como un modelo "paretiano", pues frena el deterioro de la calidad de vida de estos pacientes, mejora significativamente las variables clínicas estudiadas y disminuye los costes económicos, tanto para el financiador (SCS) como para el proveedor del servicio (hospital).
Agradecimientos
Los autores desean agradecer a Àngels Junoy (Dirección de Planificación de la CPT), Manuela García (responsable de la Unidad de Contratación y Facturación de la CPT) y a Engràcia Mestre (Unidad de Programación de la CPT) su amabilidad al facilitarnos los datos económicos utilizados, y a María José López (secretaria de Docencia de la CPT) su inestimable y desinteresada colaboración en la presentación del manuscrito.
Correspondencia: Dr. Ch. Domingo.
Servicio de Neumología. Corporació Parc Taulí.
Parc Taulí, s/n. 08208 Sabadell. Barcelona. España.
Correo elecrónico: cdomingo@cspt.es
Recibido: 3-3-2005; aceptado para su publicación: 24-5-2005.