Introducción
La EPOC se define, en términos fisiológicos, como un proceso en el que existe limitación al flujo aéreo secundario a enfermedad del parénquima pulmonar o de las vías aéreas, relativamente estable en el tiempo y no reversible, o sólo parcialmente reversible al administrar broncodilatadores1,2. La reducción del flujo aéreo progresa inexorablemente con el tiempo. El instrumento para el diagnóstico de la EPOC es la espirometría, que cuantifica el alcance de la obstrucción y permite evaluar su grado de reversibilidad. Es, además, un instrumento que permite de forma económica detectar la presencia de EPOC antes de que los pacientes presenten síntomas. Sin embargo, pocos médicos en medicina primaria usan espirómetros, ni siquiera en fumadores mayores de 45 años, para los que se viene recomendando su uso3. Ésta es una de las principales razones por las que la EPOC es una enfermedad infradiagnosticada.
El grupo de fármacos más utilizados en el tratamiento farmacológico de la EPOC son los broncodilatadores. El tipo de broncodilatadores usados en los EPOC son los mismos que en el asma; sin embargo, sus efectos no son similares, ya que en la EPOC producen un grado de broncodilatación mucho menor, e incluso en muchos pacientes el cambio observado en la espirometría tras su administración es insignificante. Dado que estos fármacos mejoran claramente la sintomatología de los pacientes, es posible que otro mecanismo diferente del de la broncorrelajación, como la reducción en el grado de hiperinsuflación pulmonar, sea el mecanismo que explique su beneficio. En este breve artículo se revisan los conceptos clásicos sobre los mecanismos de la acción de los broncodilatadores y la evidencia actual sobre su efecto sintomático en otros ámbitos; finalmente, se propone un modelo de evaluación de estos fármacos en pacientes con EPOC.
Obstrucción al flujo aéreo y respuesta broncodilatadora
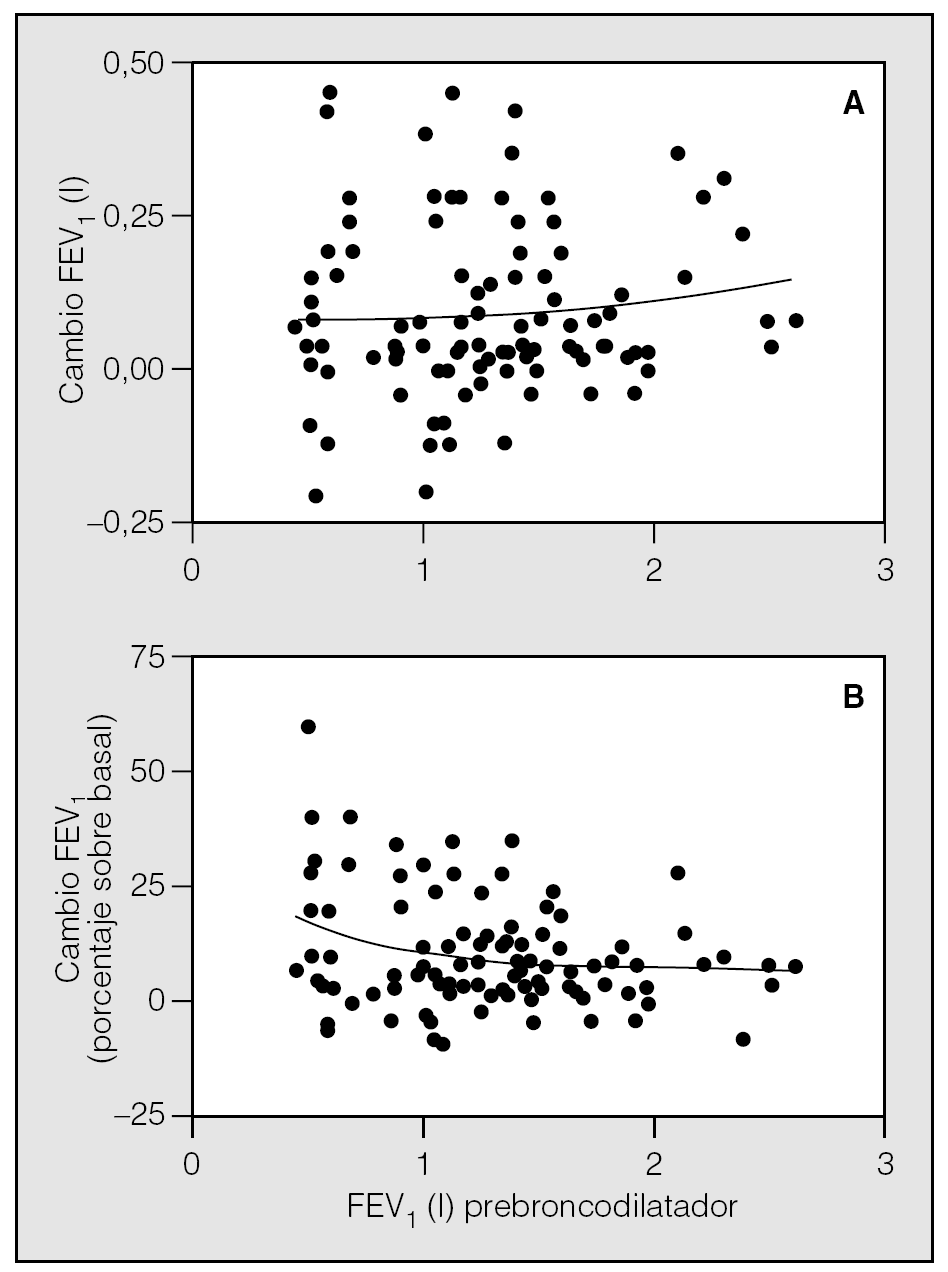
Cuando se realizan espirometrías seriadas, en personas sanas el grado de variabilidad día-día del volumen espiratorio forzado en el primer segundo (FEV1) y de la capacidad vital forzada (FVC) es del 13 y el 11%, respectivamente4. Por esto, la American Thoracic Society ha establecido como criterio de respuesta broncodilatadora (RBD) positiva un incremento del 12% del FEV1 posbroncodilatación respecto al valor basal; además, se exige que un valor absoluto de volumen de aire exhalado en la FVC sea superior a 200 ml1. La Sociedad Europea de Neumología define una RBD positiva cuando se produce un incremento > 9% del FEV1 predicho. Estos criterios son posiblemente muy restrictivos; además, debe considerarse la existencia de una gran variabilidad en la respuesta a broncodilatadores en pacientes con EPOC, ya que en éstos la distribución del cambio del FEV1, expresado como porcentaje del valor predicho tras agonistas β2, tiene un comportamiento gausiano, con una media del 4-5% y un rango máximo del 6 al 12%, con un 80% de pacientes entre el 2 y el 8%. Esta distribución es incluso más normal cuando se presentan los datos en forma de cambio del FEV1 en valor absoluto, en litros, o en cambio porcentual sobre los valores basales (fig. 1). Cuando se evalúa la función pulmonar con semanas o meses de intervalo, las variaciones anteriormente descritas son hasta del 20% en lo referente al FEV14, posiblemente por los cambios del tono broncomotor de las vías aéreas a lo largo del tiempo. Este aspecto es importante, ya que tradicionalmente se considera, por ejemplo, una respuesta positiva al ensayo de acción de los corticoides cuando éstos inducen un incremento del FEV1 del 12% en un ensayo de 2-4 semanas. Posiblemente se debería ser más estricto y exigir, al menos, un incremento del 20%, teniendo en cuenta, por otra parte, los efectos colaterales de los esteroides sistémicos.
Fig. 1. Relación entre el valor basal del FEV1 en valor absoluto (litros) y el cambio posbroncodilatador en valor absoluto (A) y en porcentaje sobre el valor basal (B) en pacientes con EPOC. Obsérvese la amplia variabilidad de la respuesta en valor absoluto y un mayor cambio porcentual a medida que el valor basal pre-BD se reduce. Datos propios de nuestro laboratorio.
Tradicionalmente se ha considerado que la EPOC es una enfermedad obstructiva "irreversible" y alrededor de esta idea se ha estigmatizado esta entidad clínica de "intratable" e "incurable". La abundante información disponible debería evitar esta situación. Anthonisen et al, hace casi 20 años, comunicó que al menos un 30% de los pacientes presenta una RBD positiva cuando se le realiza una espirometría por primera vez en su vida y un 68% con RBD negativa inicialmente presentará al menos una RBD positiva en espirometrías seriadas realizadas en meses subsiguientes5. La administración de anticolinérgicos y agonistas β2 mejora el grado de disnea y la calidad de vida, y reduce el número de exacerbaciones en pacientes con EPOC, todo ello sin modificar sustancialmente el FEV16-8. Por último, una respuesta positiva o negativa a broncodilatadores, definida por criterios de la American Thoracic Society, no se relaciona bien con la mejoría en la disnea o en la capacidad de ejercicio inducida por estos fármacos9. Por tanto, la presencia o ausencia de una RBD positiva inicial no describe el fenotipo de pacientes (respondedores frente a no respondedores a los broncodilatadores) y no debe entenderse como criterio para administrar o no estos fármacos.
Capacidad inspiratoria para determinar broncodilatación
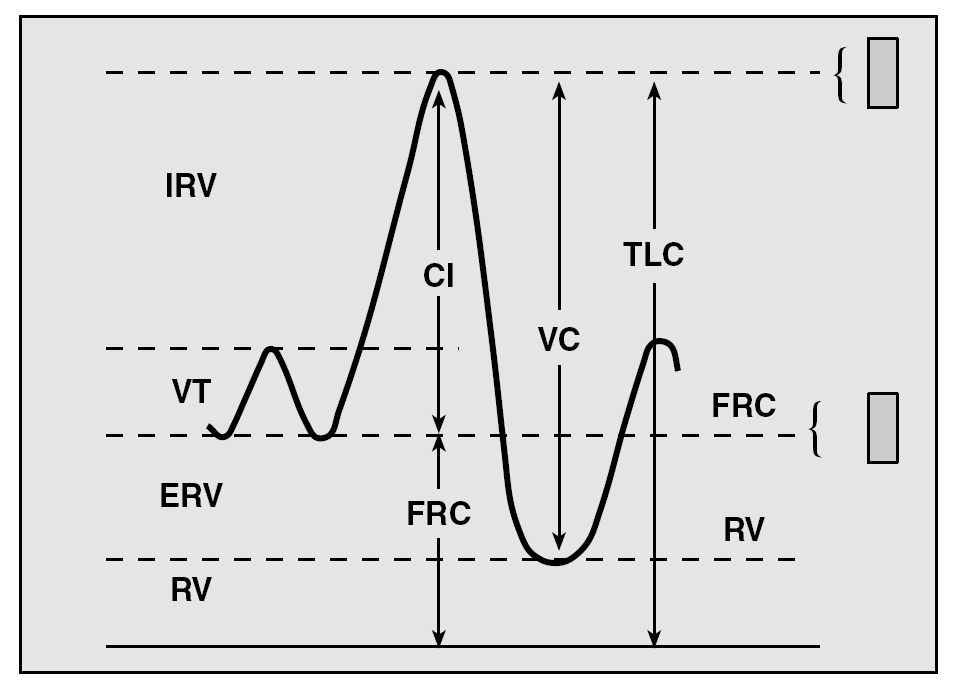
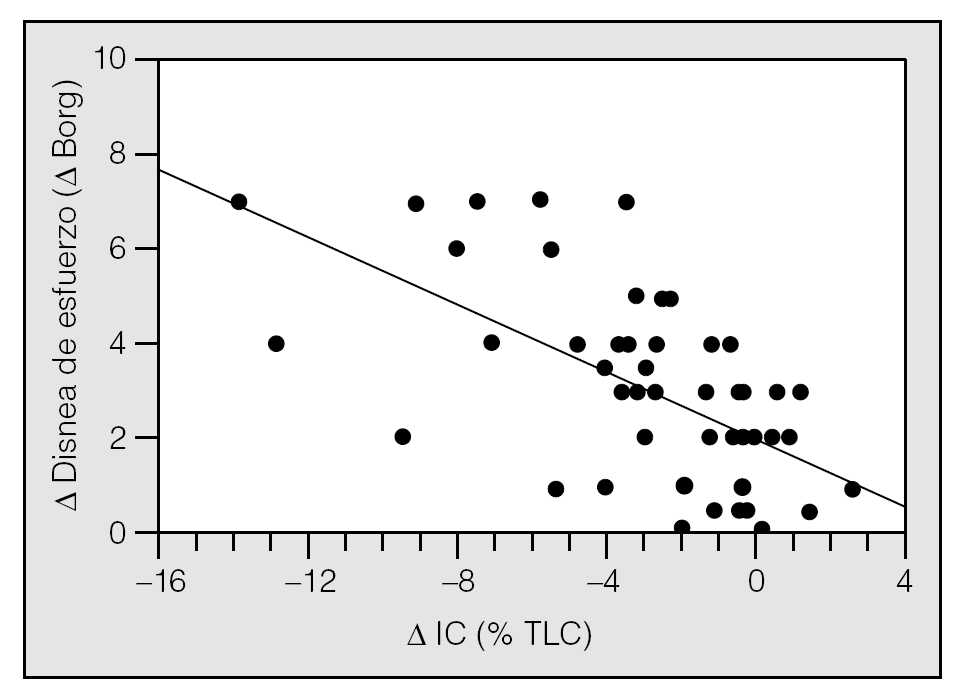
La capacidad inspiratoria (CI) es la cantidad de aire que puede tomarse en una inspiración máxima desde la posición de reposo (capacidad funcional residual [FRC]) hasta la máxima insuflación pulmonar (capacidad pulmonar total [TLC]) (fig. 2). La FRC es la cantidad de aire que hay en el tórax después de una espiración normal; este volumen de aire suele ser del 30 al 40% de la TLC en una persona sana. En pacientes con EPOC, esta relación aumenta paralelamente al grado de hiperinsuflación pulmonar. La CI es en realidad el valor inverso de la FRC y, además, puede obtenerse fácilmente durante la maniobra de espirometría. Por tanto, si se dispone de un espirómetro se puede evaluar el grado de hiperinsuflación pulmonar de los pacientes con EPOC. En los últimos años se ha demostrado que durante el ejercicio los pacientes con EPOC desarrollan una mayor hiperinsuflación pulmonar que la que ya tienen durante el reposo (hiperinsuflación dinámica [HD]). Esta HD ha demostrado ser un factor determinante en la patogenia de la disnea de esfuerzo, síntoma princeps de la EPOC10. Nuestro propio grupo ha demostrado que durante un ejercicio submáximo (como caminar) la capacidad inspiratoria se reduce y se asocia de forma paralela al grado de disnea que el paciente percibe durante el esfuerzo11 (fig. 3). Estudios experimentales han demostrado que muchos pacientes con EPOC muestran un alivio de la disnea inducida por el esfuerzo sin mejorar los flujos aéreos, mejoría sintomática que era paralela al aumento de la capacidad inspiratoria inducida por el fármaco12. Un mecanismo similar (reducción de la hiperinsuflación dinámica) parece explicar la mejoría de la disnea tras la cirugía de reducción de volumen pulmonar.
Fig. 2. Espirograma normal con los diferentes componentes de volúmenes y capacidades estáticos y dinámicos. CI: capacidad inspiratoria; TLC: capacidad pulmonar total; VC: capacidad vital; FRC: capacidad funcional residual; RV: volumen residual; ERV: volumen de reserva expiratoria; VT: volumen corriente o tidal.
Fig. 3. Relación entre el cambio de capacidad inspiratoria (DIC) en porcentaje de la capacidad pulmonar total (%TLC) y el grado de disnea provocado durante la prueba de marcha de 6 minutos en pacientes con EPOC. Tomado de Marín JM et al11.
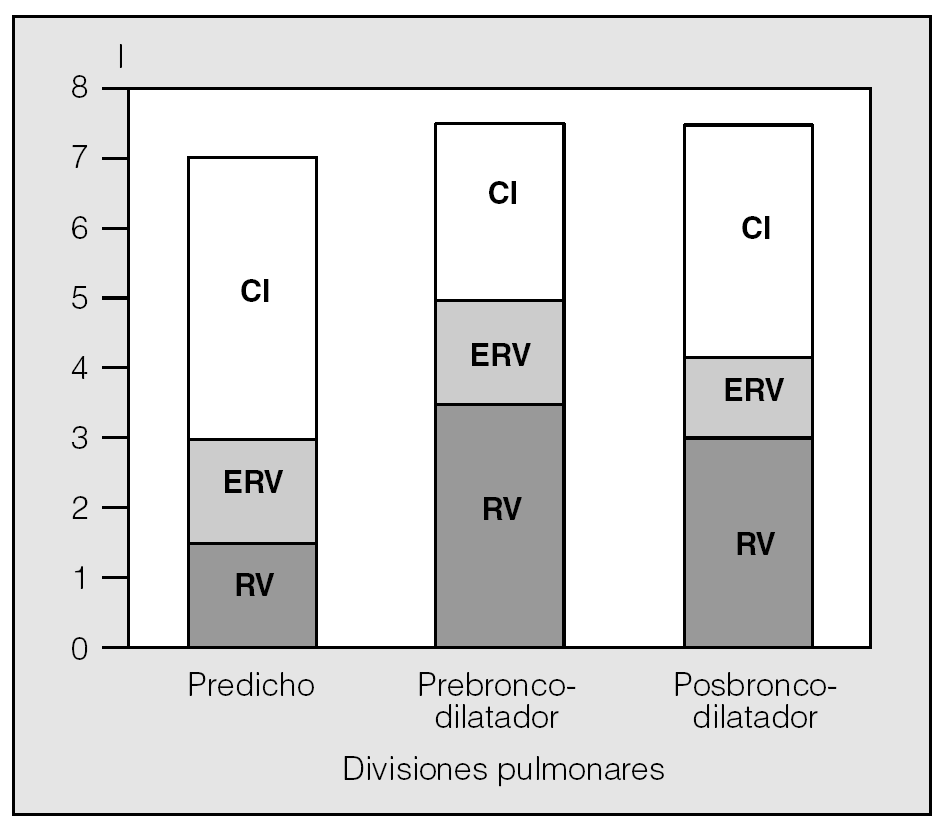
La CI, medida durante la maniobra de capacidad vital lenta en un espirómetro convencional, ha demostrado ser una maniobra sencilla de obtener y muy reproducible. Recientemente, O'Donnell et al, al administrar un broncodilatador anticolinérgico (bromuro de ipratropio) a pacientes con EPOC, comprobaron cómo la disnea de esfuerzo y la capacidad de trabajo mejoraban de forma paralela al incremento inducido sobre la CI, pese a que el efecto del fármaco sobre el FEV1 era muy modesto13. Es decir, el incremento del volumen aéreo "operativo" que implica la mejoría de la CI permite al paciente respirar de una forma eficiente (respiraciones más profundas y lentas) y aumentar su capacidad ventilatoria cara al esfuerzo. En el estudio señalado, con un incremento de la CI de tan sólo el 14% tras administrar bromuro de ipratropio, se obtuvo una mejora del 32% en la capacidad de ejercicio. El salbutamol inhalado también ha demostrado reducir el grado de hiperinsuflación en relación directa con el incremento producido en la capacidad inspiratoria14. Nuestro grupo ha confirmado, mediante la medición de volúmenes estáticos por pletismografía, la mejoría de la CI y la reducción paralela de la FRC tras la administración de bromuro de ipratropio (fig. 4). El incremento de la CI tras la administración de broncodilatadores ha demostrado relacionarse de forma directa con la mejoría que éstos producen sobre la disnea de esfuerzo y la tolerancia al esfuerzo en pacientes con EPOC11,13,15. En una amplia población de pacientes con EPOC en diversos grados de limitación al flujo aéreo, Newton et al encontraron que el incremento de la CI, tras la administración de salbutamol, era tanto mayor cuanto más elevado era el grado de hiperinsuflación pulmonar16. Finalmente, se ha comparado el efecto de cuatro broncodilatadores (salbutamol, formoterol, salmeterol y oxitropio) sobre los parámetros espirométricos, la CI y la disnea en pacientes con EPOC17, y se ha encontrado que el mayor efecto sobre la CI se produce en pacientes con CI basal más reducida, incremento que se relaciona con la mejoría de la disnea; todo ello pese a un incremento del FEV1 inferior al 20% en todos los casos. El pico de incremento de la CI para los cuatro fármacos estudiados ocurrió tras 30 min de administración.
Fig. 4. Cambio del valor medio de volúmenes estáticos tras la administración de bromuro de ipratropio en un grupo de 12 pacientes con EPOC. Obsérvese la reducción del volumen residual (RV) y el aumento paralelo de la capacidad inspiratoria (CI) sin modificación de la capacidad pulmonar total; ERV: volumen de reserva expiratoria.
Los estudios anteriormente reseñados demuestran claramente que la RBD, valorada mediante el FEV1, no evalúa de forma adecuada la respuesta sobre los volúmenes pulmonares, que puede ser mucho más relevante para el paciente sintomático. Es probable, por tanto, que la CI sea un parámetro de función pulmonar cada vez más utilizado en el tratamiento del paciente con EPOC, dada la sencillez de su obtención y su sensibilidad para detectar mejoría clínica tras la administración de broncodilatadores.
Implicaciones de la respuesta broncodilatadora
La espirometría con RBD se ha venido utilizando como ayuda en el diagnóstico diferencial entre asma y EPOC, y algunas guías de tratamiento basan su estrategia de tratamiento2,18 en los resultados del FEV1 y en la RBD. Cuando se realiza este tipo de pruebas pueden establecerse y recordarse algunas conclusiones importantes:
1. Como ya se ha señalado anteriormente, los criterios actuales para definir como "no reversible" o "reversible" una prueba broncodilatadora no son relevantes clínicamente, y probablemente reflejen las limitaciones del FEV1 como parámetro categorizador de la gravedad de la enfermedad19.
2. La prueba broncodilatadora realizada en una sola ocasión, tanto si es negativa como si es positiva, no implica que en ese paciente en visitas sucesivas esta respuesta vaya a comportarse de la misma forma.
3. Una respuesta negativa a un broncodilatador inhalado de acción rápida (p. ej., salbutamol u oxitropio) puede convertirse en positiva al administrar el otro broncodilatador.
4. El FEV1 posbroncodilatador, y no el prebroncodilatador, debe ser el parámetro que se deberá monitorizar en la evolución del paciente, ya que es más reproducible y muestra menos variabilidad.
5. El nivel de respuesta no viene determinado por el sexo, el grado de atopia, la presencia o no de tabaquismo activo o la toma previa de esteroides inhalados20.
¿Qué medir para evaluar la respuesta terapéutica en la EPOC?
En las últimas décadas ha existido un enfoque nihilista de la EPOC como una enfermedad en la que los pacientes que la padecen están inexorablemente "condenados" a padecer frecuentes exacerbaciones y finalmente a fallecer por algún episodio de insuficiencia respiratoria. Se ha venido realizando la prueba broncodilatadora con la esperanza de encontrar una respuesta positiva en la idea de que estos pacientes responderían mejor a la terapia farmacológica disponible y tendrían mejor pronóstico; de forma paralela, los pacientes "irreversibles" eran considerados como portadores de una EPOC de "mal pronóstico" y se tenía muy pocas esperanzas en que el tratamiento médico fuera de utilidad. La evidencia científica actual, brevemente revisada anteriormente, debe hacer cambiar esta impresión. La prueba broncodilatadora per se no debe considerarse como predictor de la historia natural de la enfermedad, del estado de salud del paciente o de la respuesta al tratamiento.
Además de la espirometría y de la prueba broncodilatadora, en la evaluación de la eficacia terapéutica de una determinada intervención médica (o quirúrgica) se deberían incluir otros parámetros fisiológicos y clínicos que han demostrado ser sensibles a la acción terapéutica. Estos parámetros deben ser sencillos de realizar y estar al alcance de toda la comunidad médica. Para los pacientes con EPOC, nuestra propuesta es evaluar la eficacia de una intervención terapéutica de forma periódica con al menos 3 parámetros:
1. Espirometría con prueba broncodilatadora. El FEV1 sigue siendo el mejor parámetro para establecer la gravedad de la EPOC, y el cambio del FEV1 tras la administración de broncodilatadores o antiinflamatorios permite evaluar la reversibilidad de la obstrucción al flujo aéreo y la intensidad del tono broncomotor sobre la obstrucción de la vía aérea.
2. Capacidad inspiratoria. Se puede realizar con la mayoría de espirómetros disponibles en la actualidad; es una maniobra sencilla, reproducible y no consume demasiado tiempo. Proporciona una información adicional útil que permite identificar el efecto de la intervención terapéutica sobre volumen operativo pulmonar. El incremento de la CI posbroncodilatador es un buen marcador de la mejoría sintomática de los broncodilatadores.
3. Disnea. El uso de una escala de disnea tiene la ventaja de que puede detectar a corto plazo cambios muy relevantes para el paciente con EPOC.
Los conocimientos sobre los mecanismos patogénicos de la EPOC están evolucionando rápidamente hacia la idea de una enfermedad que comporta no sólo una afección de las estructuras torácicas sino también una afección sistémica. El enfoque clásico del tratamiento farmacológico de la EPOC ha sido tratar la limitación al flujo aéreo basado especialmente en la respuesta a broncodilatadores. No obstante, esta idea es contradictoria, dado que por definición la EPOC es una enfermedad insensible a los broncodilatadores. Probablemente ambas cosas (la definición de la EPOC y la idea de la irreversibilidad de la enfermedad) no puedan sustentarse en la actualidad. El tratamiento de los pacientes con EPOC debe basarse más bien en la evaluación de la respuesta individual a cada fármaco, administrada mediante la medición, no sólo de la respuesta a la espirometría sino de las consecuencias sobre otros parámetros como los arriba propuestos a corto plazo, y probablemente la monitorización de variables que reflejen el componente sistémico de la enfermedad, como pruebas de ejercicio o calidad de vida a largo plazo. En todo caso, es urgente desprenderse de la visión nihilista de la propia enfermedad o de un resultado "negativo" de una prueba broncodilatadora en pacientes con EPOC y pensar en esta entidad clínica como un proceso evolutivo prevenible y tratable.