La tromboendarterectomía pulmonar es el tratamiento de elección en la hipertensión pulmonar tromboembólica crónica. Presentamos nuestra serie completa con esta técnica.
MétodosDesde febrero de 1996 hasta junio de 2014, hemos realizado 106 tromboendarterectomías. Analizamos las características de la población, la mortalidad y morbilidad asociadas a la técnica y los resultados a largo plazo de supervivencia, mejoría funcional y resolución de la hipertensión pulmonar.
ResultadosLa edad media de la población fue 53±14 años. El 89% estaba en clase funcional III-IV de la OMS. La presión pulmonar media prequirúrgica fue 49±13mmHg y las resistencias vasculares pulmonares 831±364 dinas.s.cm−5. La mortalidad hospitalaria fue 6,6%. La morbilidad postoperatoria más relevante fue debida al edema pulmonar por reperfusión en el 20%, que fue factor de riesgo independiente (p=0,015) para mortalidad hospitalaria. Con una mediana de seguimiento de 31 meses (rango intercuartil 50), la supervivencia a los 3 y 5 años es 90 y 84%. Al año de seguimiento, el 91% está en clase funcional I-II de la OMS, la presión pulmonar media en 27±11mmHg y las resistencias pulmonares vasculares en 275±218 dinas.s.cm−5 (significativamente menores (p<0,05) que las basales). En 14 pacientes se diagnosticó hipertensión pulmonar persistente; aun así, su supervivencia es, a los 3 y 5 años, 91 y 73%, respectivamente.
ConclusionesLa tromboendarterectomía pulmonar ofrece resultados excelentes en el tratamiento de la hipertensión pulmonar tromboembólica crónica. Proporciona una elevada supervivencia a largo plazo, mejora la capacidad funcional y resuelve la hipertensión pulmonar en la mayoría de los pacientes.
Pulmonary thromboendarterectomy is the treatment of choice in chronic thromboembolic pulmonary hypertension. We report our experience with this technique.
MethodsBetween February 1996 and June 2014, we performed 106 pulmonary thromboendarterectomies. Patient population, morbidity and mortality and the long-term results of this technique (survival, functional improvement and resolution of pulmonary hypertension) are described.
ResultsSubjects’ mean age was 53±14 years. A total of 89% were WHO functional class III-IV, presurgery mean pulmonary pressure was 49±13mmHg and mean pulmonary vascular resistance was 831±364 dynes.s.cm−5. In-hospital mortality was 6.6%. The most important post-operative morbidity was reperfusion pulmonary injury, in 20% of patients; this was an independent risk factor (p=0.015) for hospital mortality. With a 31-month median follow-up (interquartile range: 50), 3- and 5-year survival was 90 and 84%. At 1 year, 91% were WHO functional class I-II; mean pulmonary pressure (27±11mmHg) and pulmonary vascular resistance (275±218 dynes.s.cm−5) were significantly lower (p<0.05) than before the intervention. Although residual pulmonary hypertension was detected in 14 patients, their survival at 3 and 5 years was 91 and 73%, respectively.
ConclusionsPulmonary thromboendarterectomy offers excellent results in chronic thromboembolic pulmonary hypertension. Long-term survival is good, functional capacity improves, and pulmonary hypertension is resolved in most patients.
La hipertensión pulmonar tromboembólica crónica (HPTEC) es una enfermedad rara, que se desarrolla en el 0,5-9% de los pacientes con tromboembolismo pulmonar1,2 (TEP). Se han establecido varios mecanismos para explicar cómo se llega a desarrollar HPTEC. Estos son: las embolias repetidas3, el crecimiento del trombo dentro del árbol pulmonar4 y la vasculopatía secundaria al daño endotelial5. Esta vasculopatía, con cambios a nivel microvascular indistinguibles de la hipertensión pulmonar (HP) idiopática, puede ocurrir en áreas del árbol vascular no afectadas por el TEP. El tratamiento de elección para esta enfermedad, cuando es factible, es la desobliteración quirúrgica de las arterias pulmonares con una tromboendarterectomía pulmonar (TEA)6–8.
Los objetivos fundamentales de la intervención quirúrgica son hemodinámicos, aminorar los efectos de la HP sobre el ventrículo derecho, respiratorios, mejorar la eficiencia ventilatoria al liberar espacios ventilados pero no perfundidos y profilácticos, prevenir el fallo ventricular derecho, la extensión retrógrada del trombo en el árbol pulmonar y la vasculopatía secundaria en los vasos permeables.
En el siguiente trabajo presentamos los resultados de las primeras 106 TEA realizadas en el Hospital Universitario 12 de Octubre. Se ofrecen los resultados del postoperatorio inmediato en términos de mortalidad, morbilidad y parámetros hemodinámicas. También analizamos los resultados del seguimiento a largo plazo en cuanto a supervivencia, capacidad funcional, parámetros hemodinámicos y remodelado del ventrículo derecho.
Pacientes y métodosPoblaciónLas indicaciones para la cirugía fueron9,10: a) HPTEC en clase funcional III-IV de la OMS; b) resistencias vasculares pulmonares (RVP) superiores a 300 dinas.s.cm−5 o, inferiores a esta cifra, pero con HP documentada con el ejercicio y c) trombos o lesiones típicas («webs», bandas, irregularidades en la íntima) accesibles quirúrgicamente en las ramas pulmonares principales, lobares o segmentarias proximales. Se tuvo en cuenta la concordancia entre la cifra de RVP, los defectos de perfusión de la gammagrafía de ventilación/perfusión y los hallazgos en la arteriografía pulmonar. Como requisito para considerar la cirugía todos los pacientes estuvieron antiacoagulados previamente al menos durante 3 meses. La indicación quirúrgica se adoptó siempre en la sesión de la Unidad Multidisplinar de Hipertensión Pulmonar.
Se consideraron criterios de exclusión la no accesibilidad quirúrgica y la presencia de patología grave asociada (enfermedad pulmonar severa, neoplasia activa, etc.).
La colocación de un filtro de vena cava inferior se valoró de manera individual en cada paciente.
DiagnósticoEl protocolo de diagnóstico inicial fue el mismo que en el resto de etiologías de HP, utilizando la gammagrafía de ventilación/perfusión pulmonar como prueba de cribado para establecer la etiología de HPTEC10–12. La prueba de referencia, en el diagnóstico y confirmación de la HPTEC fue la arteriografía pulmonar con cateterización selectiva de las ramas lobares13–15; en el mismo acto se efectuó cateterismo cardiaco derecho. Además, a todos los pacientes se les realizó un escáner torácico multicorte con contraste16,17.
Se realizó coronariografía a los pacientes mayores de 45 años o con factores de riesgo para enfermedad arterial coronaria.
La valoración objetiva del estado funcional se realizó con la prueba de la marcha de 6 minutos (PM6M) y la ergoespirometría con consumo de oxígeno. Además, en todos los pacientes se realizó estudio de trombofilia.
Técnica quirúrgicaRealizamos la TEA según el protocolo de la Universidad de California (San Diego, EE. UU.)5,18 Hay dos principios básicos a seguir en la cirugía, esta debe ser una verdadera endarterectomía, no una embolectomía y debe ser bilateral.
El acceso quirúrgico se realiza a través de esternotomía media y, la TEA se realiza con circulación extracorpórea, clampaje aórtico y parada circulatoria en hipotermia profunda a 20°C. Para llevar a cabo la endarterectomía realizamos periodos de parada circulatoria de 10 minutos, seguidos de periodos de reperfusión de 5 minutos mínimo. Para optimizar la visión y la iluminación del campo quirúrgico, durante la TEA, se utiliza un angioscopio rígido Hopkins II (Karl Storz, Tuttlingen, Alemania), conectado a una videocámara Twinvideo (Karl Storz, Tuttlingen, Alemania).
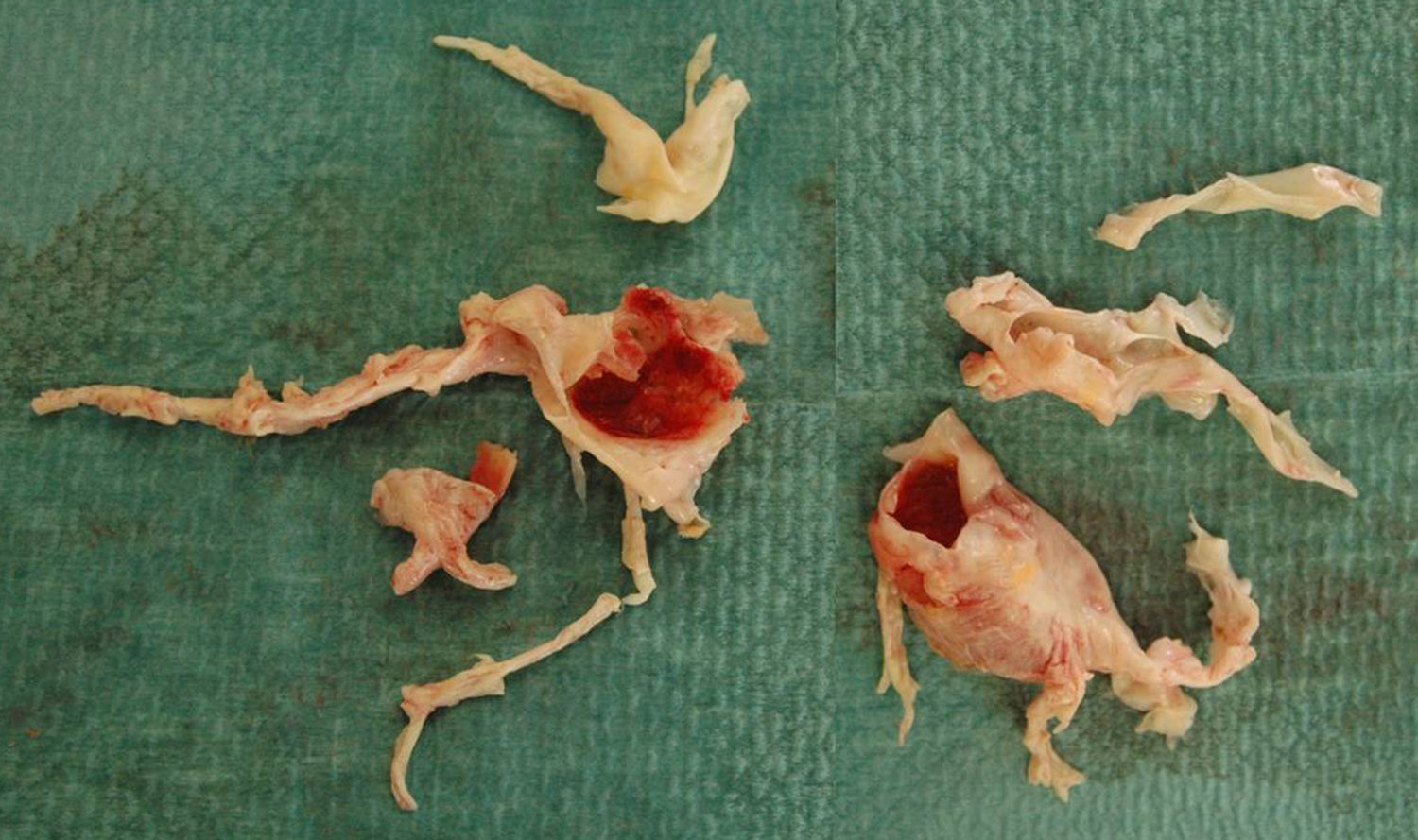
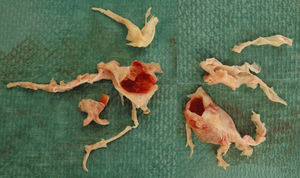
El material extraído en la TEA (fig. 1) se ordenó de acuerdo a la clasificación anatomopatológica con valor pronóstico, establecida por el grupo de la Universidad de California (San Diego, EE. UU.)19: tipo 1 o trombos en arterias pulmonares principales, tipo 2 o engrosamiento intimal y fibrosis proximal a las arterias segmentarias sin presencia de trombo, tipo 3 o afectación exclusiva de arterias segmentarias distales y subsegmentarias y tipo 4 o vasculopatía arteriolar distal.
PostoperatorioDefinimos el síndrome de edema pulmonar por reperfusión como: la insuficiencia respiratoria posquirúrgica, que cursa con hipoxia que se acompaña de infiltrados pulmonares en la radiografía de tórax, en alguna de las zonas tratadas quirúrgicamente, y precisa ventilación mecánica prolongada más de 96 horas.
SeguimientoEl protocolo de seguimiento fue el siguiente: primera revisión al mes, con examen físico, analítico y PM6M, segunda revisión a los 6 meses, con examen físico, analítico, ecocardiograma, ergoespirometría con consumo de oxígeno y cateterismo cardiaco derecho. Posteriormente, revisión anual con examen físico, analítico, ecocardiograma y PM6M. Hemos establecido el diagnóstico de hipertensión pulmonar residual o persistente, tras la TEA, cuando se calculan RVP superiores a 400 dinas.s.cm−5 en el estudio hemodinámico a los 6 meses. En estos pacientes se realiza escáner torácico multicorte con contraste.
Todos los enfermos se mantienen anticoagulados indefinidamente.
EstadísticaLas variables continuas se presentan como media±desviación estándar o mediana y rango intercuartil (RIC) y, las categóricas como frecuencias. La comparación entre variables categóricas se analizó mediante la prueba de la χ2 de Pearson o el estadístico exacto de Fisher. Las variables cuantitativas se analizaron aplicando la prueba de la t de Student o de la U de Mann-Whitney en función de la normalidad de las distribuciones según la prueba de Shapiro-Wilk. Se analizó la influencia de las siguientes variables en la mortalidad hospitalaria: tratamiento específico como puente a la cirugía, la clase funcional IV, RVP>1000 dinas.s.cm−5 en el cateterismo preoperatorio, el desarrollo de edema de reperfusión y el haber sido intervenido al comienzo de la serie (primeros 30 casos). Con aquellas variables relacionadas estadísticamente con la mortalidad, se realizó análisis de regresión logística, univariante y multivariante, para calcular el riesgo relativo y su intervalo de confianza de 95% (IC 95%).
Las curvas de supervivencia se calcularon mediante el método de Kaplan-Meier y la comparación entre ellas con la prueba de rangos logarítmicos.
Se consideró estadísticamente significativo un valor de p<0,05.
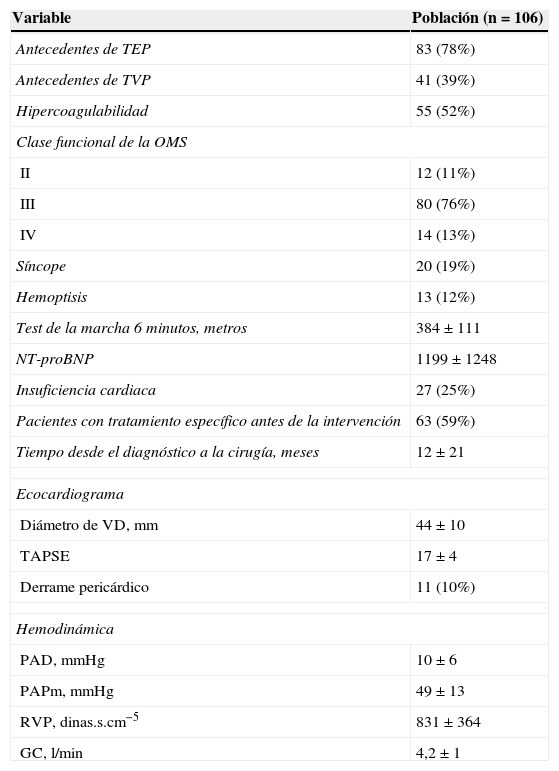
ResultadosDesde febrero de 1996 hasta junio de 2014 hemos realizado 106 TEA, de manera consecutiva en nuestro centro. La edad media de la población fue 53±14 años (rango 23-77) y el 57% eran varones. Las características clínicas y hemodinámicas de los pacientes se muestran en la tabla 1. En 29 enfermos las RVP fueron mayores a 1000 dinas.s.cm−5. Siete enfermos (6,6%) tenían cirugía cardiaca previa, tres de ellos TEA (una de ellas realizada en nuestro centro). El tiempo medio transcurrido entre el diagnóstico de HPTEC y la cirugía fue 5meses (RIC 8).
Características preoperatorias de la población
| Variable | Población (n=106) |
|---|---|
| Antecedentes de TEP | 83 (78%) |
| Antecedentes de TVP | 41 (39%) |
| Hipercoagulabilidad | 55 (52%) |
| Clase funcional de la OMS | |
| II | 12 (11%) |
| III | 80 (76%) |
| IV | 14 (13%) |
| Síncope | 20 (19%) |
| Hemoptisis | 13 (12%) |
| Test de la marcha 6 minutos, metros | 384±111 |
| NT-proBNP | 1199±1248 |
| Insuficiencia cardiaca | 27 (25%) |
| Pacientes con tratamiento específico antes de la intervención | 63 (59%) |
| Tiempo desde el diagnóstico a la cirugía, meses | 12±21 |
| Ecocardiograma | |
| Diámetro de VD, mm | 44±10 |
| TAPSE | 17±4 |
| Derrame pericárdico | 11 (10%) |
| Hemodinámica | |
| PAD, mmHg | 10±6 |
| PAPm, mmHg | 49±13 |
| RVP, dinas.s.cm−5 | 831±364 |
| GC, l/min | 4,2±1 |
GC: gasto cardiaco; PAD: presión en aurícula derecha; PAPm: presión arterial pulmonar media; RVP: resistencias pulmonares; TEP: tromboembolismo pulmonar; TVP: trombosis venosa profunda.
Se realizaron 96 (91%) TEA bilaterales. Los tiempos medios de circulación extracorpórea, isquemia y parada circulatoria han sido 205±38, 116±28 y 40±14 minutos, respectivamente. En 20 enfermos, se asoció otro procedimiento: así, se realizaron asociadas a la TEA 7 reparaciones tricúspides, 7 revascularizaciones miocárdicas, 5 cierres de foramen oval permeable y una trombectomía de ventrículo derecho. El material extraído se clasificó como tipo 1 de la clasificación de San Diego en el 49% de los casos, tipo 2 en el 42% y tipo 3 en el 9%.
En el postoperatorio inmediato la mediana del tiempo de ventilación fue 27 horas (RIC 92). La morbilidad más relevante consistió en: edema pulmonar de reperfusión en 21 pacientes (20%), hemorragia pulmonar en 4 pacientes (4%), reoperación por sangrado en 6 pacientes (6%), fallo cardiaco en 3 pacientes (3%), accidente vascular cerebral transitorio en un paciente (1%) y necesidad de ECMO o asistencia ventricular en 5 pacientes (5%). La indicación de ECMO se realizó por fallo cardiaco en 2 pacientes, y por insuficiencia respiratoria, en el contexto de hemorragia pulmonar, en 3 pacientes. La mediana de la estancia en UVI fue 5 días (RIC 7) y de la estancia hospitalaria 13 días (RIC 9). En el postoperatorio inmediato, la PAP media fue 28±7mmHg y las RVP 311±130 dinas.s.cm−5, significativamente (p<0,05) más bajas que en el preoperatorio.
La mortalidad hospitalaria en la serie global fue 6,6% (7/106, IC 95%:2,8%-13,5%). Las causas fueron insuficiencia respiratoria en 4 pacientes, hemorragia pulmonar en 2 y shock cardiogénico en uno.
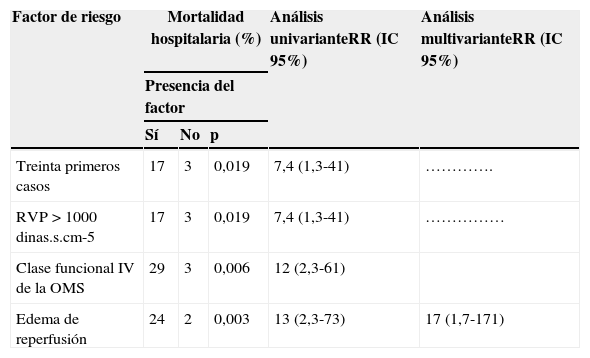
En el análisis univariante, el ser intervenido entre los 30 primeros casos (p=0,019), las RVP≥1000 dinas.s.cm−5 (p=0,019), la clase funcional IV (p=0,006) y el desarrollo de edema de reperfusión en el postoperatorio (p=0,003) se asociaron con la mortalidad hospitalaria. Tras el análisis multivariante, solo el edema de reperfusión se mantiene como factor de riesgo independiente para la mortalidad hospitalaria (p=0,015), (tabla 2).
Factores de riesgo para mortalidad hospitalaria
| Factor de riesgo | Mortalidad hospitalaria (%) | Análisis univarianteRR (IC 95%) | Análisis multivarianteRR (IC 95%) | ||
|---|---|---|---|---|---|
| Presencia del factor | |||||
| Sí | No | p | |||
| Treinta primeros casos | 17 | 3 | 0,019 | 7,4 (1,3-41) | …………. |
| RVP>1000 dinas.s.cm-5 | 17 | 3 | 0,019 | 7,4 (1,3-41) | …………… |
| Clase funcional IV de la OMS | 29 | 3 | 0,006 | 12 (2,3-61) | |
| Edema de reperfusión | 24 | 2 | 0,003 | 13 (2,3-73) | 17 (1,7-171) |
IC: intervalo de confianza; RR: riesgo relativo; RVP: resistencias vasculares pulmonares.
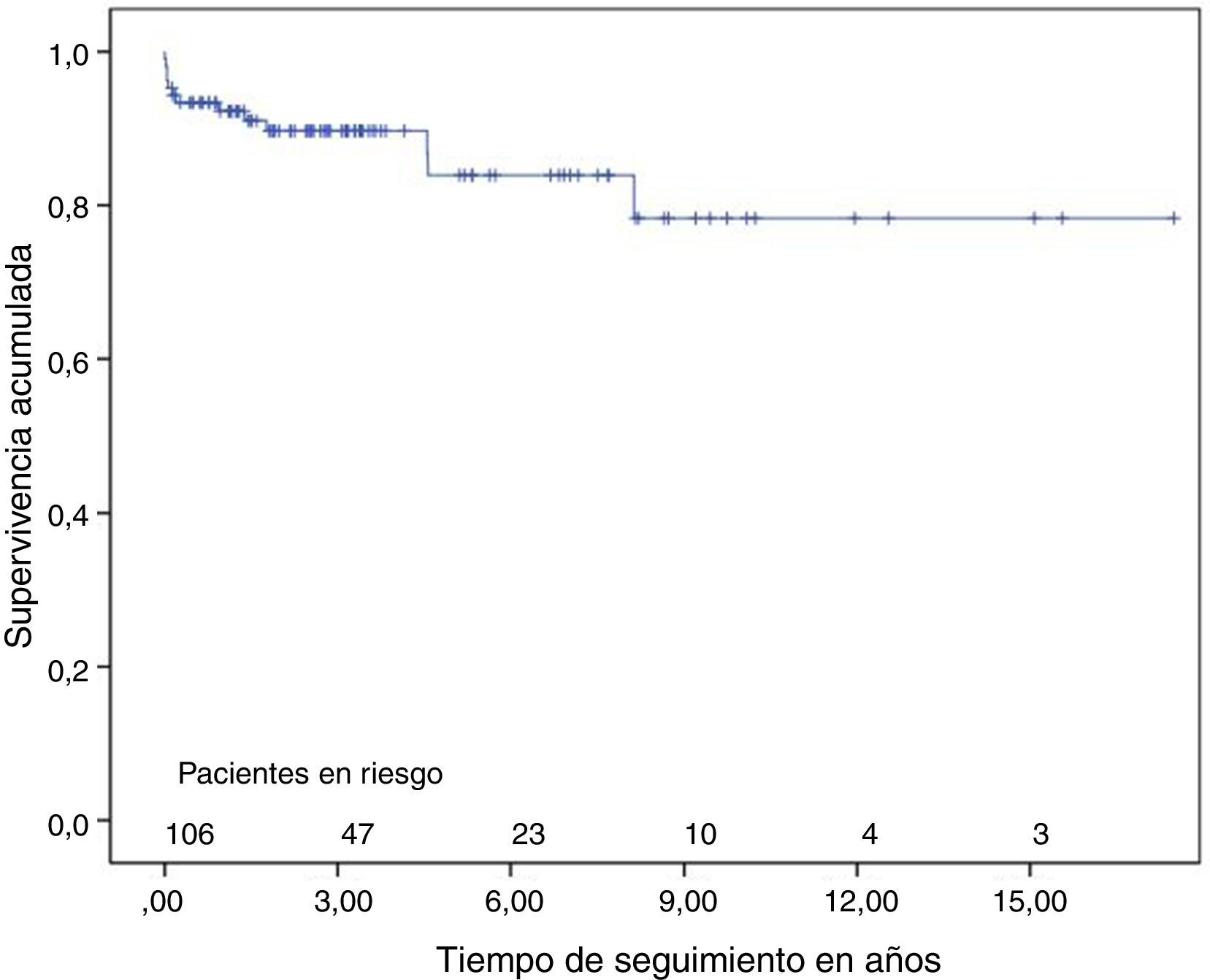
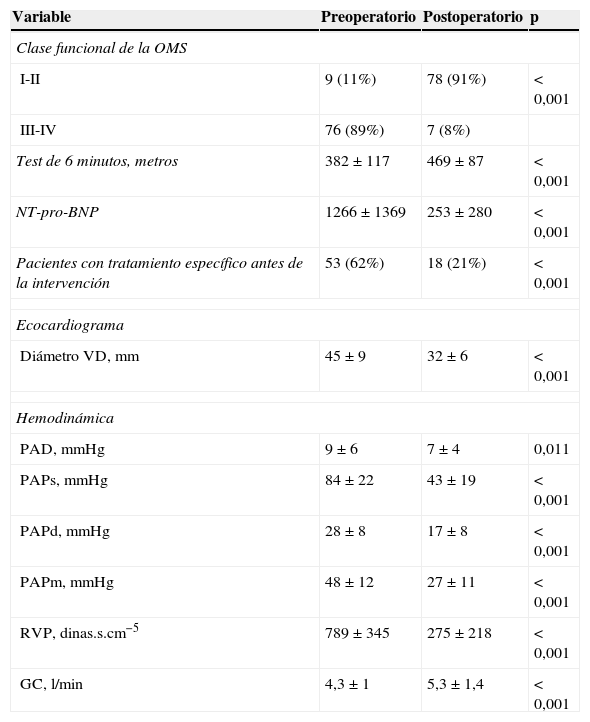
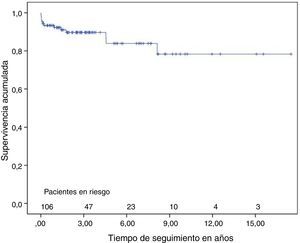
La mediana del tiempo de seguimiento es 31 meses (RIC 50). La supervivencia a los 3 y 5 años es 90±3% y 84±5% respectivamente incluyendo la mortalidad hospitalaria (fig. 2). La variación en los parámetros clínicos, ecocardiográficos y hemodinámicos, al año de seguimiento, aparecen en la tabla 3.
Diferencias clínicas, ecocardiográficas y hemodinámicas al año de seguimiento con respecto al preoperatorio
| Variable | Preoperatorio | Postoperatorio | p |
|---|---|---|---|
| Clase funcional de la OMS | |||
| I-II | 9 (11%) | 78 (91%) | < 0,001 |
| III-IV | 76 (89%) | 7 (8%) | |
| Test de 6 minutos, metros | 382±117 | 469±87 | < 0,001 |
| NT-pro-BNP | 1266±1369 | 253±280 | < 0,001 |
| Pacientes con tratamiento específico antes de la intervención | 53 (62%) | 18 (21%) | < 0,001 |
| Ecocardiograma | |||
| Diámetro VD, mm | 45±9 | 32±6 | < 0,001 |
| Hemodinámica | |||
| PAD, mmHg | 9±6 | 7±4 | 0,011 |
| PAPs, mmHg | 84±22 | 43±19 | < 0,001 |
| PAPd, mmHg | 28±8 | 17±8 | < 0,001 |
| PAPm, mmHg | 48±12 | 27±11 | < 0,001 |
| RVP, dinas.s.cm−5 | 789±345 | 275±218 | < 0,001 |
| GC, l/min | 4,3±1 | 5,3±1,4 | < 0,001 |
GC: gasto cardiaco; IC: índice cardiaco; PAD: presión en aurícula derecha; PAPd: presión arterial pulmonar diastólica; PAPm: presión arterial pulmonar media; PAPs: presión arterial pulmonar sistólica; PCP: presión capilar pulmonar; RVP: resistencias pulmonares.
Durante el seguimiento han fallecido 6 pacientes. Las causas fueron: insuficiencia cardiaca (3 pacientes), infección (uno), adenocarcinoma de vejiga (uno) y tromboembolismo pulmonar (uno).
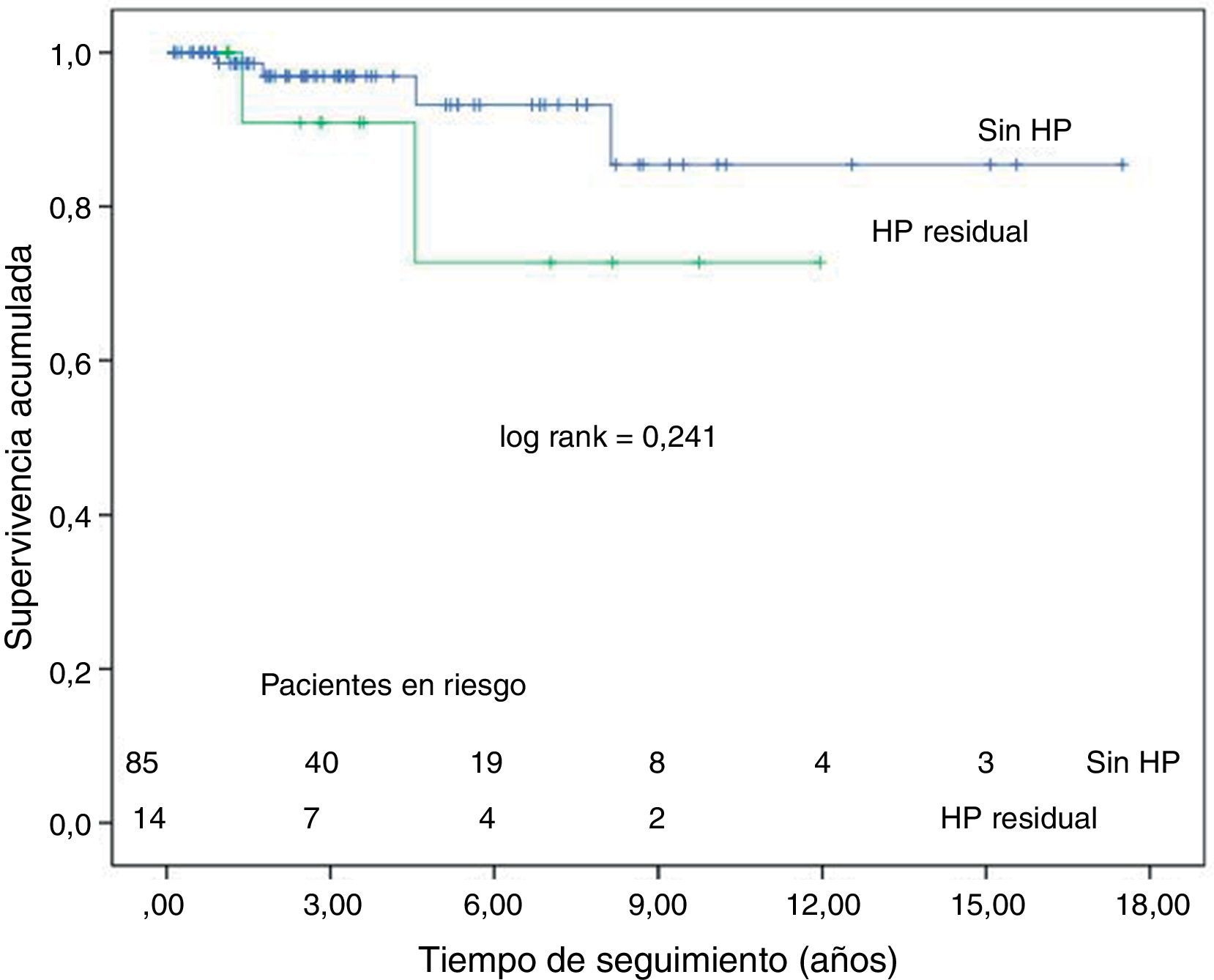
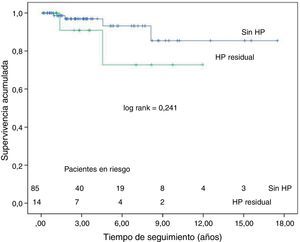
En 14 pacientes se ha diagnosticado HP persistente tras la TEA. Al año, el 64% de estos pacientes está en clase funcional I-II. Nueve (64%) enfermos necesitan tratamiento específico para la HP: antagonistas de la endotelina, inhibidores de la 5-fosfodiesterasa, análogos de las prostaciclinas o estimuladores de la guanilatociclasa soluble. Dos enfermos han fallecido por insuficiencia cardiaca. La supervivencia actuarial en el grupo de HP persistente es de 91±9 a los 3 años y 73±11 a los 5 años. En la figura 3, se muestra la curva de supervivencia de este grupo de enfermos y la de los enfermos sin HP residual, tras eliminar la mortalidad hospitalaria; entre ellas no existe diferencia significativa. Destacar que, a pesar de la persistencia de HP, las RVP disminuyeron significativamente respecto al preoperatorio (924±245 vs 641±269 dinas.s.cm−5; p=0,033).
DiscusiónLa HPTEC es una enfermedad con baja prevalencia, 8,9 casos por millón de habitantes en nuestro entorno20. Se ha demostrado que la HPTEC es una complicación a largo plazo del TEP sintomático, con una incidencia acumulada de 0,1-9,1% a los 2 años1,2. No obstante, en un número significativo de casos el episodio de TEP fue asintomático5. Por estas razones, se considera la HPTEC como una enfermedad infradiagnosticada y, muchas veces, referida tardíamente para su tratamiento. Las guías clínicas10 y los documentos de consenso15 establecen la necesidad de crear Unidades Multidisciplinares para el tratamiento de la HPTEC, con un grupo quirúrgico experto. Un enfermo no debería ser considerado no operable, definitivamente, hasta no ser evaluado en este tipo de Unidad. En el registro internacional21, hasta un 43% de los pacientes valorados no se consideraron quirúrgicos y en el registro español (REHAP)20 el 70%. En nuestra Unidad, se han intervenido el 53%22 de los pacientes presentados en sesión multidisciplinar. Sin embargo, muchos se han derivado tardíamente por ello, el tiempo entre el diagnóstico y la cirugía ha sido largo y un 13% de los pacientes se han intervenido en clase funcional IV.
Los resultados de nuestra serie son excelentes y son comparables a las series más extensas de la literatura21,23. Esto se debe a la experiencia adquirida y al trabajo de protocolización del proceso en la Unidad Multidisciplinar de Hipertensión Pulmonar del Hospital 12 de Octubre.
La serie de TEA que presentamos en este trabajo es la más extensa y consolidada de nuestro país. En el año 2009 publicamos los resultados iniciales24 con 30 TEA, similares a los recientemente publicados por el Hospital Clínic de Barcelona25 con 32 pacientes, la mortalidad hospitalaria fue del 17 y el 18,8% respectivamente. En ambos trabajos, se objetiva que los resultados quirúrgicos mejoran con la experiencia del equipo multidisciplinar que los realiza. También se obtiene mayor supervivencia y se incrementa progresivamente el número de pacientes que pueden ser considerados operables; además, la cirugía obtiene mejores resultados que el tratamiento médico. Así, la TEA es el tratamiento de elección en esta patología con buenos resultados en nuestro entorno.
La accesibilidad de las lesiones varía en función de la experiencia del grupo quirúrgico. En los grupos con más experiencia, el porcentaje de enfermos con afectación de ramas segmentarias (grupo 3 de San Diego) aumenta con el tiempo, sin por ello empeorar los resultados26–28. Los avances en la técnica quirúrgica permiten, a día de hoy, la disección y extracción de material a nivel segmentario y subsegmentario.
Aunque no disponemos de una cifra concreta en las RVP o en la disfunción ventricular derecha que contraindique la cirugía, el riesgo quirúrgico y el pronóstico, a largo plazo, empeora con las RVP preoperatorias más elevadas (mayores de 1000 dinas.s.cm−5)29,30. En todo caso y, aunque el riesgo quirúrgico es mayor, estos enfermos siguen obteniendo beneficio de la cirugía29. No hemos considerado no quirúrgico ningún enfermo por presentar RVP elevadas, ni por disfunción ventricular severa. En el estudio que presentamos, las RVP mayores de 1000 dinas.s.cm−5 fueron un factor de riesgo para mortalidad hospitalaria en el análisis univariante; no obstante, no se asociaron en el análisis multivariante, aunque también son factor de riesgo importante en el desarrollo de edema de reperfusión.
La técnica quirúrgica estándar para la TEA se basa en los principios establecidos por el grupo de San Diego4, endarterectomía en parada circulatoria con hipotermia profunda. Esta técnica ha demostrado ser segura y eficaz. La serie más reciente, publicada por este grupo27, con más de 2700 casos, comunica una mortalidad del 2,2% en los últimos 500 pacientes intervenidos. Aunque ha habido una serie de trabajos describiendo la TEA sin parada circulatoria o, al menos, con perfusión cerebral continua31–34, estas técnicas no aportan mejores resultados, incluyendo las complicaciones neurológicas. Todos hacen referencia a la dificultad de llegar a ramas distales sin la ayuda de la parada circulatoria. En nuestro trabajo solo ha habido una complicación neurológica transitoria que, por otra parte, no puede relacionarse solo con la parada circulatoria.
El edema de reperfusión es una complicación inherente a la TEA que, según las distintas series, aparece entre un 5 y un 20% de las intervenciones23. Es factor de riesgo para la mortalidad hospitalaria como se ha demostrado también en nuestra serie. La manifestación del edema de reperfusión varía, desde una hipoxia leve con poca expresión radiológica, hasta cuadros de insuficiencia respiratoria graves, similares al distress respiratorio. Es necesario, por lo tanto, establecer una definición que limite los casos a los que representen una entidad clínica con repercusión en la evolución del paciente.
La necesidad de ECMO, con las indicaciones de fallo cardiaco secundario a HP o poscardiotomía, y la insuficiencia respiratoria severa por hemorragia o edema pulmonar, se ha recogido en otras series35,36. Berman et al.36 han comunicado una supervivencia del 57% en estos enfermos; en nuestra serie fue 40%. Se trata de un grupo de pacientes que habrían fallecido sin esta asistencia; por ello, es un escalón terapéutico que debe estar presente en las unidades de referencia para TEA15.
La supervivencia tras la TEA en el trabajo que presentamos es excelente y comparable a la obtenida en las series más importantes23. Además, en la mayoría de los pacientes mejora la clase funcional, normaliza la presión pulmonar y, de forma secundaria, remodela el ventrículo derecho.
El diagnóstico de HP persistente es un tema actualmente en debate, tanto por su definición (PAPm>25, 30 o 35mmHg; RVP>400, 450, 500 o 550 dinas.s.cm−5)21,30,37, como por el momento adecuado para establecer su diagnóstico. Su incidencia se sitúa entre el 6 y el 31%, según la definición adoptada. Nuestra Unidad ha optado por definirlo cuando se presenten unas RVP>400 dinas.s.cm−5, porque estas, frente a la PAPm, tienen valor pronóstico antes y después de la cirugía. En cuanto al momento del diagnóstico, se ha situado en la revisión de los 6 meses, ya que los cambios hemodinámicos en el postoperatorio inmediato influyen en el cálculo de las RVP y, por otra parte, la prevalencia de HP residual aumenta a lo largo del seguimiento37 cuando la causa es la vasculopatía distal.
A pesar de la persistencia de la HP, la supervivencia y la mejoría funcional de este subgrupo también son buenas, posiblemente porque aún en rangos de HP, las RVP disminuyeron de forma significativa. Otros grupos como Freed et al. en el Hospital de Papworth30 (Cambridge), han publicado resultados parecidos en el grupo de pacientes con HP residual.
ConclusionesNuestro trabajo demuestra, una vez más, que la TEA es el tratamiento de elección en la HPTEC10 y puede realizarse con éxito en nuestro país. La intervención quirúrgica cambia el pronóstico de la enfermedad, ofrece una buena supervivencia largo plazo, así como la resolución de la hipertensión pulmonar y la mejoría funcional en la mayoría de los enfermos.
LimitacionesSe trata de un estudio observacional retrospectivo de la serie inicial de un solo centro.
No se dispone del perfil evolutivo del NT-pro-BNP en los enfermos intervenidos antes de 2009.
Los resultados al año de seguimiento se han analizado en 85 pacientes que superaban ese seguimiento. De ellos hemos obtenido 76 cateterismos, los 9 restantes corresponden a pacientes que se han derivado a sus centros de referencia y no han remitido esta información.
AutoríaCortina Romero JM: realización de los procedimientos quirúrgicos, recogida de datos, análisis estadístico, interpretación de resultados y elaboración del manuscrito.
López Gude MJ: colaboración en los procedimientos quirúrgicos, recogida de datos, análisis estadístico, interpretación de resultados y elaboración del manuscrito.
Pérez de la Sota E, Forteza Gil A, Centeno Rodríguez J: colaboración en los procedimientos quirúrgicos.
Eixeres A: recogida de datos.
Ruiz Cano MJ, Velázquez MT, Gómez Sánchez MA, Pérez Vela JL, Sánchez Nistal MA: diagnóstico y manejo clínico de los pacientes.
Escribano Subías P: diagnóstico y manejo clínico de los pacientes, interpretación de resultados y elaboración del manuscrito.
Todos los autores han revisado el manuscrito.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Al personal colaborador con la Unidad Multidisciplinar de Hipertensión Pulmonar del Hospital Universitario 12 de Octubre.
Al personal médico y de enfermería de la Unidad de Medicina Intensiva Cardiológica.
Al personal médico y de enfermería del quirófano de Cirugía Cardiaca.